由L-精氨酸发酵液制备结晶型精酮合剂
2012-12-25李琪倩李恒陆震鸣许泓瑜方佳茂许正宏孙志浩史劲松
李琪倩,李恒,陆震鸣,许泓瑜,方佳茂,许正宏,孙志浩,史劲松
1(江南大学医药学院,江苏无锡,214122)2(广东环西生物科技股份有限公司,广东普宁,515300)
L-精氨酸-α-酮戊二酸盐(L-arginine-α-ketoglutarate,AAKG),简称精酮合剂,是由 L-精氨酸(L-Arg)与α-酮戊二酸(α-KG)络合形成的氨基酸盐,可以从溶液中以盐的形式结晶析出。在不同的结晶条件下,AAKG可以形成单精氨酸酮戊二酸盐(MAAKG)和双精氨酸酮戊二酸盐(DAAKG)两种形式,目前研究和应用较多的主要是MAAKG,其晶型为无色棱柱状,易溶于水,微溶于乙醇,不溶于丙酮、乙醚等,在水溶液中能够完全解离为L-精氨酸和α-酮戊二酸。本文研究的AAKG均指MAAKG,其结构式如下:
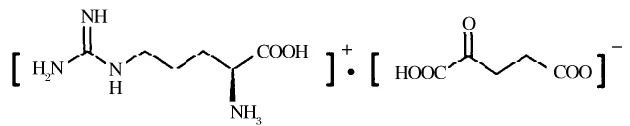
AAKG不仅兼具L-精氨酸和α-酮戊二酸的生理功能,而且可以作为功能性营养强化剂和护肝药物应用于临床,主要用于增强体格、促进肌肉的快速增长和创伤恢复[1-3],促进肝细胞对营养和能量的代谢,增强力量和精力,其生理机制在于AAKG能够在短期内提高体内NO的水平,增强蛋白质同化作用。目前,AAKG作为功能食品在国际市场上销量日益增加,并与鸟苷酸酮戊二酸盐(OKG)一起,在医学、营养、运动领域备受重视。
AAKG的制备工艺主要有3种方式:1是直接混合法,是将等摩尔的L-精氨酸、α-酮戊二酸粉末进行简单的混合而成,其制备方法简单,成本较低,是商品化生产最为通用的方法。但该法生产的AAKG不是结晶型产品,二者之间没有盐键结合,产品质量受到原料的品质、混合的均匀度影响;2是冻干法,先将L-精氨酸、α-酮戊二酸粉末进行等摩尔混合并溶解,再将溶液冷冻干燥成为冻干粉,该工艺能够得到相对稳定的结晶型AAKG,但存在晶型不可控、冻干过程能耗大等问题,一般仅适合 AAKG 注射剂生产[1-2,4];3是结晶法,一般是将L-精氨酸、α-酮戊二酸按比例混溶后,通过溶液浓缩,加入有机溶剂、降低温度等方法,使AAKG以晶体形式析出,其产品纯度高,质量可控。相比而言,混合法和冻干法,在制备过程中不能够去除原料带入的杂质,对原料品质有着较高的要求,而结晶工艺是一个能有效去除杂质的精制过程,因而能够使用纯度相对较低的原料,甚至是低浓度的发酵液。本文在研究结晶法制备AAKG工艺基础上,直接利用 L-Arg发酵液为原料,进行结晶型AAKG的制备。由于制备路线可以绕开L-精氨酸提取环节的离子吸附、洗脱、浓缩和结晶操作,因而具有工艺流程简捷、综合成本低等优点。
1 材料和方法
1.1 主要试剂
L-精氨酸(L-Arg,医药级),购自上海斐雅科技发展有限公司;α-酮戊二酸(α-KG,医药级),购自武汉银河化工有限公司。检测使用的标准品购自国药集团化学试剂有限公司。
1.2 主要仪器
电热恒温水槽(DK-80),上海精宏实验设备有限公司;旋转蒸发器(RE-52A),上海亚荣生化仪器厂;型真空干燥箱(DZF-6050),上海博迅实业有限公司医疗设备厂;液相色谱仪(Dionex UltiMate 3000),美国戴安公司;5L自动控制发酵罐(Biotech-2001),上海保兴生物设备工程有限公司。
1.3 AAKG结晶工艺研究
1.3.1 基本步骤
在50 mL,0.5~1.0 mol/L的L-Arg溶液中,缓慢加入一定量的α-KG粉末,搅拌使其完全溶解,减压浓缩至浓度为1.5~3.0 mol/L。浓缩液以一定速率缓慢降温,置于5~15℃下恒温结晶24~48 h。待结晶完全后,分离晶体,并用少量冷乙醇淋洗晶体2~3次,置于40℃下真空干燥得到结晶型AAKG。
1.3.2 L-Arg和α-KG的混溶比例对AAKG晶体组成影响
研究上述制备工艺中α-KG与L-Arg的混溶比例,分别考察 α-KG:L-Arg 为 0.8、1.0、1.2、1.4、1.6时,结晶形成的AAKG晶体中L-Arg和α-KG的摩尔比影响。
1.3.3 起晶浓度对AAKG晶体收率和晶体纯度的影响
减压浓缩L-Arg与α-KG混合溶液,控制不同的浓缩比例,分别考察 1.25、1.5、2.0、2.5、3.0(mol/L)溶液浓度对AAKG的结晶产率、晶体纯度及晶体组成的影响。
1.3.4 降温速率和结晶温度对AAKG晶体收率和晶体纯度的影响
分别考察5、10和15℃下AAKG的结晶收率和晶体纯度情况,并比较快速降温结晶(10℃/h)和缓慢降温速率(2℃/h)对晶体结构和晶体纯度的影响。
1.4 L-Arg发酵液制备AAKG的工艺研究
以实验室筛选获得的精氨酸高产突变株C.crenatum SYPH5-8为菌种进行L-Arg发酵,采用5L自动控制发酵罐。发酵培养基配方如下:
葡萄糖150,玉米浆 40,(NH4)2SO420,KH2PO41.5,MgSO4·7H2O 0.5,FeSO4·7H2O 0.02,MnSO4·H2O 0.02,121℃灭菌20 min,流加氨水控制 pH 7.0~7.2。
发酵液预处理[5]:先加入过量草酸沉淀Ca2+,在60℃下加热10 min沉淀蛋白质后,在pH 10.0,30℃下用聚丙烯酰胺(400 mg/L)对发酵液进行絮凝,离心去除菌体等固形物后,再加入活性炭(10 g/L),调节pH5.0,加热至80℃进行脱色处理30 min,最后经过滤或离心得L-Arg清液。
结晶操作:将预处理后的L-Arg发酵液减压浓缩至1 mol/L,加入α-KG固体粉末,反应充分后,进一步浓缩至1.5~3.0 mol/L,调节溶液pH 3.0~4.0,然后将浓缩液进行缓慢降温结晶。考察结晶的AAKG的产率,纯度及晶体组成比。
1.5 AAKG晶体纯度及组成比分析
AAKG在水溶液中解离为L-Arg及α-KG,采用HPLC同时测定溶液中 L-Arg和 α-KG的含量。HPLC为Dionex UltiMate 3000液相色谱仪,色谱柱Diamonsil C18(4.6 mm×250 mm),流动相采用甲醇/水/H3PO4(5/95/0.05),进样体积 10 μL,流速 0.8 mL/min,柱温30℃。采用紫外检测器,检测波长210 nm。
测试样品AAKG晶体先在60~80℃下真空干燥8 h,称取并配置成4 g/L溶液。样品的HPLC色谱峰保留时间应与L-Arg、α-KG标准品一致。根据标准品溶液浓度和峰面积分别计算AAKG中L-Arg、α-KG的含量。AAKG晶体纯度为晶体中L-Arg、α-KG的总含量与晶体质量的百分比,晶体组成比为L-Arg与α-KG的摩尔比。结晶操作中的AAKG晶体收率是指制备出的AAKG质量与反应液中L-Arg、α-KG的总含量的百分比。
1.6 AAKG的质量指标研究
AAKG纯度、晶体组成比按上述方法进行测定。水分按《食品安全国家标准——食品中水分的测定》(GB5009.3-2010)中直接干燥法进行测定;灰分按《食品安全国家标准——食品中灰分的测定》(GB5009.4-2010)一般食品的测定方法进行测定;pH测定为0.1g样品溶解在20 mL蒸馏水中的溶液pH,用pH计测量;比旋光度按《化学试剂-比旋光本领(比旋光度)测定》(GBT 613-2007)中通用方法测定,测定仪器选用WZZ-2B自动旋光仪,样品浓度为0.16g/mL(H2O),旋光管长度10 cm,温度20℃,钠光谱D线589.44波长。
菌落总数按《食品微生物学检验菌落总数测定》(GB 4789.2-2010)进行检验;大肠杆菌数按《食品卫生微生物学检验 大肠杆菌计数》(GB/T 4789.38-2008)中“大肠杆菌MPN计数”进行试验;采用石墨炉原子吸收法及原子荧光光谱法对AAKG样品中铅,砷,汞重金属含量进行测定。
2 结果与讨论
2.1 AAKG结晶工艺研究
L-Arg和α-KG均可溶于水中,但体系的不同pH值影响到二者的解离。L-Arg分子中基团α-COOH的 pK1为2.17,α-NH+3的pK2为9.04,侧链胍基上H的pK3为12.84。其PI主要决定于pK2和pK3,PI=(pK2+pK3)=10.94。因此,在小于pI的pH体系下,L-Arg主要是以α-NH+3形式存在。同样,α-KG是有机二元酸,也存在二级解离情况。实验通过滴定法测定其pK1=1.88,pK2=2.35,显然这2个解离常数相差较小,羧酸结合阳离子能力较强,因此在与LArg成盐时,单精氨酸盐与双精氨酸盐均容易形成,但是否能够从溶液中析出特定的晶体,还需要取决于他们的溶解度。
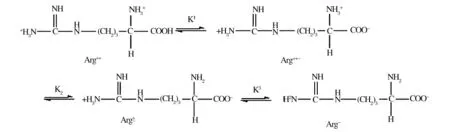
图1 L-精氨酸的解离情况
pH是影响溶解度的主要因素之一,而溶液体系的pH与L-Arg和α-KG的含量和组成比例直接有关。在自然pH体系下,随着二者摩尔分率的改变,体系pH也不断变化,图2显示的是在1 mol/L L-Arg溶液中,不断加入α-KG后,体系pH从10逐渐降低到2.3左右。初步结晶实验也表明,当体系pH为3~4时,L-Arg与 α-KG较易形成 MAAKG晶体,而DAAKG晶体形成区域主要在pH 2.5~3.5,在上述范围之外,很难通过结晶获得AAKG晶体。要获得特定组成的AAKG晶体,可以通过控制溶液体系中溶质的摩尔分率达到调控体系pH的目的。实验以制备MAAKG为目的,具体考察了混溶比例,溶液浓度,结晶温度及降温速率对晶体收率和晶体纯度的影响。
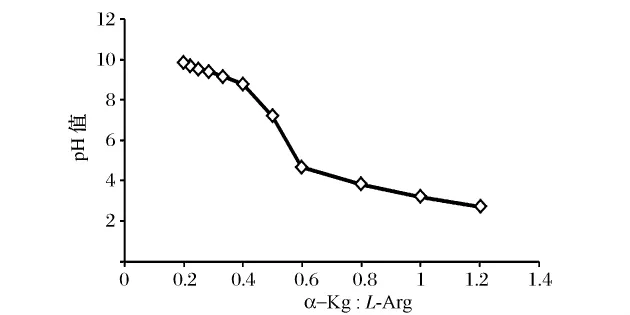
图2 不同比例L-Arg与α-KG反应,溶液pH变化情况
2.1.1 L-Arg和α-KG的混溶比例对晶体组成比影响
参照1.3.1的基本步骤,在50 mL的溶液中,考察α-KG∶L-Arg的摩尔比在0.8~1.6范围内AAKG晶体形成情况,表1数据显示,从不同比例L-Arg和α-KG反应,结晶制备出的AAKG的产率、纯度及晶体组成比有较大的差异。当反应物中L-Arg和α-KG为1∶1定量添加的时候,制备出的AAKG产率和纯度均较高,产率达到71.5%,纯度达到92.7%,且晶体中L-Arg和α-KG的摩尔比与其他组比最接近1∶1,这是制备AAKG的优化条件。
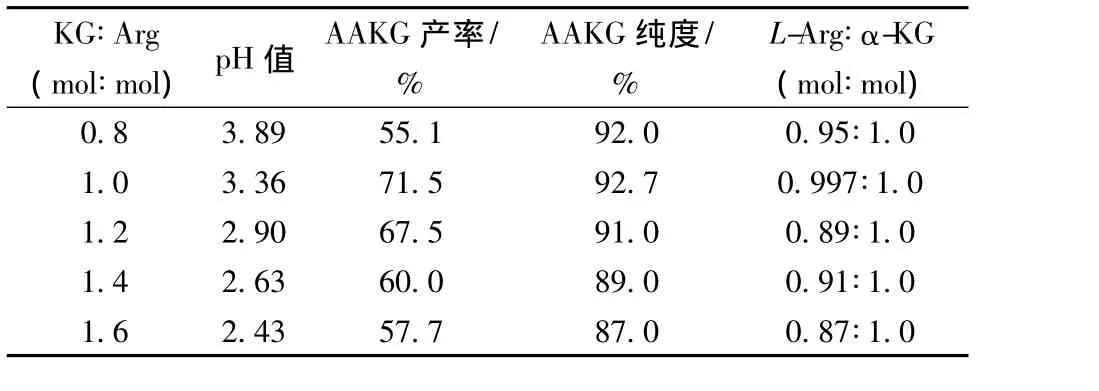
表1 L-Arg与α-KG反应比例对AAKG结晶产率和纯度的影响
2.1.2 溶液浓度对AAKG制备的影响
溶液的起晶浓度影响晶体的收率,也将对生产的能耗产生较大影响。实验通过控制不同的浓缩比,考察不同的起晶浓度对晶体产率、纯度及晶体组成摩尔比的影响(表2)。随着起晶浓度的提高,AAKG的产率也不断提高,但当溶液浓度超过2.50 mol/L时,进一步浓缩将变得十分困难,而且将使杂质浓度提高,降低晶体的纯度。由于溶液浓缩是一个十分耗能的过程,在保证一定收率的基础上,尽量降低蒸发量可以大幅度节能,因而从工业经济角度出发,适宜的起晶浓度为1.5 mol/L。更为优化的方案应该结合溶液的杂质含量、产品纯度要求以及后续的冷却过程等多方面因素得出。
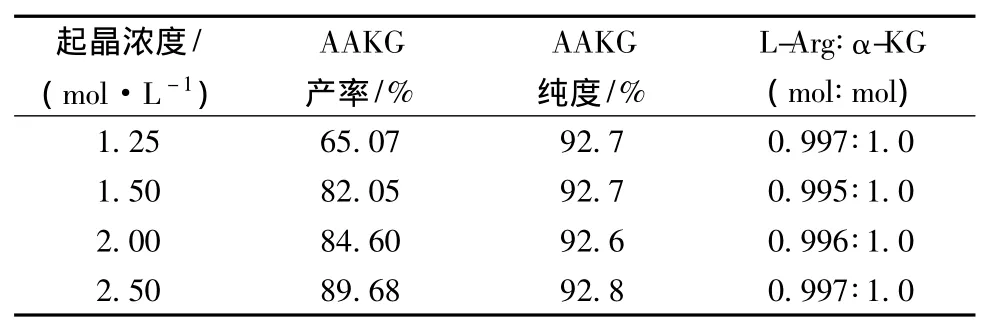
表2 不同起晶浓度对AAKG结晶产率和纯度的影响
2.1.3 结晶温度和降温速率对AAKG制备的影响
冷却结晶是通过降温使溶液成为过饱和溶液而析出结晶,这是常用的结晶方法之一,尤其适合溶解度随温度降低而显著下降的物质。由于缺少AAKG的溶解度等相关数据,不能通过理论的推导确定冷却结晶的控制参数。故实验研究了5℃、10℃、15℃下的AAKG结晶情况,并分别比较了快速降温(10℃/h)和缓慢降温(2℃/h)两种方式对晶体收率、纯度和晶体组成比的影响(表3)。
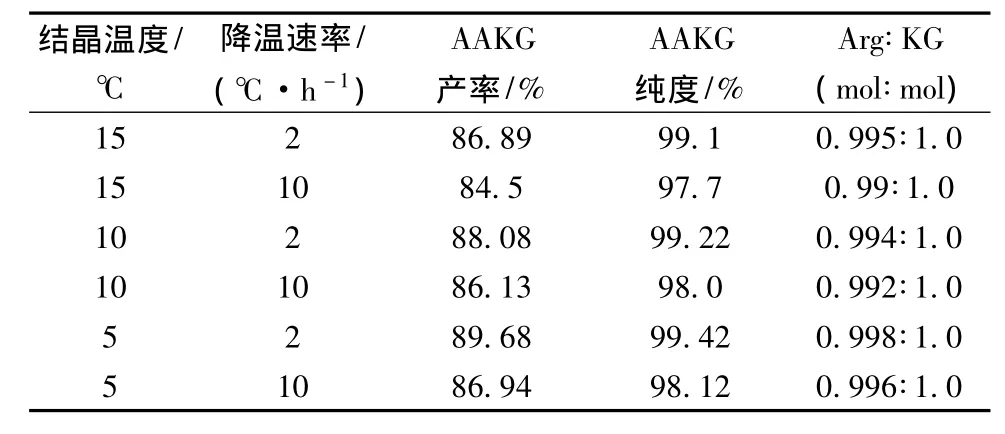
表3 结晶温度和降温速率对AAKG结晶产率和纯度的影响
数据表明,低温下的缓慢均匀的降温结晶,可以获得纯度较高的AAKG晶体,而晶体产率、组成摩尔比没有较大差异。在缓慢降温结晶中,可以获得颗粒较大的晶体颗粒,晶体的比表面积小,晶体表面对母液和杂质的吸附也减少,因而可以增加产品纯度。相比而言,快速降温所形成的晶形较小,而且快速结晶过程中,容易形成母液的晶间包藏,使晶体纯度下降。同样,溶液的冷却,尤其是10℃以下的冷却也是一个耗能过程,在满足工艺目标的前提下,为降低能耗应优先选择较高的结晶温度,显然在10℃进行控温结晶既具有良好的过程经济性,也可以获得较为理想的收率和晶体纯度。
2.2 L-Arg发酵液结晶制备AAKG的工艺研究
发酵法制备L-精氨酸是发展趋势,与水解法相比其产品具有良好的安全性,但目前L-精氨酸发酵仍存在产酸率低、发酵周期长等问题。谷氨酸棒杆菌(C.crenatum)SYPH5-8是1株高产精氨酸的突变株,产酸水平在40 g/L左右,其发酵液中除了L-精氨酸外,还含有较多的Ca2+,残余培养基成分及大量菌体,此外,还含有少量的谷氨酸、赖氨酸等副产物,在进行结晶操作前,需要通过相对简捷的预处理工艺尽可能去除这些杂质。实验采用草酸沉淀Ca2+及60℃下加热10 min沉淀蛋白质,用聚丙烯酰胺促进菌体等固型物絮凝,用活性炭吸附发酵液中色素及少量杂氨酸。
由于发酵液的L-Arg含量较低,需要进行浓缩。3.0 L发酵液浓缩至600 mL,离心去除溶液中少量的沉淀,测定浓缩液中L-Arg浓度为1.1 mol/L。参照AAKG的结晶工艺条件,按照等摩尔比例加入α-KG,待充分溶解后,进一步浓缩至体积400 mL左右,达到起晶浓度,其L-Arg浓度约为1.68 mol/L。采用缓慢降温方式使溶液冷却至室温,再置入8~10℃恒温箱中育晶24 h。回收晶体,并采用乙醇进行晶体洗涤,干燥后进行含量及组成测定(结果见表4)。再取制备出的AAKG粗晶体50 g溶解在100 mL去离子水中,加热充分搅拌后过滤。将滤液以上述同样的条件进行重结晶和乙醇洗涤,干燥后进行含量及组成测定(结果见表4)。
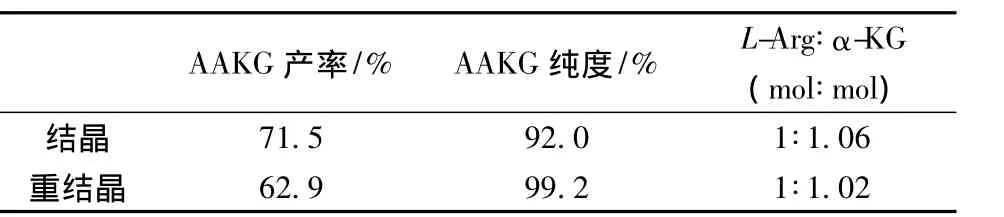
表4 L-Arg发酵液制备的AAKG的产率,纯度及L-Arg∶α-KG 的测定
由于母液中含有较多的杂质,AAKG晶体纯度较低,需要采用重结晶方式提高晶体纯度。但重结晶操作影响AAKG收率,母液中含有较多的产品成分,在工业大生产中需要考虑回收与利用。综合上述研究内容,本文初步提出由L-精氨酸发酵液制备AAKG晶体的工艺流程(图3)。图中所示的预处理包含上文提到的絮凝、活性炭吸附以及菌体分离等过程;浓缩操作可以采用减压浓缩,也可以选择反渗透等膜法浓缩,母液可以采用离子交换树脂选择性吸附,冷却结晶可以选择真空连续蒸发结晶器来提高结晶效率和晶体收率。
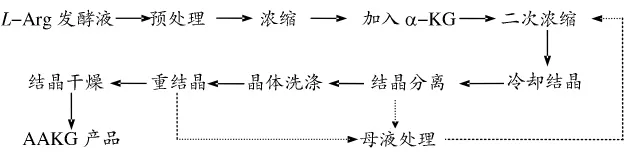
图3 L-Arg发酵液进行AAKG结晶流程示意图
2.3 AAKG质量指标研究
对L-Arg发酵液制备出的4个批次的结晶型AAKG进行理化指标、卫生指标测定,结果见表5。相关指标符合我国食品卫生质量要求,而且指标具有良好的稳定性,因此,采用结晶法进行AAKG制备,其质量可控性较高。需要采用絮凝、吸附等方法进行预处理,2是采用乙醇对晶体进行洗涤,3是利用重结晶方法可以有效提高产品纯度。
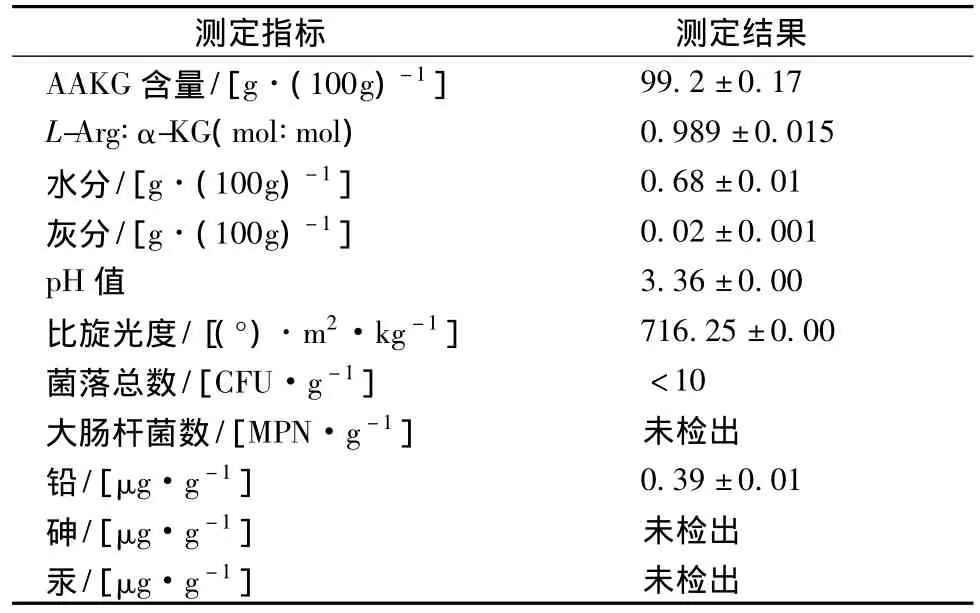
表5 AAKG的质量指标测定
本文提出从L-Arg发酵液直接制备AAKG,旨在绕开L-精氨酸的提取过程,而该过程不仅使用大量的酸碱化学品,而且涉及大规模的树脂吸附、洗脱和L-精氨酸的结晶、干燥,能耗物耗高,流程长并与AAKG制备过程部分重复,因此将L-Arg发酵生产与AAKG的制备进行耦联,能够有效缩短流程,减少排放,节省制备成本。更为重要的是,该生产路线能够保证产品的安全性和质量稳定性。但必须指出的是,对发酵液进行浓缩,也是一个高能耗的过程,为进一步降低能耗,可以采用反渗透或纳滤方法进行膜法浓缩,也可以通过超滤等方式脱除溶液体系的大分子杂质,这对提高过程效率和产品收率有显著意义,将是下一步放大试验的重要研发内容之一。
3 结果与讨论
本文对影响AAKG结晶工艺的溶液pH、L-Arg与α-KG的投料比、起晶浓度以及冷却方式进行了初步探索,在此基础上开展了L-Arg发酵液直接进行AAKG的结晶实验,获得了纯度高、品质稳定的结晶。研究认为,AAKG结晶操作的关键控制参数是溶液的pH,在pH 3~4较易形成MAAKG晶体,而L-Arg与α-KG适宜的投料比是1∶1;本研究还从减少能耗和提高工业经济性角度,提出适宜的起晶浓度为1.5 mol/L,适宜的结晶温度是10℃左右,而缓慢的降温操作有利于提高晶体纯度。以L-Arg发酵液为原料进行AAKG结晶,为提高晶体纯度和结晶效率,1是
[1] 李颖.α-酮戊二酸组合物的药物制剂及其制备方法和应用[P].中国专利:200710063477.4,2007-02-02.
[2] 温守明.一种α-酮戊二酸药物制剂及其制备方法和应用[P].中国专利:200710063478.9,2007-02-02.
[3] Campbell B,Roberts M,Kerksick C,et al.Pharmacokinetics,safety,and effects on exercise performance of L-arginine alpha-ketoglutarate in trained adult men[J].Nutrition,2006,22(9):872-881.
[4] 温守明,喻蓉.一种α-酮戊二酸-精氨酸盐制剂的制备方法及在治疗肝病中的应用[P].中国专利:200710063479.3,2007-08-08.
[5] 张义萍,张伟国,郝刚.离子交换法从发酵液中提取L-精氨酸[J]. 食品与发酵工业,2005,31(9):63-65.
