pp GalNacT-10基因真核表达载体的构建及表达*
2012-12-07刘振华冯菁华李晓云孙其喆郑文岭马文丽
高 媛,刘振华,冯菁华,李晓云,孙其喆,张 宝,郑文岭,马文丽#
1)南方医科大学基因工程研究所广州 510515 2)苏州卫生职业技术学院苏州 215009 3)华南基因组研究中心广州 510800 #通讯作者,女,1964年4月生,博士,教授,研究方向:基因诊断与基因治疗,E-mail:wenli668@gmail.com
pp GalNacT-10基因真核表达载体的构建及表达*
高 媛1),刘振华2),冯菁华1),李晓云1),孙其喆1),张 宝1),郑文岭1,3),马文丽1)#
1)南方医科大学基因工程研究所广州 510515 2)苏州卫生职业技术学院苏州 215009 3)华南基因组研究中心广州 510800 #通讯作者,女,1964年4月生,博士,教授,研究方向:基因诊断与基因治疗,E-mail:wenli668@gmail.com
pp GalNacT-10;真核表达载体;293T细胞
目的:构建pp GalNacT-10基因真核表达载体。方法:采用PCR方法合成含有酶切位点(XbaⅠ、EcoRⅠ)的pp GalNacT-10 cDNA。构建pMD19T-GalNacT-10-ORF和pMD19T-GalNacT-10-antisense,鉴定及测序证实cDNA片段大小和序列。双酶切目的载体pcDNA3.1后,与GalNacT-10-ORF和GalNacT-10-antisense片段进行连接,构建正义和反义真核表达载体pcDNA3.1-GalNacT-10-ORF和pcDNA3.1-GalNacT-10-antisense,将其分别转染293T细胞,Western blot法检测pp GalNacT-10蛋白的表达。结果:pcDNA3.1-GalNacT-10-ORF和pcDNA3.1-GalNacT-10-antisense包含大小、序列正确的pp GalNacT-10片段;pp GalNacT-10蛋白在转染pcDNA3.1-GalNacT-10-ORF的293T细胞中高表达,在转染pcDNA3.1-GalNacT-10-antisense的293T细胞中表达降低。结论:成功构建了pp GalNacT-10基因正义和反义真核表达载体。
根据糖链和肽链连接方式的不同,蛋白质的糖基化可分为N-糖基化和O-糖基化[1],目前关于蛋白N-糖基化研究较多,而蛋白O-糖基化研究较少。多肽N-乙酰氨基半乳糖转移酶(polypeptide:N-acetylgalactosaminyltransferases,pp GalNAcTs)是O-糖链合
*广东省自然科学基金资助项目 S2011040003098成的起始糖基转移酶,催化UDP-GalNAc上的Gal-NAc基团转移至蛋白质多肽链上特定序列中的Thr或Ser的羟基上,从而合成 GalNAcα-O-Ser/Thr多肽,而后在其他糖基转移酶的作用下肽链逐渐延伸[2]。酶的缺乏或者活性降低等可以导致多种疾病[3],研究[4-7]发现,pp GalNAcTs家族与肿瘤的发生、发展密切相关。多肽N-乙酰氨基半乳糖转移酶10(pp GalNAcT-10)是多肽N-乙酰氨基半乳糖转移酶家族成员之一,它对肿瘤的影响目前暂无相关报道。作者构建pp GalNAcT-10正义真核表达载体pcDNA3.1-GalNacT-10-ORF和反义真核表达载体pcDNA3.1-GalNacT-10-antisense,分别转染293T细胞,并进行表达,为进一步在分子水平研究pp GalNAcT-10对肿瘤的影响提供物质基础和实验工具。
1 材料与方法
1.1 材料 人肾上皮细胞系(293T)、大肠杆菌菌株DH5α、pcDNA 3.1(-)由南方医科大学基因工程研究所保存;Lipofectamine 2000、Trizol购自 Invitrogen公司;反转录酶、Taq酶、DNA Marker、蛋白Marker、T4 DNA连接酶、限制性内切酶 XbaⅠ和EcoRⅠ购自TaKaRa公司;胎牛血清(杭州四季青生物工程材料有限公司),DMEM高糖培养基(Hy-Clone公司),pp GalNAcT-10一抗(Abcam公司)、二抗(福州迈新生物技术开发有限公司),DNA回收试剂盒(上海晶美生物工程公司),小量质粒提取试剂盒(南京凯基生物科技发展有限公司),双抗、二甲基亚砜、胰蛋白酶(Sigma公司)。
1.2 293T细胞总RNA提取及逆转录 用含体积分数10%胎牛血清和青链霉素的DMEM高糖培养基在37℃、体积分数5%CO2和饱和湿度条件下培养293T细胞,当细胞融合度达到90%时传代。用Trizol试剂提取细胞总 RNA,测 RNA浓度、纯度。以总RNA为模板,使用Promega公司的试剂盒进行RT反应,得到ppGalNAcT-10基因的cDNA。
1.3 PCR扩增、纯化 设计pp GalNAcT-10正义载体引物,上游 GLANT-ORF-F(XbaⅠ):5’-AGTCTAGAATGAGGCGGAAGGAGAAGCGGCTC-3’,下游GLANT-ORF-R(EcoRⅠ):5’-AGGAATTCT CAGTTCCTATTGAATTTTTCCAA-3’;pp GalNAcT-10反义载体引物,上游GLANT-antisense-F(XbaⅠ):5’-AGTCTAGATCAGTTCCTATTGAATTTTTCCAA-3’,下游GLANT-antisense-R(EcoRⅠ):5’-AGGAATTCAT GAGGCGGAAGGAGAAGCGGCTC-3’。引物由 Invitrogen公司合成。PCR。扩增体系为20 mL。扩增条件:94℃5 min;94℃ 30 s,58℃ 30 s,72℃ 1 min,38个循环;72℃7 min延伸。按TIANgen琼脂糖凝胶DNA回收试剂盒说明书进行凝胶回收操作。
1.4 目的基因与T载体连接 用限制性内切酶XbaⅠ和EcoRⅠ消化PCR产物及pMD19T载体,将目的基因片段DNA、载体pMD19-T simple、SolutionⅠ加入到灭菌后的200 mL PCR管中,16℃过夜连接12 h。转化到DH5α感受态细菌,挑取单克隆,PCR及酶切筛选和鉴定重组质粒。阳性克隆抽提质粒后由Invitrogen公司完成测序,并用DNA Star软件进行核苷酸序列分析。
1.5 克隆载体质粒DNA和表达载体pcDNA 3.1 (-)连接 用限制性内切酶XbaⅠ和EcoRⅠ消化pMD19T重组载体及载体pcDNA 3.1(-),37℃保温3 h进行酶切,加10×Loading Buffer终止酶切反应。T4连接酶4℃连接过夜,连接产物转化大肠杆菌DH5α,Amp抗性筛选重组子,37℃度摇菌14 h,提取质粒进行酶切及测序验证。
1.6 转染293T细胞 将293T细胞接种于6孔板,生长至80%~90%融合时,分别采用pcDNA3.1-Gal-NacT-10-ORF和 pcDNA3.1-GalNacT-10-antisense和Lipofectamine 2000按照试剂盒说明进行转染,同时以转染pcDNA3.1(-)质粒和未转染细胞株为对照。
1.7 瞬时转染的检测 将上述细胞培养48 h,裂解,收取蛋白。以兔抗人抗体为一抗,鼠抗兔IgG为二抗,用Western blot法检测pp GalNAcT-10蛋白的瞬时表达。
2 结果
2.1 pp GalNAcT-10 cDNA的RT-PCR克隆 见图1。RT-PCR反应产物大小约1 800 bp,与预期大小一致。
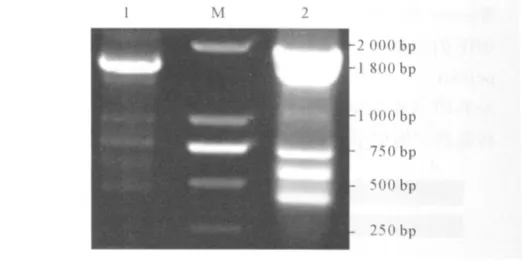
图1 pp GalNAcT-10RT-PCR产物的琼脂糖凝胶电泳鉴定
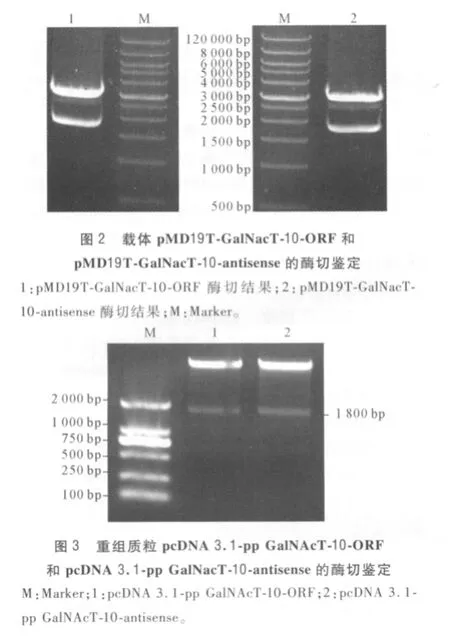
2.2 pp GalNAcT-10基因与pMD19T重组载体的构建 用XbaⅠ和EcoRⅠ酶切pMD19T-GalNacT-10-ORF 和 pMD19T-GalNacT-10-antisense,得 到1 800 bp的片段(图2),与pp GalNAcT-10 cDNA的大小一致。测序结果与GenBank公布的序列一致。
2.3 重组pp GalNAcT-10基因真核表达载体的鉴定 见图3。用双酶切鉴定和测序结果显示重组载体所含pp GalNAcT-10cDNA碱基序列与GenBank上完全一致。
2.4 目的蛋白在293T细胞中的表达 见图4。Western blot检测发现转染pcDNA 3.1-GalNAcT-10-ORF的细胞中pp GalNAcT-10蛋白表达增强,转染pcDNA 3.1-GalNAcT-10-antisense的细胞中pp GalNAcT-10蛋白表达降低,转染pcDNA 3.1空载体与未转染的细胞中pp GalNAcT-10蛋白表达相似。
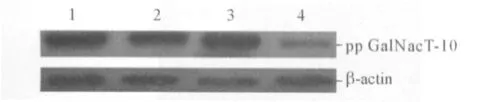
图4 目的蛋白pp GalNAcT-10在293T细胞中的表达
3 讨论
肿瘤细胞同胚胎发育中的正常细胞一样,也经历被活化和快速生长、黏附于其他各种细胞或细胞基质并侵入组织的过程。脊椎动物的胚胎发育和细胞激活伴有典型的细胞糖基化类型的改变,因此糖基化改变也是细胞恶变和肿瘤发展的普遍特征。其中如T抗原等糖抗原在脊椎动物胚胎细胞和肿瘤细胞中表现高表达,常作为肿瘤相关性糖抗原,用于肿瘤发展预后的检测[8-9]。T抗原的O型糖基化起始于pp GalNAcTs家族,在乳癌、结肠癌、胃癌、肺癌等多种癌变中已有pp GalNAcTs家族中一些成员表达异常的报道[4-7]。在偏钒酸钠诱导HL-60细胞凋亡的过程中,发现ppGalNAcT-2的活性以及表达量均发生改变;随后的试验证明ppGalNacT-2表达的变化影响偏钒酸钠诱导的HL-60细胞凋亡[10]。
pp GalNAcT-10是多肽N-乙酰氨基半乳糖转移酶家族成员之一,其对肿瘤的影响目前暂无相关报道。因此,分析该蛋白在细胞中的作用,有利于找寻与肿瘤发生、发展及其恶性特征相关的新基因。作者成功构建了pp GalNacT-10基因正义和反义真核表达载体,为进一步探其对肿瘤的影响奠定了基础。
[1]谢琴芳,赵晓东,张琴,等.人偏肺病毒融合蛋白N-糖基化位点的预测及不同N-糖基化修饰突变体的构建[J].实用儿科临床杂志,2009,24(22):1714
[2]刘春亮,吴士良.黏蛋白型O-聚糖在人类肿瘤中的结构异常及生物学功能[J].生物化学与生物物理进展,2010,37(5):475
[3]唐湘凤,栾佐.造血干细胞移植治疗黏多糖病研究进展[J].实用儿科临床杂志,2011,26(3):162
[4]Berois N,Mazal D,Ubillos L,et al.UDP-N-acetyl-D-galactosamine:polypeptide N-acetylgalactosaminyltransferase-6 as a new immunohistochemical breast cancer marker[J].J Histochem Cytochem,2006,54(3):317
[5]Gomes J,Marcos NT,Berois N,et al.Expression of UDP-N-acetyl-D-galactosamine:polypeptide N-acetylgalactosaminyltransferase-6 in gastric mucosa,intestinal metaplasia,and gastric carcinoma[J].J Histochem Cytochem,2009,57 (1):79
[6]Guo JM,Chen HL,Wang GM,et al.Expression of UDPGalNAc:polypeptide N-acetylgalactosaminyltransferase-12 in gastric and colonic cancer cell lines and in human colorectal cancer[J].Oncology,2004,67(3/4):271
[7]Wu C,Guo X,Wang W,et al.N-acetylgalactosaminyltransferase-14 as a potential biomarker for breast cancer by immunohistochemistry[J].BMC Cancer,2010,10:123
[8]吴士良.黏蛋白型O-聚糖:结构、功能及与肿瘤的相关性[J].生命科学,2011,23(6):563
[9]徐克群,张维,关乃富,等.T抗原在胃癌组织中的表达及预后价值[J].临床荟萃,2008,23(4):232
[10]Gao Y,Tu YB,Guo Y,et al.PpGalNacT2 Participating in vanadium-induced HL-60 cell differentiation[J].Mol Biol Rep,2011,38(3):1483
Construction and expression of eukaryotic expression vector for pp GalN-acT-10 gene
GAO Yuan1),LIU Zhenhua2),FENG Jinghua1),LI Xiaoyun1),SUN Qizhe1),ZHANG Bao1),ZHENG Wenling1,3),MA Wenli1)1)Institute of Genetic Engineering,Southern Medical University,Guangzhou 510515 2)Suzhou Health College,Suzhou 215009 3)South China Genome Research Center,Guangzhou 510800
pp GalNacT-10;eukaryotic expression vector;293T cell
Aim:To construct eukaryotic expression vector of pp GalNacT-10 gene.Methods:PCR synthesis full length of pp GalNacT-10 cDNA containing restriction sites(XbaⅠ,EcoRⅠ).pMD19T-GalNacT-10-ORF and pMD19T-GalNacT-10-antisense were build,and the sequence and size of pp GalNacT-10 cDNA fragment were confimed to be correct.After objective vector pcDNA3.1 was digested,it was separately connected with GalNacT-10-ORF and GalNacT-10-antisense.Sense and antisense eukaryotic expression vectors pcDNA3.1-GalNacT-10-ORF and pcDNA3.1-GalNacT-10-antisense were separately transfected into 293T cells.Western blot was used to identify the expressed product.Results:The results of digestion confirmed the right length of inserted DNA,which was the same as the pp GalNacT-10 cDNA,and pp GalNacT-10 protein was highly expressed in 293T cells which were transfected with pcDNA3.1-GalNacT-10-ORF,and low expressed in 293T cells which were transfected with pcDNA3.1-GalNacT-10-antisense.Conclusion:pcDNA3.1-GalNacT-10-ORF and pcDNA3.1-GalNacT-10-antisense have been successfully constructed.
R34
10.3969/j.issn.1671-6825.2012.06.003
(2012-02-07收稿 责任编辑赵秋民)
