镍–铜–磷化学镀层在硫酸溶液中的腐蚀行为
2012-11-30梁平王运玲史艳华
梁平,王运玲,史艳华
(辽宁石油化工大学机械工程学院,辽宁 抚顺 113001)
镍–铜–磷化学镀层在硫酸溶液中的腐蚀行为
梁平*,王运玲,史艳华
(辽宁石油化工大学机械工程学院,辽宁 抚顺 113001)
为了提高Ni–P化学镀层的抗腐蚀性能,在由NiSO4·6H2O 25 g/L、NaH2PO2·H2O 25 g/L、C6H5O7Na3·2H2O 12 g/L和CH3COONa 20 g/L组成的Ni–P镀液中加入不同质量浓度的无水硫酸铜,制备了Ni–Cu–P镀层。通过浸泡、动电位极化和电化学阻抗谱(EIS)考察了Ni–Cu–P和Ni–P镀层在5%(质量分数)H2SO4溶液中的耐蚀性,采用扫描电镜(SEM)观察了镀层的表面形貌。结果表明,加入CuSO4后得到的Ni–Cu–P镀层比Ni–P镀层结晶更细小、致密,在硫酸溶液中表现出更好的抗腐蚀性能。当镀液中硫酸铜质量浓度为0.50 g/L时,得到的Ni–Cu–P镀层晶粒最小、致密性最好,其膜电阻和电荷转移电阻达到最大,分别是Ni–P镀层的4倍和32倍。
镍–铜–磷合金;化学镀;硫酸铜;硫酸;耐蚀性
1 前言
化学镀镍磷(Ni–P)合金层由于具有良好的耐蚀性和耐磨性,在很多领域都得到了广泛应用[1-3]。但随着世界各国工业化的不断发展,很多设备的使用环境或使用条件越来越苛刻,Ni–P合金镀层很难满足现场使用要求,这就需要进一步提高该合金层的抗腐蚀性能。三元以及多元合金镀层是改善Ni–P镀层性能的有效方法之一[4-5]。
在成本增加不多的前提下,向Ni–P镀液中加入适量的CuSO4,可制备出Ni–Cu–P合金镀层[5]。目前,有关Ni–Cu–P镀层的电性能和磁性能的研究较多,且Ni–Cu–P镀层主要作为电磁屏蔽等表面功能层使用[6],有关该镀层在酸性溶液中腐蚀性能的研究相对较少,而这对于进一步扩大化学镀层在石油、化工等诸多领域中的应用又非常重要。本文主要通过电化学测试技术考察Ni–Cu–P和Ni–P化学镀层在5% H2SO4溶液中的腐蚀行为,分析其抗腐蚀原因,希望能为 Ni–Cu–P镀层的进一步应用提供参考依据。
2 实验
2. 1 Ni–Cu–P镀层的制备
2. 1. 1 工艺流程
以10 mm × 10 mm × 4 mm的20R钢为基体。化学镀Ni–Cu–P工艺流程为:打磨─酒精擦拭─碱洗除油(NaOH 25 g/L,Na2CO335 g/L,Na3PO435 g/L,温度60 °C,时间10 min)─水洗─10%(体积分数)H2SO4活化─水洗─化学镀─水洗─吹干─检测。
2. 1. 2 镀液配方与工艺
Ni–P镀液组成与工艺条件为:


向Ni–P镀液中分别加入0.25、0.50和1.00 g/L的无水CuSO4,制得不同Ni–Cu–P镀层。
2. 2 性能检测
2. 2. 1 耐蚀性
(1) 浸泡腐蚀:将Ni–P和Ni–Cu–P合金镀层置于5%(体积分数)H2SO4溶液中浸泡72 h,按式(1)计算其腐蚀速率:

式中,v为镀层的腐蚀速率[g/(m2·h)],Δm为腐蚀前后镀层的质量差(g),A为镀层腐蚀试样的表面积(m2),t为腐蚀时间(h)。
(2) 电化学腐蚀:采用美国 Princeton Applied Research Parstat 2273电化学工作站测定镀层的动电位极化曲线和交流阻抗谱。Ni–P和Ni–Cu–P镀层为工作电极(均为10 mm × 10 mm的正方形试样),铂片为辅助电极,饱和甘汞电极(SCE)为参比电极。将Ni–P和Ni–Cu–P合金镀层分别置于5%(体积分数)H2SO4溶液中浸泡1 h,待开路电位基本稳定后测定动电位极化曲线,平行试样各为 3个。动电位极化曲线的扫描速率为1.0 mV/s,腐蚀介质温度为25 °C。交流阻抗测试在自腐蚀电位下进行,测试频率为100 kHz ~ 50 mHz,扰动电位为10 mV。
2. 2. 2 表面形貌
采用捷克TESCAN扫描电镜观察镀层的表面形貌。
3 结果与讨论
3. 1 腐蚀速率
镀层试样浸泡72 h后的试验结果表明,Ni–P镀层的腐蚀速率约为4.76 g/(m2·h),镀液中CuSO4质量浓度分别为0.25、0.50和1.0 g/L时,对应的Ni–Cu–P镀层的腐蚀速率分别为 2.56、1.25和 1.72 g/(m2·h)。Ni–P镀层的腐蚀速率最高,Ni–Cu–P镀层的腐蚀速率较Ni–P镀层稍低。当镀液中CuSO4质量浓度为0.5 g/L时,所得Ni–Cu–P镀层的腐蚀速率最低,镀层的耐均匀腐蚀性最好。另外,由于浸泡时间较短,Ni–P和 Ni–Cu–P镀层都没有发生点蚀。
3. 2 极化曲线测量
图1为Ni–P及Ni–Cu–P合金镀层在5% H2SO4溶液中的动电位极化曲线。从中可以看出,这些镀层的阳极极化曲线都存在着明显的钝化区,且钝化区间范围很宽,表明Ni–P及Ni–Cu–P镀层在5% H2SO4溶液中都表现出良好的耐蚀性。
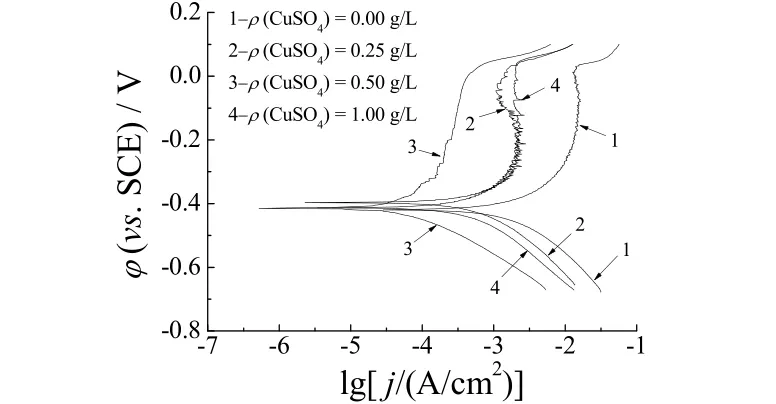
图1 Ni–Cu–P及Ni–P镀层在5% H2SO4溶液中的动电位极化曲线Figure 1 Potentiodynamic polarization curves for Ni–Cu–P and Ni–P deposits in 5% H2SO4 solution
表1为动电位极化曲线的拟合结果。从中可以看出,3种Ni–Cu–P合金镀层的自腐蚀电位φcorr较Ni–P镀层的偏正一些,但差别不是很大。另外,Ni–P镀层的自腐蚀电流密度 jcorr最高,而 Ni–Cu–P镀层的 jcorr明显降低。当镀液中CuSO4质量浓度为0.5 g/L时,所得Ni–Cu–P镀层的jcorr最小。根据法拉第定律,jcorr与金属的腐蚀速度成正比,金属的腐蚀速度越低,jcorr也越小。因此,在硫酸介质中,Ni–Cu–P镀层较Ni–P镀层具有更强的抗均匀腐蚀性能。此外,从表 1还可以看出,Ni–Cu–P镀层的点蚀电位φpit也较 Ni–P镀层有所增大,表明Ni–Cu–P合金镀层的抗点蚀性能更好。3种Ni–Cu–P镀层相比,Ni–P镀液中加入0.5 g/L CuSO4时所得Ni–Cu–P镀层的jcorr最小,φpit最大,表明其抗均匀腐蚀和抗点蚀的性能最为理想。

表1 Ni–Cu–P及Ni–P镀层在5% H2SO4溶液中的极化曲线拟合结果Table 1 Fitting results of polarization curves for Ni–Cu–P and Ni–P deposits in 5% H2SO4 solution
3. 3 交流阻抗测试
图2为Ni–P和Ni–Cu–P镀层在5% H2SO4溶液中的Nyquist曲线。可以看出,Ni–P和Ni–Cu–P镀层都表现为容抗弧,且3种Ni–Cu–P镀层的Nyquist曲线的容抗弧直径都较Ni–P镀层的大,表明前者较后者具有更好的抗蚀性。当镀液中CuSO4质量浓度为0.5 g/L时,所得镀层的Nyquist曲线容抗弧的直径最大,表明此镀层的耐蚀性最好。
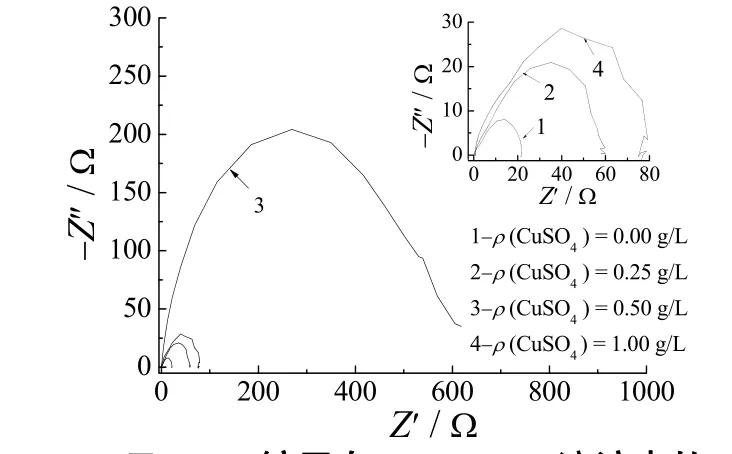
图2 Ni–Cu–P及Ni–P镀层在5% H2SO4溶液中的Nyquist图Figure 2 Nyquist plots of Ni–Cu–P and Ni–P deposits in 5wt% H2SO4 solution
采用图3的等效电路对图2的Nyquist曲线进行数值拟合。其中,Rs表示溶液电阻,Q表示镀层和溶液间形成的双电层电容,Rct表示电荷转移电阻,Cf表示镀层的膜电容,Rf表示镀层的膜电阻。

图3 等效电路图Figure 3 Equivalent circuit diagram
膜电阻和电荷转移电阻是反映镀层耐蚀性的重要参数。两者的数值越大,镀层的耐蚀性越好。图 4为Ni–Cu–P及Ni–P镀层的膜电阻Rf和电荷转移电阻Rct随镀液中 CuSO4质量浓度的变化情况。可以看出,Ni–Cu–P镀层的膜电阻Rf是Ni–P镀层的1 ~ 4倍,而其电荷转移电阻Rct是Ni–P镀层的3 ~ 32倍。当镀液中硫酸铜质量浓度为0.50 g/L时,Ni–Cu–P镀层的膜电阻Rf和电荷转移电阻Rct都达到最大值,这与极化曲线所反映的规律一致。

图4 Ni–Cu–P及Ni–P镀层的膜电阻和电荷转移电阻Figure 4 Film resistances and charge transfer resistances of Ni–Cu–P and Ni–P deposits
3. 4 表面形貌观察
镀液中CuSO4含量不同时,制备的Ni–Cu–P镀层的表面形貌如图 5所示。可以看出,当镀液中加入CuSO4以后,Ni–Cu–P镀层的胞状物比Ni–P镀层更为细小,胞状物之间的结合更紧密,尤其是当镀液中硫酸铜质量浓度为0.50 g/L时,Ni–Cu–P镀层表面胞状物最为细小,表面最为平整,致密性最好。这主要是因为镀液中加入 CuSO4以后,反应过程中会形成 Cu的微小颗粒[7],有利于增加镀层的形核位置,使Ni–Cu–P镀层晶粒得以细化,镀层质量得到改善。

图5 Ni–Cu–P和Ni–P镀层的表面形貌照片Figure 5 Surface morphology photos of Ni–Cu–P and Ni–P deposits
浸泡实验以及极化曲线、交流阻抗曲线谱等电化学测试结果均表明,Ni–Cu–P镀层具有比Ni–P镀层更好的抗均匀腐蚀和抗点蚀性能,这主要是因为:Ni–Cu–P和Ni–P镀层在硫酸溶液中都能发生钝化,形成具有保护作用的NiO、Ni(OH)2或镍的磷酸盐等钝化膜[8],由于Ni–Cu–P的晶粒比Ni–P镀层更加细小,表面更加致密平整,因此Ni–Cu–P镀层更容易发生钝化并形成膜电阻更大的钝化膜,使其在发生电化学腐蚀时,电荷传递更加困难,电极反应更慢,因此表现出更为优越的抗腐蚀性。
4 结论
向Ni–P镀液中分别加入0.25、0.50和1.00 g/L的CuSO4,所制备的Ni–Cu–P镀层在5% H2SO4溶液中均表现出比 Ni–P镀层更好的抗均匀腐蚀和抗点蚀性能。当镀液中CuSO4质量浓度为0.5 g/L时,镀层的抗腐蚀性能最好,膜电阻和电荷转移电阻约是Ni–P镀层的4倍和32倍。这主要是因为Ni–Cu–P镀层的胞状结构更加细小、表面更加平整致密,促进了钝化的发生并形成良好的钝化膜,增大了电化学腐蚀时的电荷转移阻力,提高了抗腐蚀性。
[1] PING Z X, HE Y D, GU C D, et al. Electroless plating of Ni–P coatings on carbon steel in a stirred bed of glass balls [J]. Journal of Applied Electrochemistry, 2009, 39 (6): 879-885.
[2] MAKAROV V F, PRUSOV YU V, LEBEDEVA I O. Electroless deposition of nickel coatings with high phosphorus content [J]. Russian Journal of Applied Chemistry, 2005, 78 (1): 82-84.
[3] ANKITA S, SINGH A K. Corrosion and wear resistance study of Ni–P and Ni–P–PTFE nanocomposite coatings [J]. Central European Journal of Engineering, 2011, 1 (3): 234-243.
[4] YOUNAN M M, ALY I H M, NAGEEB M T. Effect of heat treatment on electroless ternary nickel–cobalt–phosphorus alloy [J]. Journal of Applied Electrochemistry, 2002, 32 (4): 439-446.
[5] GUO R H, JIANG S Q, YUEN C W M, et al. Effect of copper content on the properties of Ni–Cu–P plated polyester fabric [J]. Journal of Applied Electrochemistry, 2009, 39 (6): 907-912.
[6] CHEN C J, LIN K L. The reactions between electroless Ni–Cu–P deposit and 63Sn–37Pb flip chip solder bumps during reflow [J]. Journal of Electronic Materials, 2000, 29 (8): 1007-1014.
[7] GEORGIEVA J, ARMYANOV S. Electroless deposition and some properties of Ni–Cu–P and Ni–Sn–P coatings [J]. Journal of Solid State Electrochemistry, 2007, 11 (7): 869-876.
[8] ELSENER B, CROBU M, SCORCIAPINO M A, et al. Electroless deposited Ni–P alloys: corrosion resistance mechanism [J]. Journal of Applied Electrochemistry, 2008, 38 (7): 1053-1060.
Corrosion behavior of electroless nickel–copper–phosphorus deposit in sulfuric acid solution //
LIANG Ping*, WANG Yun-ling, SHI Yan-hua
s:To improve the corrosion resistance of electroless Ni–P coating, Ni–Cu–P coatings were prepared by adding different mass concentrations of anhydrous copper sulfate to a bath comprising NiSO4·6H2O 25 g/L, NaH2PO2·H2O 25 g/L, C6H5O7Na3·2H2O 12 g/L, and CH3COONa 20 g/L. The corrosion resistance of Ni–Cu–P and Ni–P coatings in 5wt% H2SO4solution was studied by immersion, potentiodynamic polarization, and electrochemical impedance spectroscopy (EIS). The surface morphologies of coatings were observed by SEM. The results showed that the Ni–Cu–P coatings have smaller crystal grains and a more compact structure than the Ni–P coating, and present better corrosion resistance in H2SO4solution. The Ni–Cu–P coating prepared with 0.50 g/L Cu2SO4in bath features the smallest grain size, the best compactness, and the largest film resistance and charge transfer resistance, which are 4 times and 32 times that of the Ni–P coating, respectively.
nickel–copper–phosphorus alloy; electroless plating; copper sulfate; sulfuric acid; corrosion resistance
School of Mechanical Engineering, Liaoning Shihua University, Fushun 113001, China
TG178; TQ153.2
A
1004 – 227X (2012) 10 – 0031 – 04
2012–02–04
2012–04–27
辽宁省教育厅2012年科学研究一般项目(L2012127);辽宁石油化工大学2011年度教育教学改革研究项目(J2011068)。
梁平(1974–),男,辽宁沈阳人,博士,副教授,主要研究方向为材料的腐蚀与防护。
作者联系方式:(E-mail) liangping770101@163.com。
[ 编辑:韦凤仙 ]
