改性碳纳米管常温下吸附分离低浓度CO2
2012-11-30叶青张瑜李茗施耀,*
叶 青 张 瑜 李 茗 施 耀,*
(1浙江大学工学部化学工程与生物工程系工业生态与环境研究所,杭州310028;2浙江树人大学,杭州310015)
改性碳纳米管常温下吸附分离低浓度CO2
叶 青1张 瑜1李 茗2施 耀1,*
(1浙江大学工学部化学工程与生物工程系工业生态与环境研究所,杭州310028;2浙江树人大学,杭州310015)
采用浸渍法将四乙烯五胺(TEPA)和三乙烯四胺(TETA)负载至碳纳米管(CNTs)上,得到一种固态胺吸附剂CNTs-TEPA和CNTs-TETA,用以吸附低浓度下的CO2.利用扫描电镜(SEM)、透射电镜(TEM)、傅里叶红外(FTIR)光谱、N2物理吸附脱附、元素分析和热重分析(TGA)等方法表征样品.结果表明:CNTs-TEPA和CNTs-TETA形态并未发生变化,仍保留CNTs规整有序的孔道结构,但样品的比表面积和孔容都显著减小.在常温条件下,CNTs-TEPA和CNTs-TETA的CO2吸附量与CNTs相比有显著提高,同时,在胺浸渍质量相同的情况下,改性后的CNTs-TEPA效果优于CNTs-TETA.温度从20°C升至30°C,CNTs-TEPA和CNTs-TETA的CO2吸附量分别从126.7、101.2 mg·g-1升至139.3、110.4 mg·g-1.CNTs的吸附量随着温度的增加变化不明显.最后,采用Suyadal和Yasyerli两种模型对CO2的动态吸附穿透曲线进行拟合,结果说明Yasyerli模型对CNTs、CNTs-TEPA和CNTs-TETA的CO2吸附过程的拟合程度更高.
碳纳米管;CO2吸附;三乙烯四胺;四乙烯五胺;失活模型
1 引言
随着温室效应的加剧,以CO2为主的温室气体排放控制的研究已经引起了越来越广泛的关注.1二氧化碳不仅对气候和全球生态系统有影响,在密闭空间中,CO2浓度超过一定限度,就会对人体造成不利影响.2因此,在载人深潜器、航天器等密闭空间内低浓度CO2的清除十分必要.
目前,用于控制CO2排放的技术主要有吸收法、吸附法和膜分离法等.3-7液态胺溶液吸收CO2是目前工业化比较成熟的技术.该技术应用较早,且吸收效果好,但存在腐蚀设备、易氧化降解的缺点.8膜分离法更适用于去除相对高浓度的CO2,如天然气中CO2的去除和燃烧前CO2的捕捉.9与之相比,吸附法以其低能耗和相对简单的工艺等优点成为目前非常热门的CO2分离技术.开发新型高效的CO2吸附剂对吸附技术在CO2分离中的应用非常重要.目前,吸附剂改性的研究较多集中于对多孔材料进行氨基功能化,从而制备固态胺吸附剂.这些多孔材料载体主要有介孔二氧化硅、沸石分子筛、聚酯类多孔材料、活性炭和碳纳米管等.4,10-19Zelenak等16考察了SBA-12改性后对CO2(10%)的吸附量为45.76 mg·g-1.Huang等20发现二氧化硅凝胶和MCM-48通过氨基改性后,常温下对CO2的吸附量分别为24.99和50.16 mg·g-1.史晶金等4采用浸渍法将四乙烯五胺负载到介孔分子筛SBA-16的孔道内,用于10% CO2的吸附,在60°C下CO2饱和吸附量可达42.81 mg·g-1.前期文献的研究主要集中在改性介孔材料对烟道气环境CO2(10%,60-80°C)富集分离的考察上.
开发高效固态胺吸附剂,首先是要考虑吸附剂的吸附容量.碳纳米管(CNTs)具有典型层状中空结构特征,层与层之间距离固定,利于氨基负载.21同时与其他载体相比,CNTs还具有孔径大、水热稳定性良好、导电性好和重量轻等一系列优点.22-24Su等17考察了氨基功能化后的CNTs在常温时对CO2(15%和50%)的吸附性能,得出改性CNTs吸附剂是一种优良的常温CO2吸附剂.目前CNTs针对低CO2浓度下的CO2吸附性能和动态吸附过程鲜有报道.
本文以四乙烯五胺(TEPA)和三乙烯四胺(TETA)为氨基改性剂,多壁碳纳米管为载体,采用浸渍法制备固体胺CO2吸附剂.在固定床吸附柱实验装置上研究常温常压下制备的固体胺吸附剂对低浓度CO2(2%)的吸附性能,考察温度对其吸附性能的影响,运用两种失活模型模拟吸附穿透曲线,比较其适用性,并进行反应动力学分析.
2 实验部分
2.1 吸附剂的制备
CNTs(M8,孔容0.4887 cm3·g-1,孔径5-20 nm,中国科学院成都有机化学有限公司)的氨基功能化采用浸渍法.主要步骤如下:将0.5 g TEPA(AR,天津市博迪化工有限公司)或TETA(AR,国药集团化学试剂有限公司)溶于50 g乙醇(AR,杭州化学试剂有限公司)中,搅拌30 min后加入1 g CNTs.继续搅拌6 h后在80°C下蒸发处理去除溶剂乙醇.最后将所得样品置于通风干燥箱中,100°C下干燥1 h.冷却后所得样品即为氨基功能化CNTs材料,标记为CNTs-TEPA或CNTs-TETA.
2.2 动态吸附实验
CO2动态吸附实验在固定吸附床中进行,实验装置见图1.实验用吸附柱为耐热石英玻璃U型管,直径10 mm,长度200 mm.称取0.5 g吸附剂填入吸附柱内,之后将吸附柱放入恒温水浴箱(DKS-24,杭州蓝天仪器有限公司)中.实验用气体由高纯N2(99.99%)和CO2(15.00%)通过质量流量计(D08-3F,北京七星华创电子股份有限公司)按比例混合配制成CO2体积浓度为2%,气体流量50 cm3·min-1.进出口CO2浓度由气相色谱仪(GC)(GC-9750T,浙江福立分析仪器有限公司)测定.
CO2动态吸附容量(q,mg·g-1)由公式(1)计算得到.

式中:m为吸附剂质量,g;Q为吸附柱总气体流量, cm3·min-1;C0为吸附柱进口CO2浓度,%(体积分数);C为吸附柱出口CO2浓度,%(体积分数);t为达到吸附平衡的时间,min;T0为273 K;T为气体温度, K;Vm为22.4 m3·mol-1;MCO2为44.00 g·mol-1.
2.3 样品表征

图1 吸附实验装置Fig.1 Schematic of adsorption system
采用场发射扫描电子显微镜(SEM)(SIRON, FEI公司,荷兰)观察样品的结构.样品经过喷金对其表面进行导电性处理.采用透射电子显微镜(TEM) (JEM-1200EX,日电公司,日本)对样品进行观察,工作电压120 kV.红外光谱分析实验采用傅里叶红外光谱仪(VECTOR22,BRUKER公司,德国)来进行样品组分的定性分析,用KBr压片法制样.样品的比表面积和孔结构采用N2物理吸附-脱附法测定.实验在全自动比表面积和孔隙分析仪上进行(Trstar II 3020,麦克仪器公司,美国).材料的N元素和C元素含量测定在元素分析仪(Flash EA1112,CE仪器公司,意大利)上测定,每个样品测定三次.采用热重分析仪(TGA)(SDT Q600,TA公司,美国)测定样品重量随温度的变化情况.TGA分析是在120 cm3·min-1氮气流的保护下,升温速率10°C·min-1,温度范围为室温至600°C,样品质量为10 mg左右.

图2 CNTs,CNTs-TEPA和CNTs-TETA的SEM图Fig.2 SEM images of CNTs,CNTs-TEPA,and CNTs-TETA(a,aʹ,aʹ)CNTs,(b,bʹ,bʹ)CNTs-TEPA,(c,cʹ,cʹ)CNTs-TETA
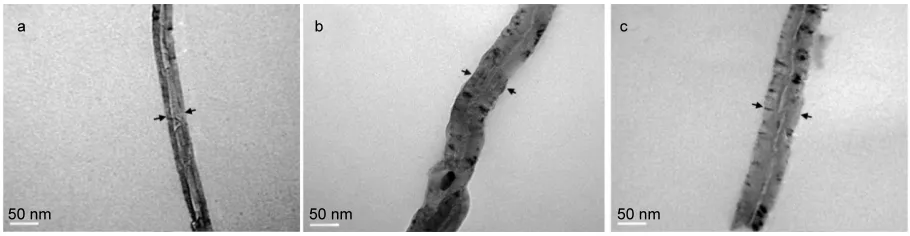
图3 CNTs,CNTs-TEPA和CNTs-TETA的TEM图Fig.3 TEM images of CNTs,CNTs-TEPA,and CNTs-TETA(a)CNTs,(b)CNTs-TEPA,(c)CNTs-TETA
3 实验结果与讨论
3.1 表征结果
图2为CNTs,CNTs-TEPA和CNTs-TETA的扫射电镜图.从SEM高倍数显微图像中可以清晰地看到碳纳米管的管状结构.经过TEPA和TETA浸渍后的样品形态并未发生变化,仍然保留了规整有序的孔道结构,表明CNTs的物理结构在浸渍改性后是稳定的.
图3为CNTs,CNTs-TEPA和CNTs-TETA的高分辨率透射电镜图.样品呈管道结构,整体形貌基本不变.但从图3b和图3c中可以看出,浸渍TEPA和TETA后,样品的管壁明显厚于原CNTs(图3a),这说明胺负载到CNTs表面上,导致CNTs上的氨基基团增加,提高了CO2吸附能力.
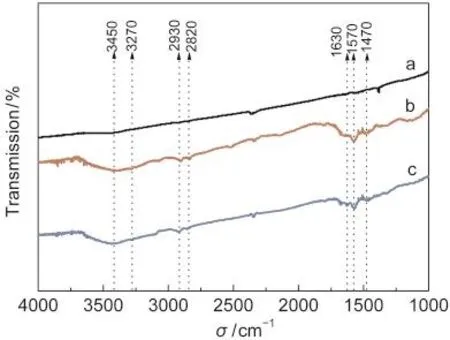
图4 CNTs,CNTs-TEPA和CNTs-TETA的FTIR光谱图Fig.4 FTIR spectra of CNTs,CNTs-TEPA,and CNTs-TETA(a)CNTs,(b)CNTs-TEPA,(c)CNTs-TETA
图4是CNTs,CNTs-TEPA和CNTs-TETA的红外光谱图.从图中可以看出,三者相应在3200-3600 cm-1范围均出现了不同程度的宽峰,主要由吸附剂与水分子结合形成的羟基形成,此外1630 cm-1为吸附水峰;CNTs-TEPA和CNTs-TETA上出现了新的吸收峰,其中在3270 cm-1处出现了N―H振动特征峰,在1570、1470 cm-1呈现了NH2和NH的N―H弯曲振动峰,进一步证明TEPA和TETA浸渍到了CNTs上.在2930和2820 cm-1处出现了C―H不对称和对称伸缩振动峰,相应在1300-1500 cm-1处出现变形振动峰.14,25,26
表1为CNTs修饰前后的物理化学性质.从表1可以看出,根据BET方程计算的CNTs载体的比表面积为87.02 m2·g-1,孔容为0.4851 cm3·g-1.经过修饰后,CNTs-TETA和CNTs-TEPA样品比表面积和孔容均明显减小.这是由于除部分TEPA对CNTs表面进行修饰,也有部分TEPA进入孔道,引起位阻效应并凝结成块,堵塞孔道.样品的元素分析见表1,所有的元素含量均转化为干燥、无灰条件下的数值.可见,CNTs样品在浸渍处理后的氮含量显著增加.
图5为CNTs,CNTs-TEPA和CNTs-TETA的TGA失重曲线.从图5中可知,样品从室温加热至110°C的过程中,样品CNTs、CNTs-TEPA和CNTs-TETA的质量损失分别为0.08%、8.69%和16.69%,这主要是样品在放置过程中表面吸附的水分蒸发引起的重量损失.在N2保护下,当温度从110°C升至600°C,这三种样品的质量损失分别为0.96%、28.55%和28.22%,后两者明显失重由负载的TEPA和TETA挥发分解引起.对结果进行分析计算, CNTs-TEPA和CNTs-TETA样品的氨基分解质量与浸渍的氨基质量相当,这也从另一方面证明TEPA和TETA基本完全负载到CNTs载体上.
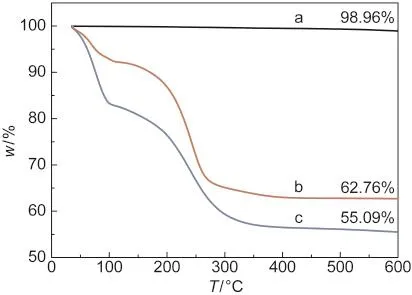
图5 CNTs,CNTs-TEPA和CNTs-TETA的TGA曲线Fig.5 TGAcurves of CNTs,CNTs-TEPAand CNTs-TETA(a)CNTs,(b)CNTs-TEPA,(c)CNTs-TETA
3.2 CO2吸附容量
图6为不同温度下CNTs,CNTs-TEPA和CNTs-TETA的CO2吸附量.由图可知,经过TEPA和TETA浸渍改性后,CNTs-TEPA和CNTs-TETA的CO2吸附量q在常温条件下与CNTs相比有了显著的提高.随着温度从20°C升至30°C,CNTs-TEPA和CNTs-TETA的CO2吸附量q分别从126.7、101.2 mg·g-1升至139.3、110.4 mg·g-1.由于温度升高,负载在CNTs的TEPA和TETA分子以及CO2分子活性都逐渐增强,从而有利于氨基活性组分与CO2的结合生成氨基甲酸酯,27,28使得吸附量q逐渐增加. CNTs的吸附量q随着温度的增加变化不明显,略有下降.未经过化学修饰的CNTs与CO2的吸附过程主要是物理吸附,结合力较弱,吸附热小.随着温度进一步升高,CO2容易脱附,降低吸附量q.同时,在胺浸渍质量相同的情况下,TEPA改性后的效果优于TETA.TEPA上的氨基活性基团多于TETA,导致CNTs-TEPA可以与更多CO2分子反应.
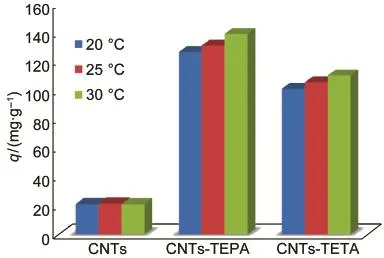
图6 不同温度下CNTs,CNTs-TEPA和CNTs-TETA的CO2吸附量(q)Fig.6 CO2adsorption capacities(q)for CNTs, CNTs-TEPA,and CNTs-TETAat various temperatures
表2比较了文献10,12,20,25,26中各种改性吸附剂在常温下对低浓度CO2的吸附性能,如胺改性后的SBA、MCM系列介孔分子筛、HSC+聚酯类多孔材料等,可见在低浓度下,经过TEPA和TETA改性后的CNTs是一种有良好发展前景的吸附剂.
3.3 吸附穿透曲线分析
CO2在吸附剂上的吸附是一种气固非催化反应过程.吸附剂的活性变化与吸附剂本身的性质变化有关.已有文献提出多种不同的模型来分析此类似气固反应的穿透曲线.29,30影响这些模型的主要因素有吸附剂孔和反应生成物层的扩散阻力,孔结构以及孔表面的变化等.失活模型正是考虑了这些因素的影响,因而能较好地模拟穿透实验数据.Suyadal等29在活性炭固定床上进行了三氯乙烯(TCE)的吸附实验,运用失活模型对反应的吸附曲线进行了模拟分析.Yasyerli等30利用失活模型很好地模拟了铜氧化物以及铜钒、铜钼混合物吸附硫化氢的吸附穿透曲线,并进行了反应动力学分析.这两种模型均能很好地模拟气固反应的吸附穿透曲线.失活模型的运用需要以下几个基本假设:(a)全床层等温;(b)忽略扩散项且只考虑Z向浓度变化;(c)保持拟稳态.基于以上假设,此两类失活模型由式(2)、(3)分别描述
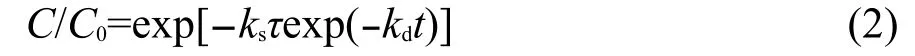
式中,ks为吸附反应速率常数(cm·min-1);τ为表面时间,即τ=S0/Q0,S0为吸附剂初始表面积(cm2);Q0为反应物初始体积流量(cm3·min-1);C0、C为进气口和出气口反应物浓度(mol·cm-3);kd为失活速率常数,min-1.

表2 文献中一些改性吸附剂的CO2吸附性能Table 2 CO2capacities of modified adsorbents from the literatures

式中,k0为起始吸附速率常数,cm3·min-1·g-1.
运用式(2)对CNTs,CNTs-TETA和CNTs-TEPA的吸附实验数据进行非线性回归分析,得出的参数值列于表3,拟合曲线比较如图7所示.吸附实验条件设定为:气体流量50 cm3·min-1,进气CO2浓度2.0%(体积),温度25°C.由表3中可以看出,吸附剂的无量纲吸附速率常数ksτ分别为3.12×102、3.74×103以及2.94×105.失活速率常数为1.267、0.508以及0.233.此外,模拟曲线与实验数据的相关系数r2均大于0.997,说明Suyadal失活模型能很好地模拟吸附CO2的吸附穿透曲线.
利用Yasyerli失活模型对吸附数据进行分析,得到的拟合参数结果列于表4,拟合曲线如图8所示.拟合相关系数r2介于0.997-0.998之间,同样很好地模拟了吸附剂对CO2的吸附过程.由表4可以看出,CNTs-TEPA和CNTs-TETA的起始吸附速率常数有所增加,说明样品的动态饱和吸附容量增加,与图2的结果相一致.失活速率常数减小说明了样品对CO2的脱附能力会随着改性后有所减弱. CNTs-TEPA的吸附速率常数和失活速率常速分别为1.31×103cm3·min-1·g-1和0.234 min-1,而对CNTs-TETA来说,其吸附速率常数和失活速率常数分别为8.25×102cm3·min-1·g-1和0.526 min-1.这一结果与两者的吸附容量和吸附活性完全对应.

表3 Suyadal失活模型对CNTs,CNTs-TEPA和CNTs-TETA的拟合结果各参数值Table 3 Parameters of Suyadal deactivation model for CO2adsorption on CNTs,CNTs-TETAand CNTs-TEPA

图7 CNTs,CNTs-TEPA和CNTs-TETA的实验吸附数据与Suyadal失活模型拟合曲线的比较Fig.7 Comparison of Suyadal experimental results with deactivation model for CO2adsorption on CNTs, CNTs-TEPA,and CNTs-TETA
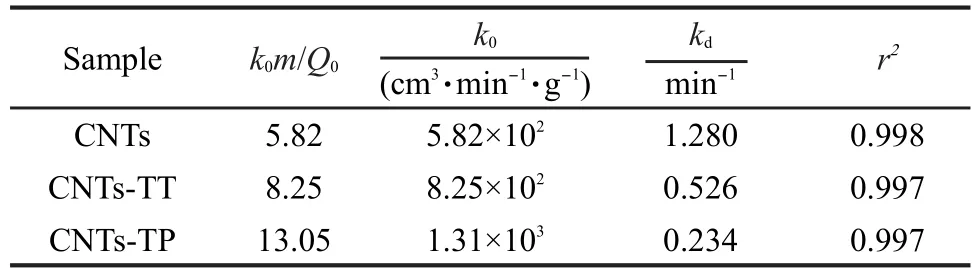
表4 Yasyerli失活模型对CNTs,CNTs-TEPA和CNTs-TETA的拟合结果各参数值Table 4 Parameters of Yasyerli deactivation model for CO2adsorption on CNTs,CNTs-TEPA,and CNTs-TETA

图8 CNTs,CNTs-TEPA和CNTs-TETA的实验吸附数据与Yasyerli失活模型拟合曲线的比较Fig.8 Comparison of Yasyerli experimental results with deactivation model for CO2adsorption on CNTs, CNTs-TETA,and CNTs-TEPA
表3和表4的拟合结果证实了Suyadal模型和Yasyerli模型都能很好地模拟样品对CO2的动态吸附过程.拟合相关系数r2均大于0.996,并且两个模型的失活速率常数kd也非常相近.考虑到无量纲吸附速率常数ksτ和k0m/Q0的数值变化,Yasyerli模型数据更加合理.所以,Yasyerli模型更适合用来分析CNTs、CNTs-TEPA和CNTs-TETA对CO2的吸附穿透曲线.
4 结论
(1)采用浸渍方法将TEPA和TETA浸渍至CNTs上,合成CO2固态胺吸附剂CNTs-TEPA和CNTs-TETA.吸附实验表明,在常温条件下CNTs-TEPA和CNTs-TETA的CO2吸附量与CNTs相比有显著提高.与文献报道相比,经过TEPA和TETA改性后的CNTs是一种在低浓度下具有良好发展前景的吸附剂.同时,在浸渍胺相同质量的情况下,TEPA改性后的效果优于TETA.
(2)通过透射电镜、红外光谱以及TGA等手段,证实TEPA和TETA基本负载到CNTs上,而且浸渍后的样品仍然保留了规整有序的孔道结构,表明CNTs的物理结构在浸渍改性后是稳定的.但改性后样品比表面积和孔容显著减小.
(3)随着温度从20°C升至30°C,CNTs-TEPA和CNTs-TETA的CO2吸附量q分别从126.7、101.2 mg·g-1升至139.3、110.4 mg·g-1.然而CNTs的吸附量q随着温度的增加变化不明显,反而略有下降.
(4)Suyadal和Yasyerli两种模型均能很好地模拟样品对CO2的动态吸附穿透曲线.但Yasyerli模型更适于分析CNTs、CNTs-TEPA和CNTs-TETA对CO2的吸附过程.
(1) Choi,S.;Drese,J.H.;Jones,C.W.ChemSusChem 2009,2,796.
(2) Serna-Guerrero,R.;Sayari,A.Chem.Eng.J.2010,161,182.
(3) Zhang,P.;Shi,Y.;Wei,J.;Zhao,W.;Ye,Q.J.Environ.Sci. 2008,20,39.
(4) Shi,J.J.;Liu,Y.M.;Chen,J.;Zhang,Y.;Shi,Y.Acta Phys.-Chim.Sin.2010,26(11),3023.[史晶金,刘亚敏,陈 杰,张 瑜,施 耀.物理化学学报,2010,26(11),3023.]
(5) Moloney,P.;Huffman,C.;Gorelik,O.;Nikolaev,P.;Arepalli, S.;Allada,R.;Springer,M.;Yowell,L.Advanced Life Support for Space Exploration:Air Revitalization UsingAmine Coated Single Wall Carbon Nanotubes.In Materials for Space Applications,Symposium on Materials for Space Applications; Boston,USA,Nov.29-Dec.03,2004;Chipara,M.,Edwards,D. L.,Benson,R.S.,Phillips,S.,Eds.;Materials Research Society: Warrendale,2005;59.
(6) Feron,P.;Jacobs,P.;Paul,P.;Savage,C.;Witt,J.Integrated CO2and Humidity Control by Membrane GasAbsorption.In ESA Special Publications,Sixth European Symposium on Space Environmental Control Systems;Noordwijk,Netherlands,1997, May 20-22,1997;Guyenne,T.D.,Eds.;European Space Agency:Paris,1997;761.
(7) Hwang,H.T.;Harale,A.;Liu,P.K.T.;Sahimi,M.;Tsotsis,T. T.J.Membr.Sci.2008,315,116.
(8) Oyenekan,B.A.;Rochelle,G.T.AIChE J.2007,53,3144.
(9) Sridharab,S.;Smithab,B.;Aminabhavia,T.M.Sep.Purif.Rev. 2007,36,113.
(10) Belmabkhout,Y.;Serna-Guerrero,R.;Sayari,A.Ind.Eng.Chem. Res.2009,49,359.
(11) Wang,X.;Schwartz,V.;Clark,J.C.;Ma,X.;Overbury,S.H.; Xu,X.;Song,C.J.Phys.Chem.C 2009,113,7260.
(12) Satyapal,S.;Filburn,T.;Trela,J.;Strange,J.Energy Fuels 2001,15,250.
(13) Somy,A.;Mehrnia,M.R.;Amrei,H.D.;Ghanizadeh,A.; Safari,M.Int.J.Green Gas Con.2009,3,249.
(14) Hsu,S.;Lu,C.Sep.Sci.Technol.2007,42,2751.
(15) Wei,J.W.;Shi,J.J.;Pan,H.;Zhao,W.;Ye,Q.;Shi,Y. Microporous Mesoporous Mat.2008,116,394.
(16) Zelenak,V.;Halamova,D.;Gaberova,L.;Bloch,E.;Llewellyn, P.Microporous Mesoporous Mat.2008,116,358.
(17) Su,F.;Lu,C.;Cnen,W.;Bai,H.;Hwang,J.F.Sci.Total Environ.2009,407,3017.
(18) Zhao,H.L.;Hu,J.;Wang,J.J.;Zhou,L.H.;Liu,H.L.Acta Phys.-Chim.Sin.2007,23(6),801.[赵会玲,胡 军,汪建军,周丽绘,刘洪来.物理化学学报,2007,23(6),801.]
(19) Mello,M.R.;Phanon,D.;Silveira,G.Q.;Llewellyn,P.L.; Ronconi,C.M.Microporous Mesoporous Mat.2011,143,174.
(20) Huang,H.Y.;Yang,R.T.;Chinn,D.;Munson,C.L.Ind.Eng. Chem.Res.2003,42,2427.
(21) Zhu,Z.Z.;Wang,Z.;Li,H.L.Appl.Surf.Sci.2008,254,2934.
(22) Krishen,K.Acta Astronaut.2008,63,324.
(23) Smart,S.;Cassady,A.;Lu,G.;Martin,D.Carbon 2006,44, 1034.
(24) Gommans,H.H.;Alldredge,J.W.;Tashiro,H.;Park,J.; Magnuson,J.;Rinzler,A.G.J.Appl.Phys.2000,88,2509.
(25)Chang,A.C.C.;Chuang,S.S.C.;Gray,M.M.;Soong,Y. Energy Fuels 2003,17,468.
(26) Serna-Guerrero,R.;Dá na,E.;Sayari,A.Ind.Eng.Chem.Res. 2008,47,9406.
(27) Danckwerts,P.V.Chem.Eng.Sci.1979,34,443.
(28) Versteeg,G.F.;van Dijck,L.A.J.;van Swaaij,W.P.M.Chem. Eng.Com.1996,144,113.
(29) Suyadal,Y.;Erol,M.;Oguz,H.Ind.Eng.Chem.Res.2000,39, 724.
(30) Yasyerli,S.;Dogu,G.;Ar,I.;Dogu,T.Ind.Eng.Chem.Res. 2001,40,5206.
October 18,2011;Revised:January 18,2012;Published on Web:February 23,2012.∗
.Email:shiyao@zju.edu.cn;Tel:+86-571-88273591.
Adsorption of Low Concentration CO2by Modified Carbon Nanotubes under Ambient Temperature
YE Qing1ZHANG Yu1LI Ming2SHI Yao1,*
(1Institute of Industrial Ecology and Environment,Department of Chemical and Biological Engineering,Faculty of Engineering, Zhejiang University,Hangzhou 310028,P.R.China;2Zhejiang Shuren University,Hangzhou 310015,P.R.China)
Solid amine adsorbents for low concentration CO2removal were developed using carbon nanotubes(CNTs)impregnated with tetraethylenepentamine(TEPA)and triethylenetetramine(TETA).The adsorbents were characterized by scanning electron microscopy(SEM),transmission electron microscopy (TEM),Fourier-transform infrared spectroscopy(FITR),N2adsorption/desorption,elemental analysis and thermogravimetric analysis(TGA).After impregnation,the shapes,fundamental channels and pore structures of the adsorbents were unchanged.However,the surface area and pore volume decreased.The adsorption behavior toward low concentration CO2was investigated in a fixed-bed column.The results indicated that the adsorption capacity was enhanced substantially by modification.The CO2adsorption capacity of CNTs-TEPA was higher than that of CNTs-TETA with the same amount of amine loading.The adsorption capacity increased steadily from 126.7 to 139.3 mg·g−1for CNTs-TEPA and from 101.2 to 110.4 mg·g−1for CNTs-TETA as the temperature increased from 20 to 30°C.The adsorption capacity of the raw CNTs experienced a modest increase,but began to decrease gradually with further temperature increases. Suyadal and Yasyerli deactivation models were applied to investigate the experimental breakthrough curves of raw and modified CNTs.It was concluded that the Yasyerli deactivation model is more appropriate to analyze the breakthrough curves of CO2adsorption on solid amine adsorbents.
Carbon nanotube;CO2adsorption;Triethylenetetramine;Tetraethylenepentamine; Deactivation model
10.3866/PKU.WHXB201202234
O647
The project was supported by the National Natural Science Foundation of China(20976159).国家自然科学基金(20976159)资助项目
