Cu-ZSM-5的NH3选择性催化还原NO性能及其稳态动力学
2012-11-30张秋林徐海迪邱春天龚茂初陈耀强
张秋林 徐海迪 邱春天 林 涛 龚茂初 陈耀强
(四川大学绿色化学与技术教育部重点实验室,成都610064)
Cu-ZSM-5的NH3选择性催化还原NO性能及其稳态动力学
张秋林 徐海迪 邱春天 林 涛*龚茂初 陈耀强*
(四川大学绿色化学与技术教育部重点实验室,成都610064)
采用浸渍法制备了一系列不同Cu载量的Cu-ZSM-5整体式催化剂.考察了该系列催化剂的NH3选择性催化还原(SCR)NO的反应特性.结果表明,当Cu质量分数为5%时,Cu-ZSM-5催化剂的SCR活性最高,此时催化剂上NO最高转化率高达96.5%,并且催化剂的活性窗口较宽,催化剂在198-470°C之间NO转化率大于80%.H2O和SO2的添加仅轻微影响Cu-ZSM-5催化剂的SCR活性.当Cu载量大于5%时,Cu-ZSM-5催化剂中出现明显的CuO物相.稳态动力学结果表明,在5%Cu载量的Cu-ZSM-5上的SCR反应中,NO的反应级数接近一级,NH3的反应级数接近零级,O2的反应级数接近1/2级.该反应的表观活化能为47.7 kJ·mol-1.
Cu-ZSM-5;选择性催化还原;稳态动力学;表观活化能
1 引言
柴油车尾气中含有的大量NOx和颗粒物(PM),对人类健康和生态系统构成了严重的威胁.如何有效地减少和控制柴油车尾气NOx的排放仍然是一个难题.而柴油车尾气中NO占NOx总量的95%以上,因此柴油车尾气NOx排放控制的关键是如何有效去除NO.目前尿素或NH3选择性催化还原(SCR)技术被认为是最有效的脱除柴油车尾气NO的技术,并且在实际柴油车尾气NO的净化中得到应用.传统净化柴油车尾气NO的SCR催化剂主要为V2O5/ TiO2催化剂(MoO3或WO3做助剂),该催化剂在300-400°C之间表现出了较好的脱氮效率.1,2然而柴油车尾气温度一般较低,冷启动时尾气的温度一般低于200°C,怠速运行时柴油车尾气温度在180-280°C,较高时也仅为440°C左右,其中城市公交柴油车和小型柴油轿车尾气温度甚至低于230°C.3,4这对催化剂的低温脱氮效率提出了较高的要求.此外,柴油车尾气后处理系统中SCR催化剂前置的颗粒捕集器(DPF)在使用时需要定期喷油燃烧活化处理,此时尾气温度会短时间内超过600°C,这要求SCR催化剂在短时间内能经受高温热冲击.因此钒基(V2O5/TiO2)催化剂狭窄的活性温度窗口(300-400°C)、较差的低温活性、较弱的抗热冲击能力(尾气温度超过550°C时,有毒的钒氧化物会挥发并随尾气进入到空气中)和钒氧化物剧烈的毒性等缺点极大地限制了钒基催化剂在柴油车尾气NO净化中的应用.因此,发展新型的低温高活性和抗高温热冲击能力强的无毒SCR催化剂已成为研究的热点.5,6
近年廉价无毒的分子筛催化剂因其良好的耐高温稳定性和在宽温度范围内的高SCR活性备受关注.7-14其中Fe-ZSM-5催化剂因其高活性、高选择性和高抗硫性被广泛研究.10-12然而Fe-ZSM-5催化剂的活性温度窗口主要集中在中高温区域(300-600°C),而在200-300°C的低温范围内净化NO的效果并不理想.Cu-ZSM-5分子筛催化剂在低温范围(200-300°C)表现出了一定的潜力,并被广泛用于CxHy-SCR和NO分解的研究,15-19但用于NH3-SCR反应的研究报道较少,且效果不太理想.9,20作者21前文以CuCl2·2H2O为前驱体采用简单易行的浸渍法制备了Cu-ZSM-5催化剂,其中Cu质量分数为8%的Cu-ZSM-5催化剂表现出了较高的NO还原活性.然而我们的进一步研究发现,该类催化剂即使在较低的负载量(如2%)下,催化剂表面仍有CuCl2物种存在,在含有约10%水汽的柴油车尾气环境下,Cl-具有较强的腐蚀性,且在高温湿气中腐蚀性更强.在实际应用中这极易导致柴油车排气管在短时间内腐蚀并破损.因此,为了避免上述问题,本文采用分解温度较低的硝酸铜为前驱体制备了Cu-ZSM-5整体式催化剂,考察了其NH3-SCR性能及其动力学.
2 实验部分
2.1 催化剂制备
采用浸渍法制备Cu-ZSM-5催化剂.以Cu(NO3)2· 2H2O(AR,成都市科龙化工试剂厂)为前驱体,将其分别按Cu质量分数为0,2.5%,5%,7.5%,10%和12.5%浸渍于ZSM-5(SiO2与Al2O3摩尔比为25,南开大学催化剂厂)分子筛上,于110°C干燥6 h,550 °C焙烧5 h,即制得不同Cu含量的Cu-ZSM-5催化剂粉末.将制得的催化剂粉末和适量的水混合,制成浆液,涂覆于堇青石蜂窝陶瓷基体小样上(2.5 mL, Corning公司),催化剂涂覆量为180 g·L-1,样品在110°C干燥6 h,550°C焙烧3 h,制得的Cu-ZSM-5催化剂按Cu质量分数为0、2.5%、5%、7.5%、10%和12.5%分别记为H-ZSM-5、Cu-ZSM-5-2.5、Cu-ZSM-5-5、Cu-ZSM-5-7.5、Cu-ZSM-5-10和Cu-ZSM-5-12.5.
2.2 催化剂的表征
催化剂的X射线衍射(XRD)分析在日本理学D/ max-rA型XRD仪上进行,使用CuKα射线,激发电压50 kV,管电流40 mA,步长0.02(°)·s-1,扫描范围2θ=5°-70°.
2.3 催化剂活性测试
催化剂活性评价在连续流动固定床石英管反应器中进行.反应气组成(体积分数)如下:0.1% NO,0.11%NH3,5%O2,Ar为稀释气.空速为30000 h-1(总流速为1250 mL·min-1).反应前后的NOx浓度用Model-42i型尾气分析仪(Thermo corporation, USA)进行定量分析.为避免未反应的NH3对分析仪的测试结果产生影响,测试气体进入分析仪前先经过装有浓磷酸的氨阱.为确保活性测试结果不受吸附的影响,在每个测试点稳定反应1 h后,再进行测试和数据记录.
催化剂的稳态动力学研究在连续流动固定床石英管反应器中进行.催化剂用量1 mL(催化剂涂覆量0.03762 g).反应气组成如下:0.08%-0.16% NO,0.08%-0.16%NH3,5%O2,Ar为稀释气.总流速为2000 mL·min-1.检测仪器同上.
3 结果与讨论
3.1 催化剂物相结构分析
图1(a)为不同Cu载量的Cu-ZSM-5催化剂的XRD谱.由图可以看出,各催化剂ZSM-5的特征衍射峰均较为尖锐,表明ZSM-5的结晶度较高.当向分子筛中添加2.5%和5%的Cu时,除了明显的ZSM-5衍射峰外,未检测到其它物相的X射线衍射峰.然而,当Cu-ZSM-5中Cu载量大于5%时,除了明显的ZSM-5衍射峰外,催化剂上还出现了较为明显的CuO衍射峰(2θ=38.8°),且随着Cu载量的增加, CuO物相的衍射峰强度逐渐增加.表明当Cu的载量大于5%时,CuO物种在催化剂表面聚集并晶化,催化剂中Cu物种的分散性降低,ZSM-5的阳离子位趋于被完全占据.而聚集并晶化的CuO物种停留在ZSM-5分子筛表面或细小孔道中,极易造成催化剂孔道的堵塞,并可能覆盖部分活性物种,使催化剂同时受扩散控制和反应控制的影响较为严重,进而降低催化剂的SCR活性.
图1(b)为不同Cu载量的Cu-ZSM-5催化剂和H-ZSM-5在2θ为22.4°-24.2°之间放大的XRD谱.由图可以看出,当向ZSM-5分子筛中添加Cu后, ZSM-5的2θ角向低角度发生了轻微的位移,且随着Cu载量的增加,ZSM-5特征衍射峰衍射角的位移更加明显.由布拉格方程可知,Cu的引入轻微地增加了ZSM-5的晶面间距,这可能是由于少量的Cu进入ZSM-5的晶格或发生了同晶取代,而Cu的离子半径大于Si和Al的离子半径,所以ZSM-5的晶胞参数增大.
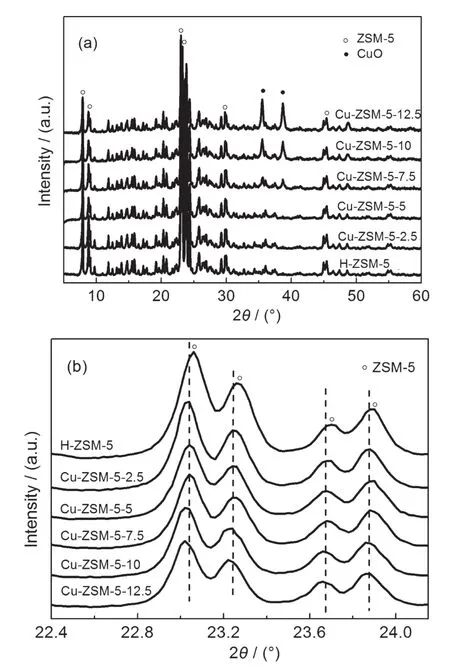
图1 不同Cu-ZSM-5催化剂样品的XRD谱Fig.1 XRD patterns of the different Cu-ZSM-5 catalyst samples(a)2θ=5°-65°,(b)2θ=22.4°-24.2°;x%in Cu-ZSM-5-x refers to Cu loading(mass fraction).
3.2 不同Cu含量对Cu-ZSM-5催化剂SCR活性的影响
不同Cu载量的Cu-ZSM-5催化剂的SCR活性示于图2.由图2可见,单一的H-ZSM-5的NH3-SCR活性较差.然而将Cu引入ZSM-5分子筛后,其NH3-SCR活性显著提高,Cu-ZSM-5表现出了极为优异的NO还原活性.当Cu载量小于5%时,随着Cu载量的增加,Cu-ZSM-5的SCR活性明显升高.当Cu载量为5%时,Cu-ZSM-5的SCR活性最佳.此时,催化剂上NO最高转化率高达96.5%,并且催化剂的活性窗口较宽,催化剂在198-470°C之间NO转化率大于80%.当Cu载量大于5%时,进一步增加Cu载量时,Cu-ZSM-5的SCR活性逐渐降低.
Cu-ZSM-5催化剂中Al原子周围的阳离子平衡电荷主要由Cu2+和H+组成.结合活性结果和文献19可知孤立的CuO粒子对NH3-SCR催化反应的促进作用较小,而螯合型的Cu2+作为主要的活性中心具有较好的NH3-SCR催化作用.当Cu-ZSM-5中Cu载量小于5%时,催化剂ZSM-5中被Cu占据的阳离子位未达到饱和,部分阳离子位被H+占据,导致催化剂活性中心偏少.由此可见,增加Cu的载量增加了催化剂的活性位,所以此时NO还原活性随着Cu载量的增加而提高.由XRD结果可知,当Cu-ZSM-5中Cu载量大于或等于7.5%时,出现明显的CuO衍射峰,表明Cu-ZSM-5中有CuO晶粒形成,可见Cu-ZSM-5中阳离子位的交换达到饱和.此时多余的Cu物种以铜氧化物的形式存在于催化剂表面或分子筛孔道中,从而影响了分子筛结构的通透性,也影响了铜物种的分散并可能造成催化剂的部分活性位被覆盖,进而降低了NH3-SCR反应的催化活性.因此Cu含量为5%时,Cu较多地占据了ZSM-5分子筛的阳离子位,而进入分子筛孔道或覆盖在催化剂表面的铜物种则较少,所以5%Cu-ZSM-5催化剂活性最高.

图2 不同Cu载量Cu-ZSM-5催化剂的NH3-SCR活性Fig.2 NH3-SCR activity of Cu-ZSM-5 samples with different Cu loadingsreaction conditions:0.1%NO-0.11%NH3-5%O2-Ar balance, gas hourly space velocity(GHSV)=30000 h-1
3.3 O2浓度对Cu-ZSM-5-5催化剂SCR活性的影响
研究22,23表明O2在NH3-SCR反应中扮演着极为重要的角色,为此本文考察了O2对Cu-ZSM-5-5催化剂SCR活性的影响,结果列于图3.当从反应气中取消O2的供给时,催化剂的NO转化率先快速下降,约20 min后下降缓慢,约40 min后NO转化率趋于稳定.当重新向反应物中引入O2时,催化剂的NO转化率快速增加,约10 min后SCR活性恢复至初始水平.由此可见O2对NH3-SCR反应极为重要.当切断O2供给之初,NO转化率并没有立即降至最低谷,而是有一个缓慢的过程.这是由于晶格氧代替了部分气相O2参与了NH3-SCR反应过程,所以切除O2供给后SCR活性降至最低点是一个缓慢的过程,这与文献22,23的研究结论一致.
3.4 H2O和SO2对Cu-ZSM-5-5催化剂SCR活性的影响
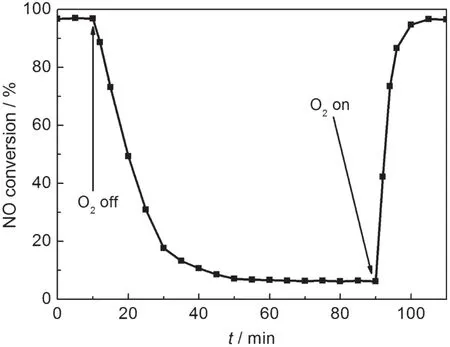
图3 O2浓度对Cu-ZSM-5-5催化剂NH3-SCR活性的影响Fig.3 Effect of O2concentration on NH3-SCR activity of Cu-ZSM-5-5reaction conditions:0.1%NO-0.11%NH3-Ar balance, GHSV=30000 h-1
由于原油中均含有一定量的硫,因此实际柴油机尾气中均含有一定量的SO2.而原油燃烧过程中均会产生一定量的H2O.H2O和SO2的存在会导致SCR催化剂中毒失活.为此本文考察了H2O和SO2对Cu-ZSM-5-5催化剂NH3-SCR活性的影响,结果如图4所示.催化剂开始测试前均在250°C连续稳定反应1 h,然后在250°C分别考察了10%H2O和10%H2O+0.01%SO2对Cu-ZSM-5-5催化剂SCR活性的影响.
当向反应体系中引入10%的H2O后,NO转化率出现轻微的下降,约1 h后趋于稳定.停止添加H2O后,NO转化率逐渐恢复至初始水平.可见H2O与反应物(NH3和NO)之间的竞争吸附是催化剂活性降低的主要原因,而且由此导致的催化剂中毒是可逆的.因此停止添加H2O后,催化剂SCR活性可恢复至初始水平.当反应体系中同时加入10%H2O和0.01%SO2时,NO转化率出现了一定程度的下降.约1.5 h后,NO转化率由初始的96.5%降至约88.7%左右后趋于稳定.停止H2O和SO2添加后,催化剂的SCR活性逐渐恢复至95%左右后趋于稳定,可见催化剂的活性并未完全恢复至初始水平.由此可见,H2O和SO2与反应物之间的竞争吸附仍是催化剂SCR活性降低的主要原因之一.且与H2O相比,SO2与反应物之间的竞争吸附更强.表明H2O和SO2同时存在造成催化剂的失活是局部不可逆的,这是由于SO2和H2O同时存在时易在催化剂表面形成硫酸盐或亚硫酸盐,并堵塞催化剂的部分孔道和覆盖催化剂的部分活性位,甚至造成活性中心的硫酸化,从而使催化剂部分失活.24-27
3.5 Cu-ZSM-5-5催化剂的稳态动力学研究
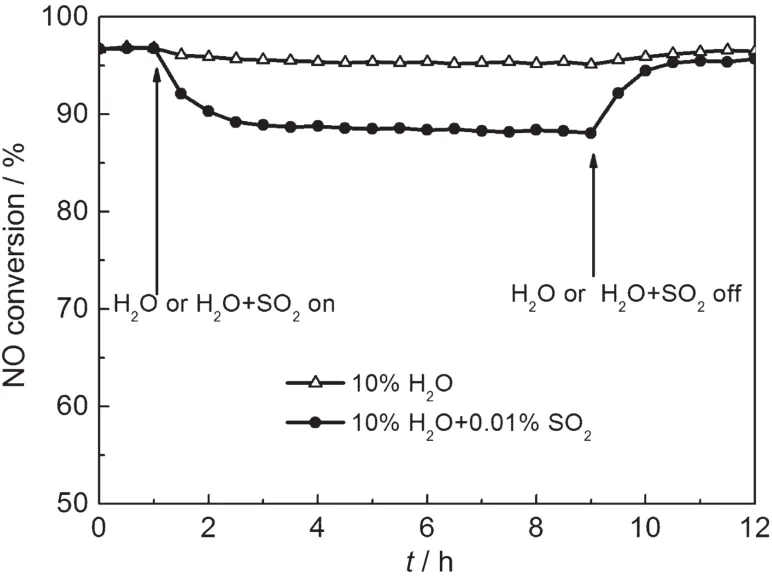
图4 H2O和SO2对Cu-ZSM-5-5催化剂SCR活性的影响Fig.4 Effect of H2O and SO2on the SCR activity of Cu-ZSM-5-5reaction conditions:0.1%NO-0.11%NH3-5%O2-0.01%SO2-10%H2O-Ar balance,GHSV=30000 h-1
催化反应的表观活化能是评价一个催化剂在催化反应中的作用以及催化剂的效率和该类催化剂进一步发展的空间的一项关键的指标.而催化反应的速率方程对我们测试并计算催化反应的表观活化能和认识催化剂的性能有较大帮助.而要得出催化反应的速率方程需要知道反应中各反应物的反应级数.为了确定Cu-ZSM-5-5催化剂上NO的反应级数,保持反应物中NH3浓度为0.12%,O2浓度为5%,NO浓度从0.08%到0.16%之间变化.同理,为了确定NH3的反应级数,保持反应物中NO浓度为0.12%,O2浓度为5%,NH3浓度从0.08%到0.16%之间变化.为了确定O2的反应级数,保持反应物中NO和NH3浓度为0.12%,O2浓度从0%到5%之间变化.为了确保NO的不完全转化,1 mL堇青石的催化剂负载量仅为0.03762 g.
NO催化转化反应的速率方程表达如下:

方程(1)中rNO为NO催化转化的反应速率,x、y和z分别为NO、NH3和O2的反应级数.
图5中显示了不同浓度的NO在不同温度下的NO转化速率.由图可见,测试温度下的NO的转化速率均随着NO浓度的增加而线性的增加,而且NO的转化速率随着温度的升高而增加.通过计算可知,200、225和250°C下NO的反应级数均接近一级.
图6中显示了不同浓度的NH3在不同温度下的NO转化速率.由图6可以看出,在0.08%-0.16%范围内,随着NH3浓度的增加,NO转化速率基本不变,即NH3浓度对Cu-ZSM-5-5上的NH3-SCR反应基本无影响.通过计算可知,200、225和250°C下NH3的反应级数均是接近零级.

图5 Cu-ZSM-5-5上NO转化速率随NO浓度的变化Fig.5 Dependence of NO conversion rate on NO concentration on Cu-ZSM-5-5reaction conditions:0.03762 g catalyst,[NH3]=0.12%,[O2]=5%,[NO]=0.08%-0.16%,Ar balance,GHSV=1.2×105h-1

图6 Cu-ZSM-5-5上NO转化速率随NH3浓度的变化Fig.6 Dependence of NO conversion rate on NH3 concentration on Cu-ZSM-5-5reaction conditions:0.03762 g catalyst,[NO]=0.12%,[O2]=5%, [NH3]=0.08%-0.16%,Ar balance,GHSV=1.2×105h-1
不同温度下NO转化速率随O2浓度变化结果如图7所示,可见O2浓度对SCR反应影响较大,当反应气中O2浓度在0%-2%范围内变化时,NO的转化速率随着O2浓度的增加而明显增加.当反应气中O2浓度大于3%时,NO的转化速率随着O2浓度的增加而变化不大.通过方程(1),可以计算得到O2浓度小于1%时O2的反应级数约为1/2级.
由于仅有0.03762 g(1 mL)催化剂参与反应,所以如文献28-30所述,此时的NH3-SCR反应基本不受扩散控制的影响.反应中O2浓度大大过量(体积分数为5%).因此方程(1)可表述为:

方程(2)中rNO为NO转化的反应速率,n为NO的反应级数,k*为一级表观速率常数(k*=k[O2]0.5).而活塞流反应器的一级表观速率常数可表达为如下方程:方程(3)中,Vʹ为实际条件下的气体流速(mL·min-1), W为催化剂的有效质量,x为NO转化率.

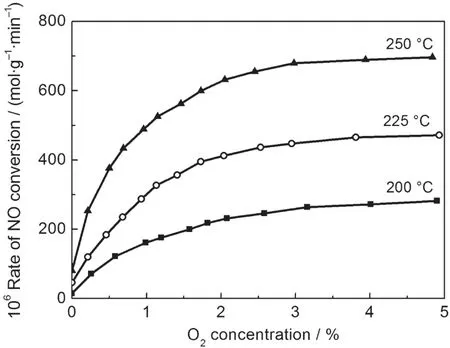
图7 Cu-ZSM-5-5上NO转化速率随O2浓度的变化Fig.7 Dependence of NO conversion rate on O2 concentration on Cu-ZSM-5-5reaction conditions:0.03762 g catalyst,[NH3]=0.12%,[NO]=0.12%, [O2]=0%-5%,Ar balance,GHSV=1.2×105h-1
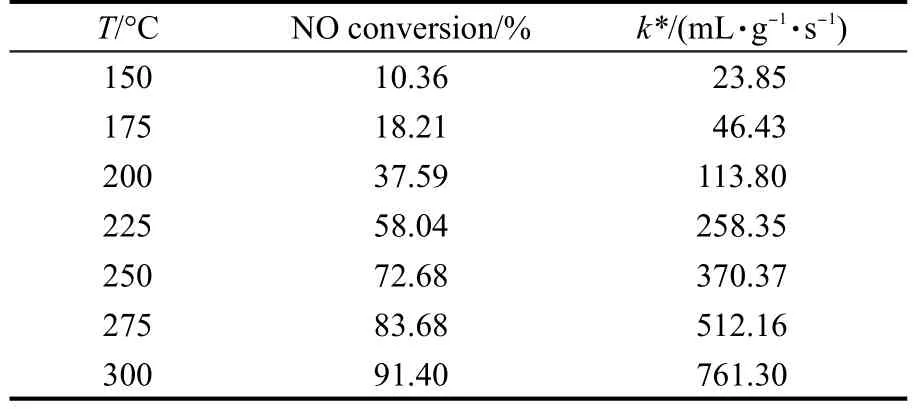
表1 Cu-ZSM-5-5的NH3-SCR活性Table 1 NH3-SCR activity of Cu-ZSM-5-5
为了避免NO完全转化并计算Cu-ZSM-5-5催化剂NH3-SCR反应的表观活化能,不同温度下低涂覆量的Cu-ZSM-5-5整体式催化剂(0.1356 g catalyst/ 2.5 mL cordierite)在30000 h-1下的NH3-SCR活性结果列于表1.由表可见,在150-300°C之间NO转化率随着温度的升高而增加,此时反应主要受反应控制,受扩散控制的影响较小,假设该催化反应不受扩散控制,通过方程(3)可计算出不同温度下的表观速率常数,结果列于表1.该催化反应的表观活化能Ea可以通过阿仑尼乌斯方程表示如下:
k*=Aexp(-Ea/RT) (4)方程(4)中,Ea为表观活化能,A为指前因子.
通过lnk*对1/T作图,结果如图8所示,由直线斜率即可得出Cu-ZSM-5-5催化剂的NH3-SCR反应的表观活化能Ea=47.7 kJ·mol-1.Cu-ZSM-5-5催化剂在NH3-SCR反应中的表观活化能低于Fe-ZSM-5(54 kJ·mol-1),29H-ZSM-5(55 kJ·mol-1)30和H-MOR(58 kJ·mol-1).31
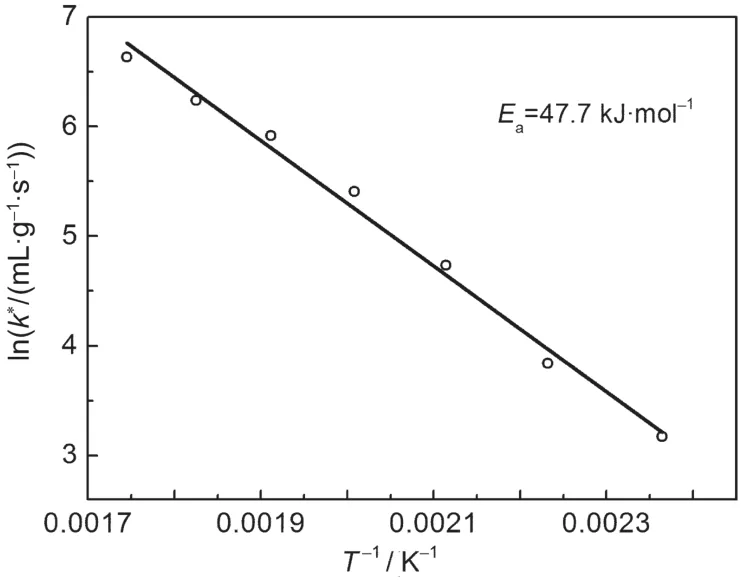
图8 NO转化速率常数的对数与温度倒数的阿仑尼乌斯图Fig.8 Arrehenius plot of the logarithm of rate constant (k*)for NO consumption against inverse temperature
文献和我们前期的研究结果22,32-34表明Cu-ZSM-5具有较高的NH3-SCR活性,尤其在低温范围展现出了较高的脱除氮氧化物的效率.Cu-ZSM-5-5催化剂上NH3-SCR反应的稳态动力学结果表明在200-250°C之间NO的反应级数接近一级,NH3的反应级数接近零级,O2的反应级数接近1/2级.大量的研究9,20,22表明,NH3-SCR催化反应的反应机理主要有两种:第一种观点认为NH3首先在催化剂表面吸附并活化,形成吸附态的氨物种或亚氨物种,再与气相中的NO反应生成N2和H2O,即典型的Eley-Rideal机理;第二种观点认为NH3同样先在催化剂表面吸附并活化,形成吸附态的氨物种或亚氨物种,而且催化剂在吸附NH3的同时,也吸附NO,形成吸附态的NO物种,然后吸附态的NH3物种和吸附态的NO物种反应生成N2和H2O,即所谓的Langmuir-Hinshelwood机理,当前的研究表明,20,30-32在NH3-SCR反应过程中两种反应机理同时进行.然而反应无论按哪种机理进行,都需要NH3在催化剂表面的吸附与活化.而Cu-ZSM-5-5催化剂NH3的反应级数为接近零级,表明反应过程中NH3能快速在催化剂表面吸附,催化剂能完全被NH3覆盖,NH3的吸附与活化不是反应的速控步骤.
4 结论
Cu-ZSM-5催化剂具有较好的NH3-SCR活性, Cu-ZSM-5催化剂的SCR活性随着Cu载量的增加先升高后降低.当Cu的负载量为5%时,催化剂的活性最佳.30000 h-1空速下,Cu-ZSM-5-5在220-384°C之间NO转化率大于90%,最高转化率高达97%.H2O和SO2的添加降低了催化剂的SCR活性,但这种影响是基本可逆的.
稳态动力学结果表明,Cu-ZSM-5-5在200-250 °C之间NO的反应级数接近一级,NH3的反应级数为接近零级,O2的反应级数接近1/2级.NH3的吸附与活化不是该反应的速控步骤.Cu-ZSM-5-5上该催化反应的表观活化能为47.7 kJ·mol-1.
(1) Stefan,B.;Thomas,H.Appl.Catal.B 2000,28,101.
(2) Garcia-Bordeje,E.;Calvillo,L.;Lazaro,M.J.;Moliner,R. Appl.Catal.B 2004,50,235.
(3) Kašpar,J.;Fornasiero,P.;Hickey,N.Catal.Today 2003,77, 419.
(4)Adams,K.M.;Cavataio,J.V.;Hammerle,R.H.Appl.Catal.B 1996,10,157.
(5) Xu,H.D.;Qiu,C.T.;Zhang,Q.L.;Lin,T.;Gong,M.C.;Chen, Y.Q.Acta Phys.-Chim.Sin.2010,26,2449.[徐海迪,邱春天,张秋林,林 涛,龚茂初,陈耀强.物理化学学报,2010,26, 2449.]
(6) Chen,Z.H.;Li,X.H.;Yang,Q.;Li,H.;Gao,X.;Jiang,Y.B.; Wang,F.R.;Wang,L.F.Acta Phys.-Chim.Sin.2009,25, 601.[陈志航,李雪辉,杨 青,李 华,高 翔,江燕斌,王芙蓉,王乐夫.物理化学学报,2009,25,601.]
(7)Carja,G.;Kameshima,Y.;Okada,K.;Madhusoodana,C.D. Appl.Catal.B 2007,73,60.
(8) van-Kooten,W.E.J.;Liang,B.;Krijnsen,H.C.;Oudshoorn,O. L.;Calis,H.P.A.;van-den-Bleek,C.M.Appl.Catal.B 1999, 21,203.
(9) Sjövall,H.;Olsson,L.;Fridell,E.;Blint,R.J.Appl.Catal.B 2006,64,180.
(10) Krishna,K.;Makkee,M.Catal.Today 2006,114,23.
(11) Rivallan,M.;Berlier,G.;Ricchiardi,G.;Zecchina,A.;Nechita, M.T.;Olsbye,U.Appl.Catal.B 2008,84,204.
(12) Grossale,A.;Nova,I.;Tronconi,E.;Chatterjee,D.;Weibel,M. Top.Catal.2009,52,1837.
(13) Balle,P.;Geiger,B.;Kureti,S.Appl.Catal.B 2009,85,109.
(14) Richter,M.;Trunschke,A.;Bentrup,U.;Brzezinka,K.W.; Schreier,E.;Schneider,M.;Pohl,M.M.;Fricke,R.J.Catal. 2002,206,98.
(15) Komvokis,V.G.;Iliopoulou,E.F.;Vasalos,I.A.;Triantafyllidis, K.S.;Marshall,C.L.Appl.Catal.A 2007,325,345.
(16) Li,L.D.;Zhang,F.X.;Guan,N.J.;Richter,M.;Fricke,R. Catal.Commun.2007,8,583.
(17) Sullivan,J.A.;Cunningham,J.Appl.Catal.B 1998,15,275.
(18) Ganemi,B.;Björnbom,E.;Demirel,B.;Paul,J.Microporous Mesoporous Mat.2000,38,287.
(19) Pirone,R.;Ciambelli,P.;Moretti,G.;Russo,G.Appl.Catal.B 1996,8,197.
(20) Ma,A.Z.;Muhler,M.;Grünert,W.Chem.Eng.Technol.2000, 23,273.
(21) Zhang,Q.L.;Qiu,C.T.;Xu,H.D.;Lin,T.;Gong,M.C.;Chen, Y.Q.Chin.J.Catal.2010,31,1411.[张秋林,邱春天,徐海迪,林 涛,龚茂初,陈耀强.催化学报,2010,31,1411.]
(22) Long,R.T.;Yang,R.T.J.Catal.2000,194,80.
(23) Qi,G.S.;Yang,R.T.Appl.Catal.B 2003,44,217.
(24) Sierraalta,A.;Bermudez,A.;Rosa-Brussin,M.J.Mol.Catal.A 2005,228,203.
(25) Tang,X.L.;Hao,J.M.;Xu,W.G.;Li,J.H.Chin.J.Catal. 2006,27,843.[唐晓龙,郝吉明,徐文国,李俊华.催化学报, 2006,27,843.]
(26) Oliveira,M.L.M.;Silva,C.M.;Moreno-Tost,R.;Farias,T.L.; Jiménez-López,A.;Rodríguez-Castellón,E.Appl.Catal.B 2009,88,420.
(27) Li,Z.J.;Flytzani-Stephanopoulos,M.Appl.Catal.B 1999,22, 35.
(28) Devadas,M.;Kröcher,O.;Elsener,M.;Wokaun,A.;Söger,N.; Pfeifer,M.;Demel,Y.;Mussmann,L.Appl.Catal.B 2006,67, 187.
(29) Huang,H.Y.;Long,R.Q.;Yang,R.T.Appl.Catal.A 2002,235, 241.
(30) Stevenson,S.A.;Vartuli,J.C.;Brooks,C.F.J.Catal.2000, 190,228.
(31) Yang,R.T.;Chen,J.P.;Kikkinides,E.S.;Cheng,L.S.; Cichanowicz,J.E.Ind.Eng.Chem.Res.1992,31,1440.
(32)Machida,M.;Uto,M.;Kurogi,D.;Kijima,T.Chem.Mater. 2000,12,3158.
(33) Brandenberger,S.;Kröcher,O.;Wokaun,A.;Tissler,A.;Althoff, R.J.Catal.2009,268,297.
(34)Akah,A.C.;Nkeng,G.;Garforth,A.A.Appl.Catal.B 2007,74, 34.
December 9,2011;Revised:February 2,2012;Published on Web:February 23,2012.
Catalytic Performance and Steady-State Kinetics of Cu-ZSM-5 for Selective Catalytic Reduction of NO with NH3
ZHANG Qiu-Lin XU Hai-Di QIU Chun-Tian LIN Tao*GONG Mao-Chu CHEN Yao-Qiang*
(Key Laboratory of Green Chemistry and Technology of the Ministry of Education,Sichuan University, Chengdu 610064,P.R.China)
A series of Cu-ZSM-5 catalysts with different Cu loadings were prepared by an incipient wetness impregnation method.These catalysts were used for studies of selective catalytic reduction (SCR)of NO by NH3.The results showed that Cu-ZSM-5 with 5%Cu loading showed the best catalytic activity,the conversion of NO was more than 80%over the temperature range 198-470°C,and the highest NO conversion was 96.5%.The SCR activity was only influenced slightly by the addition of H2O or SO2.Visible diffraction of the CuO phase was observed when the Cu content was above 5%.The results of steady-state kinetics studies indicated that the SCR reaction over Cu-ZSM-5 with 5%Cu loading was zero-order with respect to NH3,first-order with respect to NO,and nearly half-order with respect to O2.The apparent activation energy for the reaction was found to be 47.7 kJ·mol-1.
Cu-ZSM-5;Selective catalytic reduction;Steady-state kinetics; Apparent activation energy
10.3866/PKU.WHXB201202232
O643
∗Corresponding authors.LIN Tao,Email:lintaochem@scu.edu.cn.CHEN Yao-Qiang,Email:nic7501@scu.edu.cn;Tel/Fax:+86-28-85418451. The project was supported by the National Natural Science Foundation of China(20773090,20803049).
国家自然科学基金(20773090,20803049)资助项目
