复方环丙沙星乳剂安全性试验研究
2012-11-23李孝文田世杰孙志良
漆 俊,李孝文,田世杰,刘 琪,孙志良,2
(1.湖南农业大学动物医学院,长沙 410128;2.湖南省兽药工程技术研究中心,长沙 410311)
环丙沙星(Ciprofloxacin,CPLX),又名环丙氟哌酸、丙氟哌酸、悉复欣、悉复欢、适普灵等,常用其盐酸盐和乳酸盐,是目前兽医临床上使用的对革兰氏阴性菌抗菌活性最强的一种氟喹诺酮类(Fluoroquinolones,FQNs)药物。其作用机理主要是通过抑制细菌DNA旋转酶而发挥其快速杀菌作用,对革兰氏阴性菌、革兰氏阳性菌、支原体等均有很强的抗菌活性。环丙沙星具有脂溶性高,蛋白结合率低,抗菌后效应(postantibiotic effect,PAE)时间较长,药物动力学良好,不良反应少,价格低廉等优点,因此被广泛应用于医学和兽医临床[1-6]。
甲氧苄啶(TMP),又名磺胺增效剂,是合成抗菌药,抗菌谱与磺胺药类似,有强大的抑制二氢叶酸还原酶的作用,但细菌较易对其产生耐药性,很少单独使用。临床上TMP常与磺胺甲噁唑(SMZ)合用治疗呼吸系统、泌尿系统、消化系统等部位的感染[7]。
为了综合环丙沙星和甲氧苄啶的各项优点并加以利用,本实验室采用油乳剂灭活疫苗抗原缓释技术与药用乳剂制备技术相结合的方法,以乳酸环丙沙星为主药,辅以乳酸甲氧苄啶研制出了复方环丙沙星乳剂。该制剂作为一种长效制剂,稳定性好,缓释效果显著,可以充分发挥环丙沙星高效、长效的优点,从而减少临床用药次数。采用家兔对本制剂进行了热源实验、红细胞体外溶血性和肌肉局部刺激性实验,同时采用豚鼠进行了全身主动过敏性试验[8-9],为临床上安全用药提供实验依据。
1 材料与方法
1.1 材料
1.1.1 主要试剂 复方环丙沙星乳剂(批号:090810,本实验室与湖南省兽药工程技术研究中心共同研制,每毫升含50 mg乳酸环丙沙星,10 mg乳酸甲氧苄啶);乳酸环丙沙星(批号:090622,98.3%,湖南农大动物药业公司);乳酸甲氧苄啶(乳酸TMP批号:090715,99.1%,湖南农大动物药业公司);复方环丙沙星注射液(批号:090718,本实验室自制,每毫升含50 mg乳酸环丙沙星、10 mg乳酸甲氧苄啶);0.9%氯化钠注射液(批号:B080412,四川科伦股份有限公司);10%鸡蛋清溶液(取新鲜鸡蛋蛋清,以生理盐水稀释配制)。
1.1.2 仪器设备 超净工作台(SW-CJ-2FD型,苏州净化设备公司);电子天平(AY22O型,日本Electronic Balance公司);电热恒温水浴锅(HHSY11-Ni2型,上海跃进医疗器械厂);离心机(Z323K型,德国Hermle公司);恒温恒湿培养箱(LRH-250-S型,广东省医疗器械厂);全自动立式电热压力蒸汽灭菌器(YXQ-LS-50SⅡ,上海博迅公司医疗设备厂);电热鼓风干燥箱(DHG-9240A型,上海精宏试验设备有限公司)。
1.1.3 试验动物 健康家兔18只,体重2.5±0.5 kg,雌雄各半;豚鼠18只,体重300±50 g,雌雄各半。所用试验动物和饲料均由中南大学实验动物中心提供。
1.2 方法
1.2.1 热源性试验[8]在12只家兔中挑选8只健康家兔。考察标准:试验前在实验室内观察1周,体重不减轻,精神、食欲及排泄等无异常现象,雌兔无孕。将所选健康家兔在17~28℃室温条件下继续饲养3 d,给药前用电子温度计测定直肠温度4次(1 h/次),每次体温均应在38.0~39.6℃之间,据此挑选出符合要求的家兔3只。测定正常体温后15 min内,将温热至38℃的复方环丙沙星乳剂按0.5 mg/kg剂量后肢肌肉注射,然后进行1 h/次测温,共测4次,每次在1.5 min内完成。
1.2.2 溶血性试验(体外试管法)[9-13]红细胞混悬液的制备:选取健康家兔1只,心脏采血20 mL,用玻璃棒搅拌血液除去纤维蛋白,制成脱纤血液。然后将脱纤血液移入刻度离心管内,加入其10倍量0.9%氯化钠注射液,混合后2000 r/min离心10 min,弃去上清液。沉淀的红细胞再用0.9%氯化钠注射液按上述方法反复洗涤2~3次,直至上清液呈无色透明为止。将所得红细胞按其容积用0.9%氯化钠注射液稀释成2%的红细胞混悬液,供后续试验用。操作步骤:取洁净试管7支,编号排列于试管架上。第1~5号管为受试管,第6号管为0.9%氯化钠注射液对照管(阴性对照管),第7号管为蒸馏水溶血对照管(阳性对照管)。各试管中各组分加入量如表1所示。按表1依次加入2%红细胞混悬液、0.9%氯化钠注射液。将两者混匀后,置于(37±0.5)℃恒温箱中30 min;然后分别加入不同量的复方环丙沙星乳剂,再摇匀,置(37±0.5)℃的恒温箱中进行温育。分别于15、30、45、60、120、180 min观察实验结果,对照表2的判断标准并记录结果。

表1 溶血性试验设计
结果判定标准:当阴性对照管未见溶血和凝集,阳性对照管出现完全溶血,且受试物管的溶液在3 h内不发生溶血和凝集时,表明受试物可以用于注射;若受试物管的溶液在3 h内发生溶血和(或)凝集,则受试物不宜用于注射。溶血性结果判定标准如表2所示。

表2 溶血性结果判定标准
1.2.3 肌肉刺激性试验[9-13]取健康家兔6只,随机分为3组,每组雌雄各半。采用兔腿肌肉注射法,于家兔后肢左侧股四头肌注射0.5 mL/kg的复方环丙沙星乳剂,后肢右侧同一部位注射等量的0.9%氯化钠注射液作同体左右侧自身对比。注射时以30°~45°角度进针为宜。在给药48 h后,取雌雄各2只由耳静脉注入空气处死家兔,剖解取出股四头肌,纵向切开,观察注射部位肌肉组织的反应情况,并按表3确定反应级数。剩余2只家兔继续观察14 d,了解刺激性反应的可逆程度,必要时进行病理组织学检查。

表3 肌肉刺激反应分级
结果判定标准:当家兔的平均反应级数在2以下者,判断该注射样品可作肌肉注射;平均反应级数大于3者,判断该注射样品不能供肌肉注射;平均反应级数在2~3级之间者,可进行重复试验或结合其他指标综合考虑。
1.2.4 全身主动过敏性试验[9-13]取体重为300±50 g的健康豚鼠随机分为3组,每组6只,雌雄各半。供试组豚鼠腹腔注射复方环丙沙星乳剂,阴性对照组豚鼠腹腔注射0.9%氯化钠注射液,阳性对照组腹腔注射1%卵蛋白液。0.5 mL/只,隔日注射,共3次致敏。在末次给药后10 d,对每组豚鼠以2倍致敏计量的相应试剂分别于后脚掌外侧静脉进行激发,观察静脉注射后各组豚鼠30 min内的反应及相关症状出现和消失的时间。按全身致敏性评价标准进行评价并判断过敏反应发生程度(表4)。

表4 全身过敏性反应评价标准表
2 结果
2.1 热源性试验 对家兔注射温热复方环丙沙星乳剂后,测得体温数据如表5所示。

表5 热源性试验结果 ℃
由表5可见,1~3号家兔给药前后体温差分别为0.1℃、0.3℃、0.3℃,均小于0.5℃,且3只家兔体温升高总和为0.7℃,小于1.4℃,符合《中华人民共和国药典》规定[14]。结果表明,复方环丙沙星乳剂对家兔无热源反应。
2.2 溶血性试验 分别在 15、30、45、60、120、180 min观察各支试管,溶血性试验判断结果为:6号管(阴性对照管)无溶血和凝集现象,振摇后均匀分散;7号管(阳性对照管)发生全溶血;1~5号供试品管在3 h内均不发生溶血和凝集反应。结果表明,复方环丙沙星乳剂对家兔红细胞无溶血和凝集现象,可供注射使用。
2.3 肌肉刺激性试验 注射给药后48 h内肉眼观察,4只家兔注射局部肌肉均未出现红肿、变性、坏死等严重反应,个别注射局部肌肉可见轻微充血,但不明显。处死家兔,切开股四头肌观察显示:0.9%氯化钠注射液对照组平均反应级数为0.25;供试药组(复方环丙沙星乳剂)平均反应级数为0.5。0.5远小于2,表明复方环丙沙星乳剂对家兔肌肉注射给药的局部刺激性很小,可用作肌肉注射。家兔在注射过程中未见全身不良反应,剩余2只同样处理的家兔在恢复14 d后肌肉状态恢复正常,未见任何病理变化。具体结果如表6所示。
2.4 全身主动过敏试验 在末次给药第10天激发过敏反应后,可见阳性对照组中5只豚鼠出现躁动、竖毛、颤抖、持续咳嗽、甚至呼吸困难、排尿、步态不稳、痉挛、休克死亡等现象,则判断其过敏反应为极强阳性(++++),另外1只出现休克死亡之外的所有过敏反应,则判断其过敏反应为强阳性(+++)。供试药组(复方环丙沙星乳剂)和阴性对照组(0.9%氯化钠注射液)豚鼠则表现正常,未出现任何过敏反应症状,则判断其过敏反应为阴性。表明复方环丙沙星乳剂无全身主动过敏反应,可供临床注射使用。具体结果如表7所示。
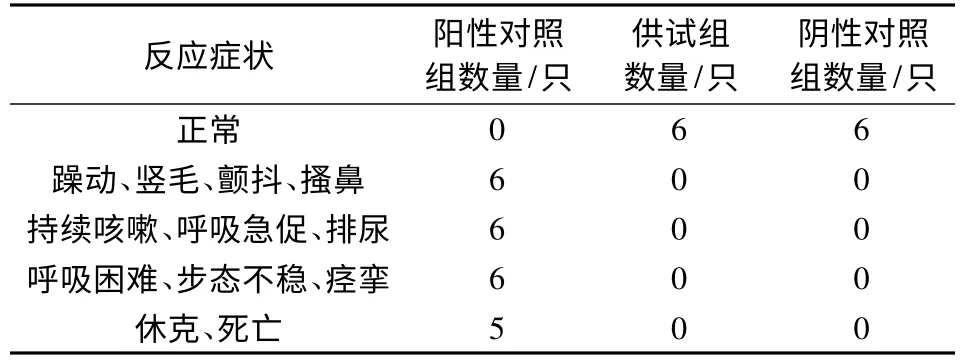
表7 各组豚鼠全身主动过敏反应及其数量表
3 分析与小结
环丙沙星在兽医临床上主要有两种剂型:可溶性粉和注射液[15]。环丙沙星除了剂型较少外,单药环丙沙星又存在严重的耐药性问题;加之环丙沙星易溶于水,所以制成口服干乳剂、微乳、亚微乳就比较困难。所以本实验室研究出了复方环丙沙星注射乳剂,目的是为兽医临床提供一种高效、安全、质量稳定的环丙沙星新制剂。
复方是指两种或两种以上的药物混合制剂,可以是中药、西药或中西药混合。这样处方中出现的各种药物可以最大程度的发挥单药的药效;同时因为每种成分的用药量相对减少,还可以减少临床上耐药性等问题的发生。
乳剂(emulsions)是指互不相容的液体组成的非均相分散体系。乳剂由水相(W)、油相(O)和乳化剂组成,三者缺一不可。根据乳化剂的种类、性质及各相体积比形成水包油(O/W)、油包水(W/O)型。也可以制备成复乳,如O/W/O或W/O/W型。乳剂较非乳剂的优点在于:①药物包被于乳剂内相中,可以减少空气对药物的污染或氧化,同时,用药后释放缓慢,可减低畜禽药物中毒的几率;②对于患病畜禽不吃食、不饮水时,注射给药是比较有效的给药方式;③对于半衰期短或需要频繁给药的药物,可以减少给药次数,药物可以在体内维持较长的时间;④注射缓释乳剂后,血药浓度可以长时间维持有效浓度,避免出现峰谷现象,更利于降低药物的毒副作用,从而更能保证药物的安全性和有效性;⑤可减少用药的总剂量,即用较小的剂量就可以达到较好的药效。
不同的给药途径,乳剂的质量要求也不相同,很难制定统一的质量标准。但是对乳剂的质量有一个基本的评定。其中包括:乳剂粒径大小、稳定性、pH 值及通针性等[16]。
在此之前,本实验室已做了复方环丙沙星乳剂的性状研究,结果表明其为淡黄色、油乳状,pH值在6.3~6.5之间,颗粒评价大小为7.6 μm,稳定性和通针性均良好,且体外抗菌效果显著强于复方环丙沙星注射液(P<0.01)。所以有必要对该制剂做进一步的安全性考察,以确定其在临床上的可用性。动物的红细胞体外溶血性、局部刺激性、热源反应、过敏性及急性毒性反应,是新药临床前安全性评价的重要组成部分。
通过对复方环丙沙星乳剂进行上述安全性评价试验,结果显示:复方环丙沙星乳剂对家兔肌肉注射给药不产生热源反应;对家兔脱纤红细胞无体外溶血性或凝集反应;对家兔后肢肌肉注射给药不产生明显的肌肉刺激性反应;对豚鼠进行腹腔注射也不产生明显全身过敏性反应。由此可见,本实验室研制的复方环丙沙星乳剂可以通过注射给药达到安全、有效等临床用药要求,值得在临床上推广应用。
[1]陈杖榴,袁忠辉,曾振灵,等.兽医药理学[M].北京:中国农业出版社,2003:239.
[2]陶金忠,杨国林,赵兴绪,等.盐酸环丙沙星在子宫内膜炎奶牛乳腺排泄的研究[J].动物医学进展,2008,29(2):6-9.
[3]Denis A,Mitchison M D.Fluoroquinolones in the treatment of tuberculosis:A study in mice[J].American J Respiratory and Critical Care Medicine,2004,169:334-335.
[4]陈新谦,金有豫,汤 光,等.新编药物学[M].第14版.北京:人民卫生出版社,1997:93.
[5]蔡卓倩,陆基宗.喹诺酮类抗菌素的新进展和临床应用[J].药品评价,2006,3(3):220-222.
[6]赵贡瑞.环丙沙星的临床应用[J].医学导刊,2006,20(14):108-109.
[7]王开贞.药理学[M].北京:人民卫生出版社,2010:257.
[8]李孝文,李佳缘,杨 亮,等.复方环丙沙星乳剂急性毒性试验[J].动物医学进展,2010,31(11):56-58.
[9]孙志良,罗永煌.兽医药理学实验教程[M].北京:中国农业大学出版社,2006:38-41.
[10]陈 奇.中药药理研究方法学[M].北京:人民卫生出版社,1996:112-170.
[11]魏海涛,于慧敏,钟家林,等.氟苯尼考悬乳剂的安全试验研究[J].中国兽药杂志,2009,43(8):25-27.
[12]GPT4-1.化学药物刺激性、过敏性和溶血性研究技术指导原则[S].
[13]GPT4-1.中药、天然药物刺激性和溶血性研究的技术指导原则[S].
[14]中华人民共和国药典委员会.中华人民共和国药典二部[M].北京:化学工业出版社,2005.
[15]中国兽药典委员会.兽药使用指南化学药品卷2005年版[M].北京:中国农业出版社,2005:4.
[16]崔福德,陆 彬,张 强,等.药剂学[M].第5版.北京:人民卫生出版社,2003:38.
