HPLC法测定肤疾洗剂中苦参碱的含量
2012-11-21张智军马久太
张智军 崔 华 马久太
(1陕西省彬县食品药品监督管理局,陕西省彬县西大街老政府院内,713500;2陕西摩美得制药有限公司;3陕西步长制药有限公司)
肤疾洗剂由苦参、百部、花椒、白鲜皮、硼砂、雄黄等6味中药组成,具有解毒杀虫、止痒收敛、活血祛瘀的功能,主治疥疮、湿疹、脂溢性皮炎、瘙痒性皮肤病及花斑癣[1]。为了更好地控制产品质量,我们在其原质量标准的基础上,对苦参碱的含量测定方法,进行了方法学研究。报道如下。
1 仪器与试剂
1.1 仪器 高效液相色谱仪(岛津LC-20AD),色谱工作站(岛津LC-solution),紫外检测器(岛津SPDM20A),电子天平(梅特勒-奥豪斯AR1140)。
1.2 试剂 苦参碱对照品(购于中国药品生物制品检定所,批号110805-200906),肤疾洗剂(陕西摩美得制药有限公司生产,批号 110305、110307、110309、110311、110313),乙腈为色谱纯,用水为重蒸水,其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件及系统适用性试验 用十八烷基硅烷键合硅胶为填充剂;检测波长220nm;0.016mol·L-1磷酸二氢钾溶液-0.016mol·L-1十二烷基硫酸钠溶液-乙腈(30︰30︰35)为流动相;流速1.0mL·min-1;理论塔板数以苦参碱计算应不低于3000。上述色谱条件下供试品分离度高,阴性无干扰。
2.2 供试品溶液的制备 精密吸取肤疾洗剂10mL,用稀盐酸调pH值至3~4,以石油醚(60℃ ~90℃)萃取3次,每次20mL,弃去石油醚液,水层用0.5%氢氧化钠溶液调pH值至9~10,用三氯甲烷萃取3次,每次20mL,合并三氯甲烷层,加无水硫酸钠脱水,三氯甲烷液蒸至3mL,过中性氧化铝柱(100~200目,10g,内径1cm),以三氯甲烷50mL洗脱,收集洗脱液,回收溶剂至干,残渣加甲醇使溶解,转移至10mL量瓶中,稀释至刻度,摇匀,微孔滤膜(0.45μm)滤过,取续滤液作为供试品溶液。
2.3 线性关系考察 精密称取苦参碱对照品10.30mg,置10mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,制得对照品备用液。精密吸取备用液各0.25mL、0.5mL、1.0mL、1.5mL、2.0mL、2.5mL,置10mL量瓶中,加甲醇稀释至刻度,摇匀,制得苦参碱对照品溶液。吸取对照品溶液各20μL,分别注入液相色谱仪,记录峰面积,结果见表1。

表1 苦参碱线性关系考察
以C代表进样量、A代表峰面积,计算回归方程为A=1427718.13C+148727.67,r=0.9999;苦参碱在0.515~5.15μg之间有良好的线性关系,标准曲线见图1。
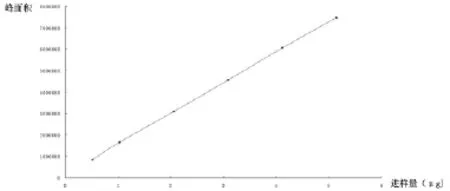
图1 苦参碱标准曲线
2.4 精密度试验 吸取苦参碱对照品溶液(浓度0.103mg·mL-1)20μL,按照上述色谱条件,注入液相色谱仪中,连续进样6次,记录峰面积,结果见表2。
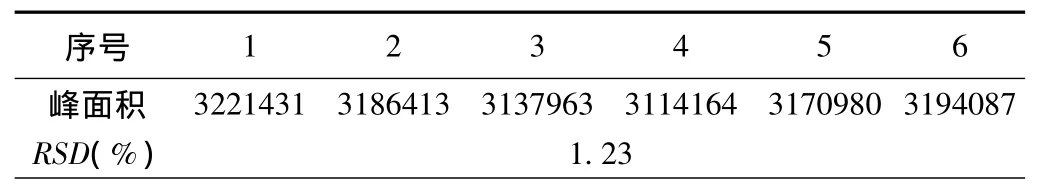
表2 精密度试验
结果表明对照品溶液峰面积RSD为1.23%,本方法精密度良好。
2.5 稳定性试验 取样品(批号110305),按照上述方法制备供试品溶液,在上述色谱条件下分别于0、2、4、8、16h时注入液相色谱仪中,进样量10μL,记录峰面积,结果见表3。

表3 稳定性试验
结果表明供试品溶液峰面积在16h内RSD为1.42%,本方法稳定性良好。
2.6 重现性试验 精密吸取样品(批号110305)10mL 5份,制备供试品溶液,按照上述色谱条件,注入液相色谱仪中,进样量10μl,记录峰面积,结果见表4。
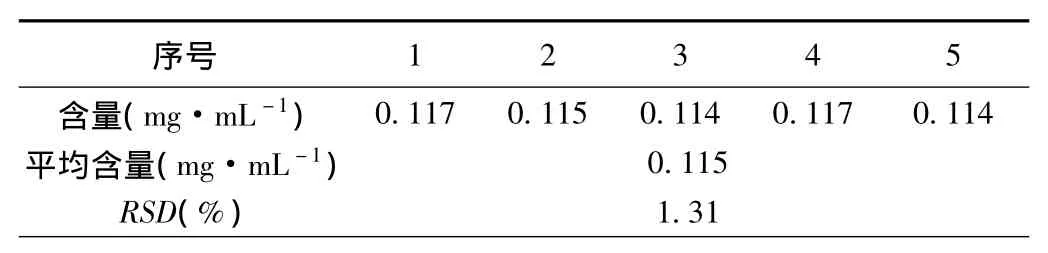
表4 重现性试验
结果表明样品含量的RSD为1.31%,本方法重现性良好。
2.7 回收率试验 精密吸取样品(批号110305)10mL 6份,分别精密加入样品中含量80%、100%和120%的苦参碱对照品,制备供试品溶液,按照上述色谱条件,注入液相色谱仪中,记录峰面积,结果见表5。
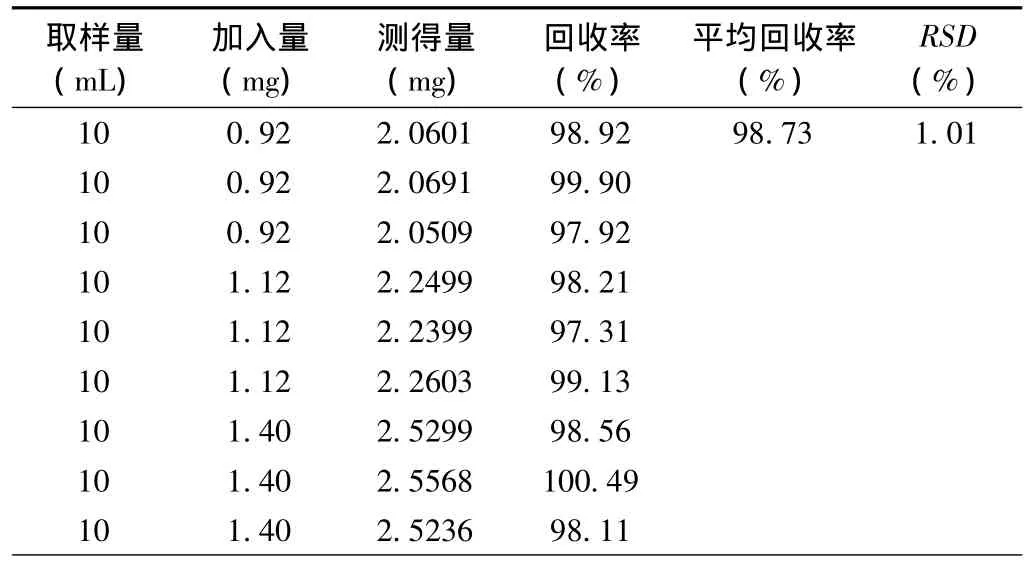
表5 回收率试验结果
结果表明平均回收率为98.73%,RSD为1.01%,本方法回收率良好。
2.8 样品测定 按照上述方法制备供试品溶液,参照上述色谱条件操作,测定苦参碱含量,结果见表6。
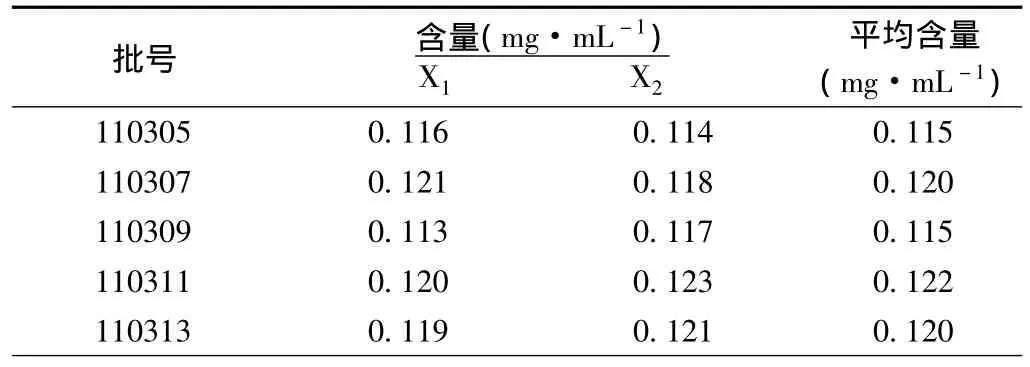
表6 肤疾洗剂中苦参碱含量测定
药品的质量受药材、生产设备、工艺等多种因素影响,根据5批肤疾洗剂的含量测定结果,在其含量平均值0.118mg·mL-1的基础上,以70%转移率计算,暂定肤疾洗剂中苦参碱含量限度为每1mL不得低于0.08mg。
3 结论
肤疾洗剂中的君药苦参,含有多种生物碱,其中苦参碱、氧化苦参碱具有抗肿瘤、抗炎、抑制皮肤过敏反应等作用[2]。原质量标准中没有含量测定项目,为了更好地控制产品质量,我们对苦参中的有效成分进行了含量测定。苦参碱含量测定方法有薄层扫描法[3]、高效液相色谱法[4]等,本产品采用高效液相色谱法对肤疾洗剂中苦参碱的含量进行了测定,结果表明方法准确、简便、快速,平均回收率为 98.73%,RSD为1.01%。
试验中曾考察了苦参碱不同的提取方法[4-5],结果以萃取提取所得到的苦参碱含量高于蒸干后回流提取法,这与苦参碱遇热不稳定有很大关系。同时由于本品为复方制剂,所含成分复杂,为有效去除杂质,我们采用了萃取加过中性氧化铝小柱方法,排除了干扰。实验中[4,6-8]曾选用乙腈 - 无水乙醇 -3% 磷酸溶液(80∶10∶10)、甲醇 - 水 - 三乙胺(105∶95∶0.04)、0.016moL·L-1磷酸二氢钾 - 0.016moL·L-1十二烷基硫酸钠-乙腈(30∶30∶35)为流动相,结果前两个条件未能达到满意的分离效果,后者分离度好,阴性无干扰,所以实验最终选用后者为流动相。
在含量测定研究过程中,发现肤疾洗剂中的氧化苦参碱几乎检测不到,可能是氧化苦参碱在药品生产过程中分解或转化为苦参碱,这与文献报到是基本一致的[3,9-10],所以后期没有对氧化苦参碱进行含量测定的方法学研究。
[1]肤疾洗剂质量标准(标准编号WS3-B-2918-98).中华人民共和国卫生部部颁标准《中药成方制剂》第十五册[S].1998:111.
[2]苗抗立,张建中,董颖.苦参的化学成分及药理的研究进展[J].天然产物研究与开发,2000,13(2):69 -73.
[3]贾敏鸽,孙文基.苦参及其复方中苦参碱与氧化苦参碱的转化研究[J].药物分析杂志,2003,23(2):90.
[4]国家药典委员会.中华人民共和国药典2010年版一部[S].化学工业出版社:188-189.
[5]赵骏,齐喜红.生物碱提取方法研究概述[J].天津中医学学报,2003,22(4):43 -44.
[6]匡海学.中药化学[M].北京:中国中医药出版社,2003:148-149.
[7]张蕾,陈晓辉,李娟.RP-HPLC法测定苦参中苦参碱的含量[J].沈阳药科大学学报,2005,22(1):33 -35.
[8]蒋珍藕.苦参碱的提取工艺及测定方法的研究进展[J].中医药导报,2005,11(8):90 -94.
[9]陆蕴如,杨钟柯,董育妹.苦参在复方中化学成分变化的研究[J].中国中药杂志,1996,21(7):412.
[10]宋小妹,考玉萍.洁身洗剂中苦参化学成分转化研究[J].西北药学杂志,2000,15(6):257.
