基本药物电子监管政策实施影响因素研究
——基于南京市的实证调研
2012-11-11丁锦希詹来明
丁锦希 詹来明 蒋 蓉 陆 慧 高 强
1.中国药科大学国际医药商学院,江苏南京 211198;2.江苏省南京市食品药品监督管理局,江苏南京 211198
基本药物电子监管政策实施影响因素研究
——基于南京市的实证调研
丁锦希1詹来明1蒋 蓉1陆 慧1高 强2
1.中国药科大学国际医药商学院,江苏南京 211198;2.江苏省南京市食品药品监督管理局,江苏南京 211198
目的探索影响医药企业实施药品电子监管政策的关键因素,为相关部门制订和完善监管政策提供依据。 方法构建药品电子监管实施影响因素指标体系,运用因子分析法进行定量分析,筛选影响药品电子实施的关键因素。 结果 实证分析发现影响电子监管政策实施的关键影响因素包括:药品管理法、专门规章、初次投入、标签成本、招标采购、技术标准和信息安全。 结论 政府部门在药品电子监管推进过程中,应针对上述关键因素制订相应的政策措施,以促进药品全品种、全过程电子监管目标如期实现。
药品电子监管政策;基本药物制度;因子分析
药品电子监管是新世纪信息化时代下的一种新型药品监管模式,其运用现代信息、网络、编码技术为药品最小包装单位建立唯一性的电子身份标识,将药品生产、流通环节的数据信息进行电子化、标准化处理,构建从药品生产企业、物流配送、批发企业、零售药店、医疗机构到消费者的全程电子化网络[1]。实施药品电子监管意义重大,通过它可以保证我国药品生产、流通和使用全程质量可控可追溯;有效打击生产、销售假劣药行为;实现问题药品快速召回;规范药品流通秩序,控制药价虚高;防止药物滥用、保障消费者用药安全;可推进医药卫生体制改革,提升药品监管能力、监管效率,实现科学监管。
自2006年实施药品电子监管以来,我国已经在打击假劣药和药品召回方面取得了一定成效。2008~2010这三年间,每年假药下降比例分别达18%、26%和63%;药品召回效率也大大提高。如实施电子监管政策后,狂犬疫苗在更短的时间实现了所有问题产品的有效召回。
尽管如此,我国药品电子监管政策在实施过程中仍然暴露出一些问题,主要体现在监管体系仍不健全等方面,导致许多生产、经营企业实施意愿不强,部分企业甚至出现消极被动的态度。因此,总结前期药品电子监管经验,继续完善现有政策不足之处,对十二五期间药品电子监管的顺利推进意义重大。本文通过因子分析法,探索影响医药企业执行药品电子监管政策的关键因素,并对其作详细分析,以期为政府进一步完善电子监管政策提供参考。
1 研究设计
1.1 电子监管实施影响因素指标构建
关于医药企业实施电子监管的影响因素,我国学者作了一定研究。陈芳等[2]从法律保障角度认为,目前药监部门只能通过行政命令或部门文件开展监管,欠缺效力等级高的法律法规是企业实施电子监管意愿不强的重要原因。王永荣等[3]及王静等[4]从生产经营的角度认为,实施药品电子监管给生产、经营企业带来成本的增加是影响其实施电子监管的最主要因素,这些成本来自生产线改造、购买赋码扫描设备、印刷费用、增加人力等方面。胡芳[5]认为限制未入网基本药物参与招标采购对制药企业加入电子监管网具有强制性促进作用。孙淑琴等[6]从信息安全角度认为,实施电子监管可能会造成企业商业信息泄露,进而不利于企业积极实施电子监管。徐徕等[7]认为实施电子监管会带来工序的增加,给企业原有运营流程造成一定的冲击,降低运营效力,这些因素亦会显著影响企业实施电子监管的积极性。
笔者在文献研究基础上,结合前期调研的专家意见,从政府与企业两个角度,分别总结了其与电子监管实施相关的影响因素见表1。

表1 药品电子监管实施影响因素
1.2 调研对象及样本来源
江苏省作为我国生物医药产业大省,其产业发展和政策实施都走在全国前列。早在2007年,江苏省就已实施药品电子监管制度,在全国起到了一定表率作用。其中南京市共有药品生产企业66家,近一半都参与基本药物生产,涉及品种359个,品规499个,占江苏省基本药物总品种的比重约60%,品种较为齐全。因此通过分析南京市药品电子监管实施影响因素,可客观反映我国药品电子监管政策的实施现状和不足。
本文选取南京市基本药物生产企业的企业负责人和电子监管工作负责人为实证调研对象,共发放问卷150份,回收有效问卷105份。调研对象基本情况见图1~4。
本次调研的受访者所在企业涉及国有企业、民营企业、合资企业及外商独资企业(图1),企业规模涵盖大、中、小三个层次(图2),分布较为全面。此外,受访者所在企业的主营业务完全覆盖了化学药、中药、生物药和原料药(图3),受访者职称分布也较合理(图4)。因此,我国医药企业电子监管政策实施影响因素能在本次调研中得到典型反映。
2 数据分析
本文选用因子分析法,并运SPSS 11.5统计软件对调研结果进行测算分析。因子分析是以最少的信息丢失为前提,将大量原有变量按内在联系综合成较少的几个综合指标的统计分析方法,适用于多变量实证分析。本文为全面、完整地刻画电子监管实施的影响因素,总结了多项二级指标。通过因子分析能将多项二级指标按内在联系归结为较少的几个因子,并得到各因子的影响权重,进而为政策分析提供量化数据支撑。

2.1 影响因素初步筛选
二级指标中27项因素对药品电子监管实施的影响程度大小不同,笔者通过总体均值分析去除一些均值较小的影响因素,初步筛选出对药品电子监管实施意愿影响较大的因素进入模型。调研题目采用5级李克特量表打分测量,根据该赋值特点,总体均值小于3的因素可被认为影响很小,应予以删除。通过SPSS 11.5进行均值计算得到总体均值小于3的因素有 7 个, 依次为:X20、X26、X21、X23、X22、X19、X18。其余20个因素总体均值都大于3,进入分析模型。
2.2 信度和效度检验
本次量表 Cronbach′sα系数值为 0.898 9,Bartlett球体检验统计值的概率和KMO值分别为0与0.649,表明测量工具内部一致性较高,问卷信度良好,提示适合进行因子分析。
2.3 公因子提取和因子载荷矩阵求解
由表2可知5个因子共解释了原有变量总方差的76.145%。总体上,原有变量信息丢失较少,因子分析效果较理想。

表2 解释的总方差
若将纳入因子分析的影响企业实施电子监管积极性的20项因素综合表示为F综合,则F综合的数学模型如下:
F综合=0.207 15因子1+0.175 60因子2+0.148 64因子3+0.121 73因子 4+0.108 33因子5(式1)。
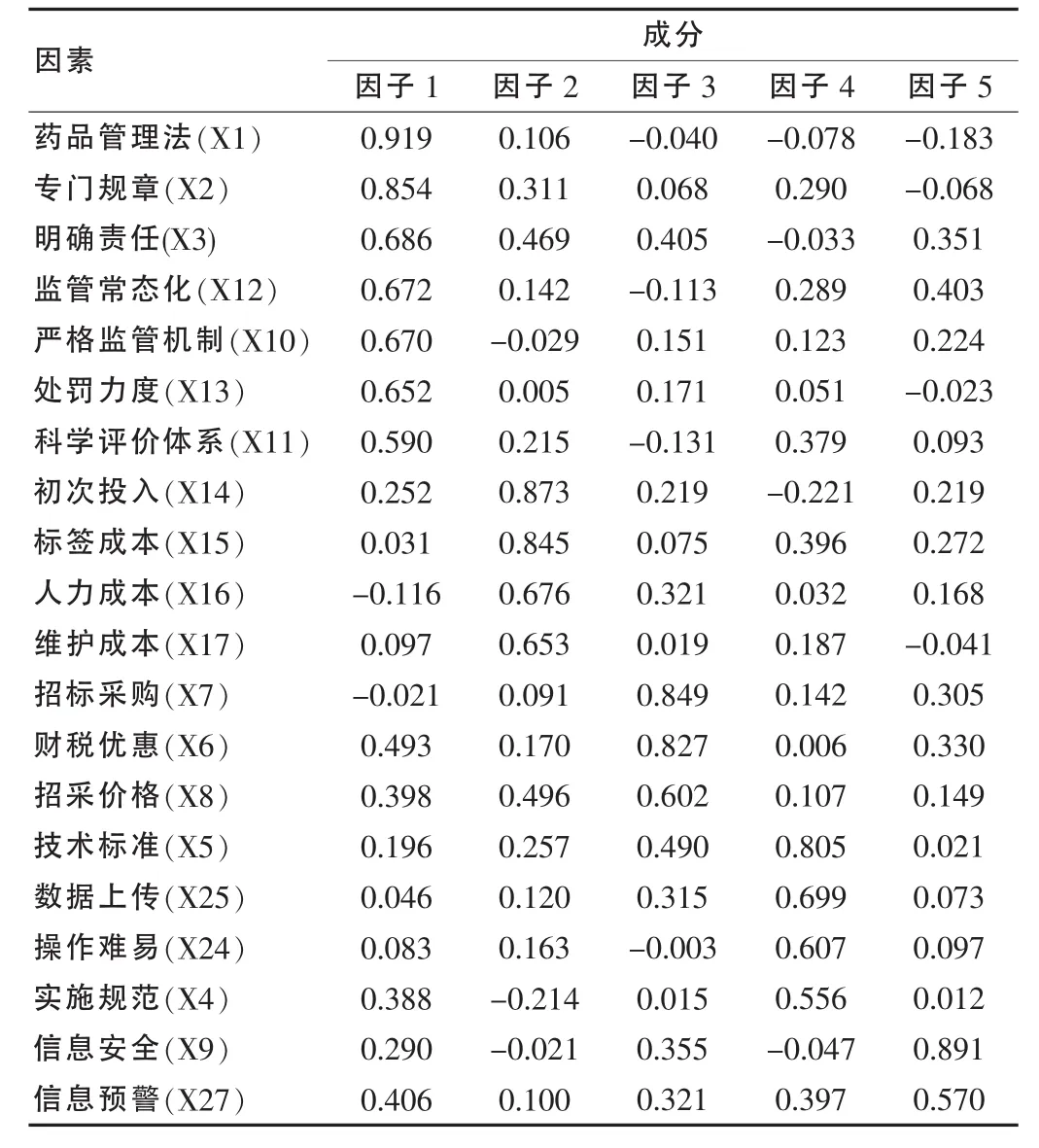
表3 旋转后的因子载荷矩阵
由表2、3 可知, 依次提取 Fact1、Fact2、Fact3、Fact4 及Fact5五个公因子是合适的。
因子 1 主要由 7 个因素(X1、X2、X3、X12、X10、X13、X11)决定,主要反映法律法规的影响,故命名为法律保障因子。
因子 2 主要由 4 个因素(X14、X15、X16、X17)决定,主要反映各种成本对企业实施药品电子监管的影响,故命名为成本因子。
因子 3 主要由 3个因素(X7、X6、X8)决定,主要反映药品销售环节相关制度的影响,故命名为销售保障因子。
因子 4 主要由 4 个主要因素(X5、X25、X24、X4)决定,主要反映药品电子监管系统技术层面因素的影响,故命名为技术因子。
因子5主要由 2个因素(X9、X27)决定,主要反映入网企业商业信息安全保障的影响,故命名为信息安全保障因子。
3 讨论
由式1可知,5个公因子对药品生产企业电子监管实施意愿均有不同程度的影响,按影响权重由大到小依次为因子1、2、3、4、5。
3.1 法律保障因子
法律保障因子(因子1)影响权重(0.207 15)最大,即企业是否积极实施药品电子监管的首要影响因素是国家颁布的法律法规,其影响甚至起决定性的作用。此结果符合我国实际情况,因为法律法规具有强制约束力,是政策实施的保障和依据,将药品电子监管政策写入法规文件会赋予电子监管政策更高的效力等级,从而促进企业积极实施该政策。
在政策法规因子中,药品管理法(X1)和专门规章(X2)是最关键因素。《药品管理法》是我国目前具有最高法律效力的药品监督管理规范性文件,是我国药品管理的基本法。将药品电子监管写入《药品管理法》将赋予其在药事法体系中最高的法律效力,会对电子监管的主客体都产生强有力的约束力,进而保障电子监管顺利推进。由于《药品管理法》是基本法,它只能确立药品电子监管的基本原则和总体目标,明确其法律地位和法律责任,具体到微观层面,还有有必要出台专门规章,以有助于实践层面的操作。
然而,我国目前尚未将药品电子监管政策写入法律法规或者针对其出台相关规章,加快药品电子监管立法已迫在眉睫。值得期待的是,药品电子监管“十二五”规划已明确提出“在《药品管理法》等相关法律法规的修订中进一步明确药品电子监管的必要性”。
3.2 成本因子
成本因子(因子2)的影响权重(0.175 60)仅次于因子1。企业以盈利为导向,成本是企业制定决策的关键依据,当实施电子监管带来的成本增加超过一定限度,企业对电子监管的态度必然趋于消极,所以成本因子对企业电子实施意愿有显著影响也能得到很好的解释。
根据调查显示,目前企业实施电子监管的成本主要存在于初次投入(X14)和标签成本(X15)两个部分。初次投入指企业为实施电子监管进行软、硬件改造产生的成本,属于一次性投入。企业每条生产线改造成本为30万~50万,对企业资金要求高,许多中小企业往往因此而产生较大的经营压力。标签成本属于长期成本,此类成本对价格低、利润空间小的基本药物影响显著。目前这两类成本完全由企业单独承担,政府尚未出台相关政策分担企业的成本,巨大的成本负担严重影响了企业实施电子监管政策的积极性。
3.3 销售保障因子
销售保障因子(因子3)的影响比较显著,影响权重为(0.148 64)。销售保障因子即指在销售环节对实施电子监管的产品给予特殊的政策支持,如优先考虑招标采购,认可产品质量、允许电子监管成本加入成本核算等。
基本药物主要通过招标采购进入销售渠道。目前,国家仅有政策要求未加入电子监管网的药品不得参加招标采购,但并未出台相关政策对中标的实施电子监管的药品在定价、医保目录遴选等方面给予一定的配套支持,大大影响了企业实施该政策的内在驱动力。
3.4 技术因子
技术因子(因子4)的影响权重为(0.121 73),反映技术层面的因素同样具有重要影响。药品电子监管系统是集信息技术、网络技术、编码技术于一体的技术系统。技术因子反映了电子监管技术系统的标准化、完善性、方便性等因素对企业电子监管实施意愿的影响。
技术因子是对所有技术因素的概括,本研究得出技术标准(X5)是技术因子中的最关键因素。另外,我国药品电子监管码为一维条形码,尚存在技术信息容量小,防伪性、便捷性不足等缺点。电子监管信息平台的可靠性、实用性、易用性、也有待进一步提高。统一药品电子监管技术标准能保障药品电子监管工作各参与方在统一的技术框架下开展工作,提高工作效率和成果的可靠性,所以技术标准对电子监管推进具有重要影响。
3.5 信息安全保障因子
信息安全保障因子(因子5)的影响权重为0.108 33,虽然该因子在五个因素中的影响权重最小,但由于药品电子监管系统包含了大量入网企业的生产、经营信息、核注核销信息、预警信息,这些信息往往是企业赖以生存的核心信息。充分保障信息安全是企业愿意积极加入药品电子监管网的前提,笔者认为药品监管管理部门应当制订相应措施保证实施电子监管企业的信息安全。
通过电子监管系统可追溯的企业产品的流向、发货量等商业信息,无形之中对企业的商业秘密带来一定隐患,本研究中企业虽然认为信息安全保障因子对实施基本药物电子监管的影响权重较小,笔者认为其中原因是企业尚未意识到电子监管系统中所潜在的大量商业秘密,因此强化信息安全保障体系建设应是药监部门的重点任务。
4 对策建议
4.1 完善药品电子监管法律保障体系
实施药品电子监管不是一个短期工程,必须形成长效机制。目前,我国药品电子监管推行模式为行政推广而不是依法实施,因此有必要完善电子监管法律保障体系,以促进企业积极加入电子监管网。
笔者建议,首先,将药品电子监管写入《药品管理法》,赋予药品电子监管最高的法律效力,从而对制度执行主体和客体都产生强有力的约束力,保障政策实施效果。其次,在其配套法规《药品管理法实施条例》中进一步加以解释,确定更具有针对性和操作性的要求。最后,应适时出台药品电子监管专门规章,将法律层面和操作层面已经成熟的规范和做法固定下来,成为后来企业实施电子监管的标准。
4.2 出台措施缓解企业实施电子的成本增加
我国制药企业数量多、规模小,很多企业以生产低附加值的仿制药为主。在激烈的竞争环境下,制药企业利润微薄,对于实施药品电子监管带来的成本增加的承受力是有限的。
由表3可知,成本因子中影响最大的就是制药企业进行软硬件改造的初次投入成本和电子监管码标签成本。目前,这两类成本完全由企业自行负担,给中小型企业造成很大的经营压力。从促进医药产业健康发展的角度,推行药品电子监管不应以给制药企业造成无谓的经营压力为代价。笔者建议,在政府不能直接分担这两部分成本的情况下,应当采取补贴或税收抵扣政策,从而间接减轻企业成本,缓解实施电子监管而增加的经营压力。
4.3 在销售环节强制激励企业实施药品电子监管
销售是制药企业运营的重要环节,而集中招标采购又是销售的关键环节。我国基本药物实行集中招标采购制度,同时SFDA将已实施电子监管作为基本药物参与集中招标采购的准入标准,以此强制激励制药企业积极实施药品电子监管。这一措施取得了很好的效果,我国基本药物已于2012年2月底前全部纳入电子监管网。
据此,笔者建议政府继续在药品集中招标采购环节加大强制激励措施,将其适用更多的药品。同时为了防止该强制激励措施对低利润药品造成负面影响,政府可以适当给予低利润药品更高的价格弹性,允许电子监管成本加入成本核算等。在集中招标采购环节外,政府还可以给予实施电子监管的药品更高的质量安全评价,以利于其销售,进而增强企业实施药品电子监管的积极性。
4.4 完善技术保障服务体系建设
药品电子监管网依托于现代信息技术而建立,技术层面的完善性对企业是否愿意积极实施电子监管影响较大。本研究中技术因子显示技术标准、数据上传、操作难易是关键因素。笔者建议政府从这几项因素出发完善电子监管网技术层面的问题,建设技术服务保障体系。首先,应出台全国统一的药品电子监管网技术标准;其次,进行技术攻关,着力提高企业数据上传的效率和成功率;再次,不断提高电子赋码及相关软硬件操作的简便性;最后,SFDA可以建立专门的技术保障服务部门或者委托有资历的专业化公司负责电子监管系统的实施、运营和维护等技术保障服务。
4.5 强化信息安全保障体系建设
药品电子监管系统包含了大量入网企业的生产、经营信息、核注核销信息、预警信息,这些信息往往是企业赖以生存的核心信息。充分保障信息安全是企业愿意积极加入药品电子监管网的前提。笔者建议进一步强化信息安全保障体系建设,依据国家关于加强信息系统安全保护的要求,根据药品电子监管工作实际需要,建设涵盖药品电子监管工作物理环境、网络、系统、应用和管理等各方面的信息安全体系,为药品电子监管工作提供统一、稳定、高效的安全保障体系。
[1] 郑平华.制药企业药品电子监管的实施[J].上海医药,2010,31(11):501-503.
[2]陈芳,陈玉文.完善药品电子监管的建议[J].食品药品监管,2010,19(16):4-5.
[3]王永容,张润洪.关于我国实行药品电子监管的行业影响力思考[J].首都医药,2012,13(2):14.
[4]王静,孟锐.基本药物电子监管相关问题探讨[J].中国药房,2011,22(12):1058.
[5]胡芳.落实新医改重大举措——基本药物力推电子监管码[N].中国医药报,2010-08-19(B01).
[6] 孙淑琴,闫春霞.关于药品远程监管的探讨[J].齐鲁药事,2009,28(9):520.
[7]徐徕,黄伟俊,蒋兰敏.药品电子监管的作用和意义[J].上海医药,2010,31(11):500.
[8]管延羡,郭华.提高药品集中招标采购运行质量的探索[J].中国卫生事业管理,2005,(5):295.
Em pirical analysis of influencing factors for im p lementing drug electronic supervision policy in Jiangsu Province
DING Jinxi1 ZHAN Laiming1 JIANG Rong1 LU Hui1 GAO Qiang2
1.School of International Business,China Pharmaceutical University,Jiangsu Province,Nanjing 211198,China;2.Nanjing Food and Drug Administration,Jiangsu Province,Nanjing 211198,China
Objective To explore the key factors influencing the implementation of drug electronic supervision policy for medical enterprise in Jiangsu Province,and thereby to provide basis for policy-making and improvement on the part of departments concerned.MethodsAn index system of influencing factors for implementing drug electronic supervision was established,and quantitative analysis bymethod of factor analysiswas conducted so as to select key factors influencing the implementation of drug electronic supervision.ResultsKey factors influencing the implementation of drug electronic supervision found by empirical analysis were the pharmaceutical administration law,specialized rules,initial investment,tag cost,public bidding,the technical standards and information security.ConclusionDuring the implementation of drug electronic supervision system,the government should formulate corresponding policies and measures aiming at the above key factors to realize the regulation goal of"all varieties and the overall process"of drug electronic supervision as scheduled.
Drug electronic supervision policy;Essential drug system;Factor analysis
R954
A
1673-7210(2012)11(c)-0005-04
2010年度国家社会科学基金项目(项目名称:创新药物研发科技投入与激励法律制度研究,项目编号:10CFX055);江苏省食品药品监督管理局政策研究课题(项目名称:基本药物制度框架下药品电子监管政策研究——基于江苏省药品电子监管的实证分析,项目编号:20110016)。
丁锦希(1971-),男,博士研究生,中国药科大学国际医药商学院副教授,硕士生导师,药事管理系主任,医药知识产权研究所所长;研究方向:医药政策与法规、医药知识产权。
2012-09-14 本文编辑:卫轲)
