杨梅中硒含量测定的消化方法
2012-11-08蒋步云柴振林吕爱华尚素微朱杰丽
蒋步云,柴振林,吕爱华,尚素微,朱杰丽
(浙江省林产品质量检测站,浙江 杭州 310023)
杨 梅 (Myrica rubra Sieb) 是 杨 梅 科(Myricaceae)杨梅属 (Myrica L.)中的一个种,是我国南方特产果树之一[1],深受广大消费者的喜爱。杨梅营养价值丰富,且有药用价值,含有碳水化合物、有机酸、蛋白质及多种维生素等成分,具有生津止渴、和胃消食、益肾利尿和解暑止泻之功效,同时也具有抗氧化和抗衰老的作用[2-3]。硒是人体必不可少的微量元素之一,具有抗氧化、保护心血管、解毒、防癌和提高免疫力等作用[4-5]。随着科技的进步,人们生活水平的提高,富硒杨梅开始日益走俏。但何谓富硒,杨梅中硒含量究竟有多少等等都是重点关注的问题,因此,准确、快速地测定杨梅中硒的含量显得尤为重要。
目前,测定硒的方法主要有原子光谱法、吸光光度法、荧光光度法、电化学法及色谱法等,各种联用技术也已经用于硒的测定及形态分析[6]。本实验使用的是氢化物原子荧光光谱法。原子荧光法测定的范围宽,具有方法简单、灵敏度高、准确性好的特点[7]。应用氢化物原子荧光光谱法测定必须对样品进行消解,为提高测定结果的正确性和效率,进行了微波消解法和湿法消解 (电热板加热消解)法对测定结果影响的实验。现将有关结果报道如下。
1 材料与方法
1.1 材料
1.1.1 仪器
AFS-930 型双道原子荧光光度计 (北京吉天仪器有限公司),Multiwave3000 微波消解仪 (奥地利安东帕公司),可控式电炉,硒空心阴极灯等。
1.1.2 试剂
硝酸,高氯酸,盐酸 (优级纯),过氧化氢(分析纯),硼氢化钾溶液10 g·L-1,硒标准储备液100 mg·L-1,硒标准使用液0.1 mg·L-1,载流5%盐酸溶液,10 g·L-1铁氰化钾溶液 (掩蔽剂:可明显消除Pb、Cu 的干扰[8]),标准茶叶对照样 (国家标准物质,样品编号GSB-7)。
1.2 方法
1.2.1 原理
样品经酸加热消化后,在6 mol·L-1盐酸介质中,将试样中的六价硒还原成四价硒,用硼氢化钾作还原剂,将四价硒在盐酸介质中还原成硒化氢,由载气(氩气)带入原子化器中进行原子化,在硒空心阴极灯照射下,基态硒原子被激发至高能态,在去活化回到基态时,发射出特征波长的荧光,其荧光强度与硒含量成正比。与标准系列比较定值[9]。
1.2.2 样品制备
取杨梅可食用部分打成匀浆后备用,余样放冷柜冰冻储藏。
1.2.3 样品前处理
湿法消解 (电热板加热消解)。参考 GB 5009.93—2010 食品中硒的测定中第1 法 (氢化物原子荧光光谱法),准确称取处理好的待测试样1~2.000 g 于消化瓶中,加入混合酸 (硝酸∶高氯酸4∶2)10 mL,盖上表面皿冷消化过夜,于次日电炉上加热。当溶液变为澄清透明并伴有白烟时,再继续加热至剩余体积2 mL 左右,不可蒸干。冷却,再加5 mL 6 mol·L-1盐酸,继续加热至溶液变为澄清透明并伴有白烟出现,将六价硒还原成四价硒。冷却,用去离子水定容到25 mL 容量瓶中,待测,同时做试剂空白。
微波消解法。准确称取处理好的待测试样0.5~2.000 g 于微波消解罐内,加混合酸为4 mL硝酸+3 mL 过氧化氢,放置过夜,次日置于微波消解仪器内按设定程序进行消解。当室内温度低于10℃时,应先放于赶酸架上40℃预热10 min 左右,以便微波消解仪能正常启动。程序运行结束后取出反应罐冷却一段时间,放置于赶酸架上120℃赶酸至剩余2 mL 左右时取下,冷却后加入5 mL 6 mol·L-1盐酸溶液,继续放回赶酸架上消化至剩余溶液澄清透明,将六价硒还原成四价硒。取下冷却至室温,0.5%硝酸溶液定容到25 mL 容量瓶中,待测,同时做试剂空白。32 位微波消解仪设置条件经多次试验摸索得到最佳化条件。
1.2.4 测定方法
原子荧光光度计仪器工作条件设置。光电倍增管负高压270 V,屏蔽气流量800 mL·min-1,原子化器温度200℃,读数时间7 s,原子化器高度8 mm,延迟时间1.5 s,灯电流80 mA,测量方式Std.Curve,载气流量400 mL·min-1,读数方式Peak.Area。
标准曲线绘制。取硒标准使用液0.1 mg·L-12.5 mL 到25 mL 容量瓶中,用5%盐酸溶液稀释,加入1 mL 铁氰化钾溶液为掩蔽剂,定容到刻度线,摇匀作为硒的标准工作溶液。仪器设置为自动进样,标准系列分别为1.000,2.000,4.000,6.000 和10.000 μg ·L-1。得出标准系列浓度(x)与荧光强度 (y)的关系式:y=15.225 1x-0.871 1,R2=0.999 8。
样品测定。向2种消化方法 (微波消解法和湿法消解法)消化好后定容到25 mL 容量瓶中的样品溶液内加入1 mL 10 g·L-1铁氰化钾溶液作为掩蔽剂,摇匀,同标准曲线一样上机测定含量。载流为5%盐酸溶液,还原剂为10 g·L-1硼氢化钾溶液。
2 结果与分析
2.1 测定值
标准茶叶对照样GSB-7 经过原子荧光光谱法测定后,2种消化方法对结果的影响见表1。
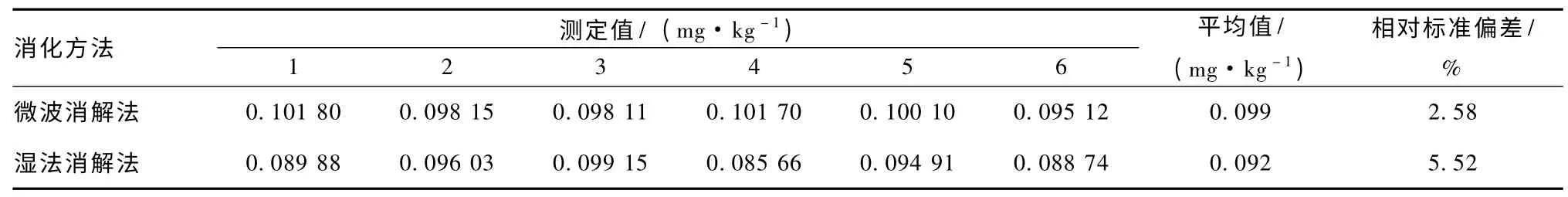
表1 微波消解法和湿法消解法测定标准茶叶对照样的结果
从表1 可知,微波消解法的测定平均值高于湿法消解法 (电热板加热法)的测定平均值,两者都在标准值范围内。微波消解法的相对标准偏差较低,说明微波消解标样更完全更彻底,硒含量损失较少且平行性良好。
从2种消化方法处理后得到的待测杨梅样品测定结果 (表2)来看,同样可得出微波消解法优于湿法消解法。
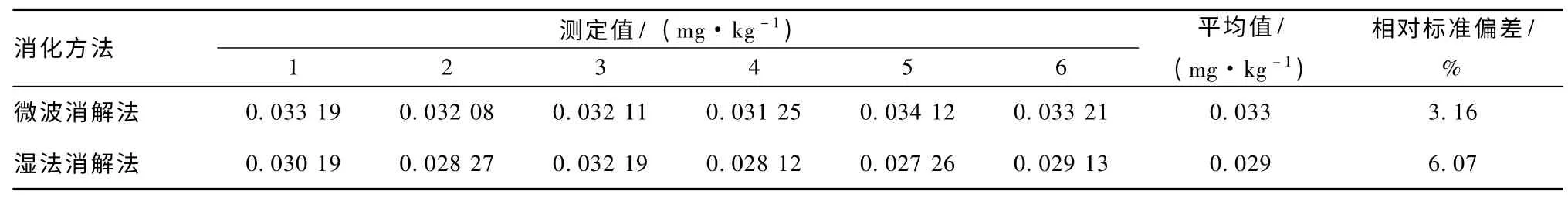
表2 微波消解法和湿法消解法测定杨梅样品的结果
2.2 加标回收率
对微波消解法作为消化方法的标准茶叶对照样进行加标回收试验,3个加标浓度得到的回收率为90%~110% (表3),符合加标回收的要求,说明微波消解法消解杨梅样品是可行有效的。

表3 微波消解法的加标回收率
通过加标回收试验评估样品预处理产生的不确定度。18个加标样品的平均回收率99.33%,标准偏差S 为2.91%,标准不确定度设为U (R),有U (R)=0.008 774,则其相对标准不确定度为U (R)/R=0.008 833。
2.3 精密度
对微波消解法消化标准茶叶对照样进行11 次精密度试验,相对标准偏差为5.11%,说明其符合要求。
3 小结
在杨梅中硒含量测定的过程中,通过2种消化方法的比较,可以看出微波消解相对于湿法消解,具有消耗样品和试剂少、消解彻底、快速简便、准确度高、精密度好等优点,是一种较理想的前处理方法,且污染少更利于操作者的安全[10-11]。因此,杨梅中硒含量测定的消化方法可采用微波消解法。
[1]谢小波,求盈盈,邱立军,等.碱性土壤对杨梅生长结果的影响[J].浙江农业学报,2008,20 (4):261-265.
[2]马瑞,徐丽珊,程跃微,等.不同品种杨梅用途研究[J].山西农业科学,2011,39 (12):1287-1290.
[3]张泽煌,卢新坤,林旗华,等.10个杨梅品种果实糖和氨基酸含量分析[J].浙江农业学报,2011,23 (7):18-20.
[4]李丽辉,林亲录.食品中硒的生理功能及其检测方法[J].食品工程,2007 (1):28-29.
[5]余光辉,温琰茂,何树悠,等.广州市26种水果中硒含量特征分析[J].食品科学,2007,28 (8):344-347.
[6]刘兴艳,马建华,朱静平,等.食品中硒的分析进展[J].微量元素与健康研究,2005,22 (1):26-28.
[7]袁菊,洪涛,陈凤凰,等.微波消解一氢化物发生原子荧光法测定土壤中硒[J].贵州工业职业技术学院学报,2011,6 (1):54-56.
[8]彭新元,朱攀.原子荧光光谱测定土壤中硒的方法研究[J].实用预防医学,2008,15 (5):1599.
[9]GB 5009.93—2010,食品中硒的测定[S].
[10]侯晓芳,迟忠云,王悦霞.氢化物发生原子吸收法测定保健食品中硒含量[J].海峡预防医学杂志,2009,15(1):55-56.
[11]冯信平.热带水果中硒形态分析的不确定度研究[J].热带农业科学,2010,30 (4):8-11.
