离子沉淀法制备菜籽饼粕中多酚的工艺
2012-10-27潘丽军韩智宏赵春华
潘丽军,韩智宏,赵春华,周 俊
(合肥工业大学生物与食品工程学院,安徽省农产品精深加工重点实验室,安徽 合肥 230009)
离子沉淀法制备菜籽饼粕中多酚的工艺
潘丽军,韩智宏,赵春华,周 俊
(合肥工业大学生物与食品工程学院,安徽省农产品精深加工重点实验室,安徽 合肥 230009)
为提高菜籽饼粕的综合利用价值,采用热水浸提结合离子沉淀的方法,对菜籽饼粕中的多酚类物质进行提取纯化,并制备出菜籽多酚。在单因素试验的基础上,通过正交试验得到的最佳浸提工艺条件为浸提温度50℃、浸提时间75min、液料比13:1、浸提2次;浸提液离子沉淀的较适参数组合为氯化锌为沉淀剂、沉淀剂用量为粗提液中多酚质量的1.5倍、pH6.0,在此工艺条件下,获得的菜籽多酚成品为淡黄色粉末,得率1.66%,纯度90.03%。
菜籽多酚;蛋白质;提取;纯化;离子沉淀
油菜是我国重要的油料作物,每年油菜籽榨油后产生的菜籽饼粕达数百万吨[1]。菜籽饼粕中蛋白含量达45%左右,但是由于菜籽多酚、植酸、硫苷等抗营养因子及毒素的存在,大大降低了菜籽饼粕的利用价值[2-4]。多酚类物质具有抗氧化活性,可广泛应用于食品抗氧化、功能性食品、医药等领域[5-8]。从菜籽饼粕中将多酚、植酸等物质分离出来,不但能提高菜籽蛋白的品质,而且有效提升了菜籽饼粕的综合利用价值[9-10]。
目前,对多酚类物质提取的常用方法主要为有机溶剂浸提法,超临界CO2流体萃取法等。有机溶剂法提取效果好,但对环境污染较大、成本较高;超临界CO2萃取法对酚类溶解度强,安全无污染,但设备投入高,萃取量一般只有几升,不宜规模化生产[11-12]。而对多酚类物质纯化的主要方法有沉淀法、膜分离法、层析法等。膜分离法操作简单,环境友好,但产品纯度偏低,膜清洗困难;层析法分离多酚的效果好、选择性强,但操作周期较长;沉淀法生产安全性好、成本低、产品品质较好,但操作条件不好控制,容易造成多酚的损失[13-14]。本实验以菜籽饼粕为原料,采用热水浸提结合离子沉淀的方法制备菜籽多酚,通过提取条件的优化及离子沉淀条件的控制,提高菜籽多酚的得率,为菜籽饼粕的综合利用提供一定的参考依据。
1 材料与方法
1.1 材料与试剂
菜籽饼粕 安徽大平油脂公司。
氯化锌(分析纯) 天津市博迪化工有限公司;无水碳酸钠(分析纯)、盐酸(分析纯) 汕头市西陇化工厂;乙酸乙酯(分析纯) 无锡展望化工试剂有限公司;福林酚(分析纯) 北京素宝来科技有限公司;无水乙醇(分析纯) 上海中试化工总公司。
1.2 仪器与设备
25型数显pH计 上海雷磁创益仪器仪表有限公司;SS300型三足离心机 上海浦东天本离心机设备机械公司;SHY-2A型水浴恒温振荡器 金坛市金城国胜实验仪器厂;721E型分光光度计 上海精密仪器有限公司;DGZ20/4-I型真空干燥箱 南京实验仪器厂。
1.3 方法
1.3.1 菜籽多酚工艺流程
菜籽饼粕→蒸馏水浸提→离心→滤液→离子沉淀→离心→菜籽多酚络合物→酸转溶→乙酸乙酯萃取→脂层→旋转蒸发→真空干燥→菜籽多酚成品
1.3.2 菜籽多酚提取
称取50.0g的脱脂菜籽饼粕(已过60目筛,含水量(9.63±0.19)%),以蒸馏水为浸提剂,控制提取温度、提取时间、液料比、提取次数,在水浴恒温振荡器中提取,转速200r/min,将料液于6000r/min离心20min,得到菜籽多酚粗提液,每组实验重复3次,结果取其平均值。
1.3.3 离子沉淀
取上述多酚粗提液50mL,在室温下,加入离子沉淀剂,控制沉淀剂的种类、沉淀pH值、沉淀剂用量,沉淀完全后立即于6000r/min条件下离心15min,得到菜籽多酚和沉淀剂的络合物沉淀,每组实验重复3次,结果取其平均值。
1.3.4 酸转溶及萃取
向上述络合物沉淀中加入0.5mol/L HCl溶液,使其完全溶解。再向溶解液中加入1.5倍体积的乙酸乙酯萃取,萃取两次。
1.3.5 旋转蒸发及真空干燥
将上述萃取液中的脂相于40℃条件下旋转蒸发,得到菜籽多酚浓缩液,并回收乙酸乙酯;在温度50℃条件下对菜籽多酚浓缩液进行真空干燥,得到菜籽多酚成品。
1.3.6 多酚含量测定以及多酚浸提得率的计算
以没食子酸为标准品,采用Folin-Ciocalteu 比色法[15],并略做改进进行测定。
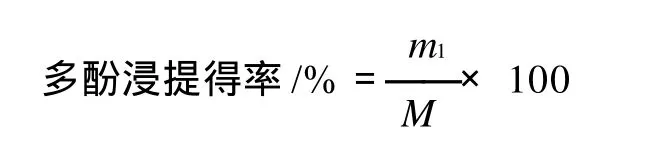
式中:m1为浸提液中多酚质量/g;M为菜籽饼粕质量/g。
1.3.7 多酚沉淀率和总得率的计算

式中:A1为浸提液中多酚初始质量/g;A2为沉淀过后浸提液中多酚质量/g。

式中:m2为多酚成品质量/g;M为菜籽饼粕质量/g。
2 结果与分析
2.1 菜籽多酚浸提单因素试验
2.1.1 浸提温度对多酚得率的影响
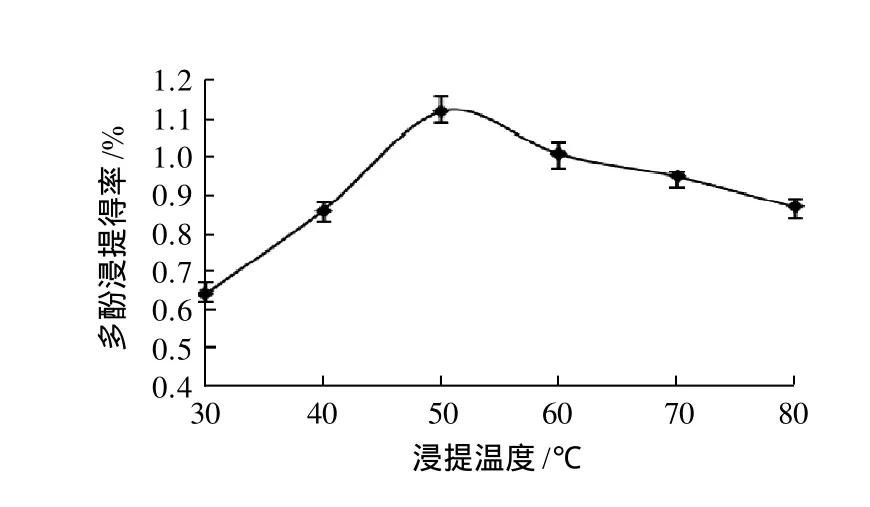
图1 浸提温度对多酚得率的影响Fig.1 Effect of extraction temperature on the yield of polyphenols
图1表示,液料比为12:1、浸提时间60min、浸提温度分别为30、40、50、60、70、80℃条件下多酚得率的变化。温度较低时,多酚的得率也较低,温度高于50℃时,多酚的得率反而下降,可能是由于温度过高,多酚发生氧化,50℃时多酚的浸提得率最大,初步确定最佳浸提温度为50℃。
2.1.2 浸提时间对多酚得率的影响
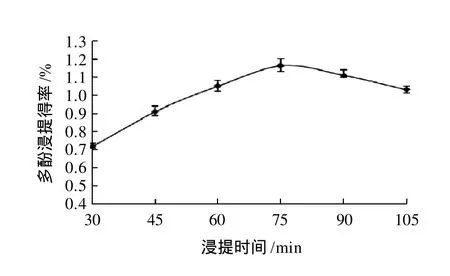
图2 时间对多酚浸提得率的影响Fig.2 Effect of extraction time on the yield of polyphenols
图2表示,浸提温度50℃,其他条件不变情况下,浸提时间分别为30、45、60、75、90、105min对多酚得率的影响。随着浸提时间的延长,多酚得率逐渐提高,在75min时达到最大值,当浸提时间继续延长时,多酚得率反而缓慢下降,可能是时间过长,多酚发生局部氧化,初步确定最佳浸提时间为75min。
2.1.3 液料比对多酚得率的影响
图3表示浸提时间60min,其他条件不变情况下,液料比分别为10:1、11:1、12:1、13:1、14:1、15:1(V/m)对多酚浸提得率的影响。随着液料比的增大,多酚得率也随之变大,在液料比为13:1时出现拐点,而后又趋于稳定,初步确定最佳液料比为13:1。
2.2 菜籽多酚浸提正交试验
在单因素试验基础上,以多酚浸提得率为考察指标,进行温度、时间、液料比的多因素试验考察,采用L9(34)的正交表进行试验,试验方案与结果分析见表1,方差结果见2。
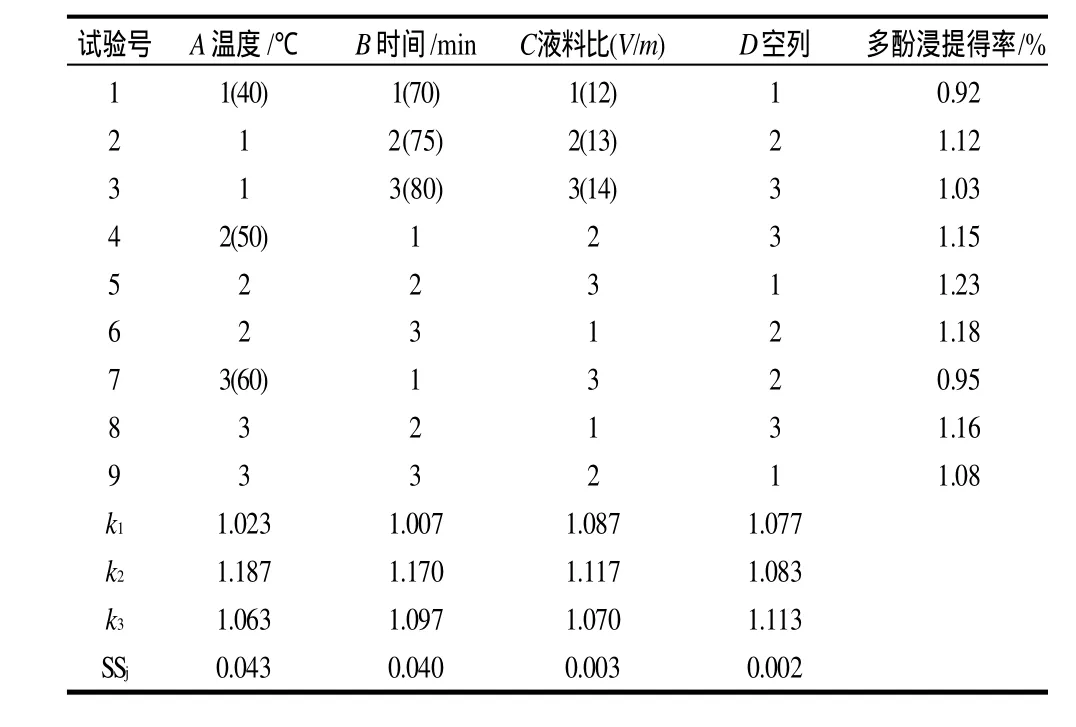
表1 菜籽多酚浸提正交试验方案与结果分析Table 1 Orthogonal array design protocol and corresponding results for extraction process optimization
由表1可知,各因素对菜籽多酚浸提的效果的影响顺序为浸提温度>浸提时间>液料比,通过对因素水平与考察指标之间关系的分析,可得最佳工艺条件为A2B2C2。

表2 方差分析结果Table 2 Analysis of variance for the experimental results of orthogonal array design
由表2方差分析可知,温度A和时间B对多酚浸提得率影响显著,液料比对多酚浸提得率不显著。虽然计算分析与直接分析最佳组合条件在C因素的水平上取值不一致,但由于C因素对指标的影响不显著,从节约成本、降低能耗的角度出发,确定最优组合条件为A2B2C2,即浸提温度50℃,浸提时间75min,液料比13:1,将该组合进行验证实验得到的菜籽多酚浸提得率为1.24%。
2.3 浸提次数的选择
由于浸提得率是随着浸提次数的增加而提高,因此,在2.2节获得的最佳浸提条件下,进行不同浸提次数的考察,其多酚得率见表3。

表3 浸提次数对多酚得率的影响Table 3 Effect of repeat extraction number on yield of polyphenols
从表3可以看出,前2次浸提已经浸提出绝大部分菜籽饼粕中的多酚,从综合成本考虑,确定浸提次数为2次。
2.4 浸提液的离子沉淀
2.4.1 最佳沉淀剂的确定
根据1.3.3节的条件,分别以氯化锌、氯化镁、氯化铝、三氯化铁、氯化钡为沉淀剂,使菜籽多酚均沉淀完全,得到不同沉淀剂的多酚沉淀率,结果见图4。

图4 不同沉淀剂对多酚沉淀的影响Fig.4 Effects of different precipitants on the precipitation of polyphenols
由图4可知,不同沉淀剂的多酚沉淀率为:氯化铝>氯化锌>三氯化铁>氯化镁>氯化钡。氯化铝和氯化锌作为沉淀剂最好,且效果几乎差不多,由于铝离子的残留可能会引发老年痴呆[16],所以选择氯化锌作为沉淀剂。
2.4.2 沉淀剂用量的确定
氯化锌作为沉淀剂,选择沉淀剂加入量分别多酚粗提液中多酚质量的0.5、1.0、1.5、2.0、2.5倍,进行多酚沉淀率影响,结果见图5。

图5 沉淀剂用量对多酚沉淀的影响Fig.5 Effect of precipitant amount on the precipitation of polyphenols
由图5可知,随着沉淀剂用量的加大,多酚的沉淀率先逐渐增大后趋于平稳。当沉淀剂的加入量大于1.5倍粗提液中多酚质量时,多酚沉淀率增幅不显著,从经济及环保的角度考虑,沉淀剂的加入量为1.5倍粗提液中多酚质量时的沉淀剂用量是最佳的。
2.4.3 沉淀pH值的确定
以氯化锌作为沉淀剂,其加入量为1.5倍粗提液中多酚质量,用1.5mol/L的NaHCO3溶液调节pH值,考察pH值分别为5.0、5.5、6.0、6.5、7.0、7.5、8.0对多酚沉淀率的影响,结果见图6。
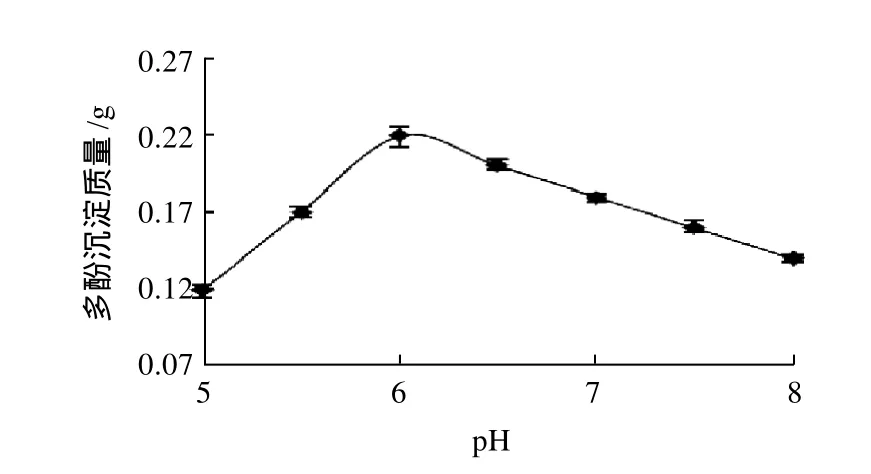
图6 pH值对多酚沉淀的影响Fig.6 Effect of pH on the precipitation of polyphenols
从图6可知,随着pH值的不断升高,多酚的沉淀率先增大后变小,在pH值为6左右时到最大值。可能是由于pH值过低,不利于多酚与锌离子形成络合物,而pH值过高,多酚易氧化。所以沉淀pH值确定为6.0。由此可得浸提液离子沉淀的较适参数组合为:氯化锌为沉淀剂,沉淀剂用量为粗提液中多酚质量的1.5倍,pH6.0。
将得到的菜籽多酚络合沉淀物,根据1.3.4节和1.3.5节的条件进行转溶、萃取、浓缩及干燥后,得到的菜籽多酚成品为淡黄色粉末,得率1.66%,纯度90.03%。
3 结 论
采用水浸提结合离子沉淀工艺,通过正交试验确定浸提温度和时间为影响菜籽多酚浸提效果的显著性因素,获得最佳工艺条件为:浸提温度50℃,浸提时间75min,液料比13:1,浸提2次;离子沉淀的较适参数组合为沉淀剂为氯化锌,沉淀剂用量为1.5倍粗提液中多酚的质量,沉淀pH值为6.0;在此条件下制备出的菜籽多酚成品为淡黄色粉末,纯度为90.03%,多酚总得率为1.66%。
目前菜籽饼粕中多酚的制备工艺大都存在成本高,能耗高,易污染环境等问题。水浸提结合离子沉淀法经济、环保且操作简便,利于实现产业化,在菜籽饼粕中多酚的制备及菜籽饼粕的综合利用方面具有广阔的应用前景。
[1]陆胜民, 郑美瑜, 陈剑兵. 食用菜籽蛋白的提取和纯化研究进展[J].中国粮油学报, 2008, 23(6): 234-238.
[2]钮琰星, 黄凤洪. 油菜籽加工技术研究进展[J]. 中国油脂, 2007, 32(10): 7-10.
[3]潘雷, 爱科, 茂基, 等. 菜籽饼粕脱毒方法研究进展[J]. 中国油脂,2009, 34(10): 32-35.
[4]MAHAJAN A, DUA S. Improvement of functional properties of rapeseed(Brassia campestrisvar toria) meal by reducing antinutritional factors employing enzymatic modification[J]. Food Hydrocolloids, 1998, 12(3): 349-355.
[5]严奉伟, 罗祖友, 薛照辉, 等. 菜籽多酚的抗氧化作用[J]. 中国油脂,2005, 30(7): 54-57.
[6]DU Guorong, LI Mingjun, MA Fengwang, et al. Antioxidant capacity and the relationship with polyphenol and vitamin C inActinidia fruit[J]. Food Chemistry, 2009, 113(2): 557-562.
[7]FALLER A, FIALHO E. Polyphenol content and antioxidant capacity in organic and conventional plant foods[J]. Journal of Food Composition and Analysis, 2010, 23(6): 561-568.
[8]严奉伟, 王辰, 严赞开, 等. 菜籽多酚对S180小鼠肉瘤及其免疫功能的影响[J]. 中国粮油学报, 2007, 22(5): 81-84.
[9]郑美瑜, 陈剑兵, 陆胜民, 等. 菜籽蛋白的提取和纯化[J] . 农业工程学报, 2008, 24(8): 267-270.
[10]严奉伟, 邓明, 朱建飞. 菜籽饼粕综合利用[J]. 粮食与油脂, 2005(9): 6-8.
[11]SILVA E, ROGEZ H, LARONDELLE Y. Optimization of extraction of phenolics fromInga edulisleaves using response surface methodology[J]. Separation and Purification Technology, 2007, 55(3): 381-387.
[12]NAWAZ H, SHI H, MITTAL G, et al. Extraction of polyphenols from grape seeds and concentration by ultrafiltration[J]. Separation and Purification Technology, 2006, 48(2): 176-181.
[13]王承明, 陈建峰, 任出杰, 等. 菜籽饼粕中多酚的提取新工艺研究[J].食品与发酵工业, 2007, 33(5): 143-147.
[14]李群梅, 杨昌鹏, 李健, 等. 植物多酚提取与分离方法的研究进展[J].保鲜与加工, 2010, 1(1): 16-19.
[15]韩菊, 魏福祥. Folin-Ciocalteu比色法测定苹果渣中的多酚[J]. 食品科学, 2010, 31(4): 179-182.
[16]韦星船, 陈小宏, 王琪莹. 微波-离子沉淀法提取茶叶中茶多酚的工艺研究[J]. 食品科技, 2007, 32(8): 132-138.
Preparation of Rapeseed Polyphenols from Rapeseed Meal by Ion Precipitation Method
PAN Li-jun,HAN Zhi-hong,ZHAO Chun-hua,ZHOU Jun
(Key Laboratory for Agricultural Products Processing of Anhui Province, School of Biotechnology and Food Engineering,Hefei University of Technology, Hefei 230009, China)
In order to improve the comprehensive value of rapeseed meal, hot-water extraction followed by ion precipitation was applied to prepare polyphenols from rapeseed meal. Using an orthogonal array design based on one-factor-at-a-time experiments, the optimal extraction conditions were determined as 50 ℃ of extraction temperature, 75 min of extraction time,1:13 of material-to-liquid ratio, and 2 of repeated extraction number. Moreover, the largest amount of rapeseed polyphenols was precipitated by adding a 1.5-fold weight excess of ZnCl2 and adjusting the pH to 6.0. The obtained rapeseed polyphenols were light yellow powder and showed a yield of 1.66% and a purity of 90.03%.
rapeseed polyphenols;protein;extraction;purification;ion precipitation
TQ914.1
A
1002-6630(2012)18-0041-04
2011-08-18
安徽省科技攻关计划项目(11010301012)
潘丽军(1955—),女,教授,硕士,研究方向为农产品资源综合利用。E-mail:panlijun1955@163.com
