氯化锌ZnCl2制备条件实验浅探
2017-04-20刘玉兰
刘玉兰
摘 要:氯化锌的用途广泛,它可应用于焊接金属时清除金属表面上的氧化物,以及有机化学中常用它作为去水剂和催化剂等, 市场需求也很大,值得研究和开发。该文从云南实际情况与经济效益的角度,对氯化锌生产的工艺流程进行了实验验证。
关键词:氯化锌 工艺流程 实验
中图分类号:0645.5 文献标识码:A 文章编号:1674-098X(2016)12(b)-0070-02
氯化锌用途十分广泛,需求量也很大,如,它可应用于焊接金属时清除金属表面上的氧化物(ZnCl2+H2O=H[ZnCl2(OH)],
FeO+2H[ZnCl2(OH)]=Fe[ZnCl2(OH)]2+H2O)以及有机化学中常用它作为去水剂和催化剂等。云南省锌矿资源藏量大,得天独厚,是藏量最大的少数省份之一,但由于云南现尚无氯化锌产品的生产厂家,年需数千吨的氯化锌产品均需要靠进口。鉴于上述原因,我们应积极利用本地资源,研制氯化锌的生产以填补氯化锌产品的需求空白,对发展该省氯化锌产品的生产,满足工业生产的需要都具有极其重要的意义。
云南不仅有可开采的锌矿,还有各种品位的氧化锌产品。这就为氯化锌生产的原料提供了保障和选择余地。此外,昆明还拥有大量的盐酸,且就地可得,这就为开发氯化锌创造了十分有利的条件。
该实验从经济效益的角度出发,对所拟定的工艺流程进行了实验验证。探索到了较适宜的条件和合格的产品,用该工艺生产的氯化锌产品可达国标GB-1625-79一级产品的标准,现将对该实验的有关工艺流程及有关事项简要归纳总结如下。
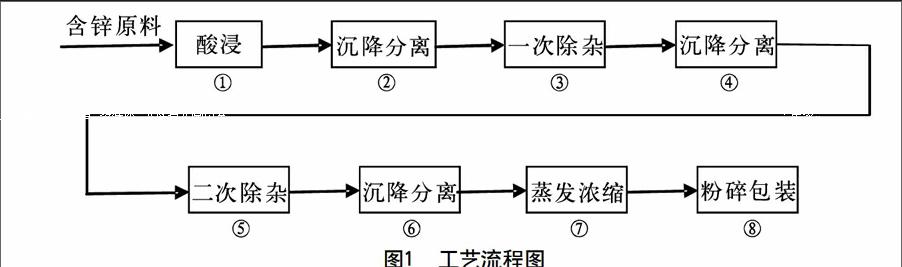
1 工艺流程
工艺流程如图1所示。
向耐盐酸和氯化锌腐蚀并有搅拌器的容器内加入工业盐酸,在搅动下缓慢加入含ZnO的原料粉。此时原料与HCl反应生成氯化锌:
ZnO+2HCl=ZnCl2+H2O
并放出大量的热而使反应溶液温度升高。
原料中的其他氧化物也随之溶解而生成相应的氯化物。酸可溶和水可溶的杂质也一并进入溶夜。
该实验的原料采用氧化锌厂的附产物:含70%~80%ZnO的沉降粉为原料。它价格低,且比锌矿的渣量小。其中含有杂质铁、铝、镉等重金属。将随矿源而异,也含有硫酸鹽和亚硫酸盐等,系锌矿中硫化物所引入,也含煤灰泥土或可溶性硅酸盐等。杂质必须除去才能提高产品的纯度,这就为酸浸后带来了后续的除杂工序。
作原料的盐酸采用工业盐酸,尝试较高而铁含量较少的为宜,以降低除杂成本。
盐酸与ZnO原料粉的配料比,按各自的分析含量,以反应式的理论比例进行配料。
ZnO与HCl的反应属中和反应,本应很快,但随反应的进行使HCl浓度越来越低,且是固-液接触,因此,仍需一定的反应(溶液)时间和搅拌,以促进反应。
中和反应放出的热量是很有利的,它不仅可加快反应,也可促进胶体(如硅酸)和悬浊物的沉降,有利于固(渣)液的沉降分离。
在操作上控制酸浸液pH=3为止,停止搅拌,让其不溶残渣沉降,然后用虹吸法吸出上边清液进入下一工序除杂。残渣排入贮渣池,到一定量后用石灰处理中和后废弃。
由于ZnCl2溶液对碳钢、不锈钢都有腐蚀性;对植物纤维沙布、尼龙纤维、涤纶纤维、聚乙烯纤维等沙布,都有溶解腐蚀作用,故酸浸液中的固液分离,还是采用沉降分离为好,以减少杂质的引入。
2 一次除杂
该工序除杂是指除上一工序所得的氯化锌溶液中的杂质Fe2+和SO42-、SO32-、Mn2+等。Fe2+是借氧化剂将其氧化成Fe3+,进而水解生成难溶的Fe(OH)3而沉降分离。SO32-也被氧化成SO42-,然后加入BaCl2溶液生成难溶的BaSO2而沉降分离。杂质中的Mn2+也被氧化成MnO2而沉降分离。
该实验采用KMnO4作为氧化剂,用时KMnO4本身又是氧化终点指示剂。
氧化温度控制在50 ℃为宜,pH=3,在搅拌下由试液(沉降分离出来的酸浸液)缓缓加入氧化剂溶液(浓度为3 g/L),特别是近终点褪色慢时要慢加,直到淡粉红色能保持10 min即不再加入,发生的反应如下:
MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O
2MnO4-+3Mn2++2H2O=5MnO2↓+4H+
溶液中剩余的SO32-也被氧化成SO42-。
然后,也在搅拌下趁热缓慢、少量加入BaCl2稀溶液(50gBaCl2/L),以使SO42-生成BaSO4难溶沉淀而除去。
至此,溶液中生成有Fe(OH)3、MnO2、BaSO4、PbSO4等难溶沉淀物,如,沉降慢可提高试液温度至70 ℃~80 ℃以促进沉降和水解。然后虹吸分离出上层清液进入下一步第二除杂工序。
3 二次除杂
向上述工序澄清分离出的试液中加入锌粉,以还原除去Pb2+、Cd2+等重金属杂质。
Cd2++Zn=Zn2++Cd↓
Pb2++Zn=Zn2++Pb↓
锌粉(120目)以少量多次加入,搅拌,保持60 ℃~70 ℃,不断取试液做锌片试验。直到锌片表面无明显黑色为合格,然后沉降分离,试液应澄清透明无色。
4 蒸发浓缩
向上一工序所得的无色透明试液,加入盐酸(无色稀酸),调节pH,使pH=3,以防止ZnCl2水解使Zn2Cl2超标。然后转入瓷蒸发器中,在电炉上加热浓缩,溶液的温度将一直上升(无恒沸点)。
在190 ℃~280 ℃时,溶液中有固体析出而变稠(ZnCl2·H2O)。在220 ℃~250 ℃冷却固化时,其中含9%~12%的水分(ZnCl2·H2O)。在310 ℃~340 ℃冷却固化时,可得含水量为1.2%(ZnCl2·H2O)的产品。如要制造无水氯化锌,则要在干燥的HCl气氛中加热脱水。无水氯化锌是白色、易潮解的固体,它的溶解度很大,吸水性很强,有机化学中常用它作为去水剂和催化剂。
5 产品与包装
产品有40%~49%氯化锌溶液与固体产品两种,全靠控制蒸发温度而得。包装采用镀锌铁桶或白铁桶包装,内衬聚乙烯塑料袋。ZnCl2·H2O有毒,能腐蚀皮肤,万一触及应立即用水冲洗。
6 结语
前面已述,氯化锌的用途广泛,市场需求也很大,且又有原料,是值得研究和开发的。但生产氯化锌产品是一个技术性强、控制严格的工艺。同时设备要求耐腐蚀、耐高温,但只要能达到这两方面要求,就可以生产出一级产品或电池用产品的。前述工艺流程和条件是可靠的,但原料的来源并非一成不变。故其杂质将随原料而异。如,在原料中含水溶性的碱金属或碱土金属的盐类较多,则产品达不到标准。工艺就将作相应的调整,为此,在工艺流程酸浸之前需加一道洗涤工序,以除去Na+、K+、Mg2+等可溶性物质,可获得优质产品。
参考文献
[1] 芦苇仪,卢爱军.无污染的氯化锌生产工艺[J].化学世界,2006,47(2):125-126.
