开胸术后多模式复合镇痛和静脉自控镇痛的疗效及安全性比较
2012-10-17王卓强王恒林王显望吕宝胜
徐 震 王卓强 王恒林 王显望 吕宝胜
解放军第三〇九医院麻醉科,北京 100091
经历开胸手术的患者,70%在术后会感到剧烈疼痛,这种疼痛并不比疾病本身所带来的痛苦小[1]。由于切口创伤、肌肉损伤及胸腔闭式引流管压迫肋间神经,刺激胸膜等,其疼痛剧烈且持续时间长,直接影响患者的咳嗽、咯痰以及呼吸运动,从而可引起术后感染、肺不张及心血管意外等并发症的发生。有效的术后镇痛不仅能减轻患者的痛苦,改善其术后肺功能,减少术后并发症的发生,而且能够有力促进机体早日康复,接受进一步巩固治疗。胸科镇痛的方式很多,大体分为全身给药和区域阻滞两类。无论何种镇痛方法,在具有一定优势的同时,也不可避免地存在局限性。因此,联合应用不同作用机制的镇痛药物,或不同的镇痛措施,通过多种机制产生镇痛作用的“多模式镇痛”概念,已得到越来越多临床医师的认可[1]。本研究旨在观察和评价综合运用术中氟比洛芬酯静脉注射、关胸前罗哌卡因肋间神经阻滞以及术后患者芬太尼-地佐辛静脉自控镇痛(patient-controlled intravenous analgesia,PCIA)的效果及不良反应,并与罗哌卡因肋间神经阻滞合并芬太尼-地佐辛PCIA,以及单纯芬太尼-地佐辛PCIA进行比较,以对其临床疗效和安全性作出评价。
1 资料与方法
1.1 一般资料
选择2010年6月~2011年12月我院90例胸外科开胸手术患者,采用标准后外侧切口。男52例,女38例;年龄23~75 岁;体重 40~90 kg;ASAⅠ~Ⅲ级,意识清楚,经讲解后能够自主进行疼痛描述和评价。排除标准:严重心肺疾病,肝肾功能不全,消化道溃疡;已知滥用酒精、药物、麻醉药品;有慢性疼痛史;术后不能即刻恢复意识;严重恶心呕吐无法接受继续镇痛治疗;不配合或无法沟通,不能理解VAS评分的患者。本研究经医院伦理委员会批准,并获患者知情同意。
1.2 方法
1.2.1 分组及给药方式 随机将90例择期开胸手术患者分为三组(每组各30例):①氟比洛芬酯+肋间神经阻滞+芬太尼-地佐辛静脉自控镇痛的多模式镇痛(multimodal analgesia,MA)组,手术开始和关胸前各静脉给予氟比洛芬酯50 mg,关胸前选择切口及上下各一肋间和放置胸引管的肋间神经,于肋间神经根部(脊柱旁1~2 cm)分别注射0.25%罗哌卡因5 mL,术后即刻静脉连接PCA泵,配方为芬太尼0.5 mg,地佐辛25 mg,托烷司琼4 mg,生理盐水81 mL;②罗哌卡因肋间神经阻滞合并芬太尼-地佐辛PCIA(Ropivacaine+PCIA,RP)组,配方用法同前;③单纯芬太尼-地佐辛PCIA组(P组)。PCIA泵给药方式:负荷量1 mL+持续输注量0.2 mL/h+患者自控镇痛1 mL/次,锁定时间为15 min。所有手术及肋间神经阻滞均由同一胸外科医师完成,参与评分的助手和患者遵循双盲原则。
1.2.2 麻醉 采用全身麻醉。患者术前禁食8 h以上,入室后监测心电图、氧饱和度、动脉血压。全麻诱导前壶入地塞米松10 mg,阿托品0.5 mg,麻醉使用咪达唑仑0.05 mg/kg、异丙酚1~2 mg/kg、芬太尼 3 μg/kg、维库溴铵 0.10~0.15 mg/kg。插入双腔气管导管,机械通气。麻醉维持期间以静吸复合方式维持麻醉深度,根据患者术中生命体征调节七氟醚、异丙酚和瑞芬太尼的用量。间断给予芬太尼,使其整个术程用量达到6 μg/kg。手术结束后送入术后恢复室(PACU),自然苏醒后拔管。
1.3 观察指标
观察并记录术后1、6、24、48 h三组的镇痛评分、镇静评分及不良反应(恶心、呕吐、皮肤瘙痒、呼吸抑制等),记录PCA泵药量累计消耗情况。镇痛效果采用视觉模拟评分法(visual analogue scale score,VAS),0 分为无痛,10 分为最痛;<3分为优良,3~5分为基本满意,>5分为不满意。镇静评分采用Ramsay评分:1分为不安静、烦躁,2分为安静合作,3分为嗜睡、听从指令,4分为睡眠状态能被唤醒,5分为呼唤反应迟钝,6分为深睡、呼唤不醒。2~4分为镇静满意,5~6分为镇静过度。
1.4 疼痛处理
患者VAS评分不超过3分时无需特殊处理,在VAS评分达到4分以上时,患者通过PCA镇痛泵追加镇痛药物。
1.5 统计学方法
所有数据均使用SPSS 13.0统计软件处理。计量资料先行正态性检验,近似服从正态分布,个别离散度大的数值经检验后舍弃,数值以均数±标准差(±s)表示,组间比较采用方差分析(Dunnett法);计数资料采用χ2检验;以P<0.05为差异有统计学意义。
2 结果
2.1 三组术后镇痛、镇静评分比较
MA组与RP组各时点VAS评分均明显低于P组(P<0.05),术后1、6 h MA组的VAS评分又明显低于RP组(P<0.05);术后1、6、24 h MA和RP组的Ramsay评分均明显低于P组(P<0.05),48 h三组 Ramsay评分未见显著性差异(P>0.05),各时点MA与RP组间均未见显著性差异(P>0.05)。见表1。
表1 三组术后镇痛、镇静评分比较(±s,分,n=30)

表1 三组术后镇痛、镇静评分比较(±s,分,n=30)
注:与P组比较,aP<0.05;与RP组比较,bP<0.05
指标 组别 术后1 h 术后6 h 术后24 h 术后48 h VAS Ramsay MA组RP组P组MA组RP组P组1.64±1.16ab 2.41±1.34a 5.99±1.78 2.36±0.35a 2.57±0.68a 3.32±0.60 2.05±1.29ab 3.29±1.42a 6.15±1.39 2.55±0.49a 2.50±0.64a 3.67±0.75 2.91±1.33a 3.45±1.90a 5.69±1.46 2.89±0.70a 3.10±0.76a 3.86±0.89 2.60±1.22a 2.96±1.55a 4.71±1.63 2.57±0.65 2.63±0.56 2.70±0.58
2.2 三组不良反应及镇痛泵药量消耗情况比较
术后三组均发生个别患者恶心呕吐和皮肤瘙痒,组间比较差异无统计学意义(P>0.05);MA组发生嗜睡2例,RP组发生3例,均与P组的10例存在差异(P<0.05);三组均未出现呼吸抑制;PCA药量消耗MA与RP组均显著低于P组(P<0.05),而MA组的消耗量又明显低于RP组(P<0.05)。见表2。
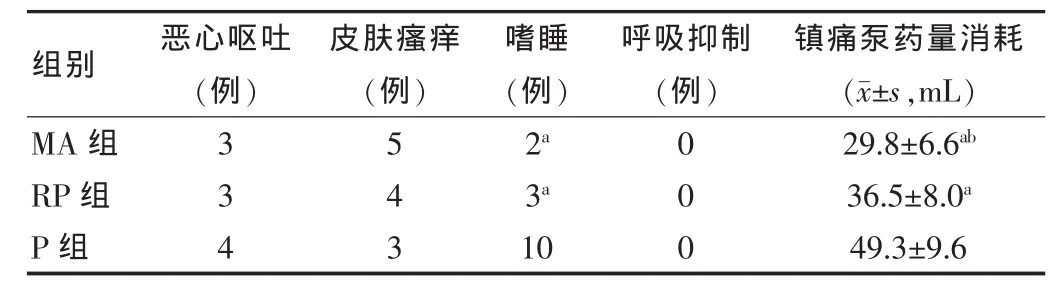
表2 三组不良反应及镇痛泵药量消耗情况比较(n=30)
3 讨论
开胸手术的术后痛是临床上最为严重的术后痛类型之一,患者常疼痛剧烈,呼吸运动受限,影响咳嗽排痰,增加低氧血症、肺不张及肺部感染等并发症的发病率;术后疼痛还会导致体内儿茶酚胺释放增加,血压上升,心率增快,从而引发心血管方面的并发症,更有30%的患者疼痛延续时间可达数月甚至转为慢性痛[1]。因此,有效的术后镇痛不仅可以缓解患者的痛苦,减少围术期并发症的发生,同时又可以促进术后早期恢复,提高长期生活质量。
开胸术后的疼痛来源主要有三个方面:一是进胸切断多组神经肌肉,牵开肋骨时损伤肋椎关节及肋横突关节韧带和竖脊肌,甚至造成肋骨断裂,这些痛觉感受主要经肋间神经传向脊髓[2];二是内脏痛,主要表现为钝性痛,常伴恶心、弥漫性胸壁疼痛,由C类神经纤维介导、自主神经伴行,迷走和交感神经可能参与此类疼痛;三是肩胛区疼痛,是由于患者改变体位引起后胸韧带或肩关节活动、术中臂丛神经受牵拉、主支气管横断及膈神经受刺激等引发的牵涉性疼痛[3]。临床上的镇痛方式包括肌内或静脉注射镇痛药物、静脉自控镇痛肋间神经阻滞或冷冻、硬膜外置管自控镇痛、胸椎旁阻滞等[4],但每一种方法的优缺点都同样明显:分次注射镇痛药物方法最简便,但往往是在患者感到明显疼痛之后主动要求下注射的,缺乏超前镇痛过程,效果难以达到患者的心理预期;静脉自控镇痛的配方以阿片类药物为主,由患者按自己需要自主给药,满意度大大提高,但如短时间给药过于频繁,嗜睡和呼吸抑制这两个副作用必须引起麻醉医生的警惕;肋间神经冷冻在术后可以维持数周的镇痛效果,但其需要特定的仪器,而且有证据显示肋间神经冷冻是增加远期疼痛,尤其是神经病理性痛发生率的危险因素之一;胸段硬膜外置管镇痛效果最佳,被认为是开胸术后镇痛方式的首选,它阻止了术后急性疼痛导致中枢敏化的过程,从而减少了慢性疼痛的发生。然而,胸段硬膜外操作难度较大,且操作不熟练易损伤胸段脊髓,造成严重的不良后果。而且,硬膜外镇痛期间需要持续监测,药物浓度或平面控制不佳可能引起呼吸抑制,同时由于双侧交感神经的阻滞,对血流动力学的影响也不容忽视。胸椎旁阻滞通过将局麻药注入术侧胸部椎旁间隙,同时阻滞肋间神经及交感神经,缓解开胸术后出现的胸壁及内脏疼痛。其优点是镇痛效果较好,对循环和呼吸影响甚微,但一次性注入25 mL以上药液时很容易扩散至对侧,形成双侧交感神经阻滞,另外个体差异的存在以及导管位置不佳也会引起镇痛失败。综上所述,采用多种药物,多种方式联合运用,发挥各自的优点而使缺点最小化的多模式镇痛才是开胸术后的最佳镇痛方案。本研究中,无论是各时间点的镇痛评分、镇静评分、不良反应还是PCIA的用药量,三种方式联用的MA组都要好于其余两组,而两种方式联用的RP组也要好于单纯的P组。
多模式镇痛没有一定之规,但多遵循局部阻滞和全身用药相结合的原则,是医师根据手术特点、患者情况以及自己对药物和神经阻滞技术掌握的熟练程度综合考量制订出的方案。本研究的多模式镇痛方案为术中氟比洛芬酯静脉注射、关胸前罗哌卡因肋间神经阻滞以及术后患者芬太尼-地佐辛静脉自控镇痛。氟比洛芬酯是非甾体抗炎药,具有显著镇痛抗炎作用,可选择性集聚在手术切口周围,提高药物局部有效浓度,通过提高痛阈,降低神经末梢痛觉传导,减轻中枢敏化从而达到超前镇痛的目的,在减少其他镇痛药物用量的同时还对减少慢性痛的发生起到积极作用[5]。罗哌卡因肋间神经阻滞操作简单,所用的0.25%的浓度可以做到“动静分离”,即在阻断肋间神经感觉传入的的同时对肋间肌参与呼吸运动不产生显著影响。文献报道,采用静脉芬太尼PCIA不能明显减轻患者术后4 h之内的疼痛状态,部分患者可出现严重的疼痛,同时伴有心率的增快和血压的升高[6],本研究中由于肋间神经阻滞技术的运用,较单用PCIA组显著地改善了术后的疼痛控制情况,减少了嗜睡发生,同时减少了PCIA的用药量。需要注意的是肋间神经与肋间血管相伴行,阻滞时要避免引起出血或血管内误注射。如同前文所说,肋间神经阻滞解决不了内脏痛和肩部痛,因此联用PCIA还是非常有必要的,本研究中用的是芬太尼-地佐辛的联用方案,该方案用地佐辛取代了传统的吗啡。已知传导神经上分布着不同的阿片受体,不同阿片类药物作用的受体不同,其镇痛效果也不同。μ受体主要与脊髓以上水平的镇痛有关,κ受体主要参与脊髓水平镇痛。地佐辛是混合型阿片受体激动-拮抗剂,主要激动κ受体产生脊髓镇痛,同时拮抗μ受体,对μ受体兴奋引起的恶心呕吐有抑制作用[7],本研究中P组除了镇痛评分高于于MA和RP组,嗜睡例数多于上述两组之外,各组在恶心呕吐、皮肤瘙痒的发生例数方面未见显著性差异,以氧饱和度低于90%,呼吸次数少于8次/min为诊断标准的呼吸抑制在三组均未出现;主诉肩胛区疼痛的患者在自控PCIA后均表述疼痛减轻或者暂时消失,证明了芬太尼-地佐辛联用的有效性和安全性。
在研究中笔者还发现,除了镇痛作用以外,PCIA的镇静作用也给患者带来了一定的益处,如术后的前两夜,患者常由于各种管道刺激、长时间平卧导致背部肌肉疲劳或较厚的敷料引发不适,这些不易被局部麻醉药所缓解,此时通过PCIA补充部分阿片类药物有利于缓解疼痛,并且提供一定镇静作用,使患者获得更好的睡眠。另外,麻醉医生还应重视术后随访中对患者的鼓励和积极引导,从一些患者在访视前后对痛觉的主观感受有所减轻来看,恰当的心理疏导也是多模式镇痛中的重要一环。
综上所述,通过对比观察,笔者发现多种镇痛方式的结合可以带来良好的镇痛效果,并且由于大幅度减少了阿片类药物的用量,与之相关的不良反应也得到控制,有利于镇痛治疗的持续进行,使患者从中获益更多。开胸术后慢性痛高发生率的应对是笔者接下来研究的兴趣所在,笔者拟从术前超前镇痛、术中完善镇痛、术后长期镇痛三方面阻止痛觉中枢敏化入手,摸索出新的多模式镇痛策略,使之在安全性、有效性、经济性方面更贴近患者的需要。
[1]De Cosmo G,Aceto P,Gualtieri E,et al.Analgesia in thoracic surgery:review[J].Minerva Anestesiol,2009,75(6):393-400.
[2]倪燕,丁正年,张国楼.复方利多卡因肋间神经阻滞联合PCIA用于胸科患者的术后镇痛[J].江苏医药,2011,37(6):675-677.
[3]Martinez BC,Busquets J,de Castro PE,et al.Randomized double-blind comparison of phrenic nerve infiltration and suprascapular nerve block for ipsilateral shoulder pain after thoracic surgery[J].Eur J Cardiothorac Surg,2011,40(1):106-112.
[4]鞠辉,冯艺.肋间神经冷冻用于开胸术后镇痛[J].中国医药,2007,42(9):32-34.
[5]萧安.氟比洛芬酯联合曲马多用于开胸患者术后镇痛的临床效果观察[J].中外健康文摘,2011,8(1):75-76.
[6]Beaudroit L,Ripart J.Nerve blocks of the trunk:indications,techniques,advantages and complications[J].Ann Fr Anesth Reanim,2009,28(3):79-83.
[7]Fischer BD,Dykstra LA.Interactions between an N-methyl-D-aspartate antagonist and low-efficacy opioid receptor agonists in assays of schedule-controlled responding and thermal nociception[J].J Pharmacol Exp Ther,2006,318(3):1300-1306.
