吉西他滨单药化疗联合适形放疗治疗老年局限晚期非小细胞肺癌的疗效分析
2012-10-17赵永利张敬慧刘倩倩仲菊维
李 波 赵永利 张敬慧 刘倩倩 仲菊维
山东省青岛市胶州中心医院放疗科,山东胶州 266300
非小细胞肺癌(NSCLC)是严重威胁人类生命健康的疾病。占全部肺病例的80%,可手术病例占20%~30%。30%~40%的患者在确诊时为局部晚期[1],放化疗是主要的治疗方式,老年人是肺癌发病的主要群体,50%以上肺癌发生在老年患者,老年患者对化疗药物及放射治疗耐受性较差,以放化疗为主的综合治疗方案是目前老年局部晚期NSCLC临床研究的热点。笔者采用西他滨单药化疗联合适形放疗治疗老年晚期NSCLC取得了较好的疗效,现报道如下:
1 资料与方法
1.1 一般资料
选择2005年6月~2009年1月我院收治的老年局部晚期NSCLC初治患者40例,其中男24例,女16例;年龄65~81岁,中位年龄 73岁,平均(71.0±8.4)岁。NSCLC均经病理组织学或细胞学检查确诊,CT影像学检查有可测量病灶,其中鳞癌24例,腺癌13例,腺鳞癌3例。所有患者经B超、胸部CT、脑MRI及ECT等检查,根据抗癌联盟(UICC)2002年修订的肺癌TNM分期,ⅢA期28例,ⅢB期12例。有慢性肺病12例,心脏疾病7例,糖尿病6例。体能状况评分(ECOG PS)≤ 2分,预计生存期≥ 3个月,患者入选后随机分为实验组及对照组,每组20例,两组患者年龄、性别、肿瘤分期、部位及合并内科疾病情况差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法
1.2.1 化疗方法 两组患者均给予口吉西他滨(法国礼来公司产品,商品名健择,批号:VIALNO.7502)单药化疗方案,吉西他滨1 000 mg/m2,第1、8天给药,21 d为1个周期。实验组治疗2个周期后行胸部CT评价疗效,停止化疗进行适形放疗;对照组行规律化疗4个周期,化疗方案同实验组。化疗期间均应用5-羟色胺(5-TH)受体拮抗剂预防及治疗消化道不良反应,化疗期间内每周复查血常规、肝肾功能,出现中性粒细胞减少时应用粒细胞集落刺激因子(G-CSF)治疗。
1.2.2 三维适形放疗方法 实验组化疗2周期后进行三维适形放疗,采用德国西门子直线加速器、立体定向放射治疗体架、三维治疗计划系统。真空定位袋置于立体定向放射治疗体架内,患者仰卧位在真空定位袋上,双手交叉置头顶,抽真空固定,参考激光灯标出患者、体模相对位置,体表定位标记,行螺旋CT增强扫描,层厚为5 mm,CT图像经网络传输到治疗计划系统(TPS)工作站,勾画靶区,按照国际辐射单位和测定委员会(ICRU)50号文件标准,根据影像解剖结构逐层勾画出大体肿瘤体积(GTV),计划靶区(PTV)由 GTV外放1.0~1.5 cm,物理技师勾画出体表轮廓及临近敏感器官。正常肺组织受量用V20作评估。放射源为6MV-X线或10MV-X线,采用4~6个共面或非共面野,90%等剂量曲线三维包绕靶区,确定处方剂量,200 cGy/次,5次/周,TPS计划完成后通过体积直方图(DVH)进行治疗计划的优化。50 Gy后在原体位下再行CT增强扫描,针对残余病灶加量照射至总剂量60~66 Gy。
1.3 疗效评价
化疗中每两周期进行胸部CT、脑MRI、同位素骨扫描、腹部超声等检查以考评疗效,放、化疗结束4周后疗效根据RECIST[2]标准进行评估,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)。 总有效率(ORR)=(CR+PR)/总数×100%。在患者接受治疗后同时进行正规随访。
1.4 毒性分度标准
化疗药物毒性分级按抗肿瘤药物毒性WHO分级标准进行评价。依据抗癌药物急性与亚急性毒性反应表现分为0~Ⅳ度,放射毒性分级标准按RTOG标准。
1.5 统计学方法
采用统计软件SPSS 13.0对实验数据进行分析,计量资料数据以均数±标准差(±s)表示,两组近期疗效及毒副反应比较采用Mann-Whitney U秩和检验,计数资料以率表示,采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者近期疗效比较
实验组 :CR6例,PR7例,SD4例,PD3例,ORR为65%。对照组:CR1例,PR5例,SD6例,PD8例,ORR为35%。实验组ORR高于对照组,差异有统计学意义(P<0.05)。见表1。
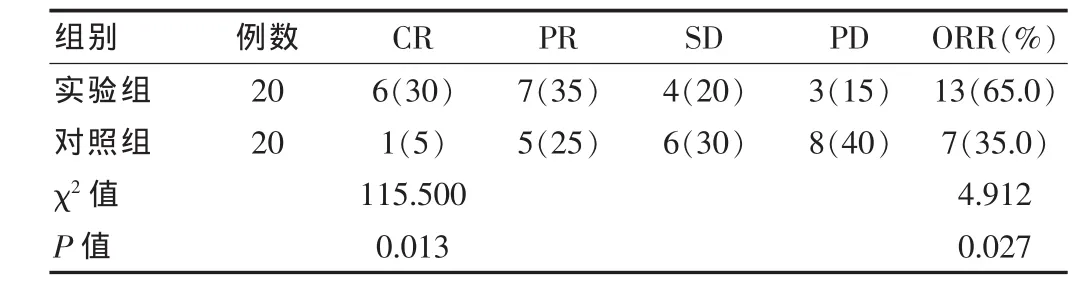
表1 两组患者近期疗效比较[n(%)]
2.2 两组患者化疗毒副反应
两组患者化疗药物毒副反应分级结果比较显示,实验组患者白细胞减、血小板减、血红蛋白下降及恶心、呕吐等消化道副反应的发生分级低于对照组,差异具有统计学意义(P<0.05)。 见表2。
2.3 实验组患者放疗副反应比较
实验组患者发生放射性肺炎7例,放射性食管炎12例,均为Ⅰ、Ⅱ级毒副反应,无Ⅲ、Ⅳ级严重放疗并发症发生,对进食及呼吸功能无严重影响,在可耐受范围。
3 讨论
随着社会人口老龄化和肺癌发病率的上升,高龄晚期肺癌患者日益增多[3]。老年人器官系统功能衰退,脏器储备功能降低,骨髓储备减少,药物廓清能力下降等,导致对抗肿瘤治疗如手术、放疗和化疗耐受性差。老年NSCLC患者对放、化疗的耐受一直存在较多的争论。有研究显示,≥65岁和<65岁的肺癌患者在化疗疗效和生存期、化疗毒副反应上两者的差异并没有统计学意义,并未表现出明显的年龄相关性。有临床试验提示,高龄患者两药方案(含铂或非铂)的疗效并不优于单药方案,但毒性更明显,总体上,以单药治疗为宜,这明显不同于年轻的肺癌患者。在意大利进行的老年肺癌研究(MILES)的Ⅱ期随机试验中[4-5],入组中位年龄74岁老年患者700例,分别接受长春瑞宾、吉西他滨以及联用这两种药物。三者中位生存时间分别为36、28、30周,1年生存率分别为38%、28%、30%,单药化疗生存率与联合化疗生存无显著性差异。一些研究资料表明,老年晚期NSCLC单药化疗与最好的支持治疗(BSC)相比,单药化疗可以提高生存率、改善生活质量[6]。
吉西他滨作为一种新型嘧啶类抗代谢剂,主要作用于DNA合成期和晚G1期,并可阻止细胞由G1期进入S期[7],它的抗癌机制系吉西他滨在细胞内经过核苷激酶的作用转化成具有活性的代谢产物双氟二磷酸脱氧胞苷(dFdCDP)和双氟三磷酸脱氧胞苷(dFdCTP),且吉西他滨本身还可以增强核苷激酶的活性,致使活性代谢产物的生成加快而起到自我增效作用。据文献报道吉西他滨单药治疗晚期NSCLC的有效率为18%~35%,中位生存期6.6~11.5个月,1年生存率为20%~44%[8]。
三维适形放射治疗充分利用现代加速器技术、计算机技术和影像学技术,对病变和剂量进行精确定位和定量,使放疗进入了精确定位、精确摆位和精确治疗的新阶段[3]。目的是提高放射治疗增益比,最大限度地将放射剂量集中到病变区,杀灭肿瘤组织而使周围正常组织和器官少受或免受不必要的照射[4]。本组病例应用吉西他滨单药对40例老年局部晚期NSCLC化疗后适形放疗,放疗结束后进行疗效观察,与吉西他滨单药化疗进行比较,两组ORR比较,差异有统计学意义(P<0.05),实验组化疗毒副反应较对照组轻,差异有统计学意义(P<0.05)。实验组发生放射治疗并发症的程度均在可接受范围内,无严重的Ⅲ、Ⅳ级放疗并发症发生,因此笔者认为,吉西他滨单药化疗联合三维适形放疗治疗老年局部晚期NSCLC疗效好、低毒、安全,可作为老年局部晚期NSCLC患者的重要治疗方案。
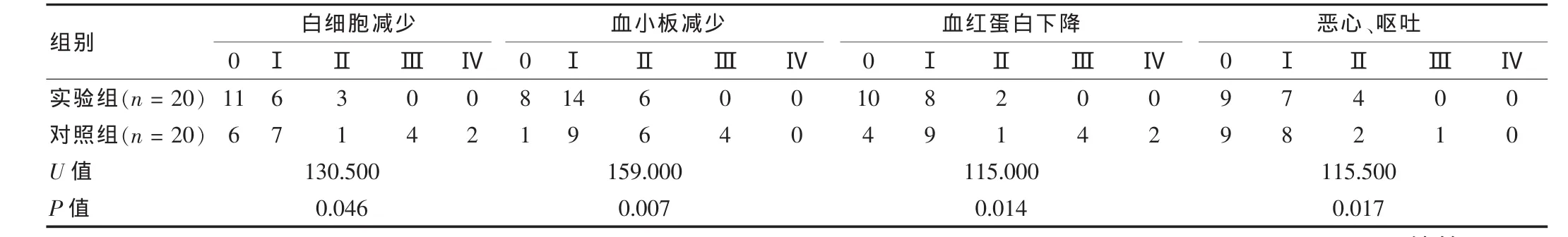
表2 两组患者化疗毒副反应比较(例)
[1]殷蔚伯,李晔雄,王绿化.肿瘤放射治疗手册[M].北京:中国协和医科大学出版社,2010:114.
[2]Livraghi T.Radiofrequency ablation,PEIT,and TACE for hepatocellular carcinoma[J].Hepatobiliary Pancreat Surg,2003,10(1):67-76.
[3]Therasse P,Arbuck S,Eisenhauer E,et al.New guidelines to evaluate the response to treatment in solid tumors [J].J Natl Cancer Inst,2000,92(3):205-216.
[4]杨玲,李连弟,陈育德.中国肺癌死亡趋势分析及发病、死亡的估计与预测[J].中国肺癌杂志,2005,8(4):274-278.
[5]Gridelli C,Perrone F,Gallo C,et al.Chemotherapy for elderly patients with advanced non small-cell lung cancer:the Multicenter Italian Lung Cancer in the Elderly Study(MILES)phaseⅢ randomized trial[J].J Natl Cancer Inst,2003,95(5):362-372.
[6]Gridelli C,Maione P,Illiano A,et al.Cisplatin plus gemcitabine or vinorelbine for elderly patients with advanced non-small-cell lung cancer:The MILES-2P Studies[J].J Clin Oncol,2007,25(29):4663-4669.
[7]王燕,张湘茹.老年晚期肺癌的治疗策略[J].癌症进展,2004,2(6):490-492.
[8]Storniolo AM,Allerheiligen S,Pearce HL.Preclinical,pharmacologic,and phase Ⅰ studies of gemcitabine[J].Semin Oncol,1997,24(1):2-7.
[9]朱蔚友.吉西他滨治疗晚期非小细胞肺癌的现状及进展[J].临床肿瘤学杂志,2004,9(1):94-98.
[10]于世英.吉西他滨用于非小细胞肺癌治疗的研究进展[J].中国癌症杂志,2001,11(4):368-370.
