镍电解液除铜技术研究进展
2012-09-23赵思佳
赵思佳
(湖南有色金属研究院,湖南长沙 410015)
·冶 金·
镍电解液除铜技术研究进展
赵思佳
(湖南有色金属研究院,湖南长沙 410015)
镍电解液除铜仍然是镍冶金中尚未有效解决的难题。文章介绍了国内外镍电解液中除铜的方法,并指出了今后的镍电解液除铜研究方向。
镍电解液;重金属;除铜
在镍的电解精炼中,无论是硫化镍阳极还是金属镍阳极都有铜杂质存在,铜在电解过程中部分会进入电解液中并且在阴极上析出,影响电解镍的质量,因此必须对镍电解液中的铜进行深度净化。目前,在镍电解精炼过程中,国内外对铁、钴的净化工艺控制得较好,唯有除铜工艺仍不能令人满意[1~3]。由于镍和铜的化学性质相似,其有效分离成为长期困扰国内外冶金界的难题。针对这一难题,也有一些专家尝试开发了一些新方法[4~7],但是至今尚未有效解决这一难题。
镍电解液中除铜方法有:氢氧化物沉淀法[8]、电化学法[9~13]、溶剂萃取与离子交换法[14~16]和硫化物沉淀法[17~19]。本文对镍电解液除铜技术进行了综述,并对今后镍电解液除铜技术的研究方向做了展望。
1 镍电解液除铜技术
镍电解阳极液除铜时,不仅要求除铜后液含Cu≤4.72×10-5mol/L,而且,为了能让除铜渣中镍的含量符合铜系统的要求,还必须要求除铜渣中的铜镍比ZCu/Ni≥15。为达到这个要求,长期以来许多学者做了大量的研究工作,提出了以下的除铜方法。
1.1 氢氧化物沉淀法
氢氧化物沉淀法是用碱调节溶液的pH值,在确保主金属离子不发生水解沉淀时,杂质金属离子以氢氧化物M(OH)n形态析出的方法。
金属离子水解按照下式进行:

镍电解液中一般含Ni2+75 g/L,而Cu2+的含量很低。在这种镍高铜低的溶液中通过调节溶液的pH值,铜在沉淀下来的同时镍也会沉淀下来。因此,通过调节溶液的pH值来获得合格的镍阴极液是比较困难的。
1.2 置换和电沉积法除铜
任何金属离子均可被比其更负电性的金属从溶液中置换出来,因此,电极电势比铜负的金属能从溶液中置换除铜,即:

考虑到经济成本,置换尽量用较为便宜的金属。同时,为了避免把其它杂质离子引入该系统,影响最终产品质量,原则上是镍系统用镍,钴系统用钴。
当用镍粉除铜时,其反应为:

1.2.1 镍粉置换法
国外镍电解厂多采用镍粉置换除铜的方法。例如,加拿大科尔鲍恩镍精炼厂、苏联北方镍公司、日本新居滨精练厂等都是用镍粉置换法净化除铜,直接用镍粉将溶液中的铜置换出来,而镍仍留存在溶液中。
金川公司镍钴研究所用液相加压氢还原得到的镍粉进行除铜研究[20]。所用镍粉含镍大于99.8%,粒度小于0.074 mm。当镍粉用量是理论量的1.4倍时,除铜后液含铜可降低至6.29×10-6mol/L,除铜率达99%以上。降低镍粉用量,除铜率明显下降。此法除铜效果较好,且不带入其它杂质,对环境无污染。但是,该方法除铜深度受镍粉活性及粒度的影响,镍粉的制备及保持活性难度大,造价较高不够经济,由于铜渣中含有较多未起作用的镍,还需进一步处理。按上述方法所得到的铜渣中ZCu/Ni比仅为12左右。
1.2.2 镍粉加硫磺置换
为了降低直接用镍粉除铜的镍粉制备难度,除铜过程除了加入镍粉外,还加入粒度小于74μm的硫粉,使Cu变为更稳定的CuS,降低生成物活度。文献[20]指出:以粒度为-147μm的镍粉,其用量与溶液中铜的摩尔量相同,按硫铜比(摩尔比)S/Cu= 0.5∶1,在温度为80~90℃,pH=2~2.5,除铜时间1~1.5 h,除铜结果如表1所示。

表1 镍粉+硫磺除铜结果
由表1可知,镍粉加硫磺除铜后除铜后液含铜1.57×10-5mol/L,能达到除铜的要求,而且除铜渣中含铜较高,其ZCu/Ni比能达50以上,能作为铜精矿直接并入铜熔炼系统。加拿大汤普森厂为了加速镍粉除铜反应,在加入镍粉的同时,还添加硫磺粉。
用镍粉或者镍粉+硫磺置换法除铜都能达到满意的结果,但是都要求镍粉粒度很细,而且还必须另建镍粉生产系统,所以不够经济。
1.2.3 一次合金置换除铜
一次合金所含Ni主要是以金属Ni的形态存在,它与溶液中的铜离子发生置换反应,如同镍粉与铜置换一样。理论上,置换反应达到平衡时,溶液中的铜浓度为5.2×10-20mol/L,达到深度除铜的要求。文献[20]报道了用一次合金置换除铜后溶液浓度变化如表2所示。
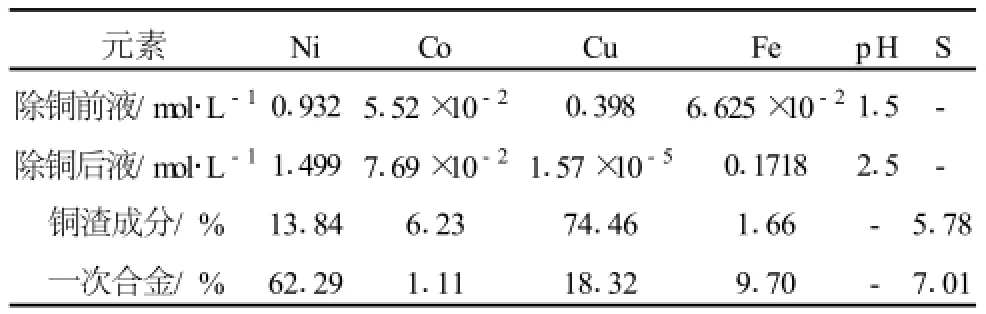
表2 一次合金除铜前后溶液浓度及除铜渣成份[20]
从表2可以看出,除铜后液铜浓度能达到1.57 ×10-5mol/L的要求。但是由于一次合金含铁高,除铜后又增加了溶液中铁的含量。虽然可以将除铁工序放在除铜工序之后进行,但仍增加了除铁工序的负担。另一方面,除铜渣中含镍高,铜镍比只有5~6,达不到铜精矿的要求,而且还会导致除铜渣中贵金属的流失,所以不宜采用。
1.2.4 电沉积法
将含Ni2+、Cu2+的混合液进行电解沉积,则Cu2+优先在阴极析出。当溶液中Ni2+浓度为1.28 mol/L时,根据式(3)可计算出溶液中铜浓度可降至5.2×10-20mol/L。日本唯一生产电镍的别子镍冶炼厂就是用电沉积法除铜[21~23],能生产出含铜95%、镍低于1%的铜粉,大大提高了镍的直收率。但该法缺点为:
1.要求电解液给液铜的浓度高达0.551 2 mol/L,并且在电解的过程中要不断地补充铜离子。
2.只适合于含铜高的镍电解液,电沉积铜后,槽内铜的浓度仍然较高,远高于式(3)的计算值,达到0.078 7×10-2~0.157 5 mol/L。
3.阴极电流效率低,只有70%左右。
此外,曾振欧等[24]采用电沉积法对金川镍电解阳极液除铜进行了研究。研究表明:在控制阴极电位不低于-0.500 V(vs.SCE.)、搅拌溶液和常温的条件下,用多孔镍做阴极的电沉积法可使得金川镍电解阳极液中铜离子浓度降至3.12×10-5mol/L以下,达到深度净化除铜要求;而且电沉积法净化除铜是以电子作沉淀剂,不引入任何有害新杂质阳离子进入溶液,净化除铜产物为99%以上的金属铜粉,简化了现有镍电解工艺流程、降低净化除铜成本、提高金属回收率和直收率。但是,此方法的能耗较高、溶液处理量小,不适合大规模生产。
1.3 硫化法除铜
在镍电解阳极液的各种元素中,以铜的硫化物溶度积为最小,并且与镍钴等主金属硫化物的差别较大,故很多专家均采用硫化法对硫化镍电解阳极液进行铜镍分离。目前,硫化法除铜剂包括硫化氢、镍精矿、“NSH”试剂、硫和二氧化硫、活性阳极泥、硫代硫酸镍或硫代硫酸钠、活性硫化镍。
1.3.1 硫化钠(氢)盐沉淀法
硫化钠(氢)盐沉淀法所利用的除铜剂是:硫化氢、硫化钠、硫氢化钠。硫化氢除铜的反应为:

硫化氢除铜过程是首先将Na2S溶液与稀H2SO4溶液反应产生H2S气体,通入镍电解阳极液中,使Cu2+和S2-充分接触生成无数的CuS沉淀晶核,这些晶核在反应过程中通过自身的运动和扩散、碰撞、吸附而长大,最终沉淀于底部。经过滤,铜便从溶液中除去。为防止硫化氢溢出,除铜应在负压下操作,并控制pH值在2以下,可控制Ni2+和Co2+因沉淀而进入除铜渣中。
我国成都电冶厂和重庆电冶厂均采用H2S除铜。其除铜过程技术条件为[20]:溶液温度>60℃;硫化氢发生器负压值0~3×10-2MPa;反应室负压值0~2.5×10-2MPa;硫化氢发生器温度33~55℃;除铜前液含铜≥7.874×10-5mol/L;除铜后液含铜<1.575×10-5mol/L;硫化钠溶液浓度0.83~1 mol/L;硫酸溶液浓度55%~57%。
当除铜剂为硫化钠、硫氢化钠时,这些沉淀剂大部分必须在碱性溶液中使用,因为在酸性溶液中容易放出硫化氢,影响人体健康,而在碱性溶液中镍、钴、铜会生成氢氧化物沉淀,使铜渣含镍、钴高,不能达到比较彻底的分离目的,还带入了钠离子。而且,由于H2S气体的腐蚀性和剧毒性,从而阻碍了它的应用。
1.3.2 硫化镍精矿加阳极泥除铜法
硫化镍精矿加阳极泥除铜的反应如下:
金川公司在镍电解除铁后液中,加入配比为3.5~5.0∶1的镍精矿与阳极泥,在温度为60~70℃, pH=2.5~3.5下进行除铜,该方法的优点是除铜操作时可同时提高溶液中镍离子浓度,采用原料和副产物做置换剂,省去了镍粉制备工序,既方便又经济,除铜后液含铜≤4.72×10-5mol/L,能达到生产要求。其缺点是:(1)渣量大,每吨电镍产铜渣约150 kg;(2)除铜渣中铜镍比低,远远达不到铜冶炼系统的要求,还要进行氯气浸出;(3)金属回收率低、损失大;(4)除铜氯气浸出渣的后续处理麻烦。
1.3.3 活性硫粉除铜法
翟秀静等[25]发现活性硫有很好的除铜效果,它与升华硫的晶格结构没有质的区别,但试验中发现,刚制备出的活性硫颗粒极小。正是由于其分散度高,又刚刚制备出来,其表面活性大,容易与铜离子反应,产生较好的除铜效果。用活性硫粉除铜的技术参数为:pH=2.8,温度为70℃,S/Cu为2.5,在此条件下,除铜渣中ZCu/Ni可达到100∶1,远高于工业生产20∶1的指标,净化后溶液含铜可降至3.15× 10-5mol/L。但是,活性硫难以制备,硫的活性也难以保证[26,27],故很难实现工业化。
1.3.4 S-SO2除铜
用S和SO2除铜就是往含铜的镍、钴溶液中同时喷入二氧化硫和硫磺粉,在有铜离子存在的条件下,镍、钴离子不会被硫化而铜离子可以被硫化沉淀,从而使铜与镍、钴分离并产生适于铜熔炼的铜精矿。
彭济时等[28]用S和SO2对镍电解液除铜进行了研究。研究表明:用S-SO2法处理镍钴生产中产出的各种含铜、镍、钴的溶液,使其中的铜硫化沉淀并产出高铜镍比的渣是完全可行的。
此法除铜范围广,可适于3.15×10-3~0.472 mol/L的含铜溶液,除铜后液含铜小于1.57×10-5mol/L,铜渣含镍、钴低,可以达到铜精矿水平,直接返回铜系统处理。而且硫粉和二氧化硫来源方便。虽然此法不引入杂质阳离子进入镍电解系统,但是除铜终点难控制,而且工作环境比较恶劣。在最近几年,日本、北美等国用该工艺,在低Cl-浓度的氨性浸出液中取得了成功,但是对我国的酸性溶液则不够理想。而且,这种方法受溶液中氯离子影响大,对高氯离子溶液,难以达到深度除铜目的。
1.3.5 活性阳极泥除铜法
活性阳极泥是指硫粉表面覆盖CuS的阳极泥,阳极泥的活性用百分数来示。舒余德等[27]采用活性阳极泥从镍电解液中除铜。氯离子浓度70 g/L时,最佳工艺条件是:活性阳极泥量3.3 g/L,阳极泥活性30%,H2SO312.5 ml/L,温度80℃,pH=3.5,时间50 min。在该条件下,镍电解阳极液中的铜脱除到1.3 mg/L,铜渣Cu/Ni比达到23.13。
但是氯离子浓度会对脱铜效果有明显的不良影响。随着氯离子浓度的增加,脱铜效果变差,但通过增加亚硫酸添加量可以克服氯离子对脱铜的影响。1.3.6 硫代硫酸镍除铜法
用硫代硫酸镍作为硫化剂来实现铜镍分离早己被人们所重视,其原理是镍、钴离子不会被硫化沉淀而铜离子可以被硫化沉淀,从而使铜与镍、钴分离。S2O32-基团中的其中一个硫原子在温度较高时不稳定,它易于分离出来而成为S2-离子,在一定温度下,便可实现硫化物溶度积不同的金属离子之间的有效分离。
根据镍电解阳极液中除铜的要求,曾德文等[29]研究了硫代硫酸镍的合成方法以及用它来除去镍电解阳极液中铜的可能性。除铜最佳工艺除铜条件为:S2O32-与Cu2+的摩尔比为5~6.25,除铜温度为65~70℃,反应150 min,用硫代硫酸镍从镍电解阳极液中除铜,当氯离子浓度不大于4.225 mol/L时,可使其中的铜含量降到3.15×10-5mol/L以下,同时渣中铜镍比大于20∶1。
从3个年级分别采用基于K-means算法的评选方法和传统评选方法的结果对比表中可以分析出:基于K-means算法的评选结果与传统评选结果存在部分重叠的情况,是因为部分班级不仅总分高,而且班级各属性值都较均衡,同时可以说明,新的优秀班集体评选方法,在传统评选方法的基础上兼顾了班级各项评价属性的均衡发展。
金川公司[30]采用硫代硫酸镍净化镍电解液中的铜。其工艺过程为:在镍电解液中按S2O32-:Cu2+= 4.4~7∶1(摩尔比)的比例加入硫代硫酸镍,在65~70℃温度下,加酸调整pH值为0.5~2;搅拌反应30~40 min,过滤分离出生成的CuS沉淀后得到除铜后液。硫代硫酸镍除铜剂的使用使铜渣量减少到现在的1/4,降低了工艺强度,节约了人力,降低了能耗。
可见,用硫代硫酸镍除铜,具有引入杂质少、除铜深度受氯离子浓度的影响小、无污染、除铜彻底、渣中铜镍比高等诸多优点,但是,硫代硫酸镍的制备条件很苛刻,而且在溶液中硫代硫酸镍是不稳定的,容易发生分解,在工业上难以实现。
1.3.7 硫化镍转化法
硫化镍有三种晶型,即α无定形、β六方晶型和γ三方晶型[31]。β与γ型由于晶型稳定,活性差,不能用来除铜,α无定形有较高活性,可用于除铜。
王飞镝等[32]用硫化镍转化法来从镍电解液中除铜。新制备的NiS的用量为电解液中铜量的1.2倍(按摩尔计)时,便可使溶液中残铜量降低至3 mg/L以下,除铜率可达99.5%以上,除铜效果很好;用NiS除铜的最佳工艺条件是:溶液pH值在2.0~3.0之间,反应温度60℃,反应时间45 min。新制备的NiS不宜暴露在空气中,否则影响除铜效果。用此试剂除铜,渣量少,并且渣中铜镍比可达6左右,渣通过酸洗,铜镍比可提高到10以上,比镍精矿法大有提高,因此具有广阔的应用前景。
1.3.8 “NSH”试剂除铜法
因而,镍电解阳极液净化用“NSH”试剂除铜是一种兼有硫化钠、二氧化硫、多硫化物等几种方法优点的新的除铜方法[33],其配方比例可根据镍电解液的成份来确定。除铜后液含铜能达到4.72×10-5mol/L以下,铜镍比也能达到20以上,但是有二氧化硫的毒性气体放出。
1.3.9 NAS和硫化镍混合物除铜法
赵中伟等[34]用新设计的NAS和硫化镍混合物除铜。结果表明:当NAS纯度α≥73%、除铜剂用量为理论量的1.2倍、溶液pH值为4.0、反应温度为60℃时反应80 min后,采用新型除铜剂从镍电解阳极液中除铜,除铜后溶液中的铜浓度可降至1.57× 10-5mol/L,除铜渣中铜镍质量比不小于25,远优于工业生产的要求(c(Cu2+)≤1.57×10-5mol/L,渣中铜镍质量比不小于15);NAS在自然条件下放置62 d后,其除铜效果仍然能够满足生产要求,且NAS在除铜过程中没有引入有害离子进入溶液。
1.3.10 新型淀粉黄原酸盐法除铜
在二十世纪七、八十年代,我国科技人员研制了ISX乳液和固剂等剂型,以淀粉为主要原料,合成了新型不溶性黄原酸镍NiISX,其结构如图1[35]。由于CuISX比NiISX的KSP值小7个数量级,因此, Cu2+与ISX成盐ISX-有疏水性,一旦Cu2+与ISX-成盐,可在短时间内迅速沉积,达到对镍液的净化目的。

图1 黄原酸镍NiISX
王飞镝等[35]利用合成的新型淀粉黄原酸盐-NiISX进行了镍电解液除铜的研究。研究结果表明,在电解液pH=3.0,温度55℃,反应时间20~30 min、NiISX用量为1.3倍理论量时,可使电解液中Cu2+的浓度从9.45×10-3mol/L降低到0.03× 10-3mol/L以下,渣中铜镍比达到4。
新型淀粉黄原酸盐法的优点是NiISX合成方法简单,易于存放;但是该法除铜渣中含镍高,铜镍比只有4,渣不符合返回铜系统的要求,而且还会导致除铜渣中贵金属的流失,所以不宜采用。
1.4 萃取和离子交换法除铜
1.4.1 萃取法
溶剂萃取是现代湿法冶金过程相似元素分离的有效技术[36]。提取铜的萃取剂分为酮肟、醛肟、二酮类、三元胺类、醇类和酯类及其复配物这几类。目前,主要使用的铜萃取剂是肟类有机化合物及其复合物。主要包括:P204,P507,Cyanex272,TIOA, TOA,Kelex系列试剂以及Henkel公司的LIX系列萃取剂等[37]。
用季铵盐从氯化物介质中萃取过渡金属的研究颇多。L.M.Ivanov等人曾用烷基氯化苄铵萃取分离钴和铜以及从镍电解液中萃取除钴、铜、铁[38]; V.V.Bagreev等人研究了从氯化物体系中用季铵盐萃取共存金属的相互影响[39];M.H.N.H.Irvins等人的研究认为Cu2+、Fe2+易发生氧化还原反应,即Cu2+被还原为Cu+,Fe2+则被氧化为Fe3+,从而Cu2+主要以CuCl2-络阴离子的形式被季铵萃入有机相,而Fe3+在氯化物介质中是以络阴离子FeCl4-形态存在,萃取机理如下[40~42]。

其萃取剂为三烷基甲基氯化铵-R3R1INCl,稀释剂为电子二甲苯,溶液中萃取金属离子浓度可达到2.18×10-2mol/L,萃余液中铜、铁的含量均少于7.874×10-5mo/L。Ni基本不萃取,铜镍分离系数达到106以上。
但是,此工艺适应范围窄,溶液中Cl-浓度不能太高,只适合于用季铵氯化物从大约1.408 mol/L氯离子浓度的镍、钴硫酸浸取液中萃取除铜。
也有采用M5640从硫酸镍溶液中萃取除铜的研究。吴芳等[43]对M5640-煤油-H2SO4萃取体系分离硫酸镍溶液中的Cu2+进行了研究。结果表明,平衡pH=2.0左右,以浓度为20%~30%的M5640为萃取剂、2 mol/L硫酸溶液为反萃剂,经3级萃取、3级反萃后,可以从含有5 g/L Cu,50 g/LNi浓度的硫酸镍溶液中分离出99.9%的Cu,反萃液中铜以硫酸铜的形式存在,Ni的萃取率小于0.5%。
蒙延双等[44]以P204为萃取剂从镍电解液中除铜。室温下P204萃铜的最佳工艺为:P204的体积浓度,相比(O/A)=1∶2,水相pH=2.0,振荡时间3 min。在最佳条件下待处理液的一级萃取率达81.33%,反萃率可达84.97%。
但是,由于萃取过程中pH应控制在2.0~3.0,而除铁后液pH在4.5左右,因此,调节溶液的pH值要消耗较多的酸,而且洗水量大。
1.4.2 离子交换法
Pb2+、Zn2+、Cu+均易和溶液中的阴离子形成配合物,其中Cu+与氯离子形成的CuCl2-、CuCl32-的稳定常数最大,而且Cu+的配合稳定常数比Cu2+、Ni2+大得多。当溶液中存在Cu+和Ni2+,Ni2+形成阴离子的可能性很小,主要是以阳离子形式存在, Cu+将优先成CuClX-x+1阴离子,再利用阴离子交换树脂进行吸附和分离。陈爱良等[45]利用此原理,用离子交换法对镍电解阳极液除铜进行了研究。研究结果表明:镍电解阳极液中Cu2+被还原为Cu+时,随着还原电位的降低,离子交换操作容量增大;当电位达到0.47~0.45 V的时候,其操作交换容量达到最大;镍电解阳极液中Cu2+被还原为Cu+的最佳条件为:硫系数(实际加入亚硫酸钠的量与理论需要量之比)为4.5,pH=2.0,反应时间为0.5 h,反应温度为40℃;离子交换过程中,随着离子交换柱高径比的增加,交换容量(用漏穿体积V2/树脂体积V1表示)增加,当高径比达到48.08之后,V2/V1基本不变;随着交前液铜离子浓度的增加,树脂操作交换容量稍有增加,交换体积减少。而且,用此法分离铜镍,在整个交换过程中SO42-浓度没有太大变化。
温俊杰等[46]在模拟氯化镍电解液中用新型硅胶-聚合胺复合材料树脂SP-C进行深度净化除铜的研究。研究结果表明:随料液pH值增大以及温度升高,铜的交换容量增大;料液中铜浓度对交换容量影响较小;最佳吸附条件为:料液pH=4、接触时间30 min,温度60℃。研究表明硫酸比盐酸显示出更好的解析效果,最佳解析条件为:H2SO42 mol/L、解析接触时间40 min。最佳工艺条件下每毫升湿树脂铜的工作交换容量及饱和交换容量分别0.453 mol和0.540 mol,铜的解析峰值液浓度为28 g/L。
尽管离子交换法由于其工艺简单、对不同离子的分离效果好,而且除铜之后无除铜渣,在冶金、化工领域广泛用于溶液的净化及相似元素的分离,但是,离子交换树脂同萃取剂一样[3,4],由于饱和容量的限制,只适合于小批量生产,镍电解阳极液镍高铜低,温度较低(<20℃)时,镍会很容易在树脂中结晶成镍盐,而且洗水量大,带来洗水的处理问题。
2 镍电解液除铜发展的方向
综上所述,在现有冶金技术发展水平下,氢氧化物沉淀法、置换法和电沉积法都不能满足从镍电解阳极液中净化除铜的要求。随着环保标准的不断提高,以及有色行业“十二五”节能减排的要求,镍冶金清洁生产是必须要进行的。因而,镍电解液除铜的研究需要在以下两个方面做出突破:
1.硫化物除铜是目前工业上很成熟的工艺,但是其副作用是会产生硫化氢气体,对环境的污染较大。由于易发生化学转变,限制了“活性硫化镍法”在除铜的应用。但是借助“活性硫化镍法”除铜的思想深入研究,将有可能获得理想的除铜试剂。
2.溶剂萃取技术在国内外的湿法炼铜厂得到广泛的应用,因此,可以考虑将溶剂萃取用于镍电解液的净化除杂。通过中试试验,对萃取的设备进行改进和优化,对萃取的工艺条件进行优化,以降低经济成本。解决萃取过程中的乳化、界面絮凝物、有机物污染等问题。
3 结 语
镍电解液除铜是镍冶金中尚未有效解决的问题,现有的除铜方法因为各自的缺点的限制而应用较少。目前,工业上广泛应用的方法是硫化物除铜法,但是其对环境污染大,工作环境比较恶劣。因此,需要找到新型的对环境污染更小或者无污染的除铜方法。要解决经济发展与环境之间的矛盾,只能靠技术的不断进步。因此,科研工作者需要研发更清洁,更经济的镍电解液中除铜技术。
[1] 黄其兴,王立川,朱鼎元.镍冶金学[M].北京:中国科学技术出版社,1990.8-10.
[2] Lazaridis N K,Peleka E N,Matis KA.Copper removal from effluents by various separation techniques[J].Hydrometallurgy,2004, 74(1/2):149-156.
[3] Ivanov I M,Nikolaeo A V,Gindin L M,et al.Solvent extraction removal of cobalt and other impurity elements from nickel electrolytes[J].Hydrometallurgy,1979,4(4):377-387.
[4] Zhang Hong-guang,Dreisinger D B.The adsorption of gold and copper onto ion-exchange resins from ammoniacal thiosulfate solutions[J].Hydrometallurgy,2002,66(1/2):67-76.
[5] Kong D,Martell A E,Motekaitis R J,et al.Two novel homodinuclear Ni(Ⅱ)and Cu(Ⅱ)complexes with a 24-membered octadentate hexaazamacrocyclic ligand:stability and X-ray crystal structures[J].Inorganica Chimica Acta,2001,317(1/2):243-251.
[6] Xu Guang-ri,Chang H Y,Cho H.Macrocyclic nickel(Ⅱ)complex and hydrophilic polyurethane film electrodes for the electrocatalytic oxidation and selective detection of norepinephrine[J].Electrochimica Acta,2004,49(24):4 069-4 077.
[7] Lee C I,Yang Wan-fa,Hsieh C I.Removal of copper(Ⅱ)by manganese-coated sand in a liquid fluidized-bed reactor[J].Journal of Hazardous Materials B,2004,114(1/3):45-51.
[8] Gamburg YD,Groshev M Y,Biallozor S,et al.The electrochemical deposition of nickel from electrolytes containing malonic acid[J]. Surface and Coatings Technology,2002,150(1):95-100.
[9] Singh V,Pandey P.Electrodeposition of nickel composites fromwater-diethanolamine bath[J].Surface and Coatings Technology, 2006,200(14-15):4 511-4 514.
[10] Fei Jing-yin,Wileox G D.Electrodeposition of zinc-nickel compositionally modulated multilayer coatings and their corrosion behaviours[J].Surface and Coatings Technology,2006,200(11): 3 533-3 539.
[11] Lira-CantúM,Sabio A M,Brustenga A,et al.Electrochemical deposition of black nickel solar absorber coatings on stainless steel AISI316Lfor thermal solar cells[J].Solar Energy Materials and Solar Cells,2005,87(1-4):685-694.
[12] Geoffroy R P,Everaldo C.Electrodeposition of nickel on carbonfelt[J].Electrochimica Acta,2004,49(27):4 933-4 938.
[13] Ger Ming-Der.Electrochemical deposition of nickel/SiC composites in the presence of surfactants[J].Materials Chemistry and Physics,2004,87(1):67-74.
[14] Lilga M A,Orth R J,Sukamto J P H,et al.Metal ion separations using electrically switched ion exchange[J].Seperation and Purification Technology,1997,11(3):147-158.
[15] HuangTing-Chia,Lin Yih-Kung,Chen Chi-Yih.Selective separation of nickel and copper from a complexing solution by a cationexchange membrane[J].Journal of Membrane Science,1988,37 (2):131-144.
[16] Belcher R,GIBbons D,West T S.The determination of copper by complex-ometric titration with ethylenediaminetetraacetie acid [J].Analytica Chimica Acta,1955,(13):226-229.
[17] Cailteux J L H,Kampunzu A B,Lerouge C,et al.Genesis of sediment-hosted stratiform copper-cobaltdeposits,central African Copperbelt[J].Joumal of African Earth Sciences,2005,42(1-5):134-158.
[18] Cailteux J L H,Kampunzu A B,Lerouge C,et al.Mineralization controls in island arc settings:Insights from PhiliPPine Metallic deposits[J].Gondwana Research,2003,6(4):767-776
[19] Raghunathan K,Weil R.The effects of some plating variables on the structure of thin nickel eleetrodeposits[J].SurfaceTechnology,1980,10(5):331-342.
[20] 邓全民.从Ni-Co-Cu溶液中分离铜方法评述[A].赵捷,李仕雄,郑隆鳌.全国第二届湿法冶金第三届有色金属物理化学学术会议论文集(下册)[C].长沙:中国有色金属学会、中国核学会,1991.895-905.
[21] William W S,Ricky C S C,Chin C L.An effective diffusion barrier metallization process on copper[J].Thin Solid Films,2000,376 (1-2):164-169.
[22] Kudelski A,Janik-Czachor M,Bukowska J,et al.Surface-enhanced Raman scattering(SERS)on copper electrodeposited under nonequllibrium conditions[J].Journal of Molecular Structure, 1999,482(1):245-248.
[23] Read D T,Cheng Y W,Geiss R.Morphology,microstructure,and mechanical properties of a copper electrodeposit[J].Microelectronic Engineering,2004,75(1):63-70.
[24] 曾振欧,曾颖如,吴鸿儒.金川镍电解阳极液净化除铜的电沉积法研究[J].湖南冶金,1994,(4):11-14.
[25] 翟秀静,王昌昊,肖碧君,等.镍浸出液净化除铜研究[J].有色冶金(冶炼部分),1997,(4):19-22.
[26] 舒余德,颜小雄,陈白珍,等.镍电解液除铜用活性阳极泥的制备[J].有色金属(冶炼部分),1996,(5):24-26.
[27] 舒余德,颜小雄,陈白珍,等.用活性阳极泥脱除镍电解液中铜的研究[J].有色冶金(冶炼部分),1994,(6):8-10.
[28] 彭济时,王成刚.用S和SO2从镍电解阳极液中分离铜的研究[J].有色冶金(冶炼部分),1992,(6):30-34.
[29] 曾德文,李作刚,徐盛明.用硫代硫酸镍从镍电解阳极液中除铜的试验研究[J].湖南有色金属,1996,12(4):49-53.
[30] 常全忠,毛西康,马岩,等.一种镍电解液净化除铜方法[P].中国专利:200410056894,2008-04-02.
[31] 拉宾诺维奇B A,哈文ЗЯ.简明化学工业手册[M].北京:化学工业出版社,1983.163.
[32] 王飞镝,王开,陈玉兰.硫化镍沉淀转化法从镍电解液中深度净化除铜的研究[J].湖南有色金属,1993,(5):21-23.
[33] 陈斌,袁志昌,程文清.镍电解液净化多硫化物试剂除铜的研究[J].西安建筑科技大学学报,1997,29(2):212-217.
[34] 赵中伟,陈爱良,孙培梅,等.镍电解阳极液深度除铜[J].有色金属学报,2009,19(4):749-753.
[35] 王飞镝,邱清华,王开毅.新型淀粉黄原酸盐从镍电解阳极液中除铜的研究[J].有色金属(冶炼部分),1999,(2):16-18.
[36] 李洪桂.冶金原理[M].北京:科学出版社,2005.264-283.
[37] 吕文东,郝志峰,王继民.湿法炼铜中的萃取剂[J].广东有色金属学报,2001,14(2):114.
[38] Groudev S N,Spasova I I,Ivanov I M.Two-stage microbial leaching of a refractory gold-bearing pyrite ore[J].Minerals Engineering,1996,9(7):707-713.
[39] PlatéN A,Lebedeva T L,Shand GA,et al.On the mechanism of metal-ions facilitated transport through pseudo-liquid membranes [J].Journal of Membrane Science,1995,104(3):197-203.
[40] 王飞摘,邱清华,王开毅.用2-羟基-4-仲辛氧基二苯甲酮肪从镍电解液中萃取除铜的研究[J].广东有色金属学报,2001,11 (1):37-40.
[41] Reddy B R,Sarma P B.Transfer of nickel from sodium sulphate solutions to the spent electrolyte through solvent extraction and stripping[J].Hydrometallurgy,2001,60(2):123-128.
[42] Wang Kai-yi,Shu Wan-yin.Separation of cobalt and nickel from ammoniacal solution by solvent extraction withβ-hydroxyoxime N530 as extractant[J].J Cent South Inst Min Metal,1998,19 (4):473-474.
[43] 吴芳,吕军.铜萃取剂M5640从硫酸镍溶液中分离铜的应用研究[J].五邑大学学报(自然科学版),2004,18(3):25-28.
[44] 蒙延双,朱福良,张峰,等.镍电解液用P204萃取除铜[J].有色金属(冶炼部分),2007,(6):7.
[45] 陈爱良,孙培梅,赵中伟,等.用离子交换法从镍电解阳极液中除铜的研究[J].矿冶工程,2005,25(6):51-54.
[46] 温俊杰,张启修,张贵清,等.新型硅胶聚合胺树脂在模拟氯化镍电解液中深度除铜[J].矿冶工程,2007,27(3):57-60.
Abstract:The removal of copper from nickel electrolyte was not solved validly in nickel metallurgy.Technologies of copper removal from nickel electrolyte at home and abroad were introduced.In addition,the future research directions of copper removal from nickel electrolyte were also pointed out.
Key words:nickel electrolyte;heavy metal;copper removal
Research Progress of Copper Removal from Nickel Electrolyte
ZHAO Si-jia
(Hunan Research Institute of Nonferrous Metals,Changsha410015,China)
TF815
A
1003-5540(2012)02-0019-07
2011-12-26
赵思佳(1983-),男,助理工程师,主要从事有色金属冶金以及功能材料研究。
