益气复原合剂微生物限度检查方法的验证
2012-09-18孔燕兴黄校锋黄亚彬
孔燕兴 黄校锋 黄亚彬
(1 广东省广州市中西医结合医院药剂科,广州510800;2 广州中医药大学中药学院,广州510800)
益气复原合剂微生物限度检查方法的验证
孔燕兴1黄校锋2黄亚彬1
(1 广东省广州市中西医结合医院药剂科,广州510800;2 广州中医药大学中药学院,广州510800)
目的 验证益气复原合剂的微生物限度检查方法是否适用于该供试品的检查。方法 细菌计数采用常规法,霉菌及酵母菌计数按常规检查法,控制菌按常规检查法。结果 稀释剂对照组的菌回收率大于70%,试验组的菌回收率大于70%;阴性对照组未检出阴性对照菌,试验组检出阳性试验菌。结论 可以用该微生物限度检查法进行益气复原合剂的检查。
益气复原合剂;微生物限度检查法;验证
益气复原合剂是我院制剂室2012年获得批准文号的新制剂品种,具有益气活血、通络开窍的作用。用于中风及中风后遗症之偏瘫肢体乏力、失语、痴呆等。为了保证检验方法的科学性,现对我院制剂室生产的益气复原合剂的微生物限度检查方法进行方法学验证,验证此方法是否适用于该供试品的检查。
1 材料与仪器
1.1 试验样品 药品名称:益气复原合剂,批号:120120,来源:广州市中西医结合医院制剂室。
1.2 验证用仪器
1.2.1 一般仪品 霉菌培养箱(MJ-160-DSM)、隔水式电热恒温箱(PYX-DHS-35X-40)、电热恒温鼓风干燥箱(DHG- 9053A)、数显立式压力蒸汽灭菌器(YXQLS-50S)、电子天平等。
1.2.2 玻璃器皿 锥形瓶、培养皿、量筒、试管、吸管等。
1.3 验证用菌种 金黄色葡萄球菌[CMCC(B)26003];大肠埃希菌[CMCC(B)44102];枯草芽孢杆菌[CMCC(B) 63501];白色念珠菌[CMCC(F)98001];黑曲霉菌[CMCC (F)98003],均由中国药品生物制品鉴定所提供。
1.4 验证用培养基及稀释剂 营养琼脂培养基;玫瑰红钠琼脂培养基;胆盐乳糖培养基;营养肉汤培养基;改良马丁培养基;曙红亚甲蓝琼脂培养基,均由中国药品生物制品鉴定所提供。
2 验证条件
无菌室环境洁净度为10000级,局部洁净度为100级,净化消毒30min以上,供试品及灭菌的器具等经传递窗紫外杀菌灯照射30min置无菌室内,试验人员手消毒后穿无菌服进入操作间。
3 方法与结果
3.1 菌液制备[1]接种金黄色葡萄球菌、大肠埃希菌、枯草芽孢杆菌的新鲜斜面培养物接种于营养肉汤培养基中,于35℃培养18~24h,分别取各菌种培养液1ml加入0.9%无菌氯化钠溶液9ml中,10倍依次稀释[3],金黄色葡萄球菌稀释至10-5,大肠埃希菌稀释至10-7,枯草芽孢杆菌稀释至10-5,约为50~100cfu/ml,备用。
接种白色念珠菌的新鲜培养物至改良马丁培养基中,于23~28℃培养23~48h,取培养液1ml加入0.9%无菌氯化钠溶液9ml中,10倍依次稀释至10-5,约为50~100cfu/ml,备用。
取黑曲霉的新鲜斜面培养物,用0.9%无菌氯化钠溶液5ml将孢子洗下,吸取此溶液1ml置于一个无菌的比色管中,加0.9%无菌氯化钠溶液适量与标准比浊管进行比浊,取比浊后的菌悬液1ml加入0.9%无菌氯化钠溶液9ml中,10倍依次稀释至10-4,约为50~100cfu/ ml,备用。
3.2 供试液制备 取供试品10ml,加pH7.0无菌氯化钠-蛋白胨[2]缓冲液至100ml,混匀,为1:10供试液。
3.3 细菌、霉菌及酵母菌计数验证试验
3.3.1 试验组 取1∶10供试液1ml,分别加入5个平皿中(每皿0.2ml),加入各阳性细菌试验菌1ml,立即倾注相应的琼脂培养基,置32℃恒温培养箱中培养48h,测定细菌数。霉菌及酵母菌计数采用常规法,取1∶10供试液1ml,加入各霉菌及酵母菌试验菌1ml,立即倾注玫瑰红钠琼脂培养基,置25℃恒温培养箱中培养72h,测定霉菌及酵母菌数。
3.3.2 菌液组 取稀释好的各菌液1ml,分别加入平皿中,加入相应培养基,置规定条件培养,测定所加的试验菌数。
3.3.3 供试品对照组 按试验组方法,测定供试品本底菌数。
3.3.4 稀释剂对照组 取稀释剂替代供试液,方法同试验组。
3.3.5 回收率三次测定结果 见表1。
试验组菌回收率(%)={(试验组平均菌落数-供试品对照组平均菌落数)/菌液组平均菌落数}×100% ;
稀释剂对照组菌回收率(%)=(稀释剂对照组平均菌落数/菌液组平均菌落数)×100%。
3.4 控制菌检查方法的验证
3.4.1 试验组 取供试液10ml及10~100cfu试验菌加入100ml胆盐乳糖培养基中,在35~37℃培养24h,取培养物0.2ml接种至含5mlMUG培养基的试管内培养,于5h、24h在366nm紫外线下观察,同时用未接种的MUG培养基作本底对照。观察后,沿培养管的管壁加入数滴靛基质试液。
3.4.2 阴性对照组 取金黄色葡萄球菌50~100cfu为对照,同法操作。
3.4.3 控制菌检查方法验证结果 见表2。
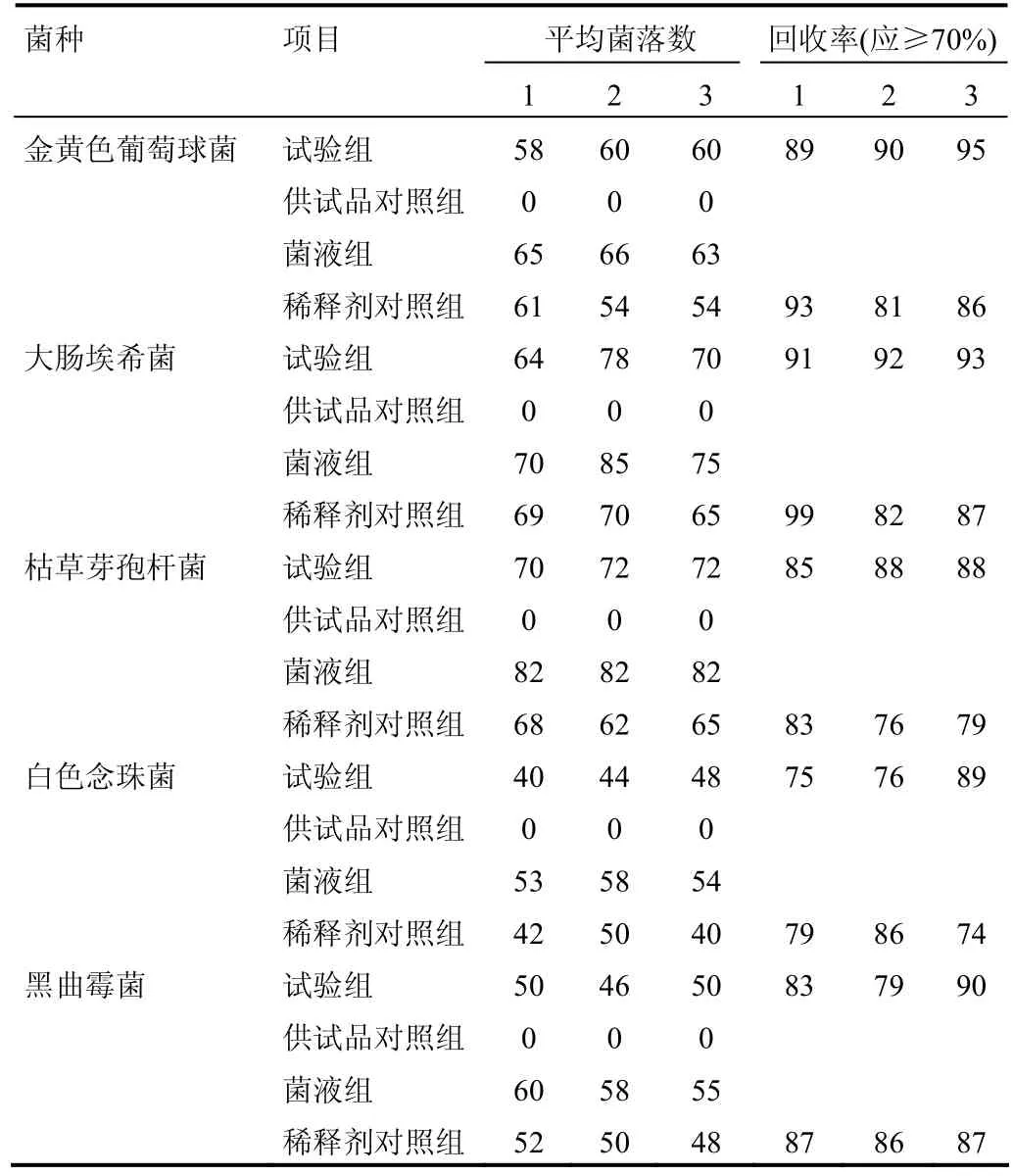
表1 常规法验证各试验菌的回收试验结果 (cfu.ml-1)

表2 控制菌检查方法验证结果
3.5 结果分析
3.5.1 细菌、霉菌及酵母菌计数验证结论 在三次试验中,稀释剂对照组的菌回收率均大于70%,试验组的菌回收率均大于70%,说明供试品无抑菌性;可采用常规法进行试验。
3.5.2 控制菌验证结论 在三次试验中,阴性对照组未检出阴性对照菌,试验组检出阳性试验菌,可用常规法进行控制菌检验。
[1] 国家药典委员会.中华人民共和国药典第一部[S].北京:化学工业出版社,2010,附录79-88.
[2] 陈建梅.微生物限度检查方法验证影响因素分析[J].药品药检,2008,5(12): 66-68.
[3] 郑继明.理气解郁合剂微生物限度检查验证[J].St rait Pharmaceutical Journal,2010,22(10):75-77.
10.3969/j.issn.1672-2779.2012.18.109
1672-2779(2012)-18-0
2012-07-26)
