阿尔茨海默症治疗药物的研发现状和发展趋势
2012-09-18郝博济
郝博济
阿尔茨海默症治疗药物的研发现状和发展趋势
郝博济
阿尔茨海默症是一种持续性神经功能障碍,早期最显著的症状为健忘,通常表现为逐渐增加的短期记忆缺失,而长期记忆则相对不受病情的影响,随着病情的加重,病人的语言能力、空间辨别能力、认知能力会逐步衰退[1]。近年来随着对老年人神经生理、生化、药理等方面研究的不断深入,相关药物的开发和新的治疗方法不断取得进展。本文借助Thomson Reuters Pharma信息平台,从药物的研发阶段、药物靶标和药物的作用机制等方面对阿尔茨海默症治疗药物的研发现状进行了统计、分析和研究,并对其可能的发展趋势和方向进行了预测和判断。
一、药物研发现状
按照新药研发工作内容的不同可将新药研发分为4个阶段:药物发现、临床研究、新药注册和药品上市,这4个阶段构成了新药研发的整个生命周期。目前,已有超过1000种化合物或药物制剂被研究并尝试用于阿尔茨海默症的治疗,其中20种药物已经上市,131种正在进行临床研究(药品注册阶段5种,Ⅲ期临床试验9种,Ⅱ期临床试验55种,Ⅰ期临床试验52种,其他临床阶段10种),290尚处于药物发现阶段。与此同时,还有189种药物处于研发终止状态,原因可能与经济条件、药物的有效性和安全性以及风险/利益的权衡结果有关,458种药物缺少进一步的研发报道,这些药物的研发活动很有可能也被终止或取消,但缺少足够的公开信息证明。本文后续部分提到的研发终止的药物指已经被公开报道暂停、终止或撤销研究的药物。(注:本文使用的资料或数据来源于Thomson Reuters Pharma信息平台,截至2012年3月)。
二、药物靶标
阿尔茨海默症病因复杂,发病涉及诸多环节,如Aβ产物过多、Tau蛋白过度磷酸化、过氧化作用、炎症因素、金属与细胞内钙稳态紊乱、遗传因素等,这些环节为药物靶标的发现和选择提供了多种靶点[10]。目前,研究报道较多的药物靶标主要有乙酰胆碱酯酶、β淀粉样蛋白、Tau蛋白、γ分泌酶、β分泌酶、N-甲基-D-天冬氨酸受体、5-羟色胺6受体(5-HT6receptor)、毒蕈碱M1受体(Muscarinic M1 receptor)、烟碱乙酰胆碱受体(Nicotinic ACh receptor)等。表2列出了按各研发阶段药物数量统计的靶标分布情况。

表2 按各研发阶段药物数量统计的靶标的分布情况
1.乙酰胆碱酯酶:阿尔茨海默症患者脑内胆碱能神经元丢失导致突触部位的ACh水平下降,影响人的短期注意力和记忆力,而乙酰胆碱酯酶抑制剂(acetylcholinesterase inhibitor,AchEI)通过抑制AchE的活性,恢复ACh的正常水平,提高胆碱能神经元的兴奋性,从而改善认知功能[11]。AchEI因其疗效确切成为最早获美国FDA批准用于治疗轻至中度阿尔茨海默症,也是目前使用最多的,20种已上市的药物中即有12种以AchE为靶标。但临床研究阶段和药物发现阶段AchE靶标使用率处于较低水平,分别为12和7,远低于其他靶标,与此同时,21种以AchE为靶标的药物被公开报道中止研究或开发,位列第2位,可见AchE靶标研究及相关新药开发可能已经趋于饱和,对此类药物的研发应谨慎对待。
2.β淀粉样蛋白:Aβ是淀粉样前体蛋白(amyloid precursor protein,APP)水解产生的含36~43个氨基酸的多肽,在阿尔茨海默症的细胞和动物模型中,Aβ是基本病变老年斑的主要成分,因此阻止Aβ沉积和聚集的药物被认为是很有潜力的[1]。虽然以Aβ为靶标的药物还未上市,但临床研究阶段和药物发现阶段分别有55种和94种药物以Aβ为靶标,两阶段药物占有率高达42.0%和32.4%,占在研药物的绝对多数。可见,Aβ已经成为研制新药最重要的靶标,并可能在不久的将来取代AchE成为利用最多的靶标,研发应用前景最为看好,其代表性药物即上文提到的Ⅲ期临床药物bapineuzumab和solanezumab单克隆抗体疫苗。
3.α、β、γ分泌酶:除阻止Aβ沉积和聚集外,针对Aβ治疗的另一个方向是调节Aβ的生成,APP蛋白水解主要有2种途径:α分泌酶途径和β、γ分泌酶途径,APP经α分泌酶催化不产生Aβ,而经β、γ分泌酶的剪切则生成Aβ,因此选择性地提高α分泌酶活性和抑制β、γ分泌酶的活性是抑制Aβ生成的有效途径[12]。从表2可以看出,β分泌酶和γ分泌酶是其中使用较多的靶标,在药物发现和临床研究阶段均有大量出现,其中,β分泌酶研发前景较好,γ分泌酶研发风险相对较高,已有7种以γ分泌酶为靶标的药物被公开报道终止研究或开发,为其在研药物总数的1/3。
4.Tau蛋白:Tau蛋白是一种微管相关蛋白,可促进管蛋白组装成微管和维持微管结构。多项研究证实,Tau的异常过度磷酸化以及其他异常修饰,包括糖基化、异常截断作用等,导致Tau成为毒性分子而聚积成双螺旋丝和束状细丝,从而发生神经元纤维变[13],因此,阻断Tau蛋白异常磷酸化及其他异常修饰对阿尔茨海默症防治具有重要意义。目前,已有5种以Tau蛋白为靶点的药物进入临床研究,19种处于药物发现阶段,总数位列第2位,而在公开报道研发终止的药物列表中并未大量出现。可见,Tau蛋白已经成为阿尔茨海默症治疗药物研究和开发的新的热点方向之一,相关研究可能尚不成熟,但机会和前景可期。
三、药物作用机制和类型
目前,已上市和在研药物主要的作用机制或类型包括:脑代谢改善剂(nootropic agent)、神经保护剂(neuroprotectant)、AchEI以及针对阻断Aβ聚集和调节Aβ生成的作用类型,如Aβ沉积抑制剂(amyloid protein deposition inhibitor)、Aβ拮抗剂(beta amyloid antagonist)、Aβ调节剂(beta amyloid modulator)、Aβ合成抑制剂(beta amyloid synthesis inhibitor)等,表3列出了按各研发阶段药物数量统计的药物作用机制的分布情况。
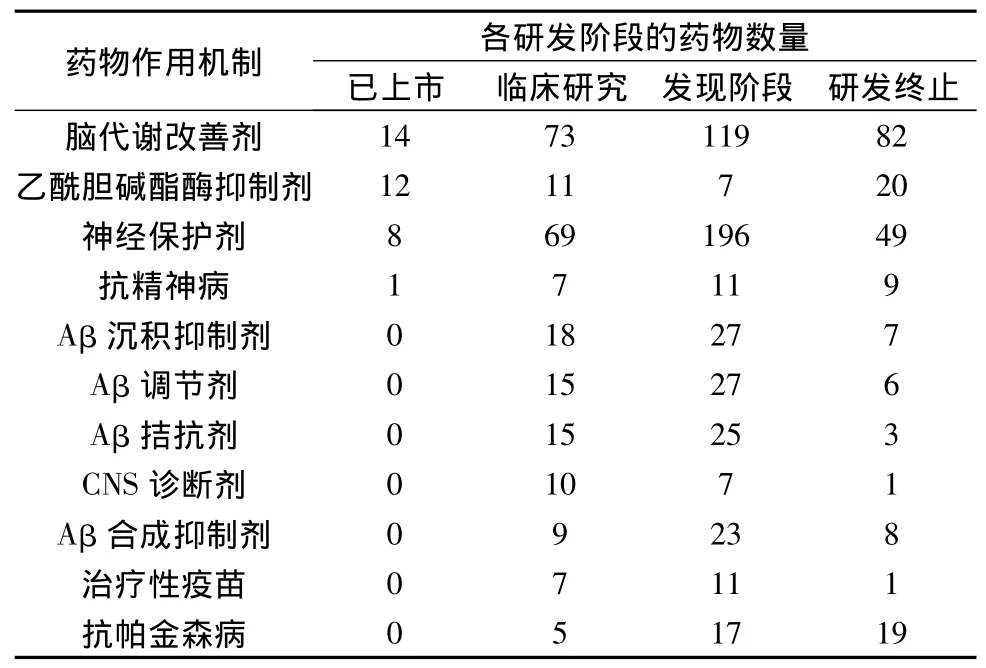
表3 按各研发阶段药物数量统计的药物作用机制的分布情况
1.脑代谢改善剂和神经保护剂:研究表明,阿尔茨海默症患者都不同程度的存在糖类、脂质、蛋白质、核酸等代谢障碍,同时其脑血流量及耗氧量明显低于正常同龄人[1]。因此,用于改善脑代谢的药物成为阿尔茨海默症治疗的一大类可供选用的药物,包括脑循环促进剂和脑代谢激活剂。脑循环促进剂有氢麦角碱(hydergin)、尼麦角林(nicergoline)、萝巴新(raubasine)等,脑代谢激活剂有吡拉西坦(piracetam)、芮拉西坦(anivacetam)、奥拉西坦(oxiracatam)、蔡非西坦(nofivecefam)等。
常用的神经保护剂包括常规抗氧化剂、钙离子拮抗剂、谷氨酸受体拮抗剂、单胺氧化酶抑制剂、自由基清除剂等,它们通过不同的作用方式保护神经元,实现防治阿尔茨海默症的目的。抗氧化剂维生素E可降低脂质过氧化、影响炎症反应、调节细胞信号传导并促进海马和皮质中生长抑素神经元的恢复[14];钙离子拮抗剂尼莫地平(nimodipine)能对抗脑血管收缩和局部缺血,防止神经元的变性和死亡;谷氨酸受体拮抗剂美金刚胺可以改善记忆过程所需谷氨酸的传递,并对兴奋毒性情况产生神经保护作用[2];单胺氧化酶抑制剂丙炔苯丙胺(deprenyl)可以阻止多巴胺被分解,提升多巴胺的浓度,预防脑细胞受到氧化损害等。
如表3中所示,脑代谢改善剂和神经保护剂是阿尔茨海默症治疗药物最常见的作用形式,药物占有率均达一半以上。然而,两者在各研发阶段的药物数量占有量有很大区别,在已上市的药物中,作为脑代谢改善剂使用的药物多于作为神经保护剂使用的药物,临床研究阶段两者数量接近相等,药物发现阶段神经保护剂已经显著多于脑代谢改善剂,成为主要的作用类型,而在终止研发的药物中神经保护剂数量仅为脑代谢改善剂的3/5。这一趋势显示出,神经保护剂已逐渐超过脑代谢改善剂,成为阿尔茨海默症新药研究和开发的首选思路和方向。
2.与Aβ相关的作用机制:与Aβ相关的作用机制也是目前在研药物中出现较多的一类,主要包括Aβ沉积抑制剂、Aβ拮抗剂、Aβ调节剂、Aβ合成抑制剂等,通过调节淀粉样前体蛋白的裂解、减少Aβ的产生、促进Aβ的降解和清除、防止Aβ的聚集和沉积、阻断Aβ作用机制的关键环节等预防和治疗阿尔茨海默症,其相应的靶标是Aβ和α、β、γ分泌酶等。该类作用机制虽然尚未出现在已上市药物中,但在研发阶段尤其是临床研究阶段已经大量涌现,以上4种主要作用机制在临床阶段和发现阶段药物占有量分别达到57种和102种,占有率达到43.5%和32.4%,同时其研发终止的药物数量合计仅为24,相对于其他作用机制处于较低水平,结合靶标研究的结果,可以判断,针对Aβ的药物研究正从探索走向成熟,相应的药物也将在不久后上市。
3.乙酰胆碱酯酶抑制剂:乙酰胆碱酯酶抑制剂是已上市药物中出现较多的作用类型,主要针对乙酰胆碱酯酶靶点,在上市、临床、发现、终止四阶段中的药物占有量分别为12种、11种、7种、20种,占有率分别为60.0%、8.4%、2.4%和6.9%,可以看出,虽然该类型在已上市药物中的出现率较高,但在研药物较少,终止研发的药物较多,暗示了相关研究可能已经趋于饱和,这也印证了针对乙酰胆碱酯酶靶点研究所得出的结论。
四、结语
本文主要从药物的研发阶段、药物靶标和药物的作用机制等方面对阿尔茨海默症治疗药物的研发现状进行了统计、分析和研究,并对其可能的发展趋势和方向进行了预测和判断,得出的主要结论归纳如下:①AchE靶标研究及相关新药开发可能已经趋于饱和;②Aβ已经成为新药研发利用最多的靶标,相应药物可能不久的将来大量上市,其代表性药物是bapineuzumab和solanezumab,已经进入Ⅲ期临床试验;③在研发药物中β、γ分泌酶靶标利用率高于α分泌酶,其中,γ分泌酶靶标研发风险相对较高;④Tau蛋白已经成为本领域研究较热的新兴靶标,相应药物处于发现和临床阶段的较多,终止研发的较少;⑤神经保护剂已经逐渐超过脑代谢改善剂,成为阿尔茨海默症新药研究和开发的首选思路和方向。
1吴思缈,周黎明.阿尔茨海默病的发病机制及药物治疗的进展[J].四川生理科学杂志,2009,31(1):36-39
2McKeage K.Spotlight on memantine in moderate to severe Alzheimer's disease[J].Drugs&Aging,2010,27(2):177-179
3Carrasco MM,Aguera L,Gil P,et al.Safety and effectiveness of donepezil on behavioral symptoms in patients with Alzheimer disease[J].Alzheimer Disease&Associated Disorders,2011,25(4):333-340
4Fujii A,Shinagawa R,Chatani Y,et al.Pharmacological profile and clinical results of the rivastigmine patch as a new therapeutic agent for Alzheimer's disease[J].Folia Pharmacologica Japonica,2012,139 (1):26-32
5Saint-Aubert L,Planton M,Hannequin D,et al.Amyloid Imaging with AV45(18F-florbetapir)in a cognitively normal AbetaPP duplication carrier[J].Journal of Alzheimer's disease:JAD,2012,28 (4):877-883
6Imbimbo BP,Ottonello S,Frisardi V,et al.Solanezumab for the treatment of mild-to-moderate Alzheimer's disease[J].Expert Review of Clinical Immunology,2012,8(2):135-149
7Panza F,Frisardi V,Imbimbo BP,et al.Anti-beta-amyloid immunotherapy for Alzheimer's disease:focus on bapineuzumab[J].Current Alzheimer Research,2011,8(8):808-817
8Seo JS,Baek IS,Leem YH,et al.SK-PC-B70M alleviates neurologic symptoms in G93A-SOD1 amyotrophic lateral sclerosis mice[J].Brain Research,2011,1368:299-307
9Park SJ,Jung HJ,Son MS,et al.Neuroprotective effects of INM-176 against lipopolysaccharide-induced neuronal injury[J].Pharmacology Biochemistry and Behavior,2012,101(3):427-433
10陈彪,马秋兰.阿尔茨海默病病因学研究进展及治疗展望[J].中华神经科杂志,2003,36(2):158-160
11费晶,刘松.阿尔茨海默病的胆碱酯酶抑制剂治疗进展[J].医学综述,2008,14(9):1397-1398
12王杉,蒋宁,周文霞,等.阿尔茨海默病防治药物靶标的研究进展[J].中国新药杂志,2007,16(11):831-836
13刘英华,王建枝.Tau蛋白异常与阿尔茨海默病的关系[J].生命的化学,2006,26(2):108-110
14赵琳,魏敏杰,金万宝.维生素E在阿尔茨海默病防治中的研究进展[J].国外医学:老年医学分册,2005,26(5):202-205
(收稿:2012-03-09)
(修回:2012-03-22)
300074天津市科学技术信息研究所
1.已上市药物:在已上市的20种药物中,属于重磅炸弹级别的是美金刚胺(Memantine)、多奈哌齐(Donepezil)和卡巴拉汀(Rivastigmine),这3种药物占据了绝对的市场份额。美金刚胺是一种具有中度亲和力的非竞争性N-甲基-D-天冬氨酸(N-methyl-D-aspartic acid,NMDA)受体拮抗剂,能有效地预防神经性和学习能力下降,同时没有明显的不良反应,是目前唯一已上市的NMDA受体拮抗剂,也是被美国食品药品监督管理局(Food and Drug Administration,FDA)批准的第1种用于治疗中度-重度痴呆症的药物,其2009年和2010年销售额分别达到了11.1亿美元和12.6亿美元[2]。多奈哌齐是第二代胆碱酯酶(cholinesterase,ChE)抑制剂,其治疗作用是可逆地抑制乙酰胆碱酯酶(acetylcholinesterase,AchE)引起的乙酰胆酰水解而增加受体部位的乙酰胆碱含量,用于治疗轻中度阿尔茨海默症,其2009年和2010年销售额分别达到了34.5亿美元和33.1亿美元[3]。卡巴拉汀是一种假性不可逆氨基甲酸乙酰胆碱酯酶抑制剂,能选择性地抑制大鼠大脑皮质和海马中的AchE活性,对日常生活中的认知行动及综合能力有显著疗效,其2010年销售额达到10.0亿美元[4]。
2.注册阶段药物:正在进行药品注册或已完成注册等待上市的药物及其相关信息如表1所示。18FFlorbetapir为核医学放射性示踪药物,可以用来侦测脑中类淀粉斑块,早期诊断阿尔茨海默症,其靶标是β淀粉样蛋白(beta amyloid,Aβ),原研单位是美国宾夕法尼亚大学,总部位于宾夕法尼亚州费城的放射性药品公司Avid(Avid Radiopharmaceuticals)资助了该项研究,并负责该药物的生产[5]。多奈哌齐和美金刚胺两系列的新药主要是针对剂型进行了创新和再开发,如透皮制剂、缓释制剂、干糖浆剂和液体制剂等。
表1 注册阶段药物的相关信息
药物原研公司作用机制或类型靶标多奈哌齐(透皮制剂)日本卫材公司美金刚胺(缓释制剂)Merz&Co GmbH盐酸多奈哌齐(干糖浆剂)日本卫材公司18F-florbetapir美国宾西法尼亚大学神经保护剂乙酰胆碱酯酶抑制剂脑代谢改善剂神经保护剂NMDA受体拮抗剂脑代谢改善剂神经保护剂乙酰胆碱酯酶抑制剂脑代谢改善剂β淀粉样蛋白调节剂显像剂PET造影剂乙酰胆碱酯酶NMDA受体乙酰胆碱酯酶β淀粉样蛋白多奈哌齐(液体制剂)日本卫材公司乙酰胆碱酯酶抑制剂乙酰胆碱酯酶
3.Ⅲ期临床药物:正在进行Ⅲ期临床试验的药物有bapineuzumab、solanezumab、INM-176、SK-PCB70M等。其中,前景较为看好的是礼来公司的solanezumab和强生公司/辉瑞公司的bapineuzumab,两者均为人源化抗β淀粉样肽的单克隆抗体,能够结合并消除阿尔茨海默症患者脑内沉积的β淀粉样肽构成的斑块,可能即将成为第一批上市的以Aβ为靶标的阿尔茨海默症治疗药物,多家分析机构预测,其年销售额将超过10亿美元,进入“重磅炸弹”药品行列。INM-176和SK-PC-B70M为天然植物提取物,具有神经保护等多种药理活性[8,9],原研公司分别是Scigenic&Scigen Harvest和SK Chemicals Life Science,相继于2005年7月和2010年11月在韩国进入Ⅲ期临床试验[6,7]。
