南海软海绵Halichondria sp.化学成分研究
2012-09-15孙见凡刘永宏
胡 静,杨 斌,孙见凡,雷 辉,刘永宏*
1中国科学院南海海洋研究所中科院海洋生物资源可持续利用重点实验室广东省海洋药物重点实验室海洋微生物中心,广州 510301;2中国科学院研究生院,北京 100049
南海软海绵Halichondria sp.化学成分研究
胡 静1,2,杨 斌1,孙见凡1,雷 辉1,刘永宏1*
1中国科学院南海海洋研究所中科院海洋生物资源可持续利用重点实验室广东省海洋药物重点实验室海洋微生物中心,广州 510301;2中国科学院研究生院,北京 100049
为了寻找有生物活性的次生代谢产物,对从采集自中国南海的软海绵(Halichondriasp.)进行了化学成分研究,从中共分离得到了9个化合物,并对部分化合物进行了抗菌活性测试。根据现代波谱技术并结合文献数据,鉴定化合物的结构为:1,2,3,4-四氢-3-羧基-2-卡波林(1),色氨酸(2),环(异亮氨酸-脯氨酸)(3),开环(脯氨酸-缬氨酸)(4),环(丙氨酸-脯氨酸)(5),胆甾醇(6),二-(2-乙基己基)邻苯二甲酸酯(7),邻苯二甲酸正丁异丁酯(8)和邻苯二甲酸二异丁酯(9)。
软海绵;化学成分;抗菌
海绵是最原始、最简单的多细胞动物,广泛分布于自赤道到两极不同深度的海域。自二十世纪五十年代以来,从海绵体内分离得到的活性次生代谢产物一直是海洋天然药物的重要来源[1-3]。Halichondria属软海绵属于寻常海绵纲、软海绵目、软海绵科动物。由于颜色、形状多变,其分类鉴定有一定难度。该属软海绵中含有结构类型丰富的次生代谢产物,如大环内酯、萜类、鞘类脂糖苷、甾醇、生物碱、内酰胺等,其中很多化合物都具有显著的抗菌、抗肿瘤、抗病毒等生物活性[4]。
我国南海地处热带亚热带,海域辽阔,海洋资源极为丰富,是世界上海绵集中分布的海域之一。为了寻找有重要生物活性和药用前景的海洋天然产物,开发我国的海洋生物资源,我们对采集自海南三亚海域的软海绵Halichondria sp.进行了化学成分研究。通过一系列硅胶、凝胶柱层析以及高效液相等分离手段,从该生物中分离得到了9个化合物,经现代波谱技术分析,并结合文献对照,确定其结构分别为:1,2,3,4-四氢-3-羧基-2-卡波林(1),色氨酸(2),环(异亮氨酸-脯氨酸)(3),开环(脯氨酸-缬氨酸) (4),环(丙氨酸-脯氨酸)(5),胆甾醇(6),二-(2-乙基己基)邻苯二甲酸酯(7),邻苯二甲酸正丁异丁酯(8)和邻苯二甲酸二异丁酯(9)。这些化合物均是首次从该属海绵中分离得到。本文运用圆形纸片法对化合物1~6在浓度为100 μg/纸片的条件下进行了抗菌活性测试,结果显示化合物1~6对金黄色葡萄球菌、枯草芽孢杆菌、大肠杆菌这三种菌株均不表现抑制作用。
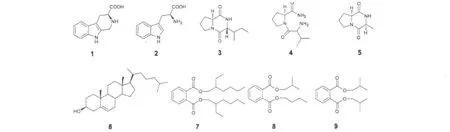
图1 化合物1~9的结构式Fig.1 Structures of compounds 1-9
1 实验部分
1.1 仪器和材料
Agilent 1200 LC-MS质谱仪;Bruker AC 500核磁共振仪;Hitachi L-2400高效液相;YMC ODS-H80 (250×10 mm i.d.,4 μm)半制备柱;Sephadex LH-20;柱层析硅胶由青岛海洋化工分厂生产;各种溶剂均为分析纯。
软海绵Halichondriasp.于2008年7月采集自我国南海海域,样品由韩国国立生物资源研究院无脊椎动物研究室的Kyung Jin Lee博士鉴定,标本保藏于广东省海洋药物重点实验室,编号为0807005。
1.2 提取与分离
将采集的新鲜的海绵样品(湿重4 kg)切成碎片后用95%的工业酒精浸泡提取3次,提取液减压浓缩,提取部位用2 L水溶解,先用2 L氯仿萃取3次,得到氯仿部位80 g,水相在用2 L正丁醇萃取3次,得到正丁醇部位52 g。氯仿部位采用正相硅胶柱分离,以氯仿:甲醇(100∶1,50∶1,25∶1,9∶1,6∶1,3∶1)梯度洗脱,经薄层板检测后合并相似流份得到15个组分(F1~F15)。F5采用正相硅胶柱分离,以氯仿:甲醇(100∶1,50∶1,25∶1,9∶1)梯度洗脱得到7个组分(F5-1~F5-7)。F5-4采用正相硅胶柱分离,以石油醚:丙酮(6∶1,3∶1,2∶1)梯度洗脱得到化合物9(8.9 mg);F5-7采用正相硅胶柱分离,以石油醚:乙酸乙酯(3∶1)洗脱得到化合物6(3.6 mg)和7 (7.4 mg)。F6先经葡聚糖凝胶柱脱色素,后采用正相硅胶柱分离,以石油醚:乙酸乙酯(3∶1)洗脱得到化合物8(9.7 mg)。F13先经葡聚糖凝胶柱脱色素,后采用薄层制备板制备,以石油醚:乙酸乙酯(1∶2)展开得到化合物5(5.4 mg)。正丁醇部位采用正相硅胶柱分离,以氯仿:甲醇(20∶1,9∶1,6∶1,3∶1,2∶1,1∶1)梯度洗脱,经薄层板检测后合并相似流份得到12个组分(f1~f12),f9先经葡聚糖凝胶脱色素,后采用高效液相色谱(YMC-Pack ODS柱,250× 10 mmI.D.,2 mL/min)分析制备,以甲醇:水(20∶80)为流动相分离得到化合物1(3.4 mg)、2(5.1 mg)、3 (4.3 mg)和4(3.3 mg)。
2 结果与讨论
2.1 结构鉴定
1,2,3,4-四氢-3-羧基-2-卡波林(1) 白色固体;ESI-MS m/z:217[M+H]+。1H NMR(CD3OD,500 MHz)δ:7.49(1H,d,J=7.8 Hz,H-6),7.33 (1H,d,J=8.0 Hz,H-9),7.12(1H,t,J=7.2 Hz,H-8),7.04(1H,t,J=7.4 Hz,H-7),4.37(2H,s,H-13),3.90(1H,m,H-2),3.33(1H,m,H-3a),3.00 (1H,t,H-3b);13C NMR(CD3OD,125 MHz)δ:40.8 (t,C-13),59.1(d,C-2),173.8(s,C-1),24.5(t,C-3),106.4(s,C-4),126.9(s,C-5),118.9(d,C-6),120.3(d,C-7),123.0(d,C-8),112.2(d,C-9),138.5(s,C-10),129.8(s,C-12)。经文献查阅,核磁数据与文献[5,6]基本一致,故该化合物鉴定为1,2,3,4-四氢-3-羧基-2-卡波林。
色氨酸(2) 白色固体;ESI-MS m/z:205[M+ H]+;1H NMR(CDCl3,500 MHz)δ:7.71(1H,d,J =8.0 Hz,H-4),7.37(1H,d,J=8.0 Hz,H-7),7.20 (1H,s,H-2),7.13(1H,t,J=7.5 Hz,H-5),7.06 (1H,t,J=7.5 Hz,H-6),3.86(1H,m,H-2'),3.53 (1H,m,H-1a'),3.16(1H,m,H-1b')。根据以上核磁共振图谱数据并与文献[5,7]对比,鉴定该化合物为色氨酸。
环(异亮氨酸-脯氨酸)(3) 白色粉末;ESI-MS m/z:211[M+H]+;1H NMR(CD3OD,500 MHz)δ: 4.22(1H,m,H-6),4.09(1H,m,H-9),3.60(1H,m,H-3a),3.52(1H,m,H-3b),2.33(1H,m,H-5a),2.18(1H,m,H-4a),2.05(2H,m,H-5b,10),1.92 (1H,m,H-4b),1.45(1H,m,H-11a),1.34(1H,m,H-11b),1.08(3H,d,H-12),0.96(3H,d,H-13);13C NMR(CD3OD,125 MHz)δ:165.0(s,C-1),47.0(t,C-3),23.4(t,C-4),29.5(t,C-5),54.8(d,C-6),169.0(s,C-7),59.8(d,C-9),37.1(d,C-10),25.4 (t,C-11),12.5(q,C-12),16.0(q,C-13)。经文献查阅,核磁数据与文献[8]基本一致,故该化合物鉴定为环(异亮氨酸-脯氨酸)。
开环(缬氨酸-脯氨酸)(4) 白色粉末;ESIMS m/z:212[M-H]-;1H NMR(CDCl3,500 MHz)δ: 4.22(1H,t,J=7.0 Hz,H-6),4.06(1H,bs,H-9),3.57(1H,m,H-3a),3.52(1H,m,H-3b),2.50(1H,m,H-5a),2.34(1H,m,H-4a),2.04(1H,m,H-5b),1.96(2H,m,H-4b,H-10),1.11(3H,d,J=7.3Hz,H-12),0.95(3H,d,J=6.9Hz,H-11)。经文献查阅,核磁数据与文献[9]基本一致,故该化合物鉴定为开环(缬氨酸-脯氨酸)。
环(丙氨酸-脯氨酸)(5) 白色粉末;EI-MS m/ z:167[M-H]-;1H NMR(CDCl3,500 MHz)δ:6.86 (1H,s,NH-8),4.10(2H,m,H-6,H-9),3.58(1H,m,H-3a),3.52(1H,m,H-3b),2.32(1H,m,H-4a),2.09(1H,m,H-5a),1.88(1H,m,H-4b),1.66(1H,m,H-5b),1.45(3H,d,J=6.5 Hz,H-10)。经文献查阅,核磁共振图谱与文献[8]基本一致,故该化合物鉴定为环(丙氨酸-脯氨酸)。
胆甾醇(6) 白色絮状晶体;1H NMR(CDCl3,500 MHz)δ:5.35(1H,m,H-6),3.50(1H,m,H-3),1.01(3H,s,H-19),0.92(3H,m,H-21),0.85(3H,m,H-26),0.82(3H,m,H-27),0.68(3H,s,H-18)。经文献查阅,核磁共振图谱与文献[10]基本一致,同时与标准品TLC对照,鉴定该化合物为胆甾醇。
二-(2-乙基己基)邻苯二甲酸酯(7) 无色油状物;ESI-MS m/z:391[M+H]+;1H NMR(CDCl3,500 MHz)δ:7.71(2H,m,H-3,6),7.53(2H,m,H-3,5),4.22(4H,m,H-1',1'),1.69(2H,m,H-2',2'),1.43 (4H,m,H-7',7'),1.34(12H,m),0.91(12H,m,H-6',6',8',8');13C NMR(CDCl3,125 MHz)δ:168.8 (s,C-7,C-8),132.5(s,C-1,2),130.9(d,C-4,5), 128.8(d,C-3,6),68.2(t,C-1',1'),38.8(d,C-2',2'),30.4(t,C-3',3'),29.7(t,C-4',4'),23.0(t,C-5',5'),14.1(q,C-6',6'),23.8(t,C-7',7'),11.0 (q,C-8',8')。经与文献对照[8],鉴定化合物为二-(2-乙基己基)邻苯二甲酸酯。
邻苯二甲酸正丁异丁酯 (8) 无色油状物; ESI-MS m/z:279[M+H]+;1H NMR(CDCl3,500 MHz)δ:7.71(2H,m,H-3,6),7.51(2H,m,H-4,5),4.30(2H,t,J=7.0 Hz,H-1'),4.08(2H,d,J=7.0 Hz,H-1'),2.03(1H,m,H-2'),1.71(2H,m,H-2'),1.44(2H,m,H-3'),0.97(6H,m,H-3',4'),0.93 (3H,t,J=7.5 Hz,H-4')。经与文献[11]对照,该化合物被鉴定为邻苯二甲酸正丁异丁酯。
邻苯二甲酸二异丁酯 (9) 无色油状物;ESIMS m/z:279[M+H]+;1H NMR(CDCl3,500 MHz) δ:7.73(2H,m,H-3,6),7.63(2H,m,H-4,5),4.07 (4H,d,J=6.5 Hz,H-1',1'),2.02(2H,m,H-2',2' ),0.99(12H,d,J=7 Hz,H-3',3',4',4')。化合物9与化合物8很相近,同时与文献[5]数据比较推断化合物为邻苯二甲酸二异丁酯。
2.2 讨论
化合物1,2属于氨基酸及其衍生物类型。化合物3~5属于二酮哌嗪类型,此类化合物最早从中草药中分离得到,后在海洋微生物的化学成分研究中非常常见。此外,其他海洋生物如海绵、海星和红藻等也有研究报道。有学者推断其他海洋生物中分离得到的二酮哌嗪类化合物可能来自于与其共生附生微生物,而非这些生物本身代谢产生,但目前缺乏足够的证据。许多二酮哌嗪类化合物显示了很好的细胞毒、抗菌、抗污损以及植物生长调节等生物活性[12]。化合物7~9是一种工业增塑剂,并非海绵自身的代谢产物,其来源可能是由于人类的活动而进入海洋,最后富集在海绵体内。
1 Ma WJ(马伟杰),Xiao DJ(肖定军),Deng SZ(邓松之),et al.New progress in the study of marine sponge metabolites having physiological activities.Nat Prod Res Dev(天然产物研究与开发),2003,15:567-571.
2 Zhu P(朱鹏),Yan XJ(严小军).Industrialization of secondary metabolitesofmarine sponges.JNingboUniv(NSEE)(宁波大学学报(理工版)),2004,17:401-405.
3 Xue S(薛松),Zhao QY(赵权宇),Zhang W(张卫).Research of natural products from Chinese sponge.Nat Prod ResDev(天然产物研究与开发),2003,15:359-363.
4 Sun JB(孙晶波),Lin HW(林厚文),Li SL(李水林),et al.Secondary metabolites and their bioactivities from marine spongeHalichondria.Chin Tradit Herb Drugs(中草药).2005,36:609-613.
5 Gao H(高昊),Chen GD(陈国栋),Tang JS(唐金山),et al.Isolation and identification of metabolites from a marine bacterial strainBacillussp.J Shenyang Pharm Univ(沈阳药科大学学报).2010,27:69-75.
6 Kuo FM,Tseng MC,Yen YH,et al.Microwave accelerated Pictet-Spengler reactions of tryptophan with ketones directed toward the preparation of 1,1-disubstituted indole alkaloids.Tetrahedron,2004,60:12075-12084.
7 Tang H(汤华),Wang XD(王旭东),LU W(陆玮),et al.Study on the chemical constituents of marine starfishAsterina pectinifera.J Pharm Pract(药学实践),2009,27:99-103.
8 Qi SH(漆淑华),Qian PY(钱培元),Zhang S(张偲).Antibacterial metabolites from marine bacteriumPseudomonassp.Nat Prod Res Dev(天然产物研究与开发),2009,21: 420-423.
9 Yang B,Dong JD,Liu YH,et al.Proline-Containing Dipeptides from the marine sponge Callyspongia species.Helv Chim Acta,2009,92:1112-1117.
10 Zhang JJ(张佳佳),Dai JB(戴静波),Chen LL(陈莉莉),et al.Chemical Constituents from Sea CucumberHolothuria nobilis.J Chin Med Mat(中药材),2008,31:538-539.
11 Wang LD(王立东),Wu SH(吴少华),Chen YW(陈有为),et al.Studies on the secondary metabolites of endophytic fungusEpicoccumsp.isolated from Azadirachta indica.Nat Prod Res Dev(天然产物研究与开发),2009,21:916-918.
12 Huang RM,Zhou XF,Xu TH,et al.Diketopiperazines from marine organisms.Chem Biodivers,2010,7:2809-2829.
Chemical Constituents of Marine Sponge Halichondria sp.from the South China Sea
HU Jing1,2,YANG Bin1,SUN Jian-fan1,LEI Hui1,LIU Yong-hong1*
1Key Laboratory of Marine Bio-resources Sustainable Utilization,Guangdong Key Laboratory of Marine Materia Medica,Research Center for Marine Microbes,South China Sea Institute of Oceanology,Chinese Academy of Sciences,Guangzhou 510301,China;2Graduate school of Chinese Academy of Sciences,Beijing 100049,China
Nine known compounds were isolated from the South China Sea spongeHalichondriasp.and the antibacterial activities of compounds 1-6 were tested.Their structures were identified as 1,2,3,4-tetrahydro-3-carboxy-2-carboline (1),tryptophan(2),cyclo-(Ile-Pro)(3),seco-((S)-Pro-Val)(4),cyclo-(Ala-Pro)(5),cholesterol(6),bis(2-ethylhexyl)phthalate(7),phthalie acid butyl isobutyl ester(8),and 1,2-benzenedicarboxylic acid diisobutyl ester(9) on the basis of detailed spectroscopic analysis and comparison with the data reported in the literature.
Halichondriasp.;chemical constituents;antibacterial activity
Q939.11+2;R931.77
A
1001-6880(2012)05-0614-04
2010-11-04 接受日期:2011-04-29
国家自然科学基金项目(30973679)
*通讯作者 Tel:86-20-89023244,E-mail:yonghongliu@scsio.ac.cn
