盐酸埃罗替尼的合成工艺改进
2012-09-12纪安成张爱华
刘 昕 ,韩 航 ,纪安成 ,张爱华
1南京工业大学药学院,南京 210009;2江苏省药物研究所,南京 210009
盐酸埃罗替尼(erlotinib hydrochloride)是一种小分子酪氨酸激酶抑制剂,化学名为N-(3-乙炔基苯基)-[6,7-二-(2-甲氧乙氧基)]-4-喹唑啉胺盐酸盐,是罗氏公司研发的用于治疗非小细胞性肺癌的新一代靶向性抗肿瘤药,可靶向地选择表皮生长因子受体(EGFR),在细胞内与底物竞争,从而抑制EGFR磷酸化,阻断肿瘤细胞信号的转导,使肿瘤细胞生长停滞,进而凋亡[1-5]。
本研究以专利WO1996030347的合成路线(见图1)为基础,以3,4-二羟基苯甲酸乙酯为起始原料经醚化、硝化、还原、环合、氯化等反应,最后与间氨基苯乙炔对接得到目标产物N-(3-乙炔基苯基)-[6,7-二-(2-甲氧乙氧基)]-4-喹唑啉胺盐酸盐。综合相关文献[6-12],对上述操作进行优化,在制备化合物2时,以DMF为溶剂,反应完直接倒入水中,简化了后处理操作,大大提高了收率,缩短了反应时间;以5%Pd/C为还原催化剂,使反应条件更加温和、安全,提高了收率,降低了成本;本合成工艺避免了高温、高压等不利于工业化生产的操作,对各步操作进行了优化,简化了后处理方法,提供了各步中间体及终产品质量,避免了频繁重结晶对收率造成的影响,使总收率从41.55%提高至58.6%。
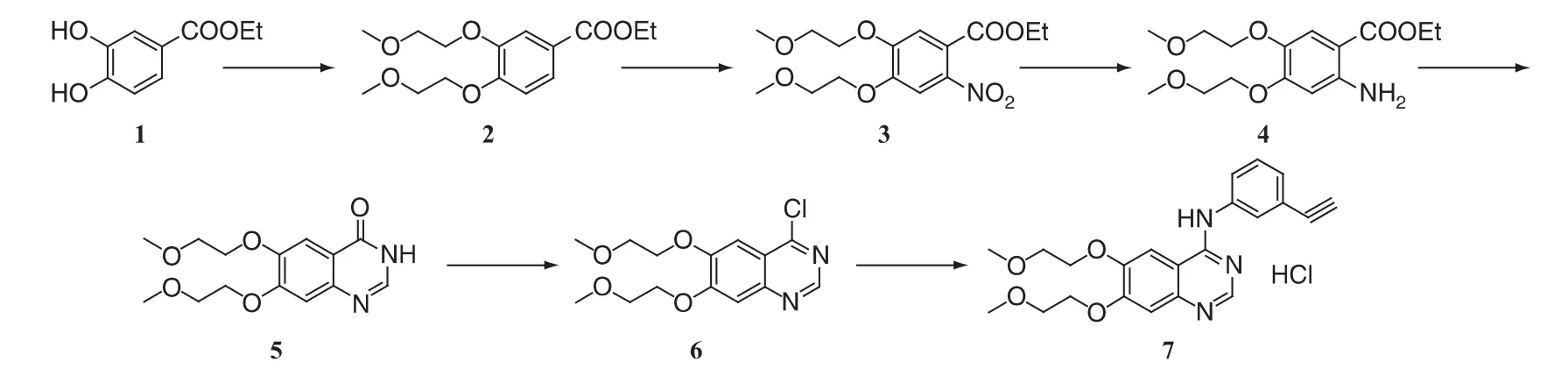
图1 盐酸埃罗替尼的合成路线
1 材 料
1.1 仪器
MP-S3熔点仪(日本柳本株式会社,温度计未校正);JEOL JNM-ECP 600型核磁共振波谱仪(内标:TMS;室温);Agilent 1100LC-MS 型质谱仪;RE-52A型旋蒸蒸发仪;85-Ⅱ型恒温磁力搅拌器;ZF-Ⅰ型三用紫外分析仪;TU-10001型分析天平;硅胶HF254高效板(烟台市德信生物科技有限公司)。
1.2 试剂
2-氯乙基甲醚(上海至鑫化工有限责任公司);醋酸甲脒(苏州市华丰精细化工有限公司);3,4-二羟基苯甲酸乙酯(上海卓锐化工有限公司);其余试剂均为市售国产分析纯。
2 合成方法
2.1 3,4-二(2-甲氧基乙氧基)苯甲酸乙酯(2)
化合物 1(91 g,0.5 mol)、1000 mL DMF 加入2000 mL反应瓶中,加入无水碳酸钾(172.5 g,1.25 mol),搅拌反应30 min后加入2-氯乙基甲醚(141.5 g,1.5 mol),缓慢升温至 80℃,反应 6 h,薄层显示反应完成,冷却反应液至室温,倒入1000 mL水中,搅拌,析出大量白色粉末状固体,过滤,烘干,得到白色固体 145.5 g,收率 97.6%,mp 53℃~56℃(文献[7]:收率 93%,mp 50℃~51℃)。
2.2 4,5-二(2-甲氧基乙氧基)-2-硝基苯甲酸乙酯(3)
1000 mL反应瓶中加入450 mL冰乙酸和化合物 2(134.1 g,0.45 mol),维持内温 20℃~30℃滴加135 mL 65%浓硝酸,加完后维持内温20℃~30℃搅拌5 h,反应完毕倒入2500 mL冰水中,搅拌。静置一段时间后用乙酸乙酯(300 mL×3)提取,依次用饱和碳酸氢钠和水洗涤,无水硫酸钠干燥,过滤,蒸干溶剂,得淡黄色油状物135.9 g,收率87.97%(文献[3]:收率 88.7%)。
2.3 4,5-二(2-甲氧基乙氧基)-2-氨基苯甲酸乙酯(4)
化合物 3(102.9 g,0.3 mol)加入 1000 mL 无水乙醇,再加入5%Pd/C(5 g),室温氢化反应,薄层跟踪,约16 h反应结束,抽滤,滤液蒸干溶剂,得到淡黄色油状物89.1 g,收率94.9%(文献 [7]:收率91.14%,mp 156℃~158℃)。
2.4 6,7-二(2-甲氧基乙氧基)喹唑啉-4-酮(5)
化合物 4(86.1 g,0.275 mol)溶于 1000 mL 无水乙醇,搅拌 10 min,加入醋酸甲脒(34.3 g,0.33 mol),加热回流反应12 h,室温冷却,析出大量白色固体,用无水乙醇洗涤,烘干,得到产品77.4 g,收率95.7%,mp 186℃~188℃(文献[8]:收率 91.14%,mp 182℃)。
2.5 4-氯-6,7-二(2-甲氧基乙氧基)喹唑啉(6)
1000 mL反应瓶中加入化合物5(73.5 g,0.25 mol)、氯化亚砜(650 mL)和 DMF(5 mL),加热回流反应10 h,反应结束后蒸干氯化亚砜,加入少量甲苯,再次蒸干,确保除去剩余的氯化亚砜,所得残余物溶于500 mL二氯甲烷中,饱和碳酸氢钠溶液洗涤,水洗,无水硫酸钠干燥,过滤,蒸干得到白色固体 69.3 g,收率 88.9%,mp>220℃(文献 [8]: 收率85.4%,mp>200℃)。1H-NMR(CDCl3,600MHz)δ:3.36(s,6H,2OCH3),3.75 ~3.88(m,4H,2CH2O),4.30 ~4.34(m,4H,2CH2O),7.28(s,1H,Ar-H),7.41(s,1H,Ar-H),8.83(s,1H,Ar-H)。
2.6 盐酸埃罗替尼(7)
2000 mL反应瓶中加入化合物6(62.4 g,0.2 mol)、三乙胺 30.3 g(0.3 mol)和异丙醇 1000 mL,搅拌全溶后加入预先已溶解的间氨基苯乙炔(35.1 g,0.3 mol)/异丙醇500 mL形成的溶液,室温搅拌反应12 h,薄层显示反应完成,反应液倒入2000 mL冰水中,过滤水洗,所得滤饼溶于500 mL乙酸乙酯中,无水硫酸钠干燥,过滤,滤液冰浴冷却至10℃以下,滴加饱和氯化氢乙醚溶液60 mL,滴完维持10℃以下搅拌1 h,过滤,乙酸乙酯洗涤,所得产品用无水乙醇300 mL重结晶,冷却析晶,过滤,无水乙醇洗涤,得白色固体72.6 g,收率84.6%,mp 229℃~231℃(文献 [6]: 收率 71%,mp 228℃~230℃)。1HNMR(CDCl3,600MHz):3.26(s,6H,2OCH3),3.64~3.73(m,4H,2CH2O),4.12(s,1H,CH),4.22~4.26(m,4H,2CH2O),7.20~7.23(m,1H,Ar-H),7.26(s,1H,Ar-H),7.42~7.45(m,1H,Ar-H),7.52(s,1H,Ar-H),7.86~7.92(m,1H,Ar-H),8.65(s,1H,Ar-H),9.16(s,1H,Ar-H);ESI-MS(m/z):394[M+H]+。
3 讨 论
①在制备化合物2时,以DMF为溶剂,替换原工艺所使用的丙酮,反应完全直接倒入水中,简化了后处理操作,大大提高了收率,缩短了反应时间,且产品纯度较好,无需纯化即可直接用于下一步反应。
②还原制备化合物4时,以5%Pd/C为还原催化剂,避免使用价格较高的二氧化钯和易燃的雷尼镍,使反应条件更加温和、安全,同时提高了还原收率,且实验证明5%Pd/C可重复使用多次。
③在制备化合物5时,以无水乙醇为溶剂,替换原工艺所使用的甲酰胺,避免了高温反应,反应完全直接析出产品,相当于将反应和重结晶合成一步,简化了后续处理,同时提高了反应收率和此步所得产品质量。
④在制备埃罗替尼时,反应完全直接将反应液倒入水中,即可析出产品,避免了需使用柱层析来纯化产品,大大降低了后处理难度,使本工艺利于工业化生产,产品用乙酸乙酯溶解后成盐,无水乙醇重结晶,完善了原工艺中未对终产品进行重结晶方面的研究,使较容易地得到质量高的终产品,简化了操作,提高了产品质量。
4 小 结
本合成工艺避免了高温、高压等不利于工业化生产的操作,对各步操作进行了优化,使每步操作更加简单、安全,同时提高了各步产品质量及收率,避免了频繁重结晶对收率造成的影响。埃罗替尼的总收率达到58.6%。
[1]Sorbera LA,Castaner J,Silvestre JS,et al.Erlotinib hydrochloride,oncolytic EGF receptor inhibitor[J].Drugs Future,2002,27(10)∶923-34.
[2]王尔兵,王肇炎.分子靶抗癌药∶埃洛替尼治疗非小细胞肺癌的新进展[J]. 癌症进展,2005,3(5):477-80.
[3]徐 浩,栗思存,黄文龙,等.埃罗替尼衍生物的合成及抗肿瘤活性[J]. 中国药科大学学报,2008,39(6):487-90.
[4]高 翔.喹唑啉类酪氨酸激酶受体小分子抑制剂的研究[D].沈阳:沈阳药科大学,2004.
[5]刘 刚,宋宝安,桑维钧,等.N-取代芳环-4-氨基喹唑啉类化合物的合成及生物活性研究 [J].有机化学,2004,24(10):1296-9.
[6]Schnur RC,Arnold LD.Quinazoline derivatives∶WO,1996030347[P].1996-10-03.
[7]Schnur RC,Arnold LD.Alkynyl and azid-o-substitubed 4-anilinoquinazolines∶US,5747498[P].1998-05-05.
[8]Lehner RS,Norris T,Santafianos DP.Processes and intermediates for preparing anti-cancer compounds∶JP,2000290262[P].2000-10-17;EP,1044969[P].2000-10-18.
[9]Jordis U,Knesl P,Ro咬seling D.Improved synthesis of substituted 6,7-dihydroxy-4-quinazolineamines∶tandutinib,erlotinib and gefitinib[J].Molecules,2006,11(4)∶286-97.
[10]李铭东,曹 萌,吉 民.盐酸埃罗替尼的合成[J].中国医药工业杂志,2007,38(4):257-9.
[11]陈海群,胡健华.6,7-二(2-甲氧基乙氧基)喹唑啉-4-酮的合成[J]. 化学世界,2010,51(4):224-31.
[12]孙海龙,初文毅,侯艳君,等.6,7-二(2-甲氧基乙氧基)喹唑啉-4-酮的合成研究[J].黑龙江大学(自然科学)学报,2011,28(2):223-8.