葡萄糖氧化酶生物传感器的构建和性能研究
2012-09-06韩文彪蔡谨石瑞黄磊徐志南
韩文彪,蔡谨,石瑞,黄磊,徐志南
(1.南京林业大学森林资源与环境学院,江苏南京210037;2.浙江大学化学工程与生物工程学系,浙江杭州310027)
葡萄糖氧化酶生物传感器的构建和性能研究
韩文彪1,2,蔡谨2,石瑞1,黄磊2,徐志南2
(1.南京林业大学森林资源与环境学院,江苏南京210037;2.浙江大学化学工程与生物工程学系,浙江杭州310027)
目的以固定化葡萄糖氧化酶酶膜构建葡萄糖生物传感器,并对其性能进行评价。方法优化载体及戊二醛交联固定化条件,制备性能良好的葡萄糖氧化酶酶膜,研究固定化酶的性能并用于构建葡萄糖传感器。结果固定化葡萄糖氧化酶的最适催化温度为40℃、pH为7.0;葡萄糖生物传感器的响应时间小于20 s,在0~1.5 g·L-1葡萄糖浓度范围内有良好的线性,具有很强抗干扰和稳定性。结论该葡萄糖生物传感器性能良好,可用于生物样品中葡萄糖测定。
葡萄糖氧化酶;固定化;葡萄糖测定传感器
葡萄糖的定量测定在临床医学、生物化学、食品科学等领域有极其重要的作用。可以用分光光度法、电流测定法、高效液相色谱法、极谱法及毛细管电泳法等测定葡萄糖含量[1],但是,这些方法有的需要复杂的前处理过程,分析速度慢,仪器设备成本较高,而生物传感器法由于具有检测速度快、选择性好、体积小、易操作等优点,受到众多研究者的重视[2,3]。目前,葡萄糖生物传感器的研究日益增多,但是其检测范围普遍较小,响应时间较长且抗干扰能力较弱[4~6],这些缺点使其在实际检测应用中受到限制较多。提高该传感器的检测范围和灵敏度是亟待解决的问题。其中,作为葡萄糖生物传感器重要组成元件——固定化葡萄糖氧化酶是影响传感器性能的重要因素[7~10]。
本文筛选了几种不同类型的材料作为固定化酶的载体,
在不同条件下通过交联法固定葡萄糖氧化酶,以期获得高比活、高稳定性的葡萄糖氧化酶膜。并着重研究基于固定化葡萄糖氧化酶膜的葡萄糖生物传感器的性能及其应用。
1 材料和方法
1.1 实验材料葡萄糖氧化酶(GOD,EC 1.1.3.4,TypeⅦfrom Aspergillus niger,100 U·mg-1)购于Sigma公司,牛血清白蛋白(BSA)和25%戊二醛购于上海生工生物工程有限公司,聚碳酸酯膜(0.2 μm)购于Whatman公司,醋酸-硝酸混合纤维素滤膜(0.22 μm、0.45 μm、0.8 μm),购于上海兴亚净化材料厂,尼龙66微孔滤膜(0.22 μm、0.45 μm、0.8 μm),购于杭州科诺过滤器材有限公司,鸡蛋壳膜自制。
1.2 实验方法
1.2.1 酶的固定化利用打孔器将各种膜切割成直径为9mm的圆片(面积S=0.635 9 cm2),分别用0.1 mol·L-1,pH 7.0的磷酸缓冲液浸泡清洗,取出用蒸馏水冲洗干净,晾干,备用。
依次吸取15 μL葡萄糖氧化酶(GOD)溶液,4 μL牛血清白蛋白(BSA)溶液于1 mL离心管中混合均匀,然后加入1 μL戊二醛溶液迅速混匀,共20 μL。吸取混合液于预处理过的膜片上,涂布均匀后置于4℃,静置反应过夜。取出置于0.05 mol·L-1,pH 7.0磷酸缓冲液中浸泡并振荡洗去未固定的酶。
1.2.2 酶活测定酶活性测定:取35℃预保温的1.5 mL溶液A和1.5 mL溶液B,于1 cm比色皿中混合,加入一定量溶液酶或剪碎的固定化酶膜,保温反应2 min,测定其在500 nm处的吸光值。其中,溶液A:称取3.5 mg辣根过氧化物酶和3.5 mg 4-氨基安替吡啉,溶于20 mL 0.2 mol·L-1,pH 7.0磷酸缓冲液中,再加入1 mL 3.0%苯酚。溶液B:6.5%葡萄糖溶液。
葡萄糖氧化酶酶活力单位(U)定义为:每分钟氧化1 μmol葡萄糖产生葡萄糖酸和H2O2所需的酶量。
1.2.3 葡萄糖生物传感器的构建将固定化葡萄糖氧化酶膜用“O”型圈紧贴固定于过氧化氢电极表面,连接信号处理系统组成葡萄糖氧化酶传感器,结构示意图见图1。反应池内待测样品和缓冲液经搅拌迅速混匀后,葡萄糖在固定化酶的作用下反应生成H2O2,通过过氧化氢电极检测H2O2浓度,由于底物浓度与H2O2浓度成线性比例关系,便可以得到葡萄糖浓度。
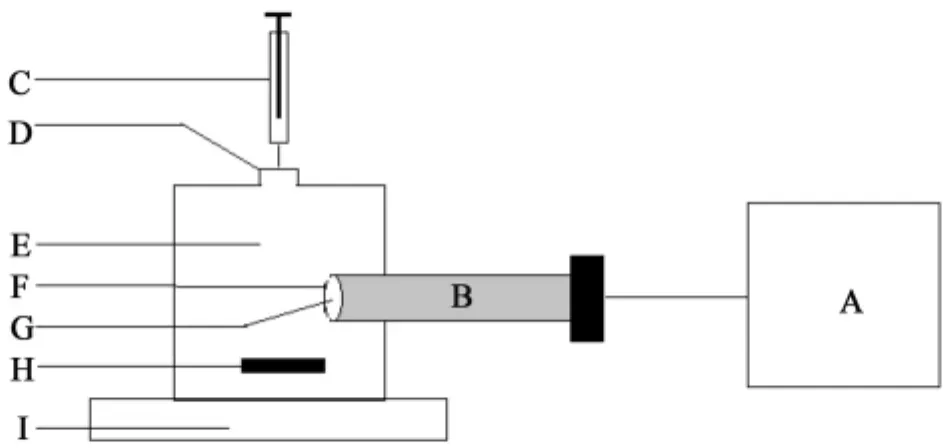
图1 葡萄糖传感器结构示意图
2 结果与讨论
2.1 固定化条件的优化
2.1.1 载体材料对酶固定化的影响载体种类直接影响固定化酶的活力、底物扩散速度及酶的稳定性。本文分别以不同材料(尼龙膜0.22 μm、混合纤维素膜0.22 μm、鸡蛋膜、聚碳酸酯膜)作为载体进行了考察,结果见图2。尼龙作载体材料时,固定化酶的活力较低;其中以混合纤维素膜为载体材料时,酶的活力相对最高,且比较稳定,重复性好。
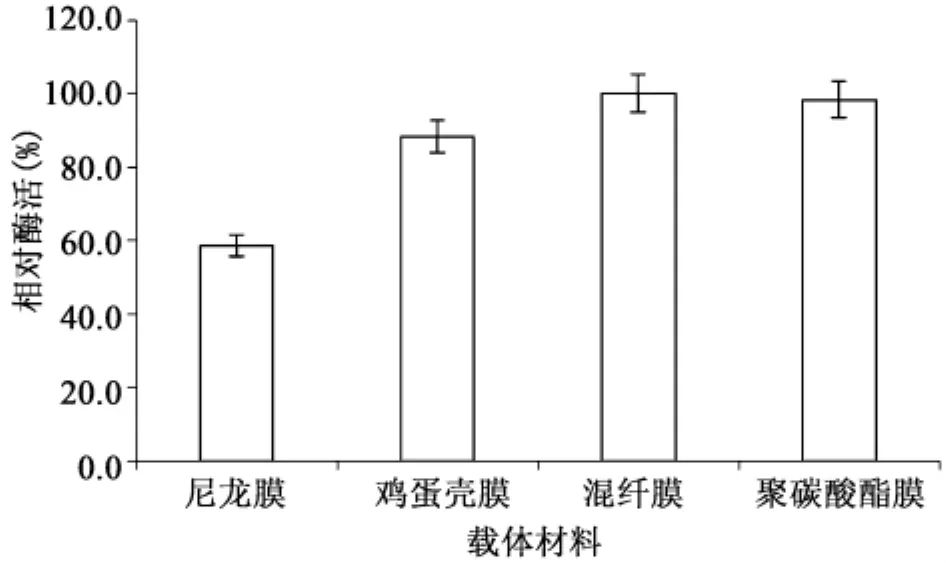
图2 载体材料对酶固定化的影响
2.1.2 载体孔径对酶固定化的影响载体的孔径大小可能会影响固定化酶的活力。本文分别以0.22 μm,0.45 μm和0.8 μm等不同孔径的混合纤维素膜作为固定化载体,考察制得的固定化酶效果,结果见图3。以孔径为0.22 μm的材料为载体时固定化酶活最高,其次是孔径为0.45 μm的,孔径为0.8 μm的固定化效果最差,说明孔径大的膜表面可固定化的蛋白量相对较少,但是以孔径为0.22 μm的材料为载体时,构建的生物传感器的分析响应较慢,孔径为0.45 μm的材料为载体时,固定化酶量和分析响应较好,所以,后续实验中选择0.45 μm的混合纤维素材料为载体。

图3 混合纤维素膜的孔径对酶固定化的影响
2.1.3 戊二醛浓度对酶固定化的影响以孔径为0.45 μm的混合纤维素材料为载体,在含2 mg·mL-1GOD和2% BSA的条件下,以不同浓度的戊二醛为交联剂,来考察戊二醛浓度对酶固定化的影响,结果见图4。戊二醛浓度较低时,随着戊二醛浓度增大,酶的总活力也在增大,当戊二醛终浓度为0.4%时,酶的活力达到最大,继续提高戊二醛浓度,酶的活力明显下降。戊二醛浓度太低时,酶未被充分交联固定,而浓度太高反而会影响酶的结构,从而影响酶活。在以上实验条件下,戊二醛终浓度为0.4%时,固定化效果最佳。

图4 戊二醛浓度对酶固定化的影响
2.1.4 BSA浓度对酶固定化的影响以孔径为0.45 μm的混合纤维素材料为载体,戊二醛浓度为0.4%,GOD的浓度为2 mg·mL-1时,考察了BSA浓度对酶固定化效果的影响,结果见图5。BSA的浓度对酶活的影响比较明显,浓度小于3%时,随着BSA浓度增加,固定化酶活也在增加。这可能是加入BSA可有效保护酶的活性中心并增加酶的固定量。但当反应体系中BSA浓度大于3%时,BSA量的增加会使固定化酶活迅速下降,这可能是过多的BSA与戊二醛交联反而阻碍了酶被充分交联固定。本实验条件下,BSA浓度为3%时效果最佳。

图5 BSA浓度对酶固定化的影响
2.1.5 加入酶量对酶固定化的影响本文考察固定化酶反应体系中加入酶量对固定化酶的影响,结果见图6。总体来看,酶活力随着酶量的增加而提高,但当酶浓度大于3.75 mg ·mL-1时,再提高酶浓度,固定化酶的活力变化不明显,酶膜固定酶量趋于饱和。在本实验条件下,酶的浓度为3.75 mg ·mL-1时效果较好。

图6 酶量对酶固定化的影响
2.2 固定化葡萄糖氧化酶的酶学性质
2.2.1 温度对酶活力的影响温度对酶的催化活性有很大的影响,pH=6.0条件下,考察温度对游离酶和固定化酶的影响,结果见图7。游离酶和固定化酶的最适反应温度都在40℃左右,与游离酶相比,固定化酶受温度变化的影响较小,说明经固定化后,酶的稳定性有所提高。
2.2.2 pH对酶活力的影响酶的催化反应都存在于溶液环境中,pH值会对酶产生一定的影响,因此,在40℃条件下,考察pH值对游离酶和固定化酶的影响,结果见图8。游离酶的最适pH在5.5左右,固定化酶的最适pH为7.0左右,且固定化酶受溶液pH变化影响较小,说明经固定化后,酶的稳定性有所提高。

图7 温度对游离酶和固定化酶的影响

图8 pH对游离酶和固定化酶的影响
2.2.3 葡萄糖氧化酶的米氏常数米氏常数Km和最大反应速度Vmax能反映酶的催化动力学。本文在40℃、pH=7.0条件下,测定了葡萄糖氧化酶的游离酶和固定化酶的Km值和Vmax,结果见图9。固定化酶的米氏常数Km=20.317 mmol·L-1,最大反应速度Vmax=0.117 6 mmol·(L· min)-1,游离酶的米氏常数Km=8.558 mmol·L-1,最大反应速度Vmax=0.077 2 mmol·(L·min)-1。说明葡萄糖氧化酶固定化后微环境发生了变化,酶与底物的亲和性稍有下降。

图9 游离酶和固定化酶的米氏常数Km
2.2.4 固定化葡萄糖氧化酶酶膜的保存稳定性将固定化葡萄糖氧化酶保存于0.1 M,pH=7.0磷酸缓冲液中,分别置于4℃冰箱和室温。考察不同温度下固定化酶活性的变化情况,结果见图10。4℃保存的固定化酶,前两周时间内,酶膜活性变化很小,20~40 d内酶活力下降比较明显,保存40 d以后,酶活下降比较缓慢,基本趋于稳定,固定化酶的半衰期为60 d左右,具有很好的稳定性;室温环境下保存的酶膜,前4 d酶活下降明显,之后酶活缓慢下降,但是在保存到20 d左右时,酶膜表面开始有霉菌生长,因此只能测定到24 d,此时,酶膜的剩余酶活大约为初始酶活的60%左右,说明4℃比室温更有利于固定化酶的保存,稳定性明显延长。
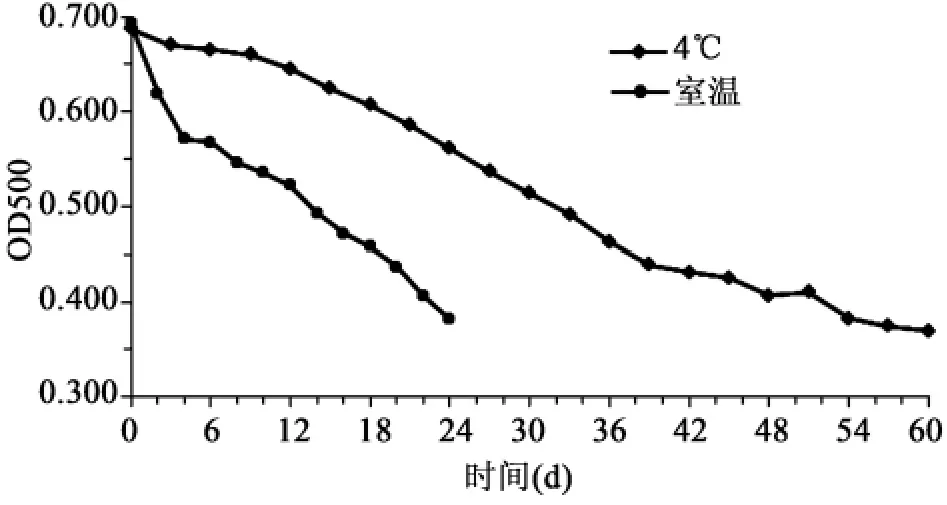
图10 葡萄糖氧化酶膜保存稳定性
2.2.5 固定化葡萄糖氧化酶酶膜的热稳定性将游离酶和固定化酶膜分别保存在pH=7.0、0.1 M的磷酸缓冲液中,置于60℃水浴条件下,对比游离酶和固定化酶的热稳定性,结果见图11。游离酶在该条件下,10 min酶活下降50%左右,半小时几乎完全失活,而酶膜在该条件下,2 h后还能保持初始酶活的一半,8 h后仅剩余不到初始酶活的10%。与游离酶相比,固定化酶的热稳定性有明显的提高。

图11 60℃时游离酶和固定化酶的热稳定性
2.3 葡萄糖生物传感器的性能本文以固定化葡萄糖氧化酶酶膜与过氧化氢电极等组装成葡萄糖生物传感器,并对其对葡萄糖的响应时间、检测范围,抗干扰能力以及对实验样品的检测准确性和传感器的使用稳定性进行了考察。
2.3.1 传感器的响应时间和检测限分别配制不同浓度的葡萄糖溶液,用传感器分别测定10 s、15 s和20 s时的响应值,考察传感器的灵敏度和检测限,结果见图12。该传感器灵敏度较高,葡萄糖浓度小于3.0 g·L-1时,15 s时响应值基本达到稳定,20 s达到稳定状态;浓度小于1.0 g·L-1时,10 s时就能达到稳定状态。另外,当葡萄糖浓度在0~1.5 g·L-1时,20 s时的响应值与实际值基本完全一致,说明,该传感器响应时间较短,能准确测定0~1.5 g·L-1的葡萄糖浓度。
2.3.2 传感器的抗干扰能力在实际使用中,待测溶液中不仅可能含葡萄糖,还可能含有其他物质。本文考察了葡萄糖生物传感器对生物样品中常见成分的抗干扰能力。分别检测1.0 g·L-1氯化钾、1.0 g·L-1氯化镁、1.0 g·L-1蔗糖、1.0 g·L-1牛血清白蛋白、1.0 g·L-1L-谷氨酸、1.0 g ·L-1尿素、1.0 g·L-1维生素C的响应值,以1.0 g·L-1葡萄糖为对照,结果见表1。除了对维生素C有极微弱响应外,其他物质均无响应,且能准确测定葡萄糖的浓度,说明该生物传感器系统有很高的选择性,抗干扰性很强。
2.3.3 传感器测定发酵液葡萄糖浓度测定发酵液样品中葡萄糖含量是葡萄糖生物传感器实际应用之一。本文使用自制葡萄糖生物传感器测定发酵液中葡萄糖含量,并与SBA-40C生物传感分析仪进行比较,结果见表2。自制葡萄糖生物传感器的测定结果与SBA-40C生物传感分析仪测定结果基本一致。

图12 传感器线性关系
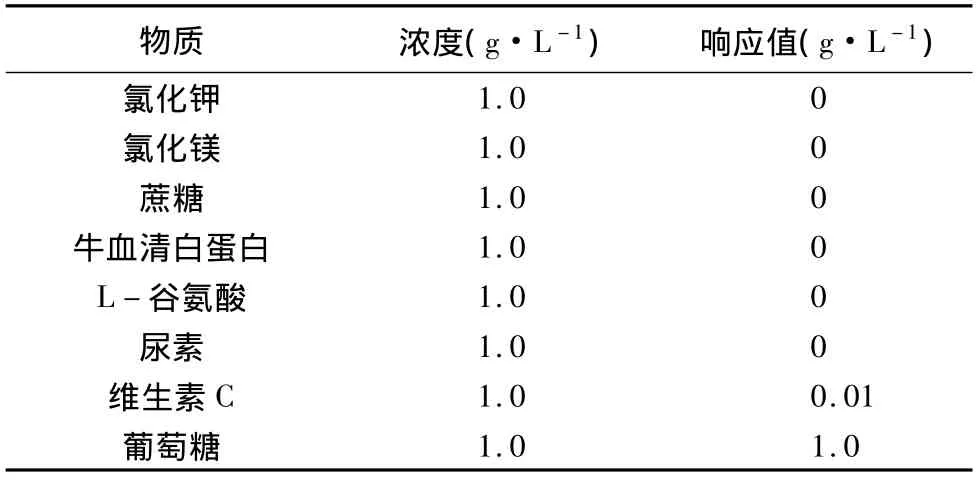
表1 葡萄糖生物传感器对干扰物质的响应

表2 发酵液中葡萄糖浓度测定结果
2.3.4 葡萄糖生物传感器使用的稳定性使用稳定性是衡量传感器的主要性能指标之一。本文在室温条件下,考察了传感器的基础活性随时间的变化情况,结果见图13。前两天基础活性下降比较快,之后酶活逐渐变缓,基本趋于稳定,40 d时的传感器的基础活性保留初始酶活的30%,说明,在室温条件下,葡萄糖传感器有较好的使用稳定性。
3 结论
综上所述,以孔径为0.45 μm的混合纤维素材料为载体,戊二醛、BSA和酶的最佳浓度分别为0.4%、3%和3.75 mg·mL-1时,可制备高比酶活的固定化葡萄糖氧化酶。固定化葡萄糖氧化酶的最适反应温度为40℃,最适pH为7.0,米氏常数Km=20.317 mmol·L-1,最大反应速度Vmax= 0.117 6 mmol·(L·min)-1。固定化酶具有很好的热稳定性。构建的葡萄糖生物传感器在葡萄糖浓度0~1.5 g·L-1之间,有良好的线性关系,且响应时间较短,能在20 s内迅速达到平衡。传感器的选择性较好,几乎不受其他物质的影响,能准确的测定溶液中葡萄糖的含量,并且具有很好的稳定性。能较好地测定发酵液中的葡萄糖浓度。
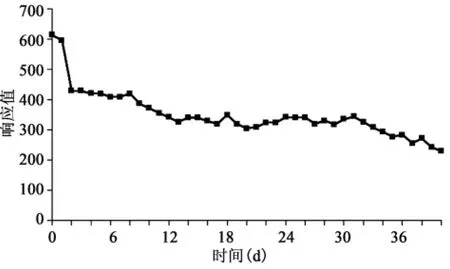
图13 葡萄糖传感器使用稳定性
[1]贾文娟,崔淼,张彦,等.鱼鳔膜为基质的生物传感器测定葡萄糖的研究[J].分析化学研究简报,2011,39 (9):1423-1426.
[2]Wu B,Zhang G,Shuang S,et al.Biosensors for determination of glucose with glucose oxidase immobilized on an eggshell membrane[J].Talanta,2004,64(2):546-553.
[3]汤琳,曾光明,沈国励.基于抑制作用的新型葡萄糖氧化酶传感器测定环境污染物汞离子的研究[J].分析科学学报,2005,21(2):123-126.
[4]Struth B,Eckle M,Decher G,et al.Hindered ion diffusion inpolyelectrolyte/montmorillonitemultilayers:Toward compartmentalized films[J].Eur Phys J E,2001,6(5): 351-358.
[5]冉旭,冉均国,苟立,等.壳聚糖凝胶固定葡萄糖氧化酶制备酶电极的工艺[J].食品与发酵工业,2003,29 (8):32-34.
[6]王文序,蔡谨,袁骏.葡萄糖氧化酶在氨等离子体改性膜上的固定化[J].浙江大学学报(自然科学版),1997,31(3):399-404.
[7]王胜娥,何洁,袁红雁,等.酶生物传感器固定化酶载体的研究[J].化学传感器,2004,24(4):30-34.
[8]Kumar J,D'Souza SF.Inner epidermis of onion bulb scale:As natural support for immobilization of glucose oxidase and its application in dissolved oxygen based biosensor[J].Biosens Bioelectron,2009,24(6):1792-1795.
[9]Bayramoglu G,Metin Au,Altintas B,et al.Reversible immobilization of glucose oxidase on polyaniline grafted polyacrylonitrile conductive composite membrane[J].Bioresour Technol,2010,101(18):6881-6887.
[10]Rauf S,Ihsan A,Akhtar K,et al.Glucose oxidase immobilization on a novel cellulose acetate-polymethylmethacrylate membrane[J].J Biotechnol,2006,121(3):351-360.
Construction and performance study on glucose determination biosensor integrated with immobilized glucose oxidase
HAN Wen-biao1,2,CAI Jin2,SHI Rui1,HUANG Lei2,XU Zhi-nan2
(1.College of Forest Resources and Environment Science,Nanjing Forestry University,Nanjing 210037,China; 2.Department of Chemical and Biological Engineering,Zhejiang University,Hangzhou 310027,China)
ObjectiveTo construct glucose determination biosensor with immobilized glucose oxidase and evaluate the characteristic of biosensor.MethodsPrepared immobilized glucose oxidase with good performance by optimizing the immobilized carriers and the immobilization conditions of glutaral cross-linking.The characteristic of immobilized enzyme was studied,and used to construct glucose biosensor.ResultsThe optimal catalytic temperature and pH of immobilization glucose oxidase were 40℃and 7.0,respectively.The response time of glucose biosensor was less than 20 s,the linear range of glucose concentration was 0~1.5 g·L-1.and had high anti-interference and stability.ConclusionThe integrated glucose determination biosensor had good performance and can be used for the determination of glucose in biological samples.
Glucose oxidase;Immobilization;Glucose determination biosensor
book=311,ebook=3
O658.9
A
1672-7738(2012)06-0311-05
国家“863”项目(2011AA02A114)
