因宁片的急性和慢性毒性实验研究Δ
2012-08-29周涛李国熊茹丽侯连兵南方医科大学南方医院药学部广州510515重庆市中山医院重庆40001广州中医药大学科技产业园广州510445
周涛,李国熊,茹丽,侯连兵(1.南方医科大学南方医院药学部,广州510515;.重庆市中山医院,重庆 40001;.广州中医药大学科技产业园,广州 510445)
因宁片为南方医院院内制剂,是由昆明山海棠、黄芪、当归等9味中药组成的复方制剂,适应证为甲状腺功能亢进(甲亢)。临床前研究与临床应用均表明因宁片对甲亢具有良好的改善作用[1,2]。其中昆明山海棠具有抗炎、免疫抑制的作用[3],黄芪具有增强免疫功能、增强机体耐缺氧与抗应激能力等作用[4]。为了进一步评价因宁片的安全性,笔者进行了急性和慢性毒性实验,为临床安全用药提供依据。
1 仪器与材料
1.1 仪器
PocH-100iV Diff型全自动动物血液分析仪(日本Sysmex公司);7080型全自动生化分析仪(日本日立公司);DMRA自动旋转荧光显微镜(德国Leica公司)。
1.2 试药
因宁片(南方医院药学部制剂中心,批号:20110618,0.3g/片,1g相当于3.38g中药材);蒸馏水(新南方药物安全性评价中心)。
1.3 动物
SPF级KM小鼠40只,♀♂兼半,体重18~22g;SPF级SD大鼠48只,♀♂兼半,体重140~160g,均由广东省医学实验动物中心提供(动物使用许可证号:SYXK(粤)2008-0014)。
2 方法
2.1 因宁片对小鼠的急性毒性实验
通过预实验,未测出半数致死量(LD50),转而测定最大耐受量(MTD)。将40只小鼠,按预编号与体重分层数字随机分为2组,即空白对照(等容生理盐水)、因宁片(32g·kg-1)组,24h内2次ig给药(间隔6h)。给药间隔期间连续观察小鼠的反应,给药结束后每天上、下午各观察1次,连续14d,每天记录小鼠的一般状况,包括外观、行为、分泌物、排泄物、死亡情况与中毒反应(中毒反应的症状、严重程度、起始时间、持续时间、是否可逆)等,并记录体重和摄食量,实验结束后大体解剖小鼠,肉眼观察各脏器的病变情况。
2.2 因宁片对大鼠的慢性毒性实验
将48只大鼠随机分为4组,即空白对照(等容生理盐水)与因宁片高、中、低剂量(6、3、0.6g·kg-1,相当于临床人日剂量的100、10、5倍)组。ig给药,每天1次,连续30d,给药期间大鼠自由摄食和饮水。每天观察记录大鼠的一般状况如进食、行为活动、粪便等。每周称体重,记录摄食量,并根据体重变化及时调整用药剂量。末次给药24h后,ip3%戊巴比妥钠溶液麻醉大鼠,腹主动脉采血,采集的血样于血液分析仪上检测红细胞(RBC)、中性粒细胞(NE)、嗜酸性粒细胞(EO)、嗜碱性粒细胞(BA)、网织RBC、单核巨噬细胞(MO)、血红蛋白(HGB)、RBC压积(HCT)、平均RBC体积(MCV)、平均RBC血红蛋白量(MCH)、平均血红蛋白浓度(MCHC)、血小板(PLT)、淋巴细胞(LY)等血液学指标。另取血分离血清,于自动生化分析仪上测定血液生化指标(谷丙氨酸氨基转移酶(ALT)、肌酐(Cre)、血糖(GLU)、尿素氮(URE)、总胆红素(BIL)、血清钙(Ca)、碱性磷酸酶(ALP)、胆固醇(CHO)、血清总蛋白(TP)、血清白蛋白(ALB)、磷酸肌酸激酶(CK)、乳酸脱氢酶(LDH)、甘油三酯(TG)、天冬氨酸氨基转移酶(AST)、血清钠(Na)、血清钾(K)、血清氯(Cl))。对主要脏器进行全面尸检,取脑、心、肝、脾、肺、肾等脏器称重,计算脏器系数(脏器/体重)。主要脏器用10%甲醛固定,进行常规病理学检查。
2.3 统计学方法
3 结果
3.1 对小鼠的急性毒性实验
3.1.1 因宁片对小鼠一般状况的影响和MTD的测定 给药间隔期间和14d观察期内,各组小鼠精神和自主行为活动状况良好、皮肤被毛清洁、大小便正常,亦未见其它毒性反应症状。根据因宁片混悬液的最大浓度(0.4g·mL-1)和小鼠的最大ig体积(40mL·kg-1),得出MTD为32g·kg-1,相当于临床人日剂量(0.06g·kg-1)的534倍。
3.1.2 因宁片对小鼠体重变化的影响 小鼠体重增长正常,各个时期因宁片组与空白对照组比较,体重无显著性差异(P>0.165),提示因宁片对小鼠的体重变化无影响。因宁片对小鼠体重变化的影响见表1。
表1 因宁片对小鼠体重变化的影响(±s)Tab 1 Effects of Yinning tablets on the variation of body weight in mice(±s)

表1 因宁片对小鼠体重变化的影响(±s)Tab 1 Effects of Yinning tablets on the variation of body weight in mice(±s)
剂量/g·kg-1n 体重/g 组别空白对照组因宁片组-322020给药前19.55±1.8219.13±1.30第1d 22.21±1.7022.80±1.30第2d 26.91±3.3127.97±2.64第7d 29.68±3.3130.88±4.51第14d 32.97±5.4934.65±6.80
3.1.3 因宁片对小鼠摄食量的影响 因宁片组与空白对照组比较,小鼠的摄食量无显著性差异(P>0.337),提示因宁片对小鼠的摄食量无影响。因宁片对小鼠摄食量的影响见表2。
表2 因宁片对小鼠摄食量的影响(±s)Tab 2Effects of Yinning tablets on food intake in mice(±s)

表2 因宁片对小鼠摄食量的影响(±s)Tab 2Effects of Yinning tablets on food intake in mice(±s)
剂量/g·kg-1n 摄食量(g·10g-1)组别空白对照组因宁片组-322020第3d 2.48±0.252.33±0.15第6d 2.06±0.202.01±0.16第13d 1.83±0.151.83±0.03
3.1.4 因宁片对小鼠各脏器的影响 给药结束后第14d大体解剖小鼠,肉眼观察各脏器,心、肝、脾、肺、肾等均无异常。
3.2 对大鼠的慢性毒性实验
3.2.1 因宁片对大鼠一般状况的影响 给药期间,因宁片高、中、低剂量组大鼠的外观体征、行为活动、进食量与粪便等状况均正常,大鼠无一死亡。
3.2.2 因宁片对大鼠体重变化的影响 大鼠体重增长正常,与空白对照组比较,各个时期因宁片高、中、低剂量组体重无显著性差异(P>0.783),提示因宁片对大鼠的体重变化无影响。因宁片对大鼠体重变化的影响见表3。
表3 因宁片对大鼠体重变化的影响(±s)Tab 3 Effects of Yinning tablets on the variation of body weight in rats(±s)
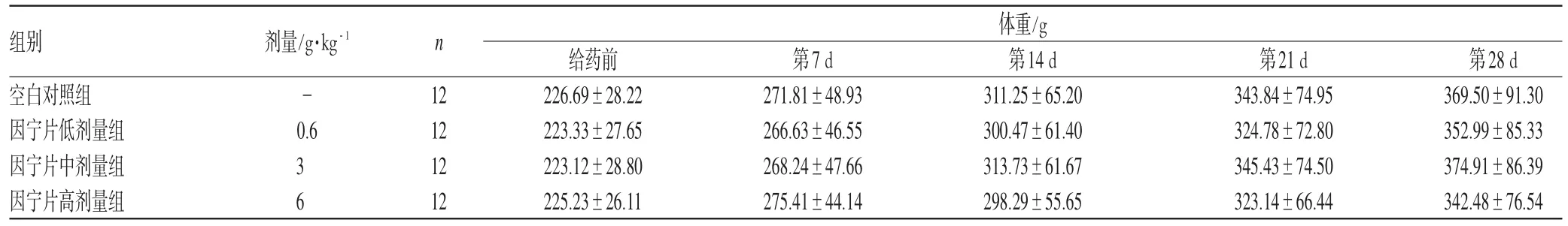
表3 因宁片对大鼠体重变化的影响(±s)Tab 3 Effects of Yinning tablets on the variation of body weight in rats(±s)
组别空白对照组因宁片低剂量组因宁片中剂量组因宁片高剂量组剂量/g·kg-1n体重/g-0.63 612121212给药前226.69±28.22223.33±27.65223.12±28.80225.23±26.11第7d 271.81±48.93266.63±46.55268.24±47.66275.41±44.14第14d 311.25±65.20300.47±61.40313.73±61.67298.29±55.65第21d 343.84±74.95324.78±72.80345.43±74.50323.14±66.44第28d 369.50±91.30352.99±85.33374.91±86.39342.48±76.54
3.2.3 因宁片对大鼠摄食量变化的影响 大鼠摄食量正常,与空白对照组比较,各个时期因宁片高、中、低剂量组摄食量无显著性差异(P>0.221),提示因宁片对大鼠的摄食量无影响。因宁片对大鼠摄食量的影响见表4。
3.2.4 因宁片对大鼠血液学指标的影响 与空白对照组比较,因宁片低剂量组RBC、HGB、HCT、LY数显著升高(P<0.01),PLT、NE、EO数显著降低(P<0.01);因宁片中剂量组NE、网织RBC数、EO数显著降低(P<0.01或P<0.05),LY、MO数显著升高(P<0.01或P<0.05);因宁片高剂量组大鼠的LY数显著升高(P<0.05),EO数显著降低(P<0.01)。因宁片对大鼠血液学指标的影响见表5。
表4 因宁片对大鼠摄食量的影响(±s)Tab 4 Effects of Yinning tablets on food intake in rats(±s)
剂量/g·kg-1n 摄食量(g·10g-1)组别空白对照组因宁片低剂量组因宁片中剂量组因宁片高剂量组-0.63 612121212第7d 9.51±0.649.00±0.299.43±0.408.98±0.30第14d 8.08±0.668.03±0.138.15±0.518.10±0.32第21d 8.40±0.657.73±0.538.18±0.318.38±0.82第28d 7.78±0.687.53±0.507.33±0.337.75±0.17
表5 因宁片对大鼠血液学指标的影响(±s)Tab 5 Effects of Yinning tablets on hematology index in rats(±s)
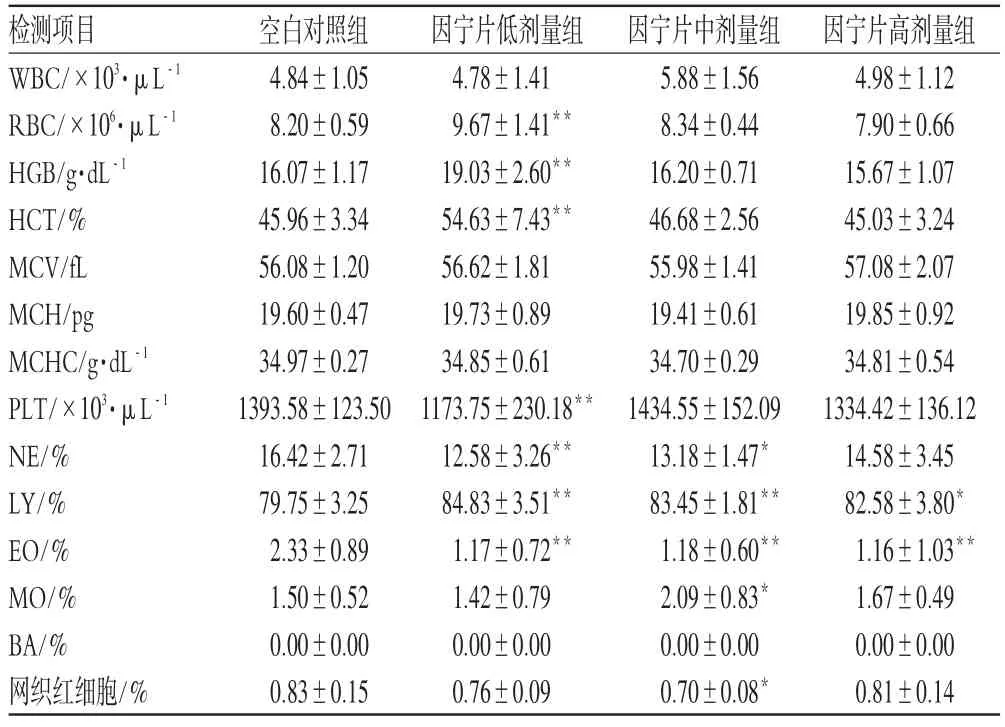
表5 因宁片对大鼠血液学指标的影响(±s)Tab 5 Effects of Yinning tablets on hematology index in rats(±s)
与空白对照组比较:*P<0.05,**P<0.01vs.blank control group:*P<0.05,**P<0.01
检测项目WBC/×103·μL-1 RBC/×106·μL-1 HGB/g·dL-1 HCT/%MCV/fL MCH/pg MCHC/g·dL-1 PLT/×103·μL-1 NE/%LY/%EO/%MO/%BA/%网织红细胞/%因宁片高剂量组4.98±1.127.90±0.6615.67±1.0745.03±3.2457.08±2.0719.85±0.9234.81±0.541334.42±136.1214.58±3.4582.58±3.80*1.16±1.03**1.67±0.490.00±0.000.81±0.14空白对照组4.84±1.058.20±0.5916.07±1.1745.96±3.3456.08±1.2019.60±0.4734.97±0.271393.58±123.5016.42±2.7179.75±3.252.33±0.891.50±0.520.00±0.000.83±0.15因宁片低剂量组4.78±1.419.67±1.41**19.03±2.60**54.63±7.43**56.62±1.8119.73±0.8934.85±0.611173.75±230.18**12.58±3.26**84.83±3.51**1.17±0.72**1.42±0.790.00±0.000.76±0.09因宁片中剂量组5.88±1.568.34±0.4416.20±0.7146.68±2.5655.98±1.4119.41±0.6134.70±0.291434.55±152.0913.18±1.47*83.45±1.81**1.18±0.60**2.09±0.83*0.00±0.000.70±0.08*
3.2.5 因宁片对大鼠血液生化指标的影响 与空白对照组比较,因宁片低剂量组TG含量显著降低(P<0.05);因宁片中剂量组GLU含量显著降低(P<0.01),Na显著升高(P<0.05);因宁片高剂量组TP、ALb、TG含量显著降低(P<0.01或P<0.05)。因宁片对大鼠血液生化指标的影响见表6。
表6 因宁片对大鼠血液生化指标的影响(±s)Tab 6Effects of Yinning tablets on blood biochemical index in rats(±s)
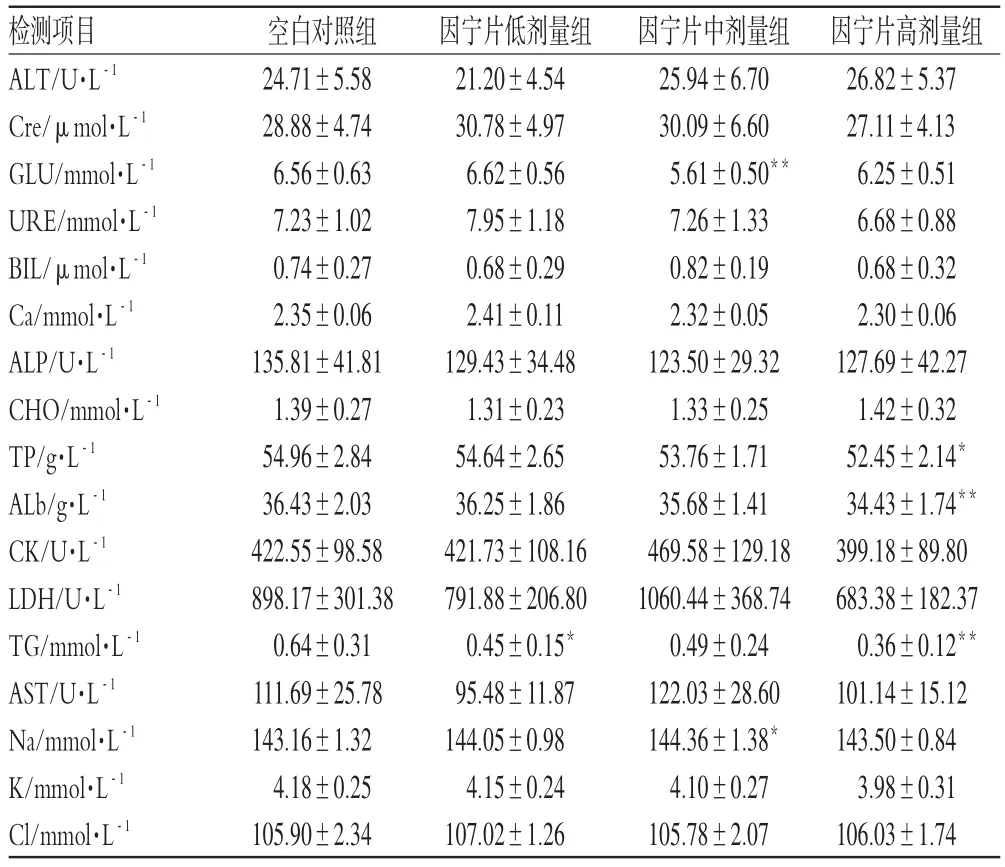
表6 因宁片对大鼠血液生化指标的影响(±s)Tab 6Effects of Yinning tablets on blood biochemical index in rats(±s)
与空白对照组比较:*P<0.05,**P<0.01vs.blank control group:*P<0.05,**P<0.01
检测项目ALT/U·L-1 Cre/μmol·L-1 GLU/mmol·L-1 URE/mmol·L-1 BIL/μmol·L-1 Ca/mmol·L-1 ALP/U·L-1 CHO/mmol·L-1 TP/g·L-1 ALb/g·L-1 CK/U·L-1 LDH/U·L-1 TG/mmol·L-1 AST/U·L-1 Na/mmol·L-1 K/mmol·L-1 Cl/mmol·L-1因宁片高剂量组26.82±5.3727.11±4.136.25±0.516.68±0.880.68±0.322.30±0.06127.69±42.271.42±0.3252.45±2.14*34.43±1.74**399.18±89.80683.38±182.370.36±0.12**101.14±15.12143.50±0.843.98±0.31106.03±1.74空白对照组24.71±5.5828.88±4.746.56±0.637.23±1.020.74±0.272.35±0.06135.81±41.811.39±0.2754.96±2.8436.43±2.03422.55±98.58898.17±301.380.64±0.31111.69±25.78143.16±1.324.18±0.25105.90±2.34因宁片低剂量组21.20±4.5430.78±4.976.62±0.567.95±1.180.68±0.292.41±0.11129.43±34.481.31±0.2354.64±2.6536.25±1.86421.73±108.16791.88±206.800.45±0.15*95.48±11.87144.05±0.984.15±0.24107.02±1.26因宁片中剂量组25.94±6.7030.09±6.605.61±0.50**7.26±1.330.82±0.192.32±0.05123.50±29.321.33±0.2553.76±1.7135.68±1.41469.58±129.181060.44±368.740.49±0.24122.03±28.60144.36±1.38*4.10±0.27105.78±2.07
3.2.6 因宁片对大鼠各脏器的影响 因宁片高、中、低剂量组大鼠的各脏器系数与空白对照组比较,均无显著性差异(P>0.05)。因宁片对大鼠各脏器系数的影响见表7。
3.2.7 因宁片对大鼠组织器官的影响 末次给药24h后,处死各组大鼠,肉眼观察心、肝、脾、肺、肾、胃等脏器外形、体积、色泽均属正常,无充血、肿胀、坏死等异常现象。各脏器用10%甲醛固定48h后,按常规法做病理切片,光镜下观察。结果,因宁片高、中、低剂量组大鼠的心、肝、脾、肺、肾等脏器与空白对照组比较,均未见异常。病理组织学检查未见到由于因宁片毒性引起的病理改变。脏器病理切片见图1。
表7 因宁片对大鼠各脏器系数的影响(±s)Tab 7 Effects of Yinning tablets on organ coefficient in rats(±s)
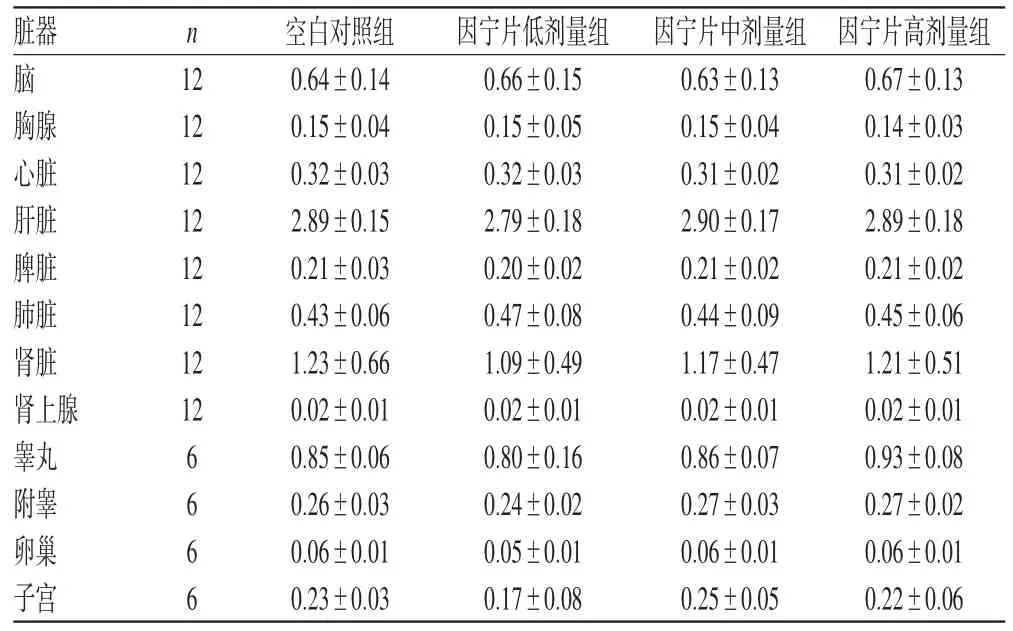
表7 因宁片对大鼠各脏器系数的影响(±s)Tab 7 Effects of Yinning tablets on organ coefficient in rats(±s)
n脏器脑胸腺心脏肝脏脾脏肺脏肾脏肾上腺睾丸附睾卵巢子宫12121212121212126 6 6 6空白对照组0.64±0.140.15±0.040.32±0.032.89±0.150.21±0.030.43±0.061.23±0.660.02±0.010.85±0.060.26±0.030.06±0.010.23±0.03因宁片低剂量组0.66±0.150.15±0.050.32±0.032.79±0.180.20±0.020.47±0.081.09±0.490.02±0.010.80±0.160.24±0.020.05±0.010.17±0.08因宁片中剂量组0.63±0.130.15±0.040.31±0.022.90±0.170.21±0.020.44±0.091.17±0.470.02±0.010.86±0.070.27±0.030.06±0.010.25±0.05因宁片高剂量组0.67±0.130.14±0.030.31±0.022.89±0.180.21±0.020.45±0.061.21±0.510.02±0.010.93±0.080.27±0.020.06±0.010.22±0.06

图1 脏器病理切片A1.空白对照组心脏;A2.因宁片高剂量组心脏;B1.空白对照组肝脏;B2.因宁片高剂量组肝脏;C1.空白对照组脾脏;C2.因宁片高剂量组脾脏;D1.空白对照组肺;D2.因宁片高剂量组肺;E1.空白对照组肾脏;E2.因宁片高剂量组肾脏;F1.空白对照组胃;F2.因宁片高剂量组胃Fig 1 Pathological section of several organsA1.blank control group heart;A2.Yinning tablet high dose group heart;B1.blank control group liver;B2.Yinning tablet high dose group liver;C1.blank control group spleen;C2.Yinning tablet high dose group spleen;D1.blank control group lung;D2.Yinning tablet high dose group lung;E1.blank control group kidney;E2.Yinning tablet high dose group kidney;F1.blank control group stomach;F2.Yinning tablet high dose group stomach
4 讨论
甲亢是由多种原因引起甲状腺激素过多导致机体代谢过高的内分泌疾病。甲亢可以影响多个器官系统,包括心血管系统、神经系统、胃肠道与肝脏等[5]。前期实验证明,因宁片可以降低甲亢大鼠的三碘甲状腺原氨酸(T3)、甲状腺素(T4)、游离三碘甲状腺原氨酸(FT3)、游离甲状腺素(FT4)水平,升高促甲状腺激素(TSH)水平,具有抗甲亢的作用[1,2]。
甲亢性肝损害临床常见,其发生率国内、外报道不一,国内学者研究得出111例新诊Graves患者中有52.6%存在肝功能异常[6]。甲亢性肝损害的发生机制主要有肝脏的氧化应激反应、肝细胞的凋亡等。本研究结果表明,因宁片各剂量组与空白对照组比较,肝功能指标(ALT、AST、BIL、ALP、TP)均无显著性差异,说明因宁片对肝脏无毒性作用。与此同时,本课题组前期研究发现:因宁片对甲亢性肝损害具有保护作用,可能机制如下:降低肝脏丙二醛(MDA)含量,增强超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷胱甘肽过氧化物酶(GSH-Px)活性,提高抗氧化系统清除自由基的能力,纠正氧化和抗氧化系统失衡[2];降低甲亢性肝损害大鼠肝脏脂肪酸合成酶(Fas)、Fas配体(FasL)、肿瘤坏死因子-α(TNF-α)的表达[7];使甲亢大鼠肝细胞天冬氨酸蛋白酶(Caspase)-3蛋白表达明显下调,B细胞淋巴瘤/白血病(Bcl)-2蛋白表达明显上调[8]。
本研究结果表明,急性毒性实验未测出因宁片的LD50,在MTD的情况下也未出现毒性反应;慢性毒性实验在高剂量的情况下,大鼠一般状况正常,未出现明显毒性反应和死亡,可见因宁片比较安全。因宁片对实验大、小鼠的体重和摄食量都没有影响。因宁片各组RBC、HGB、HCT、LY、EO、PLT、NE、网织RBC、GLU、TP、ALb、TG较空白对照组有轻微变化,但均在允许范围之内[9],产生原因尚不明确,可能的原因是昆明山海棠具有抗炎、免疫抑制等药效学与毒理学性质有关[10],但在本组方中用量较小,无显著性影响。
综上,本文急性毒性和慢性毒性实验证明,因宁片毒性低,可为临床安全用药提供理论依据。
[1] 刘 婷,侯连兵,钟延松.因宁片对甲状腺片诱导的甲亢阴虚型大鼠的影响研究[J].医药导报,2009,28(11):1452.
[2] 周 静,王成蹊,侯连兵.因宁片对甲亢性肝损害模型大鼠肝功能和氧化应激的影响[J].中药材,2011,34(2):278.
[3] Bai L,Chen SZ,Liang S,et al.The influence of tripterygium hypoglaucum hutch on the HIF-1α expression in the CIA rat models[J].Xi Bao Yu Fen Zi Mian Yi Xue Za Zhi,2011,27(10):1061.
[4] 刘树民,姚珠星,张丽霞.黄芪对苍耳子肝毒性影响的实验研究[J].药物不良反应杂志,2007,9(1):17.
[5] Khemichian S,Fong TL.Hepatic dysfunction in hyperthyroidism[J].Gastroenterol Hepatol(N Y),2011,7(5):337.
[6] 马丽娜,张晓宙.新诊断的Graves病患者肝功能测定的临床意义[J].临床内科,2003,20(5):257.
[7] 周 静,王成蹊,侯连兵.因宁片对甲亢性肝损害大鼠肝脏Fas,FasL,TNF-α表达的影响[J].中国药房,2011,22(7):597.
[8] 周 静,王成蹊,潘弟仪.因宁片对甲亢大鼠肝细胞凋亡调节蛋白Caspase-3和Bcl-2表达的影响[J].中国药业,2011,20(11):9.
[9] 赵毓梅,郑定仙,黄业宇.SD大鼠血常规、血液生化指标、脏体比正常参考值范围研究[J].中国卫生检验杂志,2002,12(2):165.
[10] 杨录军,余厚勇,黄 萍.昆明山海棠水提液的急性毒性研究[J].第三军医大学学报,2003,25(17):1524.
