RP-HPLC法测定银天颗粒中主要药效成分的含量Δ
2012-08-29李金玲王永胜张聪聪徐晓玉西南大学药学院重庆市药效评价工程技术研究中心重庆400715
张 辉,李金玲,王永胜,张聪聪,徐晓玉(西南大学药学院/重庆市药效评价工程技术研究中心,重庆400715)
银天颗粒是本课题组研制的中药复方保健品,主要用于防治春夏之交瘟疫流行、热毒所伤;或夏季伤暑、烦热口渴;或嗜食香燥、火毒内生等。它是本课题组科技扶贫项目“秀山金银花产业开发”的产业链深加工产品,是从秀山灰毡毛忍冬(山银花)、栀子等物质中提取的有效成分制成的一种药食两用保健品,已经申报国家技术发明专利,具有自主知识产权。其中,山银花主要功效成分为绿原酸,具有抗菌、抗病毒、保肝利胆等药理作用[1,2]。栀子的主要功效成分为栀子苷,具有抗炎利胆、抗肿瘤、降血糖等多种药理作用[3,4]。为了更好地控制银天颗粒的质量,本试验采用反相高效液相色谱(RP-HPLC)法对其主要药效成分绿原酸和栀子苷进行了含量测定。
1 仪器与试药
1200Series型HPLC仪(美国Agilent公司);EL-2046型电子天平(梅特勒-托利多仪器上海有限公司);KQ5200E型超声波清洗器(江苏昆山市超声仪器有限公司)。
绿原酸、栀子苷对照品(中国食品药品检定研究院,批号分别为110753-200413、110749-200714);银天颗粒(西南大学中药研究所研制,规格:2g/袋,批号:2010092801、2010092802、2010092803);乙腈、磷酸为色谱纯,甲醇为分析纯,水为双蒸水。
2 方法与结果
2.1 RP-HPLC法测定银天颗粒中绿原酸的含量
2.1.1 色谱条件 色谱柱:Platisil-ODS(250mm×4.6mm,5µm);流动相:乙腈-0.2%磷酸(20∶80);流速:1.0mL·min-1;检测波长:326nm;柱温:25℃;进样量:20µL。
2.1.2 对照品贮备液的制备 精密称取绿原酸对照品0.0108g,置于100mL容量瓶中,加50%甲醇溶解并定容,摇匀,即得浓度为108.0µg·mL-1的对照品贮备液。
2.1.3 供试品溶液的制备 取银天颗粒适量,研成细粉,取0.3g,精密称定,置25mL棕色容量瓶中,加50%甲醇20mL,超声处理(工作频率:40kHz,功率:220W)30min,放冷至室温,加50%甲醇定容,摇匀,滤过。精密量取续滤液1mL,置5mL棕色容量瓶中,加50%甲醇定容,摇匀。用0.22µm微孔滤膜滤过,取续滤液作为供试品溶液。
2.1.4 阴性对照溶液的制备 按处方量制备仅含辅料的颗粒作为阴性样品,按“2.1.3”项下方法制备阴性对照溶液。
2.1.5 系统适用性试验 分别取对照品溶液、供试品溶液和阴性对照溶液适量,按“2.1.1”项下色谱条件分别进样检测。结果表明,阴性对照对绿原酸的测定无干扰;绿原酸的保留时间为5.5min,峰形良好,与其他组分峰分离较好;理论板数不低于5000,分离度均>4。色谱见图1。
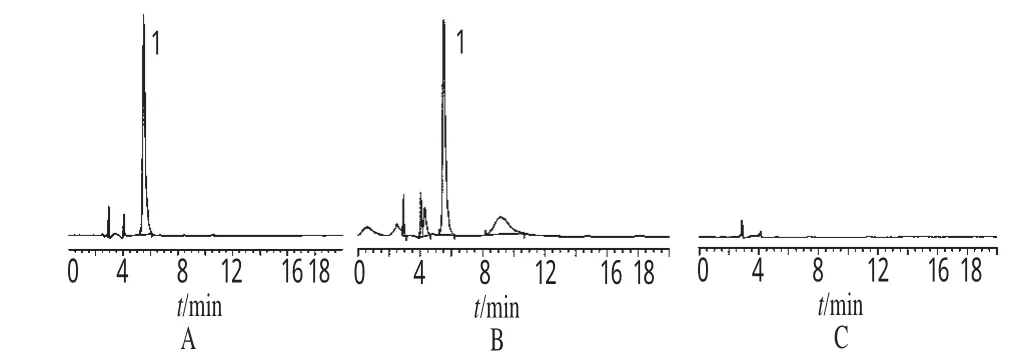
图1 绿原酸的HPLC图A.对照品;B.供试品;C.阴性对照;1.绿原酸Fig 1 HPLC chromatograms of chlorogenic acidA.substance control;B.test samples;C.negative control;1.chlorogenic acid
2.1.6 标准曲线的制备 分别精密吸取绿原酸对照品贮备液0.5、1.0、2.0、5.0、10.0mL,置10mL棕色容量瓶中,加50%甲醇定容,摇匀,用0.22µm微孔滤膜过滤后按“2.1.1”项下色谱条件进样检测,记录峰面积。以绿原酸浓度(c,µg·mL-1)为横坐标,峰面积积分值(A)为纵坐标,进行线性回归,得回归方程为A=11.022c-5.5739(r=0.9999,n=5)。结果表明,绿原酸检测浓度在5.4~108.0µg·mL-1范围内与峰面积积分值呈良好线性关系。
2.1.7 精密度试验 取绿原酸对照品溶液(21.6µg·mL-1)适量,连续进样测定6次,记录峰面积。结果,RSD=0.15%(n=6),表明仪器精密度良好。
2.1.8 稳定性试验 取同一供试品溶液适量,分别于0、2、4、8、12、24h按“2.1.1”项下色谱条件进样测定,记录峰面积。结果,RSD=1.79%(n=6),表明供试品溶液在24h内稳定。
2.1.9 重复性试验 精密称取同一批样品(批号:2010092803)适量,共6份,分别按“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样,测定绿原酸的含量。结果,6份样品中绿原酸的平均含量为11.08mg·g-1,RSD=0.16%(n=6),表明该方法重复性良好。
2.1.10 加样回收率试验 精密称取已知含量的同一批次样品(批号:2010092803,绿原酸含量:11.08mg·g-1)适量,共6份,分别精密加入适量的绿原酸对照品,按“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定。结果,绿原酸的平均回收率为99.04%,RSD=2.66%(n=6)。
2.1.11 样品含量测定 按上述方法测定3批样品(批号:2010092801、2010092802、2010092803)含量,各平行操作 3份。结果,3批样品中绿原酸的平均含量分别为11.32、11.81、11.08mg·g-1(n=3)。
2.2 RP-HPLC法测定银天颗粒中栀子苷的含量
2.2.1 色谱条件 色谱柱:Agilent Zorbax SB-C18(250mm×4.6mm,5μm);流动相:乙腈-水(10∶90);检测波长:238nm;流速:1.0mL·min-1;柱温:25℃;进样量:20µL。
2.2.2 对照品贮备液的制备 精密称取栀子苷对照品0.0110g,置于100mL容量瓶中,加甲醇溶解并定容,摇匀,即得浓度为110µg·mL-1的对照品贮备液。
2.2.3 供试品溶液的制备 取银天颗粒适量,研成细粉,取3g,精密称定,置具塞锥形瓶中,精密加入甲醇25mL,摇匀,称重,超声处理(工作频率:40kHz,功率:220W)30min,放冷至室温,再称重,加甲醇补足失重,密塞,摇匀。用0.22µm微孔滤膜滤过,取续滤液作为供试品溶液。
2.2.4 阴性对照溶液的制备 按处方量制备仅含辅料的颗粒作为阴性样品,按“2.2.3”项下方法制备阴性对照溶液。
2.2.5 系统适用性试验 分别吸取供试品、对照品和阴性对照溶液适量,按“2.2.1”项下色谱条件分别进样检测。结果表明,阴性对照对栀子苷的测定无干扰;栀子苷的保留时间为19.2min,峰形良好,与其他组分峰分离较好;理论板数不低于4000,分离度均>4。色谱见图2。

图2 栀子苷的HPLC图A.对照品;B.供试品;C.阴性对照;1.栀子苷Fig 2HPLC chromatograms of gasminoidinA.standard sample;B.test samples;C.negative control;1.gasminoidin
2.2.6 标准曲线的制备 分别精密吸取栀子苷对照品贮备液1.0、2.0、4.0、6.0、8.0、10.0mL,置10mL棕色容量瓶中,加甲醇定容,摇匀,用0.22µm微孔滤膜滤过后按“2.2.1”项下色谱条件进样检测,记录峰面积。以栀子苷浓度(c,µg·mL-1)为横坐标,峰面积积分值(A)为纵坐标,进行线性回归,得回归方程为A=25.583c+4.8044(r=0.9999,n=6)。结果表明,栀子苷的检测浓度在11~110µg·mL-1范围内与峰面积积分值呈良好线性关系。
2.2.7 精密度试验 取栀子苷对照品溶液(55µg·mL-1)适量,连续进样测定6次,记录峰面积。结果,RSD=0.45%(n=6),表明仪器精密度良好。
2.2.8 稳定性试验 取同一供试品溶液适量,分别于0、0.5、2、4、8、12h按“2.2.1”项下色谱条件进样测定,记录峰面积。结果,RSD=2.06%(n=6),表明供试品溶液在12h内稳定。
2.2.9 重复性试验 精密称取同一批样品(批号:2011092802)适量,共6份,分别按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样,测定栀子苷的含量。结果,6份样品中栀子苷的平均含量为0.168mg·g-1,RSD=0.82%(n=6),表明该方法重复性良好。
2.2.10 加样回收率试验 精密称取已知含量的同一批次样品(批号:2011092803,栀子苷含量:0.178mg·g-1)适量,共6份,分别精密加入适量的栀子苷对照品,按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进样测定。结果,栀子苷的平均回收率为97.69%,RSD=2.07%(n=6)。
2.2.11 样品含量测定 按上述方法测定3批样品(批号:2010092801、2010092802、2010092803)含量,各平行操作3份。结果,栀子苷的平均含量分别为0.147、0.168、0.178mg·g-1。
3 讨论
为了控制银天颗粒中山银花和栀子的含量,笔者参照药典及相关文献[5~8],分别建立了银天颗粒中绿原酸、栀子苷含量测定的RP-HPLC法。结果表明,在本试验所选的色谱条件下,银天颗粒中药用辅料对绿原酸、栀子苷的含量测定无干扰,目标成分峰形良好,且能与其他组分峰较好地分离。2种方法均具有回收率高、重复性好、分析快速、结果准确、专属性强的优点,可用于银天颗粒的质量控制。
[1] 国家药典委员会.中华人民共和国药典(一部)[S].2010年版.北京:中国医药科技出版社,2010:28.
[2] 王 辉,田呈瑞,马守磊,等.绿原酸的研究进展[J].食品工业科技,2009,30(5):341.
[3] 倪慧艳,张俊慧,傅海珍.中药栀子的研究与开发概述[J].中国中药杂志,2006,31(7):538.
[4] 李葆华.栀子的研究概况[J].时珍国医国药,2004,33(5):583.
[5] 徐 玲,张继芬,吴芳洲,等.HPLC法测定双花颗粒中绿原酸的含量[J].中国药房,2011,22(23):2156.
[6] 陈 辉.HPLC法测定复方感冒颗粒中绿原酸的含量[J].中国中药杂志,2008,33(5):583.
[7] 孙文武.HPLC法测定栀柏合剂中栀子苷的含量[J].中国药房,2007,18(33):2609.
[8] 笔雪燕,刘晓凤,张清波.HPLC法测定清开灵泡腾片中栀子苷的含量[J].中国药房,2011,22(8):240.
