HPLC法测盐酸左西替利嗪颗粒的含量
2012-08-28洪江游洪志慧凌日金谢清春
洪江游 洪志慧 凌日金 谢清春
HPLC法测盐酸左西替利嗪颗粒的含量
洪江游 洪志慧 凌日金 谢清春
目的建立盐酸左西替利嗪颗粒含量的高效液相色谱测定法。方法采用C18柱,以甲醇-磷酸二氢钠溶液(70∶30)为流动相,流速1ml/min,检测波长230nm。结果在4.98~49.8μg/ml范围内呈线性关系,进样精密度、重复性试验和中间精密度的RSD分别为0.25%、0.49%和0.61%,低中高三个浓度的回收率分别是99.41%、99.55%和99.64%。结论本法可用于盐酸左西替利嗪颗粒含量测定。
盐酸左西替利嗪;HPLC;含量测定
盐酸左西替利嗪是选择性组胺H1受体拮抗制剂,作为新型抗组胺药,主要用于缓解变态反应性疾病的过敏症状,临床上用于治疗变应性鼻炎、荨麻疹、血管神经性水肿等皮肤黏膜过敏性疾病,具有口服吸收迅速,受体选择性高,临床疗效强,副作用小,安全性好等多方面优点[1,2]。其对组胺H1受体的亲和力比西替利嗪高出2倍,是右西替利嗪的30倍,且受体结合时间更长[3]。本文研究了高效液相色谱法测定盐酸左西替利嗪颗粒剂含量的方法。
1 仪器与试剂
岛津LC-10A高效液相色谱仪;Chromstation色谱工作站;电子天平(型号:ALC,d=0.0001)。盐酸左西替利嗪(湖南九典制药有限公司,批号200604J03,含量:99.4%);盐酸左西替利嗪对照品(中国药品生物制品检定所,批号100659-200401);三批盐酸左西替利嗪颗粒(海南中瑞康芝制药有限公司制备,批号:060601、060602、060603);磷酸(分析纯),甲醇(色谱纯),水为双蒸水。
2 方法和结果
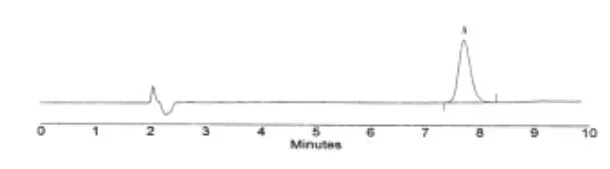
图1 对照品
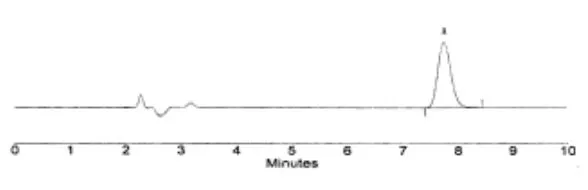
图2 样品

图3 阴性对照
2.1 溶液的配制 供试品溶液:取盐酸左西替利嗪颗粒研细粉末适量(约相当于盐酸左西替利嗪2.5mg),置100ml量瓶中,加水适量,振摇使溶解并稀释至刻度,摇匀,滤过,即得。
阴性对照溶液:取空白辅料适量(约相当于盐酸左西替利嗪2.5mg),置100ml量瓶中,加水适量,振摇使溶解并稀释至刻度,摇匀,滤过,即得。对照品溶液:取线性与范围下25μg/ml即得。
2.2 色谱条件与系统适用性 色谱柱:Apollo C18柱(250×4.6mm,5μm);流动相:甲醇-磷酸二氢钠溶液(取 NaH2PO4·2H2O 3.12g加水至1000ml溶解)(70∶30);流速1ml/min 检测波长 230nm;进样量 20μl。
精密量取供试品溶液、阴性对照溶液、对照品溶液各20μl,注入液相色谱仪,记录色谱图。同法测定。结果盐酸左西替利嗪保留时间为7.758min,理论板数为5040;空白辅料峰均在4min之前,不干扰测定,见图1、图2和图3。
2.3 线性与范围 精密称取盐酸左西替利嗪25mg,置50ml量瓶中,加水适量,振摇使溶解并稀释至刻度,摇匀,再分别精密称取 1、3、5、7、10ml,置 100ml量瓶中,用水稀释至刻度,摇匀。分别精密量取20μl,注入液相色谱仪,记录色谱图,结果线性方程:A=16083C+1136.4,R2=0.9994。盐酸左西替利嗪在4.98~49.8μg/ml浓度范围内,浓度与峰面积呈良好的线性关系。
2.4 进样精密度 取线性与范围项下的3号溶液,精密量取20μl,注入液相色谱仪,记录色谱图,连续进样6次峰面积的RSD值为0.25%,精密度好。
2.5 重复性试验 取盐酸左西替利嗪颗粒研细粉末适量(约相当于盐酸左西替利嗪2.5mg),置100ml量瓶中,加水适量,振摇使溶解并稀释至刻度,摇匀,滤过,平行配制六份,分别精密量取20μl,注入液相色谱仪,记录色谱图。另取105℃干燥2h的盐酸左西替利嗪对照品适量,加水溶解并稀释制成每1ml中约含25μg的溶液,同法测定,按外标法以峰面积计算。结果盐酸左西替利嗪颗粒的6份平行样品的含量测定结果的RSD为0.49%,方法重复性好。
2.6 中间精密度 不同分析人(两个人)、不同日期(两天),取盐酸左西替利嗪颗粒研细粉末适量(约相当于盐酸左西替利嗪2.5mg),置100ml量瓶中,加水适量,振摇使溶解并稀释至刻度,摇匀,滤过,平行配制六份,分别精密量取20μl,注入液相色谱仪,记录色谱图。另取105℃干燥2h的盐酸左西替利嗪对照品适量,加水溶解并稀释制成每1ml中约含25μg的溶液,同法测定,按外标法以峰面积计算,结果不同分析人、不同日期检测盐酸左西替利嗪颗粒样品的含量测定的RSD为0.61%,方法中间精密度好。
2.7 回收率试验 分别精密称取盐酸左西替利嗪20、25、30mg各3份,置1000ml量瓶中,并按处方比例加入辅料,加水适量,振摇使溶解并稀释至刻度,摇匀,滤过,平行配制六份,分别精密量取20μl,注入液相色谱仪,记录色谱图。另取105℃干燥2h的盐酸左西替利嗪对照品适量,加水溶解并稀释制成每1ml中约含25μg的溶液,同法测定,按外标法以峰面积,计算回收率,结果见表1,高中低三浓度的回收率均在98.0% ~102.0%范围内,符合规定。
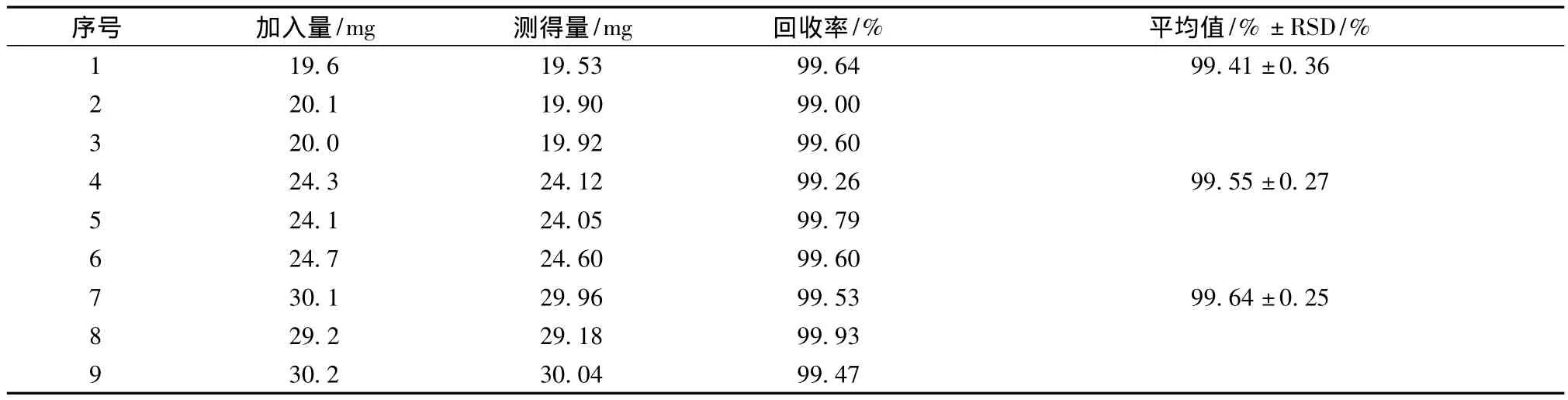
表1 盐酸左西替利嗪颗粒含量测定回收率试验结果
2.8 溶液稳定性试验 取重复性试验项下样品溶液之一,于室温条件下放置,分别于0、2、4、6、8h测定,结果盐酸左西替利嗪颗粒含量测定溶液在室温放置8h,各时间点峰面积的RSD为0.20%,小于2%,说明在盐酸左西替利嗪颗粒的水溶液8h内稳定。
2.9 含量测定 取本品10袋,倾出内容物,混匀研细,称取细粉适量(约相当于盐酸左西替利嗪2.5mg),置100ml量瓶中,加水适量,振摇使溶解并稀释至刻度,摇匀,滤过,精密量取20μl,注入液相色谱仪,记录色谱图。另取105℃干燥2h的盐酸左西替利嗪对照品适量,加水溶解并稀释制成每1ml中约含25μg的溶液,同法测定,按外标法以峰面积计算,结果见表2。计算公式为:
C对照品:盐酸左西替利嗪对照品溶液的浓度(μg/ml)
C供试品:盐酸左西替利嗪颗粒供试品溶液的浓度(mg/ml)
A对照品:盐酸左西替利嗪对照品溶液主峰面积
A供试品:盐酸左西替利嗪颗粒供试品溶液主峰面积
W:盐酸左西替利嗪颗粒平均装量(g)

表2 三批样品含量测定结果
结论:本品可采用高效液相色谱法进行含量测定。经方法学研究结果表明,方法灵敏度、准确度、重复性、精密度、线性均符合要求。
2.10 含量均匀度 取本品1袋,将内容物置100ml量瓶中,加水适量,振摇使溶解并稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液,照含量测定项下的方法测定,应符合规定(中国药典2005年版二部附录X E)。三批样品含量均匀度检查结果见表3,三批样品的A+1.8S均小于15.0,含量均匀度符合药典规定。
3 讨论
本文的流动相先后考察过流动相1:甲醇-磷酸二氢钠溶液(取NaH2PO4O2H2O 3.12g加水至1000ml溶解)(75∶25),结果此条件下,盐酸左西替利嗪出峰较快(约5.5min)。流动相2:庚烷磺酸钠溶液(取庚烷磺酸钠0.3g,加水580ml溶解)-乙腈(58∶42)(用稀磷酸调pH至2.4),结果主峰拖尾较严重,加入三乙胺也不能改善峰的拖尾情况。如将流动相1的比例改为70∶30则出峰时间适宜,约8min,可满足本品分析方法的要求。
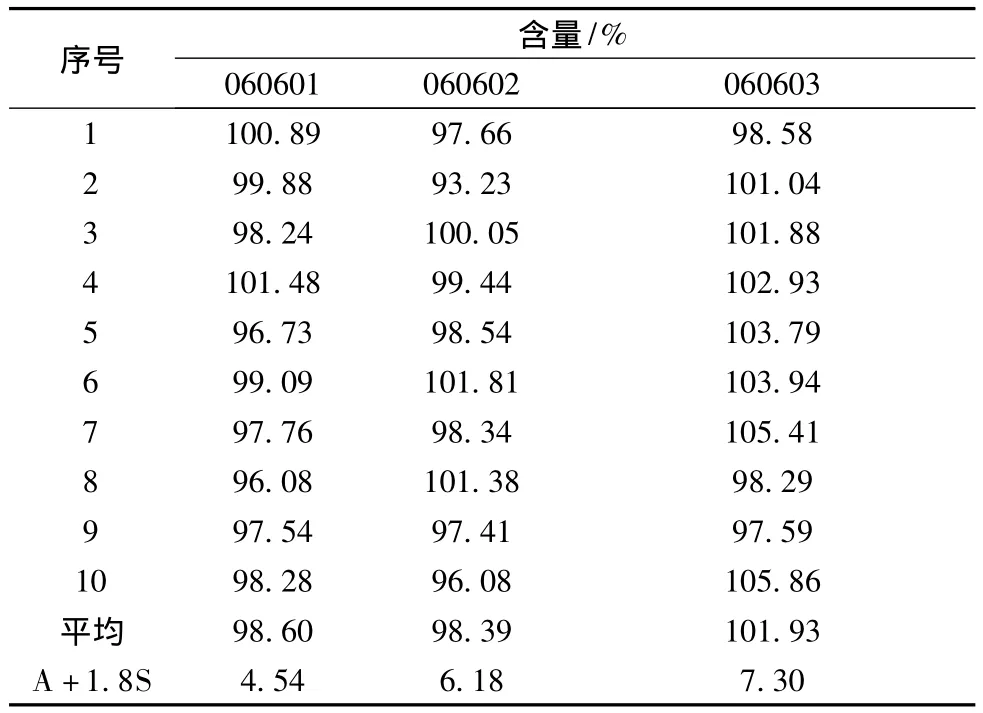
表3 盐酸左西替利嗪颗粒含量均匀度检查结果
[1]Clough GF,Boutsiouki P,Church MK.Comparison of the effects of levocetirizine and loratadine on histamine-induced wheal,flar,and itch in human skin.Allergy,2001,56(10):985-988.
[2]张壹.盐酸左西替利嗪.中国新药杂志,2004,13(12):1420-1421.
[3]Gillard M,Van Der Perren C,Moguilevsky N,et al.Binding characteristics of cetirizine and levocetirizine to human H1histamine receptor’s:Contribution of Lys(191)and Thr(194).Mol Pharmacol,2002,61:391-399.
Content detemination of levocetirizine granules by HPLC method
HONG Jiang-you,HONG Zhi-hui,LING Ri-jin,et al.Kangzhi Pharmaceutical Co.LTD of Hainan,Hainan 570311,China
ObjectiveTo establish a HPLC method to determine the content of levocetirizine granules.MethodsC18column was used,menthol alcohol-Sodium dihydrogen phosphate(70∶30)as mobile phase,flow rate at 1ml/min,detection wavelength at 230nm.ResultsIn 4.98~49.8μg/ml was line.Instrument precision,Repeatability test,middle precision was 0.25%,0.49%and 0.61%respectively.Recoveries(low level,middle level,and high level)were 99.41%,99.55%and 99.64%respectively.ConclusionThe assay method can be used to determine content of levocetirizine granules.
Levocetirizine hydrochloric;HPLC;Content determination
570311海南康芝药业股份有限公司(洪江游 凌日金);深圳市红会医院(洪志慧);广东药学院(谢清春)
谢清春
