实时灰阶超声造影在肝恶性肿瘤射频或微波消融治疗中的作用
2012-08-09刘景丰黄秀烟曾锦树魏凌琳
刘 晖,叶 真*,刘景丰,黄秀烟,许 翔,曾锦树,魏凌琳
1.福建医科大学附属第一医院超声影像科(福建福州350005)
2.福建医科大学附属第一医院肝病中心(福建福州350005)
近年来射频消融(radiofrequency ablation,RFA)和微波消融(microwave ablation,MW)等微创技术治疗肝恶性肿瘤已为临床广泛应用。实时灰阶超声造影技术(以下简称超声造影,Contrast enhanced Ultrasound,CEUS)在肝肿瘤消融治疗中的应用价值正日益受到重视,对辅助肝癌的消融治疗具有重要的临床意义。本文就CEUS在肝癌消融治疗前、治疗过程中、治疗后的作用分别进行了探讨。
1 资料和方法
1.1 研究对象 2003年11月至2010年6月共92例140个肝恶性肿瘤在我院行超声引导下RFA或MW治疗,其中男74例、女18例;年龄32~79岁,平均年龄57.3岁。其中肝细胞肝癌(HCC)87例131个病灶,肝转移癌(MLC)5例9个病灶。术前均行CEUS和(或)增强CT(contrast enhanced CT,CECT)、增强 MRI(contrast enhanced MRI,CEMRI)及活检证实。病灶最大直径11.4 cm,最小0.6 cm。其中实行RFA治疗68例96个病灶,MW治疗24例44个病灶。73例109个病灶消融术前行CEUS检查,其中51例73个病灶同期均行CECT/CEMRI检查;19例31个病灶消融术后行CEUS检查,同期均行CECT/CEMRI检查。
1.2 仪器与方法 采用意大利百胜公司DU8彩色多普勒超声诊断仪,美国西门子SEQUOIA-512彩色多普勒超声诊断仪和荷兰飞利浦IU22彩色多普勒超声诊断仪。微波采用南京亿高微波系统工程公司生产的ECO-100微波治疗仪,射频采用美国RITA MODEL 1500型射频治疗仪。
造影剂用声诺维SonoVue(Bracco SpA,Milan,Italy),主要成分为磷脂包裹的六氟化硫(SF6),产品为瓶装冻干粉剂,使用前在冻干粉剂中注入生理盐水5 ml,用力振荡数秒,直至冻干粉剂完全溶解。
病人采用平卧位或左侧卧位,CEUS前先行常规超声检查,观察病灶形态和病灶内部回声,测量大小,得出初步诊断后启动CEUS软件,经患者左肘静脉快速注入1.0~2.4 ml声诺维混悬液,随即推注5 ml生理盐水。在注射造影剂同时启动机器内置硬盘和蓝韵工作站实时同步录像和留图,记录CEUS过程,观察病灶动脉相、门脉相及实质相,观察6~10 min,可疑病例10 min后将机械指数调高,将残余造影剂爆破后,再次注入声诺维混悬液1 ml反复观察,CEUS结束后将记录的内容进行回放。由两位有经验的超声医师对录像进行观察,记录病灶的形态及造影增强特点,分析并做出CEUS诊断。
1.3 统计学处理 采用SPSS 14.0统计学软件,计量资料以±s表示,行t检验,计数资料采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 肝癌病灶消融术前常规超声及CEUS所测病灶边界清晰、最大直径、面积的情况 73例109个肝癌病灶消融术前行CEUS,观察病灶的边界(见表1),测量病灶的大小范围,于CEUS增强期(动脉期至门静脉期)进行病灶的测量[1],CEUS前后病灶的最大直径、面积均测量3次取平均值 (见表2)。

表1 73例109个肝癌病灶局部消融术前常规超声与CEUS所测病灶边界清晰的比较
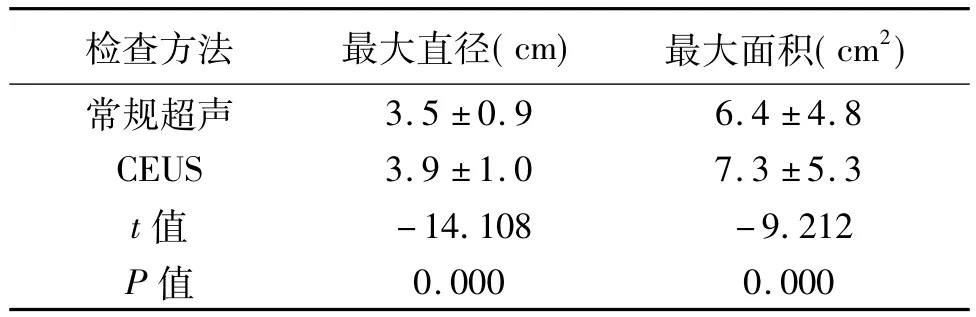
表2 73例109个肝癌病灶局部消融术前常规超声与CEUS所测病灶最大直径、面积的比较
2.2 肝癌病灶局部消融治疗术后CEUS的表现19例31个肝癌病灶局部消融治疗术后CEUS的表现可分为二种。(1)回声三相缺损:CEUS后肝实质有增强而病灶区三相均无增强;(2)局部“快进快出”:CEUS动脉相病灶区增强或部分增强,延迟相病灶区增强部分回声减低,呈”快进快出”的灌注方式(见表3)。

表3 19例31个肝癌病灶局部消融治疗术后CEUS声像表现
2.3 肝癌病灶消融治疗后最终诊断结果及肿瘤灭活情况 19例31个肝癌病灶消融术后肿瘤灭活或残留的最终诊断依两种以上增强影像学检查(CECT、CEMRI、CEUS)并结合 AFP 检查、穿刺活检、患者6个月以上随访综合判断。以临床随访的最终诊断为标准。当两种影像学检查结果为阴性,AFP检查正常,经6个月以上随访病灶无明显变化,可评价为肿瘤灭活。当病灶增大、周边出现弱回声结节,CEUS及CECT/CEMRI显示结节有强化或消退,AFP升高或正常,穿刺活检阳性,为肿瘤复发或残留(见表4)。
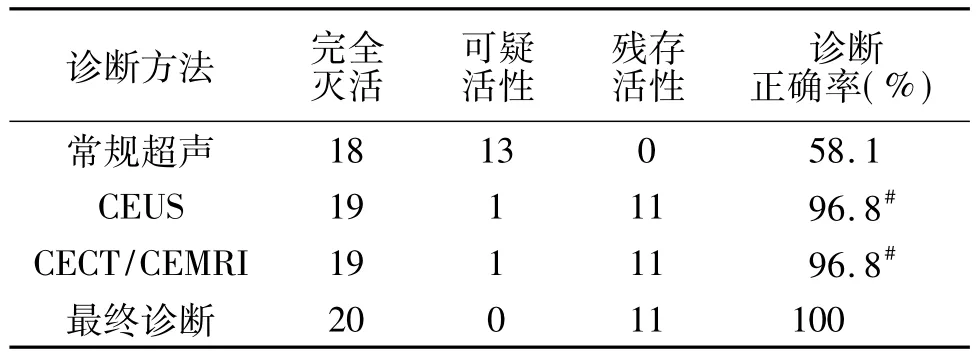
表4 19例31个肝癌病灶消融治疗后最终诊断结果及肿瘤灭活情况
3 讨论
3.1 CEUS在消融治疗前的应用价值
3.1.1 病灶荷瘤血管的观察 热消融治疗肝癌,往往受病灶内血供的影响,对于富血供,以及毗邻大血管的病灶,由于受热传导效应,会影响消融治疗的疗效[2]。CEUS可准确识别荷瘤血管及进入肿瘤的位置,动脉相早期常可观察到造影剂经荷瘤血管流入肿瘤内。由于动脉灌注快速,荷瘤血管的显影时间较短暂,可先参考彩色多普勒超声检查结果选择扫查切面。
CEUS不仅在治疗前明确肿瘤的性质,并且识别荷瘤血管,从而在消融治疗时有针对性地加强对滋养血管区域的治疗,提高了肿瘤的灭活率。
3.1.2 明确病灶的边界、大小、数目,确定治疗方案 肝癌的治疗应力求做到根治,消融范围应该超过肿瘤边界的0.5~1.0 cm,保证安全的“无瘤边缘”,以减少术后复发。因此在肝癌消融治疗前,正确测量肿瘤的实际大小,准确判断肿瘤浸润范围对制定方案至关重要。常规超声测量受肿瘤部位、测量方法等因素影响,对形态不规则、边界不清晰的肿瘤常有测量误差。如表1所示,本组73例109个病灶CEUS增强期106(97.2%)个病灶边界显示清晰,多于常规超声检查的68(62.4%)个病灶边界显示清晰;表2所示,本组73例109个病灶CEUS增强期的大小、面积测值要大于常规超声,更加准确地反映了病灶的大小。
Livraghi T等[3]指出浸润型肿瘤与非浸润型肿瘤存在显著的疗效差异,故消融治疗前充分了解肿瘤生长特征和范围有重要意义。陈敏华[4]认为有部分病例在3~6个月瘤周发现残留复发而影响疗效,与治疗前未能准确判断肿瘤浸润范围或遗漏微小卫星灶或肿瘤血供丰富不易灭活等相关。CEUS可灵敏显示主瘤灶周围3~5mm卫星灶及肝内1cm左右微小癌灶,对确定肿瘤数目、选择适应证有重要的参考应用价值。CEUS的高灵敏性对于10 mm以下的肝肿瘤的早期发现意义十分重大。消融治疗前CEUS提供的信息是筛选适应证的重要手段,重视应用可有效减少消融治疗后复发新生率。
3.2 CEUS在消融治疗中的应用价值 显示常规超声未能显示的肝硬化背景下的病灶并引导消融治疗,术后即时评价有无残余病灶,以确定是否需要继续消融治疗,从而有效灭活肿瘤,避免损伤肝组织。本组有1个肝硬化背景下的HCC病灶常规超声未能清晰显示,CEUS清晰显示病灶,明确病灶位置和大小,在CEUS引导下行射频治疗并获得完全灭活。本组术后即时评价5个病灶(MW:2个,RFA:3个),均获得完全灭活。
初次消融肿瘤即获整体灭活是降低复发转移的关键[5]。肝癌消融治疗后,常规超声对坏死区只能进行粗略的估计,不能作为有效的评估方法。以CECT通常在治疗后l周时被用来评价局部疗效,但若发现病灶残留再次进行补充治疗却相当复杂和困难[6]。CEUS如果发现病灶残留,即可在CEUS的引导下即时完成补充治疗,最大程度地保证一次治疗达到病灶的完全灭活,缩短了疗程,提高了疗效。
3.3 CEUS对评价消融治疗疗效的作用 以临床随访的最终诊断为标准,本研究结果显示,对MW/RFA治疗效果的判断,常规超声准确率为58.1%,CEUS和CECT/CEMRI均为96.8%,与常规超声相比,差异有统计学意义。
肝癌局部消融术后的肿瘤灭活的彻底性单靠常规超声难于明确诊断,既往彻底性的判断主要是根据CECT/CEMRI。本组19个病灶CEUS提示病灶灭活彻底,结果与CECT/CEMRI一致。经临床密切随访6~12个月,常规超声和CT/MRI均未发现相应肿瘤的增大或肿瘤内血流信号等复发迹象。1个病灶CEUS及CECT提示可疑活性,但经临床密切随访12个月以上未见残留复发,证实完全灭活。11个病灶CEUS提示仍有部分存活组织,CECT亦做出同样的判断,其中10个再次行介入治疗,均以CEUS的影像作为指导针对存活组织进行消融治疗。经过平均2.3次治疗,均获得完全灭活肿瘤细胞。另1例由于患者肝功能较差而未继续治疗,此例随访中出现肿瘤增大,即证实肿瘤未彻底灭活。
总之,CEUS以其简便、无创、安全、无放射性、可重复性好的优点,在肝肿瘤消融治疗中的应用价值正日益受到重视;对消融治疗过程中的每一步都具有显著的促进作用,有助于取得最佳的治疗效果,有着良好的应用前景。
[1]陈敏华,杨薇.超声造影对射频消融治疗肝癌的应用价值[J].中华医学超声杂志(电子版),2010,7(12):2004-2007.
[2]罗葆明,智慧,文艳玲,等.低机械指数谐波超声造影在局灶性肝病治疗适应证选择中的作用[J].中国临床医学影像杂志,2006,17(9):512-514.
[3]Livraghi T,Goldberg SN,Lazzaroni S,et al.Hepatocellular carcinoma:radio-frequency ablation of medium and large lesions[J].Radiology,2000,214(3):761-768..
[4]陈敏华.重视影像指导规范化射频消融提高肝癌疗效[J].中华医学杂志,2007,87(20):1377-1379.
[5]Tateishi R,Shiina S,Teratani T,et al.Percutaneous radiofrequency ablation for hepatocellular carcinoma.Ananalysis of 1000 cases[J].Cancer,2005,15,103(6):1201-1209.
[6]曾燕荣,陈敏华,严昆,等.超声造影界定肝癌浸润范围的应用价值[J].中华医学杂志,2006,86(46):3294-3298.
