通经补肾复方对铝诱导阿尔茨海默病模型大鼠海马乙酰胆碱酯酶、胆碱乙酰转移酶、乙酰胆碱的影响
2012-08-02程书珍王丽君王晓梅刘爱民骆朋好河北工程大学医学院河北邯郸05600
程书珍 王丽君 刘 恒 王晓梅 刘爱民 骆朋好 (河北工程大学医学院,河北 邯郸 05600)
Tomimoto等〔1〕研究表明,痴呆的首发症状是记忆障碍,中枢胆碱功能损伤对记忆功能的影响有重要意义。在对阿尔茨海默病(AD)的诸多研究中,胆碱能神经系统退行性改变的发病机制已被多数学者接受,但铝对AD模型大鼠胆碱能系统的影响报道较少。鉴于此,采用铝饲料喂饲大鼠制备AD动物模型,观察了铝摄入对大鼠海马组织中乙酰胆碱酯酶(AchE)和胆碱乙酰转移酶(ChAT)活性及乙酰胆碱(Ach)含量的影响,并研究了通经补肾中药复方对AD模型大鼠海马胆碱能神经系统的保护作用。
1 材料与方法
1.1 主要试剂和仪器 AlC13·6H2O,分析纯,天津双船化学试剂厂;ChAT和AChE测定试剂盒,由南京建成生物工程研究所提供。大鼠乙酰胆碱ELISA试剂盒(美国Sigma);中药复方(通经补肾复方)由淫羊藿、熟地、黄芪、水蛭等组成,由河北省石家庄医药公司提供,生药经河北医科大学药学院生药教研室鉴定均为纯品。中药经浸泡、文火煎熬,每毫升生药含量为2.7 g,4℃冰箱保存,用前进行巴氏消毒。其他试剂均为国产,分析纯。UV-250型紫外可见分光光度计(日本岛津公司)。电子天平(上海精天电子仪器有限公司产品),TGL-16G台式高速离心机(上海安亭科技仪器厂)。
1.2 动物分组与处理 选用北京医科大学实验动物中心购得的体重(350±20)g健康清洁级3月龄 SD大鼠84只(合格证号SCXK-00-0004)。采用普通饲料适应性饲养1 w后,按体重随机分为7组,每组12只,其中对照组喂普通饲养,模型组及3个中药组在普通饲料的基础上,按体重8%的进食量添加A1C13·6H2O,剂量分别为:11.2、55.9、111.9 mg/kg 体重,喂饲铝饲料当天起,3个中药组用中药煎剂灌胃,剂量分别为:10.8、21.6,30.4 g·kg-1·d-1,各模型组、对照组大鼠每天灌服等量温开水。动物自由饮水,动物房温度(20±2)℃。
1.3 ChAT及AchE的活性、Ach的水平测定 上述实验到第90天时,大鼠禁食24 h,断头处死,快速取出全脑,置于冰盒上,分离海马并称重。按照重量和体积比1∶10的比例,加入生理盐水冰浴匀浆,4℃离心(3 000 r/min,10 min),取上清液,立即测定。紫外可见分光光度法测定海马ChAT、AchE活性,其中蛋白测定采用考马斯亮蓝法,所有操作按试剂盒说明书进行。最后用紫外可见分光光度计测定各管吸光度,计算ChAT及AchE的活性。双抗体夹心法ELISA法测定海马Ach的水平。用纯化的大鼠ACh抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入ACh再与HRP标记的ACh抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的大鼠Ach含量呈正比。通过标准曲线计算样品中ACh浓度。
1.4 统计学分析 采用SPSS13.0统计软件,计量资料用±s表示,成组设计的两样本均数比较的t检验。
2 结果
2.1 各剂量铝饲料组大鼠海马ChAT、AchE的活性及Ach的水平 见表1,与对照组比较,中、高剂量铝饲料组大鼠海马中AchE的活性明显增高(P<0.01),ChAT活性明显降低(P<0.01),Ach含量显著减少(P<0.01)。低剂量铝饲料组与对照组比较,均无统计学意义(P>0.05)。
2.2 各中药组大鼠海马ChAT、AchE的活性及Ach的水平
见表1,与高剂量铝饲料组比较,中、高剂量中药组大鼠海马中AchE活性显著降低(P<0.01),ChAT活性显著升高(P<0.01),Ach含量明显增加(P<0.01)。低剂量中药组与高剂量铝饲料组比较,均无统计学意义(P>0.05),但有改善趋势。
表1 各组大鼠海马ChAT、AchE的活性及Ach的水平(±s,n=12)
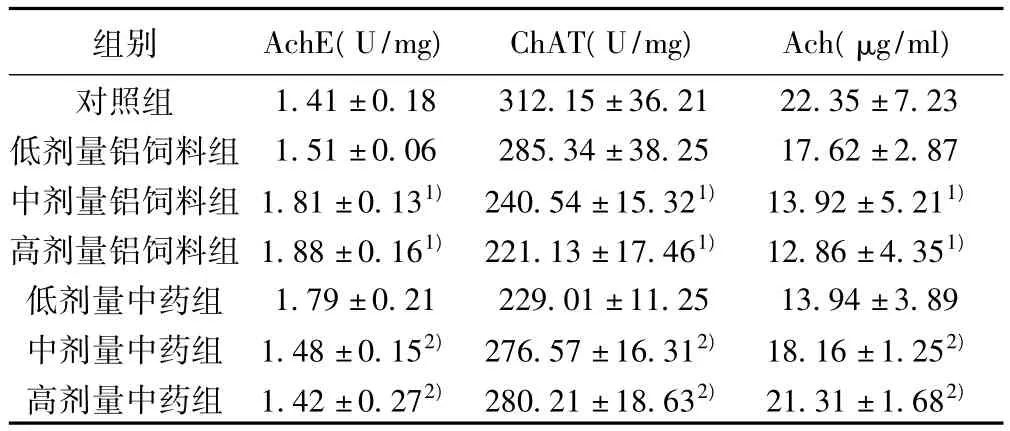
表1 各组大鼠海马ChAT、AchE的活性及Ach的水平(±s,n=12)
与对照组比较:1)P<0.01;与高剂量铝饲料组比较:2)P<0.01
组别 AchE(U/mg) ChAT(U/mg) Ach(μg/ml)对照组1.41±0.18 312.15±36.21 22.35±7.23低剂量铝饲料组 1.51±0.06 285.34±38.25 17.62±2.87中剂量铝饲料组 1.81±0.131) 240.54±15.321) 13.92±5.211)高剂量铝饲料组 1.88±0.161) 221.13±17.461) 12.86±4.351)低剂量中药组 1.79±0.21 229.01±11.25 13.94±3.89中剂量中药组 1.48±0.152) 276.57±16.312) 18.16±1.252)高剂量中药组 1.42±0.272) 280.21±18.632) 21.31±1.682)
3 讨论
AD病因及发病机制主要有微量元素学说、胆碱能递质途径异常学说、淀粉样蛋白神经毒性学说、细胞凋亡学说、基因突变学说、钙代谢紊乱学说、自由基损伤学说、雌激素缺乏学说等。研究表明,铝与AD关系密切,过量接触与体内蓄积可能是AD的病因之一〔2〕。
现代医学认为,调节学习记忆功能的机制是多方面的,其中中枢胆碱能系统是构成学习记忆的主要通路,与学习记忆关系密切,其核心是Ach,是促进学习记忆的重要神经递质,对中枢神经系统有兴奋和抑制双重作用,以兴奋为主,参与大脑皮层的唤醒、情绪和运动的协调等功能的调节,特别是对学习和认知等方面被认为是关键环节之一〔3〕。Ach广泛分布在脑内,由胆碱、乙酰辅酶A在ChAT的催化下合成,并由AchE分解,ChAT和AchE共同作用维持Ach含量的动态平衡,二者的活性反映了Ach在脑中的合成和代谢速率。AD患者脑内ChAT活性下降被认为是AD的一个标志性生化特征。Lopez等〔4,5〕多个研究报道显示,老年性痴呆患者Ach合成减少,ChAT的活性下降,且与痴呆的严重程密切相关。AchE作为胆碱能纤维的标志,其活性增高,Ach分解加速,影响学习记忆和认知能力〔6,7〕。本结果显示,铝的过多摄入使大鼠海马Ach减少可能是AD发病的机制之一。
AD多属于脾肾亏损、脾虚痰阻,常表现为面色晄白,气短乏力,可兼有头晕眼花、腰膝酸痛、心悸等症,表明体内气血不足,阴虚阳弱。淫羊藿,性辛、甘、温,温肾阳,有补肾强阳、调节免疫和分泌系统、改善机体代谢和各器官功能;黄芪味甘,气微温,具有补肺益气固表,补气补血,能补五脏诸虚;熟地,味甘,微温质润,既补血滋阴,又能补精益髓,通血脉,益气力。水蛭,活血逐瘀,通经,具有减轻脑组织炎症反应,改善局部血流循环,保护脑组织免遭坏死及促进神经功能的恢复等功效。根据扶正固本、通经补肾、益气养血的治则,由上述组分为主配方组成通经补肾复方防治铝诱导的AD大鼠,本结果表明该复方能明显提高大鼠海马中ChAT活性,抑制AchE活性,增加Ach的合成,显著改善AD大鼠胆碱能系统功能,证明复方对海马组织有一定的保护作用,为临床治疗AD提供了理论依据。
1 Tomimoto H,Ohtani R,Shibata M,et al.Loss of cholinergic pathways in vascular dementia of the Binswanger type〔J〕.Dement Geriatr Cogn Disord,2005;19(5-6):282-8.
2 Gonda Z,Lehotzdy K,Midlsi A.Neurotoxicity induced by prenatal aluminum exposure in rats〔J〕.Neurotoxicology,1996;17(2):459.
3 索国玲,洪 丽,王秀利.丹参对幼年大鼠癫痫持续状态学习记忆及海马ChAT、AChE活性的影响〔J〕.东南大学学报(医学版),2007;26(4):271-4.
4 Lopez OL,Hamilton RL,Becker JT,et al.Severity of cognitive payments and the clinical diagnosis of AD with Lewy〔J〕.Bodies Neurology,2000;54(9):1780-7.
5 Zhong CB,Xu XH,Wang XL.Advance in research on cholinergic theory of Alzheimer′s disease〔J〕.Chin Pharmacol Bull,2003;19(7):727-31.
6 Bartolucci C,Siotto M,Ghidini E,et al.Structural determinants of Tor-pedo Californian acetyl cholinesterase inhibition by the novel and orally active carbonate based anti-Alzheimer drug ganstigmine(CHF-2819)〔J〕.J Med Chem,2006;49(17):5051-8.
7 Gil-Bea FJ,García-Alloza M,Domínguez J,et al.Evaluation of cholinergic markers in Alzheimer′s disease and in a model of cholinergic deficit〔J〕.Neurosci Lett,2005;375(1):37.
