开郁宁片溶出度研究及方法学考察
2012-07-25黄志军朱立彬李崇明
黄志军, 朱立彬, 翟 莉, 李崇明
(湖北省暨武汉市中药现代化工程技术研究中心,湖北武汉430052)
开郁宁片是中药5类制剂,处方由贯叶金丝桃总黄酮[1]加适宜辅料制成。本品为抗抑郁药,用于治疗轻、中度抑郁症。目前临床试用的抗抑郁症药主要为化学药,这些化学药虽然有较明显的疗效,但往往有明显的副作用,一般不能长期服用,而中药目前尚无上市的抗抑郁药。贯叶金丝桃在欧洲作为民间草药用于治疗创伤和抗抑郁药物已有较长历史[2],Linde等[3]报道,治疗轻度和中度抑郁症患者时,含有金丝桃素类成分的贯叶金丝桃提取物效果明显优于安慰剂,与标准抗抑郁药物 (三环类)相比,疗效相同而副作用小。溶出度测定是利用体外试验方法对药物在体内生物利用度进行研究和评价的有效的评价方法,是今后口服固体制剂的研究方向[12],文献对中药溶出度的报道较少,本实验以总黄酮为指标,对开郁宁片进行了溶出度试验的研究。
1 仪器与试剂
ZRS-8G智能溶出试验仪 (天津市天大天发科技有限公司);Agilent 8453紫外-可见分光光度计;芦丁对照品 (供定量测定用,批号:10080-200306,购自中国药品生物制品检定所);开郁宁片 (武汉健民药业集团股份有限公司提供);试剂均为分析纯。
2 溶出度检查中总黄酮的测定方法[4-5]
2.1 对照品溶液的制备 取芦丁对照品25 mg,精密称定,置50 mL棕色量瓶中,加乙醇适量,超声处理使溶解,放冷,加乙醇至刻度,摇匀。精密吸取20 mL,置50 mL棕色量瓶中,加水至刻度,摇匀,即得 (每1 mL含芦丁0.20 mg)。
2.2 标准曲线的制备 精密量取上述对照品溶液1.0、2.0、3.0、4.0、5.0、6.0 mL,分别置25 mL量瓶中,各加水至6.0 mL,加5%亚硝酸钠溶液1 mL,摇匀,放置6 min,加10%硝酸铝溶液1 mL,混匀,放置6 min,加1 mol/L氢氧化钠试液10 mL,再加水至刻度,摇匀,放置15 min,以相应的试剂为空白,照紫外-可见分光光度法(《中国药典》2010年版一部附录ⅤA),在500 nm波长处测定吸收值,以吸光度为纵坐标,质量浓度为横坐标,绘制标准曲线。
2.3 测定法 取本品,照溶出度测定法(《中国药典》2010年版二部附录XC溶出度测定法第二法),以2%聚山梨酯80溶液600 mL为溶出介质,转速为100 r/min,依法操作。经60 min,取溶液15 mL,滤过,精密量取续滤液5 mL,置25 mL量瓶中,照标准曲线制备项下的方法,自“加水至6.0 mL”起,依法测定吸光度,得吸光度A1,再精密量取续滤液5 mL,以1 mL水代替10%硝酸铝,按上述方法制备供试品溶液,依法测定吸光度,得吸光度A2。按下式计算供试品溶液得吸光度A,从标准曲线上读出供试品溶液中芦丁的质量浓度,计算每片的溶出量,限度为含有量的70%,应符合规定。
供试品溶液的吸光度A=A1-A2
3 溶出度的测定方法及其方法学研究
3.1 溶出度测定方法 中药制剂大多采用浆法[6-7],经试验,本品如采用转篮法,药片会黏在篮上,对溶出有较大影响,故本品的溶出度测定亦采用桨法。具体测定方法见2.3项。
3.2 溶出介质的选择 参照2010年版《中国药典》二部,分别选择水、9‰盐酸溶液、磷酸盐缓冲液 (pH6.8)[8]346、5%乙醇、10%乙醇、磷酸盐缓冲液 (pH7.8~8.0)0.2%十二烷基硫酸钠溶液作为溶出介质[8]259,343,皆不能得到满意的溶出度结果。经咨询有关专家,采用聚山梨酯80溶液作为考察溶剂。
对0.5%聚山梨酯80溶液、1.0%聚山梨酯80溶液、1.5%聚山梨酯80溶液、2%聚山梨酯80溶液、2.5%聚山梨酯80溶液分别进行了考察,通过考察,选择2%聚山梨酯80溶液作为溶出介质。
3.3 溶出介质对样品显色后的吸收波长的影响 取本品,以2%聚山梨酯80溶液600 mL为溶出介质,制备供试品溶液并显色 (溶液①);然后以水为溶剂 (溶液②),采用超声法制备供试品溶液并显色,比较这两种溶液在可见光区的吸收曲线,见图1、图2,由曲线可知以2%聚山梨酯80溶液作为溶出介质对本品吸收无干扰。
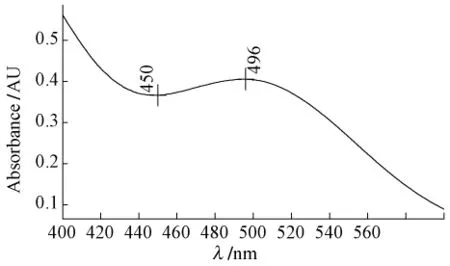
图1 溶液①可见光区吸收曲线
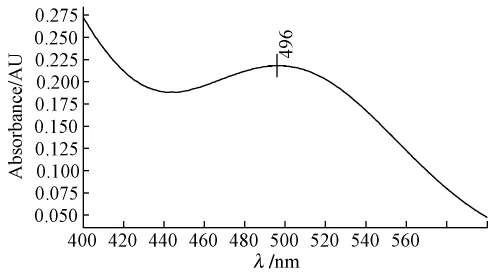
图2 溶液②可见光区吸收曲线
3.4 转速的考察 取本品,以2%聚山梨酯80溶液600 mL为溶出介质,分别以 50 r/min,100 r/min,150 r/min进行试验,经60 min时取样,对同一批样品 (批号:20070601)进行测定。结果表明样品在100 r/min的溶出良好。
3.5 线性关系试验 按照2.1项制备对照品溶液(0.2013 mg/mL),精密量取上述对照品溶液1、2、3、4、5、6mL,分别置25 mL量瓶中,各加水至6.0 mL,加5%亚硝酸钠溶液1 mL,混匀,放置6 min,加10%硝酸铝溶液1 mL,摇匀,放置6 min,加1 mol/L氢氧化钠试液10 mL,再加水至刻度,摇匀,放置15 min,以相应的试剂为空白,照紫外-可见分光光度法(《中国药典》2010年版一部附录ⅤA),在500 nm波长处测定吸光度,以吸光度为纵坐标,质量浓度为横坐标,得回归方程Y=12.835X-0.0082,r=0.9998,说明以本法测定总黄酮含有量,总黄酮质量浓度在8.052~48.312 μg/mL之内,吸光度与质量浓度线性关系良好。
3.6 溶出曲线的测定 取本品 (批号:20070601),以2%聚山梨酯80溶液为溶出介质,转速100 r/min,按上述溶出度检查方法试验,分别在 15、30、45、60、75、90 min时取溶液适量 (每次取样后立即补足溶出介质),测定总黄酮的含有量,以各时间点的溶出量对时间绘制曲线,溶出曲线见图3。根据结果综合分析,本品的取样时间为60 min时较为合适。
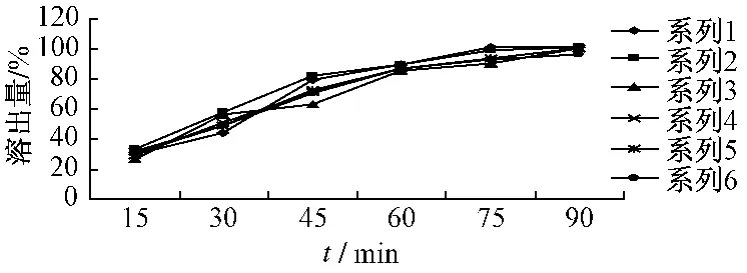
图3 溶出曲线
3.7 专属性试验 取开郁宁片阴性对照品,照上述方法测定,计算每片的溶出量,结果吸收值几乎为零,说明样品中其它成分和溶出介质不影响本品的溶出度测定。
3.8 回收率试验 取开郁宁片阴性对照品6片,照溶出度测定的方法操作,所得阴性对照溶液待用。另取芦丁对照品适量,精密称定,置50 mL量瓶中,加阴性对照溶液适量,超声处理使溶解,放冷,加阴性对照溶液至刻度,摇匀。分别精密量取3、3.5、4 mL,置25 mL量瓶中,依法测定含有量,计算回收率。每个质量浓度平行试验3次,结果见表1,平均回收率为97.12%,RSD为1.33%。由结果可见,采用本方法进行溶出度检查,回收率良好。
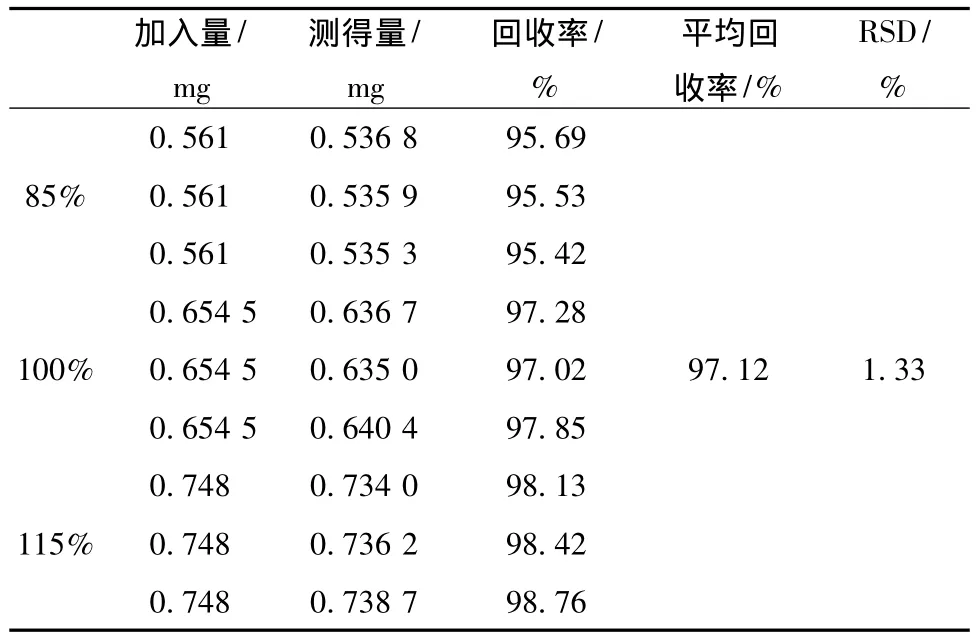
表1 回收率试验结果
3.9 精密度试验 照溶出度检查方法制备溶出溶液,对同一溶出杯内溶出溶液制备6份供试品溶液,依法测定,计算溶出量,由试验结果 (见表2)可见,本试验精密度较好。

表2 精密度试验结果
3.10 溶液稳定性试验 取溶出度测定项下的对照品溶液与供试品溶液于室温下放置,分别于 0、10、20、30、40 min时测定其吸光度,由试验结果可见,本品溶出溶液显色后在室温下避光放置40 min,溶液基本稳定。
4 样品溶出度检查及溶出度限度的制定
用上述所建立的溶出度测定方法对3批样品进行测定,结果均符合规定。结果见表3。
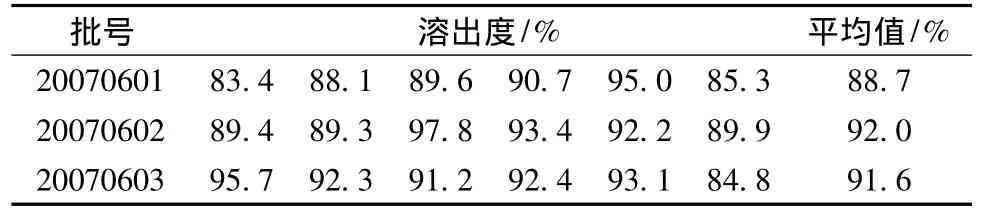
表3 样品溶出度测定结果
根据中试3批样品溶出度测定结果,结合中药的实际情况,暂定本品总黄酮的溶出度限度为70%。
5 讨论
5.1 中药溶出度的研究尚处于摸索阶段,主要由于中药成分复杂,有效成分不明确,有效成分和无效成分之间互相干扰,使药物的溶出不规律。溶出介质的选择必须以接近消化道内体液环境为原则,消化道内体液环境通常采用以下几种溶出介质来涵盖[9]:(1)pH值1~3的盐酸溶液;(2)不同浓度的醋酸盐或磷酸盐缓冲溶液;(3)水。而中药制剂 (有效成分为碱性的除外),很难在接近消化道内体液的环境中得到合理的溶出量,这时可以考虑加入一定量的表面活性剂来改善溶出,主要依据是人体内胃肠道表面存在一定浓度的天然表面活性剂。
5.2 口服固体制剂的核心就是生物利用度,评价生物利用度最直接的手段是直接抽取人体血样,测定血药浓度,实际生活研究中很难实现,而溶出度试验已成为证明药物体内释放特性的一种简单、廉价而不失严谨的实验室检测方法。中药成分复杂,与西药纯度较高的单体成分不同,溶出机制复杂,其他成分对主要有效成分的溶出有较大的影响。而溶出度是反映药品质量的关键指标,随着我国医药事业的发展,溶出度的研究必定会越来越深入,甚至有专家[10]提出“多条溶出曲线就是一个固体制剂的指纹图谱”!由此观之,中药未来的溶出度研究“任重而道远”!另外本文成文时还参考了相关文献 [11-14]。
[1]韩妮娜.5类中药新药开郁宁片的制备工艺及质量标准研究[D].武汉:湖北中医学院,2007.
[2]施正福,范 焱.贯叶金丝桃的药理作用研究进展[J].中国现代应用药学杂志,2000,17(3):190.
[3]Linde K,Ramirez G,Mulrow D,et al.St John's Wort for depression-an overview and meta-analysis of randomized clinical trials[J].BMJ,1996,313(7052):253.
[4]籍学伟,郝美玲.UV法测定悬钩子木中总黄酮含量[C] //2010年中国药学大会暨第十届中国药师周论文集.北京,2010:7663-7666.
[5]曾 彬,易进海.左金分散片的溶出度测定[J].华西药学杂志,2006,21(2):190-191.
[6]卫莹芳,闫 婕,王化东,等.赤小豆总黄酮UV-VIS分析方法建立及全国不同产地药材含量测定[C] //中华中医药学会第十届中药鉴定学术会议暨WHO中药材鉴定方法和技术研讨会论文集.北京,2010:378-384.
[7]王晓辉.药物溶出度的测定方法及其研究进展[J].天津药学,2006,18(2):68-71.
[8]国家药典委员会.中华人民共和国药典:2010年版二部[S].北京:中国医药科技出版社,2010.
[9]韦广辉.常用中药固体制剂溶出度的研究概况[J].中国现代药物应用,2011,5(3):228-229.
[10]谢沐风.如何科学、客观的评价口服固体制剂的内在品质—纵论我国固体制剂仿制药质量[J].药品评价,2010,7(14):19-23.
[11]贾存勤.药用大孔吸附树脂及其在中药分离纯化方面的应用[D].兰州:甘肃农业大学,2003.
[12]秦文杰.短柱肖菝葜化学成分及质量控制研究[D].北京:北京中医药大学,2007.
[13]刘承萍.野菊花成分稳定性与药材质量研究[D].广州:广州中医药大学,2011.
[14]陈亚强,杨爱淑,李文春.高效液相法测定刺五加脑灵液中五味子醇甲的含量[J].民营科技,2011,(3):98-100.
