超声辅助萃取-高效液相色谱荧光检测法测定贻贝中的多环芳烃
2012-07-12陈雪昌孙秀梅胡红美郭远明梅光明
陈雪昌,孙秀梅,胡红美,陈 朋,郭远明,梅光明
(浙江海洋学院海洋与渔业研究所,浙江省海洋水产研究所,浙江省海水增养殖重点实验室,浙江舟山 316100)
多环芳烃(Polycyclic Aromatic Hydrocarbons,PAHs)是一种持久的环境和食品有毒污染物,广泛分布于土壤、水体、空气、食品以及一些日常用品中。其在环境中虽含量不高,由于难以通过生物降解消除,会经过过食物链逐步富集浓缩会逐渐达到相当高的含量。因此,寻找一种简单、快速、高灵敏的多环芳烃的分离分析技术具有重要的意义。
目前,多环芳烃主要采用高效液相色谱法(HPLC)[1-2]、高效液相色谱质谱法(HPLC-MS)[3],气相色谱法(GC)[4-5]、气相色谱-质谱法(GC-MS)[6]、毛细管电泳分析法(CE)[7]、薄层扫描法[8]、超临界流体色谱法(SFC)[9]以及荧光光度法[10],分析检测。分析对象多为大气,水体,沉积物,鱼、虾等水产品。
贻贝作为人类的食物,又是海洋食物链的一环,有国际贻贝监测报告[11]认为,用贻贝作为近海污染指示物,比选择像海藻、鱼类或海水更具有代表性和价值。本文以贻贝为研究对象,建立了超声辅助萃取-高效液相色谱荧光检测法测定贻贝中的多环芳烃的方法。
1 材料与方法
1.1 材料
紫贻贝Mytilus edulis:新鲜,购自舟山市普陀东河市场。
1.2 主要试剂
环己烷、二氯甲烷(农残级,美国J T Baker公司);甲醇、乙腈(色谱纯,德国Merck公司);氢氧化钾(优级纯,中国医药集团上海化学试剂公司);无水硫酸钠(分析纯,上海化学试剂总厂),使用前650℃烘干4 h;硫酸(优级纯,国药集团化学试剂有限公司);多环芳烃混合标准储备液:分别称取一定量的荧蒽、苯并[b]荧蒽、苯并[k]荧蒽、苯并[a]芘,苯并[g,h,i]芘和茚并[1,2,3-cd]芘标准品(中国计量科学研究院),用丙酮定容至10 mL,配置成10 mg/L混合标准储备溶液,4℃避光保存,使用时用流动相逐级稀释至所需浓度。
1.3 主要仪器与设备
Waters Alliance高效液相色谱仪(美国Waters公司),配2695荧光检测器;高速离心机(德国Eppendorf公司);涡旋混合器(德国Ika公司);旋转蒸发仪(瑞士Buchi公司);Florisil固相萃取柱(250 mg,3 mL,德国CNW Technologies GmbH公司)。
1.4 实验方法
1.4.1 样品制备
将紫贻贝用海水洗净泥沙,滤干水分。用小刀剥开外壳,取出整个贻贝。称取约250 g置于高速组织捣碎机中制成匀浆。
1.4.2 样品提取
准确称取5.00 g试样,置于50 mL聚四氟乙烯管中,加入25 mL甲醇和10 mL 50%的氢氧化钾溶液,超声萃取1 h(30℃)后,6 000 r/min离心5 min,提取上清液于另一50 mL聚四氟乙烯管中,加入10 mL环己烷,超声10 min(30℃),2 000 r/min涡旋2 min,6 000 r/min离心5 min,吸取上层环己烷于125 mL分液漏斗中,下层液体再用10 mL环己烷重复萃取2次,合并环己烷层。
环己烷萃取液依次用10 mL 50%甲醇/水溶液、5 mL水、5 mL水和1 mL 60%硫酸溶液重复振摇,静置分层,弃去下层液体,并用30 g/L硫酸钠水溶液洗环己烷层至中性,以达到清洗萃取液目的,将环己烷层经无水硫酸钠脱水后转移至100 mL梨形瓶中,在40℃水浴中旋转蒸发(35 r/min,152 mbar),浓缩至1~2 mL即可。
1.4.3 样品净化
依次用3 mL二氯甲烷、5 mL环己烷活化Florisil固相萃取柱。将浓缩后的提取液转移至柱子中,并依次用1 mL、2 mL环己烷清洗梨形瓶,全部转移至柱子中;用9 mL环己烷-二氯甲烷溶液(3:1,v/v)洗脱,收集于100 mL梨形瓶中,40℃水浴中旋转蒸发(35 r/min,152 mbar)至干。准确加入2 mL乙腈,充分溶解后,用0.22 μm微孔滤膜过滤,供高效液相色谱仪测定。
1.4.4 色谱工作条件
色谱柱:Supelcosiltm LC-PAH 柱(250 mm×4.6 mm×5.0 μm);流动相:乙腈-水(65:35,v/v);流速:1 mL/min;柱温:30℃;进样量:20 μL;以保留时间定性,外标法-峰面积定量。
2 结果与讨论
2.1 检测条件的选择
多环芳烃常用的检测器有紫外、荧光、化学发光等方法,通常紫外检测法灵敏度较低,而化学发光检测法虽然无需光源、背景噪音低,检测灵敏度高,但需要引入化学发光反应。本研究选择操作简单,灵敏度高的荧光检测法。根据各化合物保留时间、最大吸收波长设定相应的荧光条件。苯并[b]荧蒽和苯并[k]荧蒽性质相近,选择同一荧光条件。各多环芳烃的荧光检测程序见表1。

表1 6种多环芳烃的荧光检测程序Tab.1 Fluorescence detection program for six PAHs
2.2 色谱分离条件
为了获得满意的分离度,对流动相、柱温、流速等因素进行了考察,得到的优化结果见1.4.4。优化条件下,6种多环芳烃标准品色谱图如图1。结果表明,该条件下,6种多环芳烃实现了很好的分离。

图1 6种多环芳烃(10 μg/L)标准品色谱图Fig.1 Chromatogram of 6 kinds of PAHs standard
2.3 萃取方式的选择
本试验选择超声波辅助萃取法,操作简单,萃取效率高。首先,试样中加入皂化剂超声处理,有效的除去脂类物质的干扰。接着加入环己烷对皂化后的上清液超声萃取,使亲脂性的多环芳烃转移进入环己烷层。
2.4 提取液净化
试样经造化萃取后,还残留痕量的脂肪族化合物和一些极性较强的组分,需要进一步净化。采用甲醇-水体系能有效去除正己烷层中脂肪组织水解的脂蛋白。60%硫酸溶液可以有效地净化生物样品中脂肪和其他杂质。
比较了C18和Florisil柱的净化效果,确定选择对分离脂肪族和芳香族化合物效果较好的Florisil柱为固相萃取柱。
2.5 工作曲线和检出限
用流动相稀释多环芳烃混合标准储备液,得到0.002~0.5 mg/L混合标准工作溶液,按照色谱工作条件进行检测。结果表明,6种多环芳烃在0.002~0.5 mg/L范围内呈线性关系,工作曲线、相关系数及检出限见表2。

表2 方法线性回归方程和检出限Tab.2 The linear regression equations and determination limits of the proposed method
2.6 回收率和精密度试验
采用标准加入法对待测试样进行加标回收率和精密度试验,以考察方法的准确性和重现性。对市售的紫贻贝,进行样品制备后,分别加入高(500 μg/kg)、中(100 μg/kg)、低(10.0 μg/kg)3 种浓度水平混合标准溶液,平行测定6次,实验结果见表3。结果表明,3个加标浓度下,回收率为78%~92%,相对标准偏差为2.8%~6.3%,满足分析检测要求。
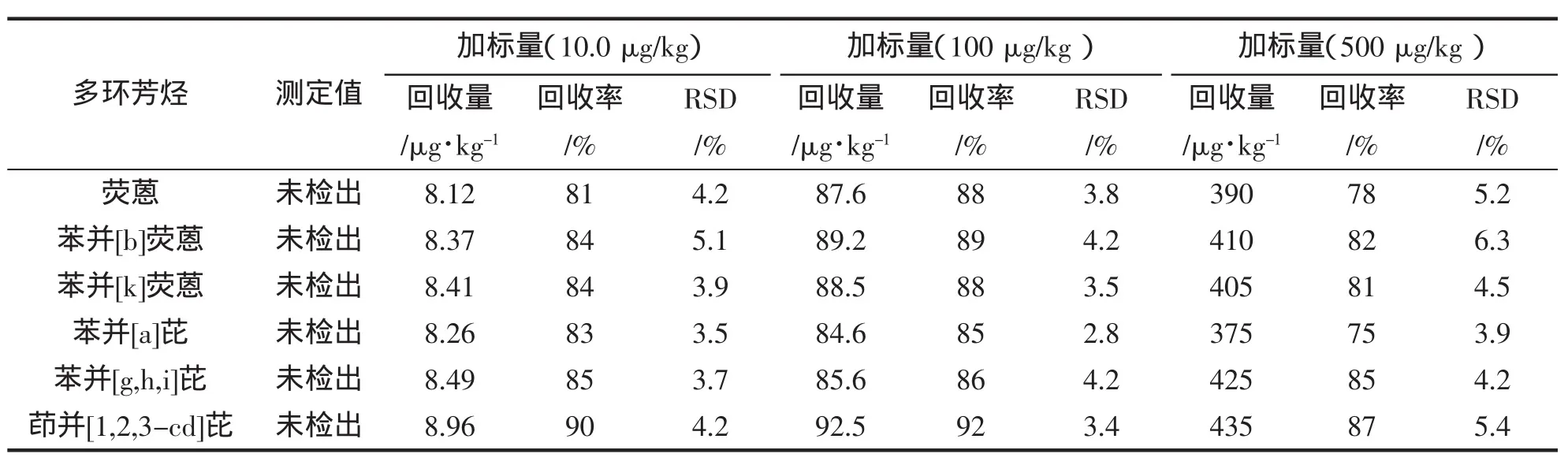
表3 方法的回收率和精密度试验结果(n=6)Tab.3 Result of test of recovery and precision of the proposed method(n=6)
3 结论
本工作建立了超声波辅助萃取-高效液相色谱荧光检测法测定紫贻贝中6种多环芳烃的方法。方法灵敏,超声萃取简单,重现性好,准确度高,实验结果令人满意,可以适用于贻贝中多环芳烃的检测,并有望应用于其他水产品中多环芳烃的检测。
[1]饶 竹,李 松,何 淼,等.高效液相色谱-荧光-紫外串联测定土壤中16种多环芳烃[J].分析化学,2007,35:954-958.
[2]李先国,阎国芳,周 晓,等.固相萃取-高效液相色谱-荧光检测法测定海水中的多环芳烃[J].中国海洋大学学报,2009,30(5):1 087-1 092.
[3]赵恒强,陈军辉,程红艳,等.高效液相色谱-电喷雾银离子诱导电离飞行时间质谱定性分析高沸点多环芳烃[J].分析化学,2010,38:1 599-1 603.
[4]徐 媛,刘文民,赵景红,等.固相萃取搅拌棒萃取-气相色谱分析海水中的多环芳烃[J].分析化学,2005,33:1 401-1 404.
[5]张廉奉,李秀娟,刘翠霞,等.三甲基杯[6]芳烃固相微萃取-气相色谱法测定土壤中的多氯联苯[J].分析化学,2007,35:1 269-1 273.
[6]李晓敏,张庆华,王 璞,等.搅拌子固相吸附-热脱附-气相色谱/质谱/质谱法快速测定空气中多环芳烃[J].分析化学,2011,39:1 641-1 646.
[7]宋冠群,林金明.多环芳烃的浊点萃取毛细管电泳分析[C]//第二届全国环境化学学术报告会论文集.2004.
[8]厉曙光.薄层扫描法测定食物油及其加热产物中多环芳烃的研究[D].南京:南京铁道学院,1989.
[9]孙云鹏.多环芳烃的超临界流体色谱分离研究[J].色谱,1995,13(5):398-399.
[10]於立军,李耀群,睦 蔚.多环芳烃的Shpol’skii低温荧光光谱分析[J].光谱学与光谱分析,2002,22(5):819-821.
[11]The international mussel watch report of a workshop sponsored by the environmental studies board commission on natural resources national research council[C].Washington D C:National Academy of Science,1980.
