锂离子电池正极材料尖晶石型LiMn2O4的制备及电化学性能研究
2012-06-25朱希平
朱希平
(深圳市欧赛科技有限公司,广东深圳 518109)
锂离子电池具有工作电压高、比能量大、自放电率小、循环寿命长、无记忆效应、绿色环保等优点,在便携式电子产品方面得到了广泛的应用,同时也是动力电池的首选产品。目前锂离子电池正极使用的材料主要是钴酸锂(LiCoO2),但是由于Co 资源缺乏,导致LiCoO2价格昂贵;另外,钴元素有毒,这些缺陷限制了其更大规模的应用。而作为锂离子电池正极材料的尖晶石型锰酸锂(LiMn2O4)具有无毒、能量密度高、制备简单、锰来源广泛、成本低等优势,被认为是最具有应用前景的锂离子电池正极材料之一,尤其在动力电池上的应用,因而尖晶石型LiMn2O4已经被研究者广泛的研究[1-5]。
目前已有各种各样的方法来制备尖晶石型LiMn2O4,如高温固相法[6-10]、固相配位法[11]、微波法[12]、熔融盐法[13]、燃烧法[14]、溶胶-凝胶法[15-18]、水热法[19]等。制备方法众多,但不易制出电化学性能优异的材料。其中,溶胶-凝胶法可以使原料达到原子级水平的混合,高温烧结时离子所需扩散路径短,可以在较低的温度下得到所需的材料,而且得到的物相纯度高、均匀性好、比表面积大,因此用此种方法制备的尖晶石型LiMn2O4放电比容量较高,循环性能较好。但绝大多数文献报道的用溶胶-凝胶方法合成这种材料时采用的是柠檬酸等单一络合剂。
本文采用复合有机物作为络合剂合成尖晶石型LiMn2O4,特别是基于复合络合剂柠檬酸和β-环糊精的溶胶凝胶法制备尖晶石型LiMn2O4的报道还没有,本研究采用基于复合络合剂的溶胶凝胶法制备了电化学性能良好的尖晶石型LiMn2O4正极材料。
1 实验部分
1.1 主要试剂
二水合乙酸锂,四水合乙酸锰,柠檬酸,β-环糊精,氨水,均为分析纯;实验用水为去离子水。
1.2 LiMn2 O4 粉末的制备
将化学计量比Li ∶Mn = 1∶2 的二水合乙酸锂和四水合乙酸锰在机械搅拌下溶于200 mL 去离子水,然后加入适量的β-环糊精,搅拌得到溶液A。将与β-环糊精的质量相当的柠檬酸溶于40 mL 去离子水中得到溶液B,剧烈搅拌下将溶液B 滴加到溶液A 中。滴加完毕,用氨水调节溶液pH 值为7。接着将溶液转移到80℃的水浴中加热搅拌使溶液转变为溶胶,将水蒸发得到凝胶。将凝胶置于真空干燥箱中于120℃干燥12 h 得到干凝胶。干凝胶置于马弗炉中于350℃预烧6 h,650℃-750℃煅烧12 h,研磨得到最终产品,所得三种样品分别标记为样T650、T700 和T750。
1.3 模拟电池的制作
集流体的预处理:将裁剪过的铝片分别用0.1 M 的氢氧化钠(NaOH)溶液和0.1 M 的草酸(H2C2O4)溶液超声波清洗10 min,120℃真空干燥2 h、称量待用。
将实验所得尖晶石型LiMn2O4粉末、乙炔黑、粘结剂(聚偏氟乙烯PVDF)按照85∶10∶5 的质量比与适量的N-甲基吡咯烷酮混合均匀得到浆料,并将其涂覆在预处理过的铝片上,120℃真空干燥12 h、压实、称量得到电极片。模拟电池的装配在充满高纯氩气的手套箱中进行,金属锂片为对电极和和参比电极,聚丙烯微孔膜(Celgard2320)为隔膜,1 M LiPF6的EC+DMC(体积比为1∶1,EC∶Ethylene carbonate,DMC∶Dimethyl carbonate)为电解液。具体的操作为:在负极电池壳上依次加上弹簧片、垫片、锂片、隔膜,在隔膜上滴加电解液,将涂有活性物质的电极片放在隔膜上,最后盖上正极电池壳封装。
1.4 模拟电池的测试
电池的充放电测试在力兴测试柜上进行,电压范围为3.5 ~4.3 V,电流大小采用不同的倍率(1C=148 mAh/g)。电池的循环伏安和交流阻抗测试在电化学工作站(Gamry Instrument model PCI 4-750)上进行,循环伏安测试的电势范围为3.5 ~4.3 V,扫描速率为0.1 mV/s;交流阻抗的测试频率范围为10 mHz ~100 kHz,交流信号幅度为5 mV。
2 结果与讨论
图1 是在不同煅烧温度下制备的三个样品(样T650、T700 和T750)在0.2 C 电流下的充放电曲线图。从图中可以看出在三个样品的充电曲线和放电曲线上分别有两个平台,这是尖晶石型LiMn2O4典型的电化学反应特征。其中,样T700 具有最长的充放电曲线,样T750 具有最短的充放电曲线。样T700的放电比容量为109 mAh/g,样T750 的放电比容量仅有100 mAh/g,样T650 的放电比容量居中为102.7 mAh/g。750℃煅烧制备的材料的放电比容量最低,这可能与温度过高,材料结晶度过高,材料颗粒急剧生长不利于材料的容量发挥有关;650℃制备的材料的容量较750℃的样稍高可能与温度较低材料颗粒较小有关,但是650℃的样的放电比容量又较700℃的样低,可能与温度低材料结晶不完善有关,所以用此种方法制备尖晶石型LiMn2O4的最佳温度为700℃。

图1 不同煅烧温度下制备的三种尖晶石型LiMn2 O4 样品(样T650、T700 和T750)在0.2 C 电流下的充放电曲线图(电压范围为3.5 ~4.3 V)
图2 为不同煅烧温度下制备的三种尖晶石型LiMn2O4样品(样T650、T700 和T750)在0.1 mV/s扫描速率下的循环伏安图,扫描电势范围为3.5 ~4.3 V。从图中可以看出每个样品都有两个氧化峰与相应的两个还原峰,这与样品充放电曲线上出现的两个充电平台和两个放电平台相对应。其中样T700的两个氧化峰分别位于4.03 V 和4.16 V,两个还原峰分别位于3.96 V 和4.09 V,相应的氧化峰和还原峰之间的电势差为0.07 V;样T750 的两个氧化峰分别位于4.06 V 和4.19 V,两个还原峰分别位于3.93 V 和4.06 V,相应的氧化和还原峰之间的电势差高达0.13 V,从中可知样T700 的电化学可逆性远远高于样T750。另外,样T700 的氧化还原峰比样T750 和T650 的尖锐,同时样T700 的氧化还原峰的峰面积比样T750 和T650 的大,表明样T700 的容量比样T750 和T650 的大,这和充放电的结果一致。
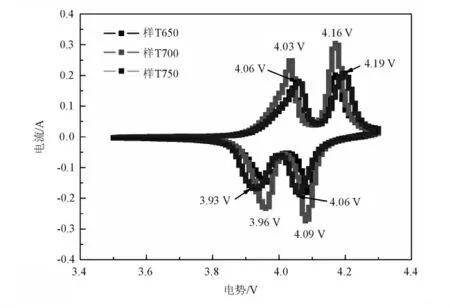
图2 为不同煅烧温度下制备的三种尖晶石型LiMn2 O4 样品(样T650、T700 和T750)在0.1 m V/s 扫描速率下的循环伏安图(扫描电势范围为3.5 ~4.3 V)
图3 为不同煅烧温度下制备的三种尖晶石型LiMn2O4样品(样T650、T700 和T750)在3 C 电流下的循环性能图。样T700 在3 C 电流下的首次和第200 次放电比容量分别为102 mAh/g 和90.8 mAh/g,容量保持率为89%,材料表现出良好的循环性能。样T650 在3 C 电流下最高放电比容量为100 mAh/g,200 次时仅为84.1 mAh/g。而样T750 在3 C 电流下的放电比容量仅有80 mAh/g 左右。样T700 的电化学性能最好,可能与温度适中,材料结晶完善,同时材料颗粒大小适中有利于锂离子的脱嵌有关。

图3 不同煅烧温度下制备的三种尖晶石型LiMn2 O 4 样品(样T650、T700 和T750)在3 C 电流下的循环性能图
图4(a)为不同煅烧温度下制备的三种尖晶石型LiMn2O4样品(样T650、T700 和T750)活化之后的交流阻抗图。三个样的交流阻抗谱图具有相似的特征,可分为三个部分:在高频区有一个非常微弱的小半圆,在中频处有一个较大的半圆,在低频处为一条斜线。锂离子在表面膜中迁移对应于高频区的半圆,锂离子在表面膜和活性物质的界面发生的电子交换对应于中频处的半圆,而锂离子在固相中的扩散与累积则与低频处的斜线有关。图4(b)是样T650、T700 和T750 交流阻抗图的模拟电路图。其中Re为电解质溶液阻抗,Rs为表面膜电阻,Rct为电荷转移阻抗,Cs为表面膜电容,Cd为双电层电容,Zw为Warburg 阻抗。其中样T700 的电荷转移阻抗最小,小的电荷转移阻抗有利于材料的电化学性能。
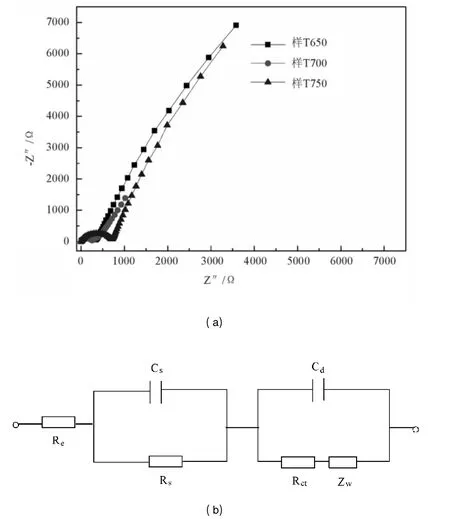
图4(a)不同煅烧温度下制备的三种尖晶石型LiMn2 O4 样品(样T650、T700 和T750)活化之后的交流阻抗图;(b)样T650、T700 和T750 交流阻抗图的模拟电路图
3 结语
用基于复合络合剂柠檬酸和β-环糊精的溶胶凝胶法在不同的煅烧温度下制备出尖晶石型LiMn2O4,其中在700℃煅烧制备的材料表现出良好的电化学可逆性,优异的倍率和循环性能,同时表现出小的电荷转移阻抗。所以采用此种方法制备尖晶石型LiMn2O4的最佳煅烧温度为700℃。
[1]Son J,Kim H. New investigation of fluorine-substituted spinel LiMn2O4-xFxby using sol-gel process[J]. J Power Sources,2005,147(1/2):220-226.
[2]Liu H,Cheng C,Hu Z,el al. The effect of ZnO coating on LiMn2O4cycle life in high temperature for lithium secondary batteries[J]. Mater Chem Phys,2007,101(2/3):276-279.
[3]Liu D,He Z,Liu X. Increased cycling stability of AlPO4-coated LiMn2O4for lithium ion batteries[J]. Mater Lett,2007,61(25):4703-4706.
[4]Yi T,Zhu Y,Zhu X,et al. A review of recent developments in the surface modification of LiMn2O4as cathode material of power lithium-ion battery[J]. Ionics,2009,15(6):779-784.
[5]Doh C,Lee J,Lee D,et al. The quantitative analyses of the dissolved manganese in the electrolyte of Li/LiMn2O4cell using by ion chromatography[J]. Bull Korean Chem Soc,2009,30(10):2429-2432.
[6]Fu Y,Su Y,Lin C,et al. Comparision of the microwave-induced combustion and solid-state reaction for the synthesis of LiMn2O4power and their electrochemical properties[J]. Ceram Int,2009,35(8):3463-3468.
[7]Avdeev G,Amarilla J,Rojo J,et al. Composition and structure of acid leached LiMn2-yTiyO4(0.2≤y≤1.5)spinels[J]. J Solid State Chem,2009,182(12):3226-3231.
[8]Preparation and performance comparision of LiMn2O3.95Br0.05and LiMn2O3.95Br0.05/SiO2cathode materials for lithium-ion battery[J]. J Solid State Electrochem,2011,15(4):725-730.
[9]Jung K,Kim H,Park Y. Effects of protecting layer[Li,La]TiO3on electrochemical properties of LiMn2O4for lithium batteries[J]. J Alloys Compd,2011,509(12):4426-4432.
[10]Yuan A,Tian L,Xu W,et al. Al-doped spinel LiAl0.1Mn1.9O4with improved high-rate cyclability in aqueous electrolyte[J]. J Power Sources,2010,195(15):5032-5038.
[11]Huang Y,Jiang R,Jia D,et al. Preparation,microstructure and electrochemical performance of nanoparticles LiMn2O3.9Br0.1[J]. Mater Lett,2011,65(23-24):3486-3488.
[12]Balaji S,Mutharasu D,Shanmugan S. Influence of Sm3+ion in structural,morphological,and electrochemical properties of LiMn2O4synthesized by microwave calcination[J]. Ionics,2010,16(4):351-360.
[13]Helan M,Berchmans L,Kumari V,et al. Molten salt synthesis of LiGd0.01Mn1.99O4using chloride-carbonate melt[J]. Mater Res Innovations,2011,15(2):130-134.
[14]Ragavendran K,Sherwood D,Vasudevan D,et al. On the observation of a huge lattice contraction and crystal habit modifications in LiMn2O4prepared by a fuel assisted solution combustion[J]. Physical B,2009,404(16):2166-2171.
[15]Tang W,Wang X,Hou Y,et al. Nano LiMn2O4as cathode material of high rate capability for lithium ion batteries[J]. J Power Sources,2012,198:308-311.
[16]Hwang J,Park S,Park C,et al. The sintering temperature effect on electrochemical properties of LiMn2O4[J]. Bull. Korean Chem Soc,2011,32(11):3952-3958.
[17]Qing C,Bai Y,Yang J,et al. Enhanced cycling stability of LiMn2O4cathode by amorphous FePO4coating[J]. Electrochim Acta,2011,56(19):6612-6618.
[18]Xu W,Yuan A,Tian L,et al. Improved high-rate cyclability of sol-gel derived Cr-doped spinel LiCryMn2-yO4in an aqueous electrolyte[J]. J Appl Electrochem,2011,41(4):453-460.
