两个海洋环肽Galaxamide类似物的合成及抗肿瘤活性研究
2012-05-07徐石海
陈 萌,曲 桐,徐石海
(暨南大学生命科学技术学院化学系,广东 广州 510632)
环肽类化合物是海洋生物次生代谢的产物,不仅具有多样及独特的化学结构,而且具有抗菌、抗病毒、抗癌、抗炎和免疫抑制等多种生物活性。Galaxamide是从中国南海西沙群岛的海藻中分离得到的一个新型环五肽环(亮氨酰-N-甲基亮氨酰-亮氨酰-N-甲基亮氨酰-亮氨酰),体外抗肿瘤实验表明该化合物对人体肾癌细胞(GRC-1)、人肝癌细胞(HepG2)有较好的细胞毒性(IC50分别为4.26 μg·mL-1、4.63 μg·mL-1)[1]。由于环肽的环状结构及其特殊的构象约束作用[2],与线性肽相比,稳定性更好,抗酶解能力更强。正是由于环肽独特的空间三维结构,其对于研究药物作用机理及开发新药都有着重要作用[3]。为了进一步探讨构效关系(SAR),作者在前人研究的基础上[4]采用经典的“3+2”全合成方法,同时改变原料亮氨酸构型和环肽的N-甲基的数量,设计合成了两个Galaxamide类似物(图1),对其结构进行了表征,并研究了其体外抗肿瘤活性。Galaxamide类似物的合成路线见图2。

图1 Galaxamide类似物的结构式

图2 Galaxamide类似物的合成路线
1 实验
1.1 试剂与仪器
试剂均为市售AR或CP,未进一步纯化。
1200型高效液相色谱仪,Agilent公司;4000 Q TRAP型质谱仪,美国应用生物系统公司;INOVA 500 MHz型核磁共振仪,美国Varian公司;R-210BUCHI型旋转蒸发仪,瑞士Buchi公司;柱层析硅胶(200~300 目),青岛海洋化工厂。
产物纯度由HPLC 检测分析。色谱条件:C18柱(4.6 mm×100 mm,220 nm),流动相70%~100% CH3OH/0.1% TFA,流速1 mL·min-1,梯度洗脱。
1.2 合成
1.2.1 Boc-Leu(a1)的合成
向250 mL的圆底烧瓶中连续加入THF(56 mL)、H2O(42 mL)和NaOH(1 mol·L-1,42 mL)溶液,冰浴冷却下一次性加入L-Leu(2.62 g,20 mmol),搅拌10 min使L-Leu溶解,然后一次性加入Boc2O(5.24 g,24 mmol),冰浴下继续搅拌10 min,然后缓慢升至室温并调pH值为10~11,搅拌过夜。减压蒸除溶剂后用无水乙醚(80 mL×2)萃取,水相在冰浴下冷却,用盐酸酸化至 pH值为2~3,然后用乙酸乙酯(80 mL×3)萃取,合并有机相并用饱和食盐水(80 mL)洗涤,无水硫酸钠干燥,过滤后蒸除溶剂,得到无色晶体 2.44 g,收率93%。MS(ESI),m/z:232.2[M+H]+,249.2[M+NH4]+,254.3[M+Na]+。
1.2.2 Boc-Leu-N-Me-D-Leu-OBn(a2)的合成

1.2.3N-Me-Leu-OBn(a3)的合成
氮气保护、冰浴冷却下,向250 mL的圆底烧瓶中一次性加入a1(2.31 g,10 mmol)和THF(30 mL),缓慢滴加碘甲烷(3.15 mL,15 mmol),反应30 min后,缓慢加入60%氢化钠(50 mmol,1.2 g)。冰水浴下反应1 h后,室温下反应过夜。冰水浴下,滴加饱和氯化铵水溶液(10 mL),再加饱和碳酸氢钠水溶液(20 mL),减压蒸去THF。水溶液用石油醚洗涤(25 mL×2)后,冰水浴冷却下,滴加1 mol·L-1的盐酸调节水溶液pH值至 2~3,用乙酸乙酯提取(50 mL×4)。合并有机相,依次用5%的硫代硫酸钠(75 mL)、饱和食盐水(75 mL)洗涤,无水硫酸钠干燥。过滤,浓缩,油泵干燥,得黄色油状物1.99 g,收率为87%。MS(ESI),m/z:246.2[M+H]+,263.2[M+NH4]+,268.3[M+Na]+。
1.2.4 Boc-Leu-N-Me-Leu-OBn(a4)的合成

1.2.5 Boc-Leu-N-Me-Leu-Leu-OBn(a5)的合成
取a4(8 mmol,3.59 g)溶于30 mL CH2Cl2中,氮气保护下加入苯甲醚(16 mmol,1.7 mL),冰浴下搅拌,缓慢滴加TFA(8 mL),反应4 h后,减压蒸除溶剂,再加入CH2Cl2,减压蒸除,重复操作除去TFA,干燥,得到油状物直接用于下一步实验。

1.2.6 五肽Boc-Leu-N-Me-Leu-Leu-Leu-N-Me-D-Leu-OBn(a6)的合成
取a2(1.94 mmol,1.0 g)溶于20 mL CH2Cl2中,氮气保护下加入苯甲醚(3.98 mmol,0.4 mL),冰浴下搅拌,缓慢滴加TFA(5 mL),反应4 h后,减压蒸除溶剂,再加入CH2Cl2,减压蒸除,重复操作除去TFA,干燥,得到油状物直接用于下一步实验。
向50 mL二口圆底烧瓶中加入a5(2.3 mmol,1.0 g)的甲醇溶液(20 mL),氮气保护下加入0.2 g 10% Pd/C,封口,搅拌下通入氢气,室温下反应,TLC跟踪,3 h后,原料点消失,停止通入氢气,过滤,回收Pd/C,减压蒸除溶剂,干燥,得到无色固体直接用于下一步实验。
将上步无色固体溶于5 mL THF中,置于冰水浴中搅拌,氮气保护下连续加入DEPBT(2.9 mmol,0.87 g)、DIEA(2.9 mmol,0.5 mL)反应5 min后,滴加溶于CH2Cl2(5 mL)的上述油状物,自然升至室温,TLC跟踪反应。24 h后反应完成,减压蒸除溶剂。直接进行硅胶柱层析(淋洗剂V正己烷∶V丙酮=20∶1),得无色固体1.27 g,三步收率82%。MS(ESI),m/z:803.1[M+H]+,820.1[M+NH4]+,825.1[M+Na]+。
1.2.7 环五肽c(Leu-N-Me-Leu-Leu-Leu-N-Me-D-Leu)(a7)的合成
取保护五肽(a6)(0.15 mmol,0.12 g)溶于20 mL甲醇中,通入氮气保护后加入0.2 g 10% Pd/C,通入氢气,室温下反应3 h。过滤回收Pd/C,滤液蒸干,干燥得产物,加入20 mL CH2Cl2溶解,冰浴搅拌下,加入5 mL TFA,冰浴下反应3 h,减压浓缩,再加CH2Cl2,减压浓缩,重复3次,再用油泵抽干得到产物,溶于25 mL THF-CH3CN-CH2Cl2(2∶2∶1),室温下连续加入2-(7-偶氮苯并三氮唑)-N,N,N′,N′-四甲基脲六氟磷酸酯(HATU,0.134 g)、DEPBT(0.130 g)和N,N,N′,N′-四甲基异脲四氟化硼(TBTU,0.14 g),每12 h LC-MS检测,连续反应3 d后,反应完全,减压抽干,用CH2Cl2溶解后,依次用饱和碳酸氢钠溶液、水洗涤,无水硫酸钠干燥,浓缩,用反相HPLC分离得到环五肽白色固体(a7)37.9 mg,收率42.5%。
1.2.8 环五肽c(Leu-N-Me-Leu-Leu-N-Me-Leu-N-Me-Leu)(b1)的合成
取保护五肽Boc-Leu-N-Me-Leu-Leu-N-Me-Leu-N-Me-Leu-OBn(0.15 mmol),按照1.2.7方法,合成分离后得到环五肽白色固体(b1)35 mg,收率38.0%。
1.3 体外抗肿瘤活性筛选
采用MTT法对所合成的目标化合物进行体外细胞毒活性筛选,所选细胞株为人肝癌细胞(HepG2)、人肺癌细胞(A549)、人宫颈癌细胞(Hela),将其抑制活性与Galaxamide进行对照。
2 结果与讨论
2.1 产物表征
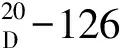

2.2 环合试剂的选择
在环肽合成过程中,环合试剂的选择对目标化合物的合成至关重要,决定着关环是否成功及收率的高低,既是合成的重点也是难点。本研究选择DEPBT、HATU、TBTU作为环合试剂,溶剂体系为THF-CH3CN-CH2Cl2(2∶2∶1),对环五肽的关环效果理想。同时对文献[4]所报道的环合步骤进行改进,减少一半溶剂体积、增加一倍环合试剂用量,不仅能够提高环合的收率,同时在该反应的副产物中,含有25%~28%的五肽二聚体(环十肽),已对该部分进行了进一步的谱图分析,以确定其结构。
2.3 分离技术及条件的选择
天然产物的全合成不仅要求合成方法得当、合成步骤合理,而且对分离技术及条件的选择要求也很高。尤其是环肽的分离,绝大部分都是用HPLC反相制备柱分离,耗费大量的时间和金钱。因此,作者对合成的中间体及目标化合物的分离采用了不同的方法和条件:(1)对线性肽中间体分别采用石油醚与丙酮、正己烷与丙酮体系为淋洗剂,硅胶柱层析分离。(2)对目标产物环肽的分离采取甲醇与水体系为淋洗剂,C18反相硅胶柱分离。经HPLC分析,产物纯度在98%以上。
2.4 体外抗肿瘤活性分析(表1)

表1 体外抗肿瘤活性比较
由表1可知:(1)含有D构型的环肽a7能增强抗肿瘤活性,可以对其进行进一步的药理研究。(2)环肽b1相比Galaxamide多了一个氮上甲基,其IC50较高,表明甲基数量的增多并不能增强环肽活性。
3 结论
以亮氨酸为起始原料,改变环合位点,全合成了两个海洋环肽Galaxamide[环(亮氨酰-N-甲基亮氨酰-亮氨酰-N-甲基亮氨酰-亮氨酰)]类似物。通过1HNMR、13CNMR、MS对其结构进行了表征,并对人肝癌细胞(HepG2)、人肺癌细胞(A549)、人宫颈癌细胞(Hela)进行了体外抗肿瘤活性的研究。结果表明,含有D构型的环肽能增强抗肿瘤活性,而环肽氮上甲基数量的增多并不能增强环肽抗肿瘤活性。
参考文献:
[1]Xu W J,Liao X J,Xu S H,et al.Isolation,structure determination,and synthesis of Galaxamide,a rare cytotoxic cyclic pentapeptide from a marine algaeGalaxaurafilamentosa[J].Org Lett,2008,10(20):4569-4572.
[2]Fairlie David P,Abbenante Giovanni,March Darren R.Macrocyclic peptide-mimetics forcing peptides into bioactive conformations[J].Current Medicinal Chemistry,1995,2(2):654-686.
[3]Aungst Bruce J,Saitoh Hiroshi.Intestinal absorption barriers and transport mechanisms,including secretory transport,for a cyclic peptide,fibrinogen antagonist[J].Pharmaceutical Research,1996,13(1):114-119.
[4]郭伟,邓攀,杨会付,等.环(亮氨酰-N-甲基亮氨酰-亮氨酰-N-甲基亮氨酰-亮氨酰)的合成[J].精细化工,2010,27(9):855-858.
