我院2011年药品不良反应报告分析
2012-05-01丁长玲赵永德张树平
丁长玲,赵永德,张树平,姜 宏,高 菲
(1.滨州医学院附属医院,山东 滨州 25660;2.滨州医学院,山东 烟台 264003)
药品不良反应(ADR)监测是对药品的有害性进行安全性防范的一系列措施,是药品安全监管的重要手段,通过全面收集ADR信息,进行科学地分析评价,从中提取出有价值的警戒信号,达到有效预警药害事件,更好地维护公众健康的目的。本文对我院2011年上报的有效ADR报表进行回顾性分析,了解ADR发生的特点和规律,旨在更好地促进我院ADR监测工作的开展及促进临床合理用药,减少ADR给患者造成的危害。
1 资料与方法
收集2011年各科室上报的有效ADR报表332份,根据患者基本情况、药品信息、ADR累及器官或系统及临床表现、ADR报告类型等方面数据进行统计分析。
2 结果
2.1 性别与年龄分布 我院2011年全年共收到332例ADR报告,其中男性159人,占47.89%,女性173人,占52.11%,女性略高于男性。男性患者年龄最小2个月,最大为90岁;女性年龄最小4个月,最大为88岁,各年龄段分布见表1。

表1 发生ADR患者的年龄与性别分布
2.2 患者家族史、既往药物过敏史情况 332例ADR报告中,有药物过敏家族史的6例,占1.81%;无过敏史的133例,占40.06%;不详的193例,占58.13%。患者既往有过敏史的38例,占11.45%;无过敏史的158例,占47.59%;不详的136例,占40.96%,有既往过敏史的患者ADR涉及药品与主要临床表现,见表2。

表2 有既往过敏史的患者ADR涉及药品与主要临床表现
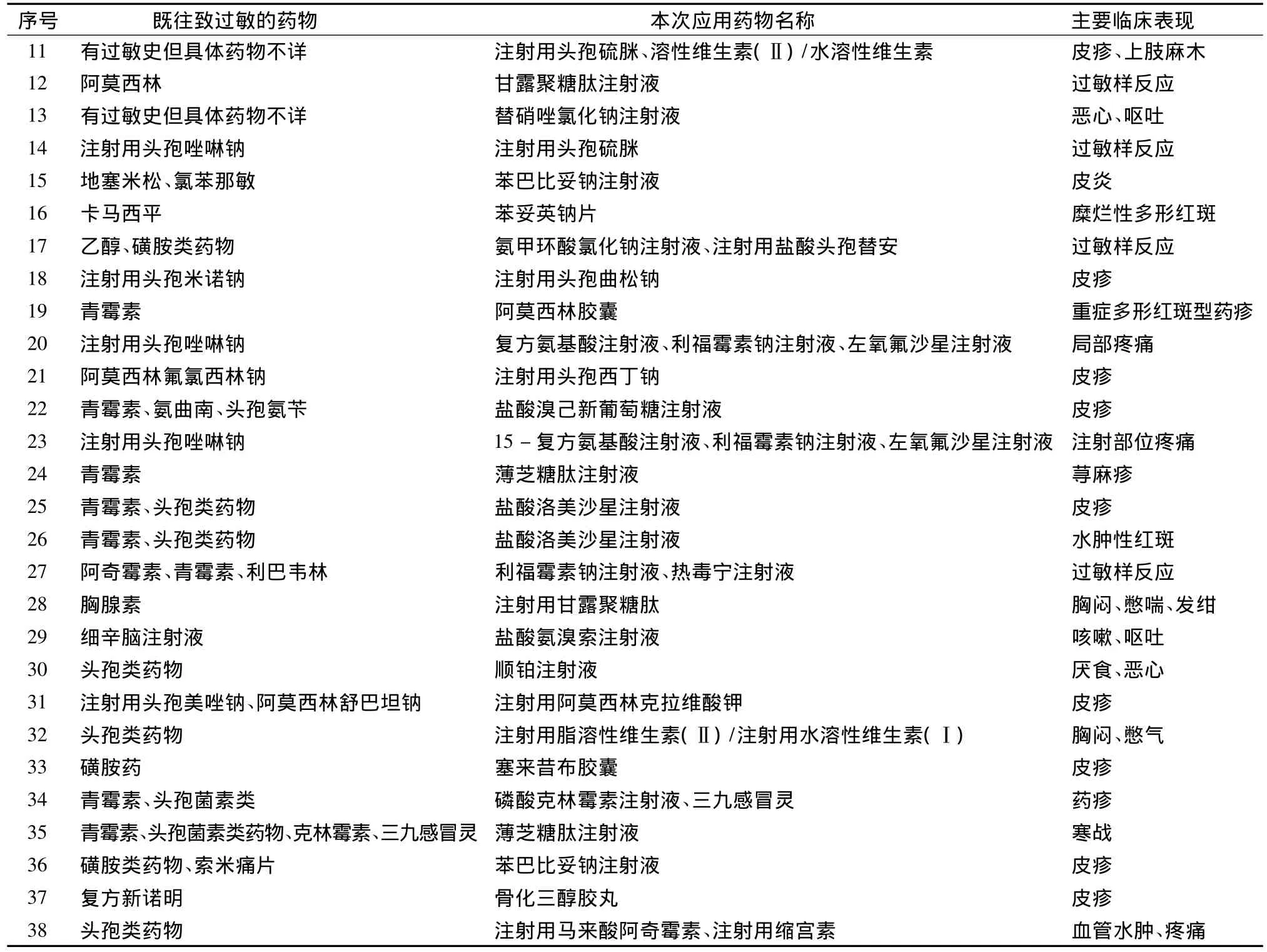
续表2
2.3 患者门诊、住院分布及转归情况 332例ADR中,门诊患者15例,占4.52%;住院患者317例,占92.48%。好转108例,占32.53%;治愈224例,占67.47%。所有患者经积极治疗均好转或痊愈。
2.4 药品剂型分布 全年病例报告涉及药品515种,剂型9种,其中注射剂、粉针剂、片剂为主要剂型。其分布及所占比例,见表3。

表3 332例ADR报告涉及药品剂型分布统计
2.5 报告类型及所占比例 332例ADR报告中,新的一般报告46例,占13.86%;新的严重2例,占0.60%;严重的43例,占12.95%;一般报告241例,占72.60%。我院报道的严重ADR主要是导致住院或住院时间延长,大多集中在皮肤科,一方面是由于在基层医疗机构、诊所用药出现药疹后来我院就诊的患者较多;另一方面是由于出现过敏样反应的患者,多表现为皮肤损害而到皮肤科治疗。经我院皮肤科及相关科室积极治疗后患者基本都好转或痊愈。
2.6 按照《新编药物学》第17版对ADR报告涉及的药品进行分类,332例报告涉及药物515种,其中涉及抗微生物药物引起的ADR报告例数最多,有185种,占35.92%。引起不良反应的药物居第二位的是中药注射剂,63例,占12.23%。中药注射剂的不良反应主要为Ⅰ型变态反应,发生快,且较危险。临床应用时要注意药物配伍、溶媒选择、超适应证用药、超剂量用药等有关。提醒临床用药时应在用药后半小时内密切观察,一旦发生ADR,应立即停药并采取措施对症处理。
2.7 用药途径 全年病例报告涉及用药途径8种,其中静脉给药、口服给药为主要用药途径,报告数量合计占总数的97.48%。其次为肌肉注射7例,占1.36%。
2.8 ADR累及的器官或系统及临床表现 332例ADR中,以皮肤及其附件损害的病例最多,见表4。
2.9 报告数量前10位的药品统计 引发ADR前10位药物中,抗菌药物6种,占60.0%,见表5;与2010年度80%相比有所下降,可能与2011年度抗菌药物使用率下降有关。

表4 ADR累及器官或系统及临床表现

表5 前10位ADR报告涉及药品及报告数量
2.10 不良反应分析及关联性评价情况 332例报告的关联性评价中,我院评价“肯定”的为25例,占7.53%;“很可能”的为237例,占71.39%;“可能”的为68 例,占 20.48%;“可能无关”的2例,占0.60%,与市监测中心、省监测中心评价基本一致。

表6 332份报告不良反应分析统计表
从表6看出,我院在处理ADR患者时,为确保用药安全,大部分患者未再继续用药,而是及时采取停药处理的措施,同时说明我院根据报表分析评价原则和方法基本能做出正确评价。
3 讨论
3.1 从报表数量和质量看,我院2011年332例报告中,新的、严重的报告数量为91份,占总报告数的27.41%,上报新的、严重的比例较高。
3.2 从患者年龄看,0~10岁报告总例数为 77例,占23.19%,低于2010年报告的152例(39.38%)。332例ADR报告中,患者有既往药物过敏史的38例,占11.45%;无过敏史的158例,占47.59%;不详的136例,占40.96%。说明药物过敏情况没有引起患者的高度重视,应加大宣传力度,提高患者及家属的警惕意识。同时可以看出有药物过敏史的患者,再次发生ADR的几率较高。38例患者对青霉素或头孢菌素类药物过敏者高达23例,占60.53%,其中对青霉素过敏的患者9例,占28.13%,提醒临床对有青霉素或头孢菌素类药物过敏的患者选药时要特别慎重,同时要密切关注患者用药后的反应。我们应加大对患者既往过敏史情况的询问,避免患者重复发生ADR,给患者带来不必要的损害。另外要注意含有相同成分或相似化学结构的药物,如38例有既往药物过敏史的患者中有5例对磺胺药物过敏。其中表2中第33例患者既往有磺胺药过敏史,又口服塞来昔布胶囊出现药疹,在该药说明书中明确注明有磺胺药过敏史者禁用,应引起临床高度关注。同时应加强对患者的用药教育,告知不能应用的药物,如颠茄磺苄啶片[1]、柳氮磺胺吡啶、磺胺嘧啶银等磺胺类药物。
3.3 从药品剂型及用药途径看,主要为注射剂、粉针剂,占83.50%,用药途径为静脉滴注,占 85.44%,与报道一致[2]。提示静脉给药品种为高风险品种,在药品安全监管中应给予高度关注。
3.4 从ADR涉及药物看,抗菌药物仍然占有较高的比例,引发ADR前10位药物中,抗菌药物6种,占60.0%;与2010年度80%相比有所下降,可能与2011年度抗菌药物使用率降低有关。
3.5 从ADR累及器官或系统及临床表现看,上报的主要为皮肤损害、全身性损害、胃肠、呼吸、神经系统损害,其中皮肤及其附件损害占53.01%。主要集中在皮肤科、小儿科两个病区,可能与皮肤反应比较容易观察、科室负责人重视程度有关。有关肝功能损害的上报病例数为14例,高于2010年度,但是血液系统损害、心血管系统损害上报较少,其他系统损害漏报率也较高,说明上述相关科室对于ADR监测工作没有引起高度重视,上报意识不强。我们应加大心内科、血液内科、肾内科等相关科室ADR监测力度,密切关注患者用药后的种种变化,尤其是肝肾功能相关检查指标,发现异常信号,及时停药并采取措施对症处理,利用预警信息,及时有效防范严重ADR发生,不断提高监测水平。
3.6 ADR因果关系判断中,关联性评价为“肯定”的为38例,根据国家药品不良反应监测中心ADR因果关系评价标准,评价为“肯定”的标准必须包括“再次使用可疑药品后出现相同症状”,而临床上一旦发生ADR,一般立即停药,不会再使用可疑药品,所以“肯定”的评价结果不多[3]。但是在评价时不能简单套用因果评定的5项准则,涉及到具体病人或病例报告中可疑药物与不良反应间因果相关性的总结,还应基于知识与经验,应立足于主动寻找资料,在全面掌握不良反应发生的前后过程中,理清思路,具体病例,具体分析。对于撤药后反应症状好转的,应辨别是撤药的作用还是因使用了减轻症状的药物或是病理变化的结果。
总之,药学部与临床科室密切协作,通过深入临床参与典型ADR分析、及时调查原因,及时发现风险信号,采取停药、更换药品批号、减量等措施,及时避免了ADR重复发生。如我院临床在应用复方麝香注射液[4]时,发现该药易引起患者胸闷、憋气、呼吸困难、口唇发绀等过敏样反应,及时更换三个生产厂家,更换8个批次后,仍有患者出现上述反应,为确保用药安全,药学部及时写出分析、评价报告并作报道,及时停用该药物,避免了ADR的重复发生,起到干预预警作用。药师通过对患者加强用药教育,不断强化人们安全用药、合理用药意识,使ADR监测向药物警戒方向发展。为患者建立安全用药防线,最大限度减少药物性损害事件的发生,创造一个良好的用药环境,确保患者用药安全、有效。
[1]丁长玲,张海霞,李海英,等.颠茄磺苄啶片致固定型药疹1例[J].中国药物警戒,2011,8(5):318 -319.
[2]司继刚,赵群.我院532例药品不良反应报告回顾与分析[J].中国药业,2011,20(2):58-59.
[3]刘华强,王少华,孙福生.我院2006 -2007年药品不良反应报告分析[J].中国药房,2008,19(26):2058-2060.
[4]丁长玲,刘呈华,孙静,等.我院15例复方麝香注射液致不良反应报告分析[J].中国药房,2007,18(33):2614-2615.
