血脂康对早期糖尿病肾病患者氧化应激的影响
2012-04-26常万松薛迪中沈学飞
魏 娜,常万松,薛迪中,沈学飞
糖尿病肾病 (diabetic nephropathy,DN)是糖尿病常见的并发症,临床特征为蛋白尿、渐进性肾功能损害、高血压、水肿,晚期出现肾衰竭,严重影响糖尿病患者的生活质量,是糖尿病患者的主要死亡原因之一。越来越多的研究表明,在DN诸多发病机制中,氧化应激是重要的共同机制[1-2]。血脂康胶囊作为一种天然他汀类调脂药,具有调节血脂、降低尿蛋白排泄率、改善内皮细胞功能等多种作用[3]。本研究旨在观察血脂康对早期DN患者氧化应激的影响,探讨血脂康在DN治疗中的作用。
1 资料与方法
1.1 一般资料 选取2010年10月—2011年6月在本院住院及专科门诊长期随访的早期DN(DN 3期)患者56例,均符合2000年世界卫生组织 (WHO)制订的糖尿病诊断标准,男24例,女32例;年龄41~68岁,平均50.6岁;糖尿病病程4.5~30.0年,平均11.8年;尿清蛋白排泄率 (UAER)介于30~300 mg/d;排除:酮症酸中毒、心脑血管疾病、严重肝肾疾病、各种急慢性感染以及服用影响尿蛋白排泄药物者;无风湿、类风湿关节炎病史,未使用各种止痛剂、类固醇类药物、他汀类降脂药、血管紧张素转换酶抑制剂和血管紧张素Ⅱ受体阻滞剂。所有入选者糖化血红蛋白 (HbA1c) <9.0%,空腹血糖 (FPG) <10.0 mmol/L,肌酐 (Cr) <105.0μmol/L,尿素氮 (BUN) <7.1 mmol/L。
根据UAER水平,把患者分为:UAER<100、100~150、151~200、201~250、251~300 mg/d 5档,然后将每档内的患者随机分配到血脂康组和安慰剂组中,以避免两组患者初始UAER相差悬殊。血脂康组28例,安慰剂组28例,两组患者的性别构成、年龄及糖尿病病程间有可比性 (P>0.05,见表1)。另选取20例健康体检者作为正常对照组,其年龄、性别构成与血脂康组和安慰剂组比较差异无统计学意义 (P>0.05);而FPG及HbA1c水平则显著低于血脂康组和安慰剂组(p<0.05,见表1)。
1.2 方法 血脂康组给予口服血脂康胶囊0.6 g/次,3次/d;安慰剂组口服与血脂康外形相同的含淀粉的胶囊,0.6 g/次,3次/d,均连续给药12周。分别于给药前和治疗12周后留取血标本待测。两组患者均使用胰岛素控制空腹血糖于正常范围,在干预治疗期间避免同时服用具有抗氧化应激作用的药物,如维生素E、维生素C、β胡萝卜素、谷胱甘肽等。
1.3 观察指标 采用羟胺法检测3组受试者血超氧化物歧化酶 (SOD),用硫代巴比妥酸比色法检测丙二醛 (MDA),试剂盒购自南京建成生物研究所;三酰甘油 (TG)、总胆固醇(TC)、低密度脂蛋白胆固醇 (LDL-C)、极低密度脂蛋白胆固醇 (VLDL-C)、高密度脂蛋白胆固醇 (HDL-C)均采用全自动生化仪测定。研究开始及结束时分别检测各组UAER。测定方法:留取当日晨7点至次日晨7点的24 h尿液,用二甲苯作为防腐剂。测量24 h尿容积,混匀后取标本用放射免疫法检测尿微量清蛋白,计算出UAER。嘱患者在留尿的前24 h和留尿过程中不进食高蛋白饮食,不做剧烈运动。
1.4 统计学方法 采用SPSS 13.0软件进行统计检验。计量资料以表示,多组间比较采用方差分析,两组间比较采用t检验。UAER呈偏态分布,取自然对数后符合正态分布。以p<0.05为差异有统计学意义。
2 结果
2.1 治疗前后血脂水平的变化 治疗前,血脂康组及安慰剂组早期DN患者血脂 (包括TC、TG、LDL-C和VLDL-C)均显著高于正常对照组,而HDL-C水平则显著低于正常对照组 (p<0.05)。血脂康组治疗12周后,血清TC、TG、LDLC和VLDL-C水平较本组治疗前及安慰剂组治疗后显著降低(p<0.05),但仍显著高于正常对照组 (p<0.05);而HDL-C水平则较本组治疗前及安慰剂组治疗后显著升高 (p<0.05),但仍显著低于正常对照组 (p<0.05,见表2)。
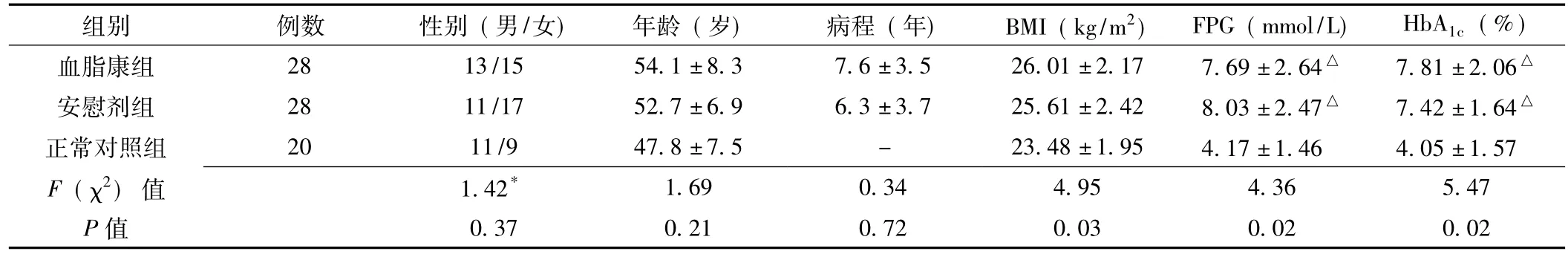
表1 3组受试者一般资料比较Table 1 Comparison of general information among three groups
表2 3组受试者治疗前后血脂水平比较 (,mmol/L)Table 2 Comparison of blood lipid levels among three groups before and after the treatment
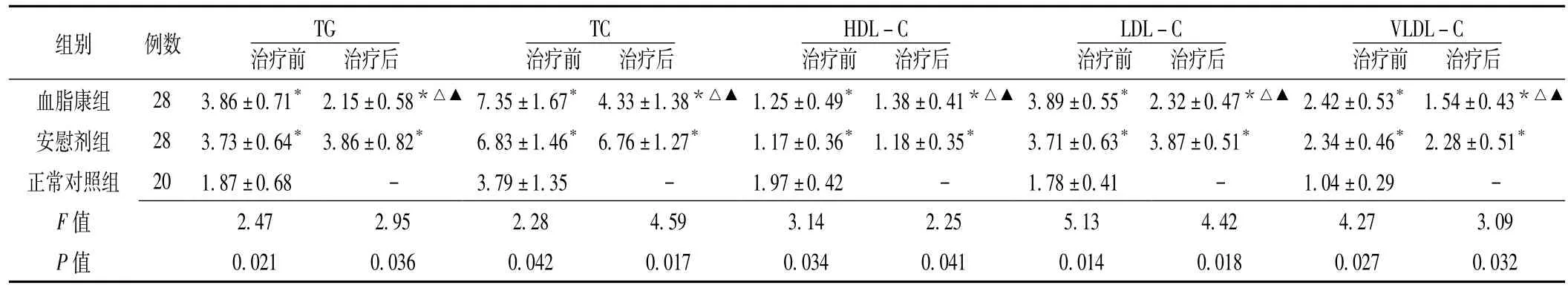
表2 3组受试者治疗前后血脂水平比较 (,mmol/L)Table 2 Comparison of blood lipid levels among three groups before and after the treatment
注:与正常对照组比较,*p<0.05;与安慰剂组比较,△p<0.05;与本组治疗前比较,▲p<0.05;TG=三酰甘油,TC=总胆固醇,HDL-C=高密度脂蛋白胆固醇,LDL-C=低密度脂蛋白胆固醇,VLDL-C=极低密度脂蛋白胆固醇
治疗后血脂康组 28 3.86±0.71* 2.15±0.58*△▲ 7.35±1.67* 4.33±1.38*△▲ 1.25±0.49* 1.38±0.41*△▲ 3.89±0.55* 2.32±0.47*△▲ 2.42±0.53* 1.54±0.43组别 例数 TG治疗前 治疗后TC治疗前 治疗后HDL-C治疗前 治疗后LDL-C治疗前 治疗后VLDL-C治疗前*△▲安慰剂组 28 3.73±0.64* 3.86±0.82* 6.83±1.46* 6.76±1.27* 1.17±0.36* 1.18±0.35* 3.71±0.63* 3.87±0.51* 2.34±0.46* 2.28±0.51*正常对照组 20 1.87±0.68 - 3.79±1.35 - 1.97±0.42 - 1.78±0.41 - 1.04±0.29 -F 值8 0.027 0.032 2.47 2.95 2.28 4.59 3.14 2.25 5.13 4.42 4.27 3.09 P值 0.021 0.036 0.042 0.017 0.034 0.041 0.014 0.01
2.2 治疗前后血清SOD及MDA的变化 与正常对照组比较,治疗前血脂康组和安慰剂组早期DN患者血清SOD水平显著下降,而MDA水平则显著上升 (p<0.05)。血脂康组患者治疗12周后,其血清SOD水平显著升高,而MDA水平则显著下降,与本组治疗前及安慰剂组治疗后比较差异均有统计学意义 (p<0.05)。而安慰剂组患者治疗前后血清SOD及MDA比较,差异均无统计学意义 (P>0.05,见表3)。
2.3 治疗前后UAER变化 治疗前血脂康组和安慰剂组患者UAER分别为 (157.5±28.6)ng/d和 (165.9±24.1)ng/d,二者比较差异无统计学意义 (t=1.09,P>0.05);治疗12周后,血脂康组和安慰剂组患者UAER分别为 (110.0±21.5)ng/d和 (155.7±23.7)mg/d,二者比较差异有统计学意义(t=2.31,P=0.039);且血脂康组治疗后UAER亦显著低于本组治疗前 (p<0.05)。
表3 3组受试者治疗前后血清SOD及MDA水平比较 Table 3 Comparison of serum SOD and MDA levels among the three groups before and after treatment
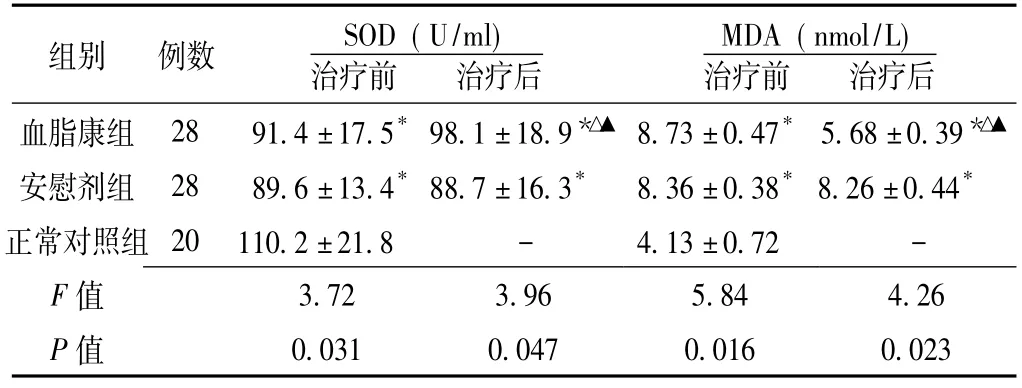
表3 3组受试者治疗前后血清SOD及MDA水平比较 Table 3 Comparison of serum SOD and MDA levels among the three groups before and after treatment
注:*与正常对照组比较,p<0.05;△与安慰剂组比较,p<0.05;与本组治疗前比较,▲p<0.05;SOD=血超氧化物歧化酶,MDA=丙二醛
组别 例数 SOD(U/ml)治疗前 治疗后血脂康组 28 91.4±17.5*98.1±18.9*△▲ 8.73±0.47* 5.68±0.39治疗后MDA(nmol/L)治疗前*△▲安慰剂组 28 89.6±13.4*88.7±16.3* 8.36±0.38*8.26±0.44*正常对照组 20 110.2±21.8 - 4.13±0.72 -F 值0.031 0.047 0.016 0.023 3.72 3.96 5.84 4.26 P值
3 讨论
DN是糖尿病常见的慢性并发症之一,其确切的发病机制尚未完全阐明。近年来,氧化应激在DN发病机制中的作用日益引起人们的关注[4]。氧化应激是指活性氧簇 (ROS)或活性氮簇产生增多和 (或)清除减少,导致ROS在体内蓄积而引起的分子、细胞和机体的损伤。研究显示,高糖环境可通过晚期糖基化终末产物 (AGEs)形成、葡萄糖自身氧化、多元醇通路 (PP)的活性增高、蛋白激酶C(PKC)活化等机制,引起体内ROS产生增加[5]。ROS作为细胞内信号分子,介导了多种信号转导通路、转录因子的激活,参与了糖尿病肾组织损害的发生、发展。Aksun等[6]指出 ROS可通过一氧化氮(NO)参与肾小球高灌注和高滤过;Susztak等[7]研究表明,高糖通过ROS启动足细胞凋亡,诱导其从基底膜上脱落,使肾小球内足细胞数目减少。由于ROS能迅速与周围物质发生反应,其t1/2短暂,难以直接检测其水平。但ROS与DNA、脂质、蛋白质反应后生成的产物可作为检测氧化应激的指标。本研究结果显示,早期DN患者治疗前血清MDA水平较健康者显著升高,而血清SOD水平则显著下降,反映DN患者体内脂质过氧化程度增高和机体清除自由基的能力下降,与国内外研究一致。
高脂血症是2型糖尿病患者代谢紊乱的常见症状,也是促进DN进展的重要因素。血脂异常时,氧化应激使脂蛋白被氧化修饰,特别是低密度脂蛋白 (LDL)在体内被氧化修饰形成氧化型脂蛋白 (OX-LDL),OX-LDL具有细胞毒性作用,可以直接损伤内皮细胞本身[8],还可使血管内皮产生的超氧化物阴离子增加,细胞外NO的灭活增加[9]。最近研究表明OX-LDL可以显著抑制内皮细胞、巨噬细胞一氧化氮合酶(NOS)基因表达,从而抑制NO合成,增加活性氧的产生[10]。因此积极调脂治疗,减少过氧化脂质的产生,可能对减轻糖尿病内皮细胞损伤、减缓微血管并发症的发生有积极意义。
血脂康是由中药红曲精炼而成的一种调脂药,其有效成分是HMG-CoA还原酶抑制剂,包含以洛伐他汀为主的13种天然他汀,同时含有多种不饱和脂肪酸、必需氨基酸、生物碱以及黄酮类物质。本研究结果显示,早期DN患者存在血脂紊乱,血脂康组患者在连续治疗12周后血清TC、TG、LDL-C水平较治疗前显著降低,表明血脂康具有良好的降脂作用。研究显示,血脂康组治疗后血清SOD水平显著上升、MDA水平显著下降,提示血脂康具有清除自由基、增加SOD活性、降低脂质过氧化物作用。同时血脂康组治疗后UAER显著降低,这可能与血脂康调节血脂,减少LDL水平,使氧化应激的脂质底物减少,OX-LDL的产生相应减少,从而减轻对内皮细胞的损伤并抑制活性氧的产生有关。此外,血脂康含有的多种他汀类物质、生物碱以及黄酮类物质,对改善氧化应激也有促进作用。
综上所述,早期DN患者体内存在氧化-抗氧化平衡失调所致的氧化应激。氧化应激可通过损伤血管内皮细胞,在DN的发病过程中起一定的作用。血脂康能够降低早期DN患者血中TC、TG和LDL-C水平,并显著降低MDA水平,增加SOD活性,降低UAER,对早期DN的治疗有积极意义。
1 Xu M,Dai DZ,Dai Y,et al.Normalizing NADPH oxidase contributes to attenuating diabetic nephropathy by the dual endothelin receptor antagonist CPU0213 in rats[J].Am J Nephrol,2009,29(3):252 -256.
2 Haidara MA,Mikhailidis DP,Rateb MA,et al.Evaluation of the effect of oxidative stress and vitamin E supplementation on renal function in rats with streptozotocin-induced Type 1 diabetes[J].J Diabetes Complications,2009,23(2):130-136.
3 丁俊蓉,周益伟,许华强.血脂康对2型糖尿病肾病血脂和微量白蛋白的影响[J].现代中西医结合杂志,2008,17(10):1461-1462.
4 Browlee M.The pathobiology of diabetic complications,a unifying mechanism[J].Diabetes,2005,54(6):1615 -1625.
5 Brownlee M.Biochemistry and molecular cell biology of diabetic complications[J].Nature,2001,414(6865):813-820.
6 Aksun AS,Ozmen B,Ozmen D,et al.Serum and urinary nitric oxide in type 2 diabetes with or without microalbuminuria:relation to glomerular hyperfihration [J].J Diabetes Complications,2003,17(6):343-348.
7 Susztak K,Raft AC,Schiffer M,et al.Glucose-induced reactive oxygen species cause apoptosis of podocytes and podocyte depletion at the onset of diabetic nephropathy[J].Diabetes,2006,55(1):225 -233.
8 Hadi HA,Carr CS,Suwaidi JAI.Endothelial dysfunction:cardiovascular risk factors,therapy,and outcome [J].Vasc Health Risk Manag,2005,1:183-198.
9 Naseem KM.The role of nitric oxide in cardiovascular diseases[J].Mol Aspects Med,2005,26:33-65.
10 Jiang Y,Zhang J,Xiong J,et al.Ligands of peroxisome proliferatoractivated receptor inhibit homocysteine-induced DNA methylation of inducible nitric oxide synthase gene[J].Acta Biochim Biophys Sin(Shanghai),2007,39:366-376.
