AB位掺杂对La2NiO4同时催化还原脱除NOx和柴油机碳烟颗粒性能的影响
2012-04-10朱云峰秦永宁李志军
马 智,朱云峰,丁 彤,秦永宁,李志军
(1.天津大学化工学院,天津 300072; 2.天津大学内燃机国家重点实验室,天津 300072)
近年来,随着人们生活水平的不断提高,私家车数量一路飙升,而随之而来的汽车尾气污染物问题也越来越严重。机动车排放的尾气严重污染了我们的生活环境,损害了我们的身体健康。研究新型的汽车尾气催化转化催化剂,降低机动车尾气污染物的排放已经迫在眉睫,对这一领域的研究已成为一个全球性的课题[1]。自1892年柴油机问世以来,因其循环的热效率高、燃油经济性好、CO2排放量低等特点,得到人们的广泛应用,其尾气的污染问题也随之而来。由于其燃烧的性能特点,产生的主要污染物有碳氢化合化物(CH)、CO、氮氧化合物(NOx)和碳烟颗粒(PM)。和汽油机相比,CH和CO的排放量减少,NOx的含量基本相同,而PM约为汽油机的30~50倍。因此控制柴油机尾气污染物的排放目标是综合治理,以达到降低PM和NOx的目的。1989年,日本科学家Yoshida最早提出了利用柴油机尾气中的碳颗粒在含氧气氛下催化还原脱除NOx的理论[2],研究表明钙钛矿具有良好的催化性能。La0.8K0.2Cu0.05Mn0.95作为催化剂,NOx的转化率为58%[3];La0.7Ag0.3MnO3作为催化剂,NOx的转化率可达72%[4]。在我们前面的研究[5]中发现,La2NiO4具有良好的催化性能,少量的掺杂改性能够提高催化剂的活性,并且不会改变催化剂的主体结构。
本研究用溶胶凝胶法制备了一系列的La2NiO4型氧化物催化剂,对A、B位进行了高程度的掺杂改性,并分别考察了A和B掺杂改性对其催化性能的影响。
1 试验部分
1.1 催化剂的制备
用溶胶-凝胶法制备[5],按照2∶1∶1的物质的量之比称取一定量的硝酸镧、硝酸镍和柠檬酸试剂,分别将其配成1 mol/L的溶液,溶解均匀后将其混合,超声搅拌溶解2 h,放入烘箱中在130 ℃的温度下加热24 h,蒸干水分得到前躯体,将其放入煅烧炉中,以10 ℃/min的升温速率加热至400 ℃,恒温4 h,冷却后将煅烧得到的粉末以10 MPa的压强进行压片成型,再以10 ℃/min的升温速率进行煅烧,温度升至800 ℃,恒温4 h,冷却后得到催化剂La2NiO4。
其它催化剂亦采用相似的方法制得。
1.2 催化剂表征
日本理学D/MAX-2038型X射线衍射仪分析催化剂的物相结构,辐射源为Cu靶,滤波片Ni,管电压20~30 kV,管电流30 mA,测角仪转动速度4 (°)/min(2θ),扫描范围20~90°(2θ)。
H2-TPR在内径为6 mm的石英反应器中进行,反应气为N2+H2混合气,H2体积分数10%,流速50 mL/min,催化剂粒度30~40目,用量0.3 g。检测器为热导池,桥电流100 mA,衰减1/4。试验开始前将催化剂装入反应器中,通入N2,温度升至500 ℃,恒温吹扫30 min,自然冷却至室温,通入氮氢混合气,待色谱基线稳定后以10 ℃/min的升温速率升至800 ℃,记录数据得到TPR谱图。
1.3 催化剂活性评价
催化剂的活性评价采用内径为16 mm的固定床石英反应器。进气组成(体积分数)为1%NO+5%O2+94%He,气体总流速为50 mL/min。催化剂0.95 g,碳颗粒0.05 g。试验前通氦气吹扫,直到色谱检测不出氮气。从200 ℃开始程序升温,每隔50 ℃进行取样分析。
采用2台色谱(北分SP3420)在线分析原料气和尾气的组成,5A分子筛:N2、O2、CO,载气H2,柱温42 ℃,柱前压0.09 MPa;porapak Q柱:CO2、N2O,载气H2,柱温20 ℃,柱前压0.09 MPa。
催化剂的活性评价指标[6-7]: NO的转化率X为2[N2]out/[NO]in;反应的选择性SN2为[N2]out/[CO2]out;[NO]in为入口处NO的体积分数;[N2]out为出口处N2的体积分数;[CO2]out为出口处CO2的体积分数。
2 结果与讨论
2.1 XRD结果
A2BO4型氧化物是一种比较难成型的类钙钛矿结构,需要在非常高的温度下煅烧才能生成良好的晶型。图1是所合成催化剂的XRD谱图。
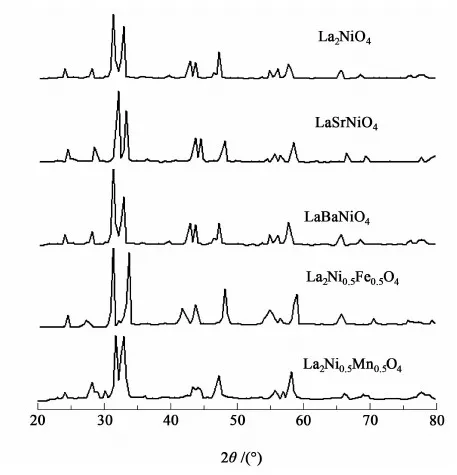
图1 催化剂的XRD谱图Fig.1 XRD patterns of the catalysts
从图1中可以看出不同的催化剂其主要衍射峰的强度稍微有所变化,但其衍射峰位置基本没有变化。对于Mn掺杂的样品,出现少量的杂峰,基线比较粗糙,主体峰仍保持不变。根据JCPDS参考卡片的信息,A2BO4型类钙钛矿氧化物的主要衍射峰应该在2θ为24.0、31.3、32.9和47.0 (°)处。对比谱图1可以看出所制备的催化剂都属于都具有良好的类钙钛矿晶型,对A、B进行一定程度的掺杂改性不会改变其主体物相结构。
2.2 H2-TPR结果
图2是所合成催化剂的H2-TPR谱图,其中还原峰数据分析见表1。

图2 催化剂的H2-TPR谱图Fig.2 H2-TPR curves of the catalysts

表1 H2-TPR谱图的还原峰分析
从图2和表1中可以看出,每个催化剂都有2个还原峰,第1个命名为α峰,第2个命名为β峰。催化剂氧种的活动能力可以通过TPR谱图表示,出峰温度越高,氧种的活动能力越弱,出峰温度越低,表示该氧种的活动性越强。通过Spinicci等[8]的研究,α峰主要代表吸附氧的活泼性,β峰主要反映催化剂上晶格氧的活泼性。对比A位掺杂改性的催化剂LaSrNiO4、LaBaNiO4与未掺杂的样品La2NiO4的TPR谱图,可以看出A位掺杂主要影响到α峰温的变化,而β峰温变化较小。对于B位掺杂的样品,TPR的谱峰变化主要体现在β峰上,相对于La2NiO4来说,B位掺杂改性的La2Ni0.5Mn0.5O4以及La2Ni0.5Fe0.5O4样品,它们的β峰温提高了300 ℃。可以推测,对La2NiO4进行A位掺杂改性会改变其吸附氧的活泼性,而B位掺杂会影响其晶格氧的活泼性。
2.3 催化剂的活性测试
图3是La2NiO4催化剂在含氧及无氧气氛下的活性对比图。

图3 La2NiO4在有氧和无氧条件下同时催化还原脱除NOx和碳烟颗粒的效果Fig.3 Catalytic performance of La2NiO4 for simultaneous removal of NOx and soot with and without the presence of O2
从图3中可以看出,在无氧气氛下目标反应只能发生在较高的温度范围(500~750 ℃),NO转化率不到10%,当反应气中同时含有氧气和NO时,反应温度降低到300 ℃,且NO的转化率有了很大的提高。因此,氧气对于目标反应具有非常重要的促进作用。
图4是催化剂的活性评价效果,具体数值见表2。

图4 催化剂同时脱除NOx和碳烟颗粒的催化性能Fig.4 Catalytic performance of catalysts for simultaneous removal of NOx and soot
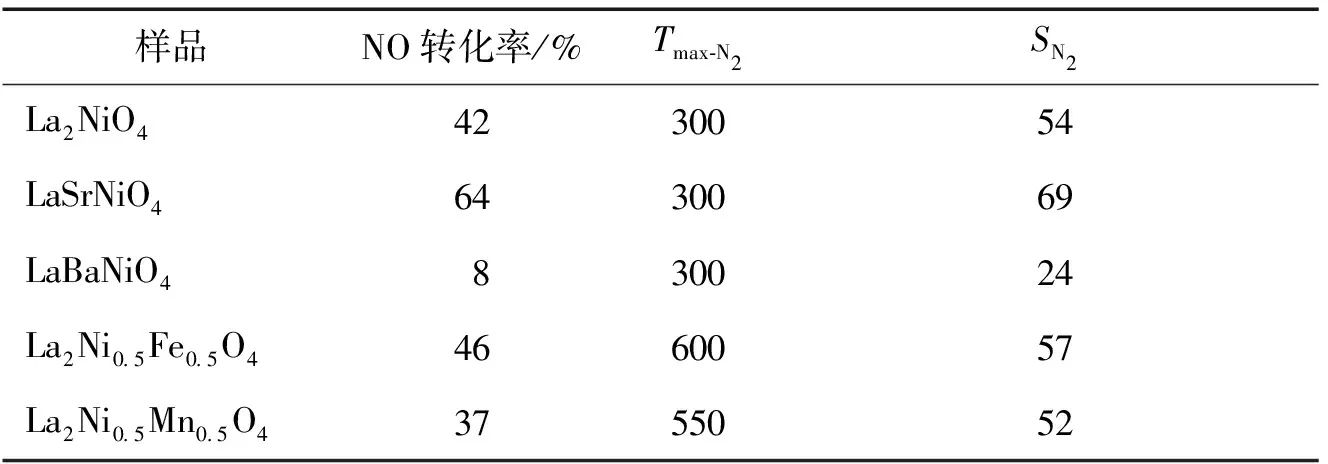
样品NO转化率/%Tmax⁃N2SN2La2NiO44230054LaSrNiO46430069LaBaNiO4830024La2Ni0 5Fe0 5O44660057La2Ni0 5Mn0 5O43755052
从图4和表2可以看出,未掺杂改性La2NiO4催化剂,300 ℃时NO的转化率最高,为42%,选择性S为54%。A位掺杂改性的LaSrNiO4与LaBaNiO4,它们的最适宜反应温度都是300 ℃,而选择性相对于La2NiO4来说有较大变化,LaSrNiO4为69%,提高了15%,LaBaNiO4为24%,降低了30%,推测A位掺杂改性可能会主要影响到反应的选择性。对比B位掺杂改性的La2Ni0.5Fe0.5O4、La2Ni0.5Mn0.5O4和La2NiO4,它们的选择性分别为57%、52%、54%,非常接近,而最适宜反应温度却有非常大的变化,掺杂后的La2Ni0.5Fe0.5O4,由300 ℃提高到了600 ℃,La2Ni0.5Mn0.5O4提高到了550 ℃。推测B位掺杂可能会主要影响到反应的最适温度。
2.4 讨论
目标反应是一个三相接触的反应过程:固体催化剂-固体还原剂(碳烟颗粒)-气相反应气(O2NO),还原剂碳烟是固体颗粒,因此很难直接跟NO发生反应,图3表明在不含氧气的条件下,NO的还原效率是非常低的,而当反应气氛包含氧气时,不仅反应温度大大降低,而且NO转化率有了很大的提高,氧气作为一种中间介质促进了碳烟颗粒与NO之间的催化反应。
Zhao等[9]的研究表明,在NO在La2NiO4上会存在2种吸附形式,负吸附态的NO-物种及正吸附态NO+物种,吸附态的NO+很容易与催化剂表面的吸附氧发生反应生成NO2,NO2比氧气具有更强的氧化能力。Lin等[10]研究发现,在反应过程中由于氧化剂的作用会生成碳氧中间体C(O),具有非常强的还原性。我们推测,在目标反应过程中,正吸附态的NO+与吸附氧反应生成强氧化性的NO2,然后NO2激活碳颗粒形成的CO*中间体,该物种具有非常强的还原性,在催化剂的作用下,不仅能与吸附在催化剂表面的氮氧化物反应,而且能与表面吸附的活泼氧种反应生成CO2。当催化剂表面的吸附氧中非常活泼时,CO*会优先跟吸附氧反应,因此会降低还原NO的选择性;当催化剂表面的吸附氧不活泼时,CO*会优先与NO反应,降低了与吸附氧反应的概率,从而提高反应的选择性。
H2-TPR结果表明,LaSrNiO4的α峰温由400 ℃升高到420 ℃,表明A位掺杂Sr会降低催化剂上吸附氧的活泼性,对比图4及表2的活性评价结果,表明掺杂Sr之后,反应的选择性从54%提高到69%;LaBaNiO4的α峰温由400 ℃降低到360 ℃,A位掺杂Ba会提高吸附氧的活泼性,对应的活性评价结果表明掺杂Ba之后,反应的选择性从54%降低到24%。因此,对La2NiO4进行A位掺杂改性,会影响到催化剂吸附氧的活泼性,进而影响目标反应的选择性。
对比H2-TPR数据及活性评价结果,B位掺杂改性的La2Ni0.5Fe0.5O4、La2Ni0.5Mn0.5O4和La2NiO4的变化主要体现在的β峰温及最适宜还原温度上。B位掺杂Fe、Sr之后,晶格氧的活泼性大大降低,NO的还原温度随之升高。推测B位改性主要会影响到La2NiO4晶格氧的活泼性,从而影响到目标反应的最适宜还原温度。对于催化反应性能与吸附氧活性间的关联上,以Lin等[10]的观点以及我们的试验结果为基础,建立了一个CO*中间体模型,解释了其选择性与吸附氧活泼性的关系;而对于催化反应性能与晶格氧活性间的关联上,试验结果表明晶格氧越活泼,催化反应的还原温度越低,晶格氧越不活泼,催化反应的还原温度越高,我们推测晶格氧的活泼性可能与该反应的诱导反应(碳激活步骤)有关,目前还不能类比吸附氧活泼性与反应选择性的关系建立一个比较系统的反应模型,暂时还停留在假设阶段,需要进一步完善,这也是我们今后的研究重点。
3 结论
La2NiO4型类钙钛矿氧化物是一种有效的同时催化还原脱除NOx和PM的催化剂,试验结果表明,氧气的存在能极大的提高反应效率,对于未掺杂改性的La2NiO4,300 ℃时NO的转化率为42%,选择性为54%;A位、B位取代会起到不同的作用,A位取代会改变催化剂上吸附氧的活泼性,从而影响到CO*中间体还原氮氧化物及吸附氧的选择性,进一步影响到目标反应的选择性,B位取代会改变催化剂上晶格氧的活泼性,从而影响到催化反应的还原温度。催化剂上不活泼的吸附氧能提高反应的选择性,活泼的晶格氧能降低还原温度,因此,对比未改性的La2NiO4催化剂,Sr掺杂改性之后催化性能有了很大的提高,在300 ℃时,NO的转化率从42%提高到64%,选择性从54%提高到69%。
参考文献:
[1]LIU J,ZHAO Z,XU C.Simultaneous removal of NOxand diesel soot particulates over nanometric La2-xKxCuO4complex oxide catalysts[J].Catal Today,2007(119):267-272
[2]YOSHIDA K,MAKINO S,SUMIYA S,etal.SAE Paper[OL].1989,http: //www.sae.org/technical/paper/892046
[3]PENG X,LIN H.A highly efficient and porous catalyst for simultaneous removal NOxand disel soot [J].Catal Commun,2007(8):157-161
[4]WANG K,QIAN L,ZHANG L,etal.Simultaneous removal of NOxand soot particulates over La0.7Ag0.3MnO3perovskite oxide catalysts[J].Catal Today,2011(158):423-426
[5]MA Z,ZHU Y,LI Z,etal.Simultaneous catalytic removal of NOxand diesel soot particulates over La2-xAxNi1-yByO4perovskite-type oxides[J].Catal Commun,2011(12):817-821
[6]TERAOKA Y,KANADA K,KAGAWA S.Synthesis of La-K-Mn-O perovskite-type oxides and their catalytic property for simultaneous removal of NOxand diesel soot particulates[J].Appl Catal B, 2001(34):73-78
[7]SHANGGUAN W F,TERAOKA Y,KAGAWA S.Simultaneous catalytic removal of NOxand diesel soot particulates over ternary AB2O4spinel-type oxides[J].Appl Catal B,1996(8):217-227
[8]SPINICCI R,TOFANARI A.Analysis of the properties of lithium-yttrium catalysts for methane coupling[J].Mater Chem phy,1997(49):110-114
[9]ZHAO Z,YANG X,WU Y.Compare study of nickel-based perovskite-like mixed oxide catalysts for direction decomposition of NO[J].Appl Catal B, 1996(8):281-297
[10]LIN H,LI Y J,SHANGGUAN W F.Soot oxidation and NOxreduction over BaAl2O4catalysts[J].Combust Flame, 2009(156):2 063-2 070
