固相法合成高电压正极材料镍铬锰酸锂*
2012-04-04刘恒徐艺林王巍
李 渊,刘恒,徐艺林,王巍
(四川大学材料科学与工程学院,四川成都610065)
固相法合成高电压正极材料镍铬锰酸锂*
李 渊,刘恒,徐艺林,王巍
(四川大学材料科学与工程学院,四川成都610065)
5 V尖晶石型LiNi0.5Mn1.5O4以其高能量密度、价格低廉、无环境污染等特点被视为最具发展潜力的锂离子电池正极材料之一。分别采用蔗糖、葡萄糖、柠檬酸3种不同碳源,通过固相混合、掺铬、球磨、高温煅烧制备出镍铬锰酸锂。通过XRD、SEM、粒度测量和电池充放电性能测试,对样品的结构、形貌、粒径、粒径分布及电性能等进行了分析。结果表明,加柠檬酸可制得粒径更细、粒径分布更窄的亚微米级的尖晶石型LiCr0.2Ni0.4Mn1.4O4,且其具有更好的电化学性能,在3.4~5.2 V、1 C下放电比容量可达149 mA·h/g,循环100次后容量保持率为98.0%。
锂离子电池;正极材料;镍铬锰酸锂;高电压
锂离子电池是20世纪90年代以后发展并得到应用的一种新型二次电池。由于具有高能量密度、长寿命、自放电小、无记忆效应以及性价比高、环境友好等优点,锂离子电池在逐步应用中已显示出巨大的优势,已广泛应用于移动电话、笔记本电脑、摄像机、数码相机、航天以及电动工具、电动汽车等各领域[1]。继钴酸锂[2]、锰酸锂[3]、磷酸铁锂[4]之后,第三代锂离子电池正极材料镍锰酸锂已经走进大家的视线。镍锰酸锂以高能量密度、价格低廉、无环境污染等特点而被视为最具发展潜力的锂离子电池正极材料之一,特别是其高充放电平台(5 V)引起人们广泛关注。高电压可使其提供更多的能量,相对于钴酸锂等更适合应用于电动车动力电池[5],然而其不足之处在于循环稳定性还不令人满意[6-7]。目前镍锰酸锂的合成方法主要有固相法[8]、燃烧法[9]及溶胶-凝胶法[10]等。笔者采用蔗糖、葡萄糖、柠檬酸3种不同碳源,通过掺铬,固相混合,高温煅烧制备出LiCr0.2Ni0.4Mn1.4O4。并对材料的结构、形貌、粒径及电性能等进行了分析。
1 实验
1.1 LiCr0.2Ni0.4Mn1.4O4的制备
按n(Li)∶n(Cr)∶n(Ni)∶n(Mn)=1.05∶0.2∶0.4∶1.4称量 LiOH·H2O(AR)、Cr2O3(AR)、NiCO3·2Ni(OH)2· 4H2O(AR)、MnCO3(AR)。将一定量的碳源(AR)与原料混合物混合,加入少量去离子水搅拌。用球磨机球磨2 h,经研磨后得到前驱体。前驱体放置于程序控温管式炉里,在空气中以2℃/min升温至900℃煅烧1 h,冷却至室温,研磨后得到镍铬锰酸锂LiCr0.2Ni0.4Mn1.4O4。未添加任何碳源所制备的样品标记为A,以蔗糖为碳源制得的样品标记为B,以葡萄糖为碳源制备的样品标记为C,以柠檬酸为碳源的样品标记为D。
1.2 LiCr0.2Ni0.4Mn1.4O4的表征
采用Philips X′Pert Pro MPD型X射线衍射仪对所合成的材料进行物相分析;使用JSM-5900 LV型扫描电子显微镜观察材料形貌和颗粒大小;通过JL-1155型激光粒度分析仪分析样品的颗粒粒径与粒度分布。
电化学性能测试采用上述正极材料制成的CR2032型纽扣电池进行。实验电池的制备方法如下:将正极活性物质(镍铬锰酸锂)和作为导电剂的乙炔黑以及作为粘结剂的聚偏氟乙烯(PVDF)按72∶17∶11的质量比混合后,加N-甲基吡咯烷酮调成正极浆料,用GM-3B小型振摆式球磨机混合均匀,涂布在厚度为0.04 mm的铝箔上,然后在真空干燥箱中100℃干燥12 h,用冲切机剪裁成直径为1.6 cm的圆片,经压制制成电池正极片。负极为圆片状金属锂(成都建中锂业有限公司生产),其直径为1.7 cm,厚度为0.1 mm。隔膜材料选用Celgard 2400PE单层膜,剪裁成直径为1.8 cm的圆片并用酒精浸泡,然后经超声波清洗除油、干燥后使用。以1.0 mol/L LiPF6的碳酸乙烯酯(EC)/碳酸二甲酯(DMC)(体积比为1∶1)溶液为电解液,在99.999%高纯氩气保护的手套箱中装配成纽扣式电池。在BTS高精度电池性能检测仪上进行恒电流充放电测试,充放电电压范围设置为3.4~5.2 V。
2 结果与讨论
2.1 表面结构与形貌分析
图1为制备的 LiCr0.2Ni0.4Mn1.4O4的 XRD衍射图。从图1可看出,4个样品在37.5°、43.6°、63.3°处均没有杂质峰出现,从而说明没有生成二次相NiO和 LixNi1-xO的杂质[11],合成了纯度较高的LiCr0.2Ni0.4Mn1.4O4样品。尖晶石型LiCr0.2Ni0.4Mn1.4O4最可能为两种结构:面心尖晶石(Fd3m)和原始简单立方晶体(P4332)。在面心尖晶石结构中,锂离子占据8a位置,镍锰离子占据16d位置,氧离子占据32e位置。在原始简单立方晶体中,锰离子占据12d位置,镍离子占据4a位置,氧离子占据24e以及伴随着锂离子占据8c的位置[12]。难以从XRD谱图辨别为哪种结构。在Fd3m中Mn3+和Mn4+同时存在,而在P4332中只有Mn4+[13]。从后面的充放电曲线中可以发现,在4.1 V左右有一个关于Mn3+/Mn4+的充放电平台,因此可以推断出LiCr0.2Ni0.4Mn1.4O4为面心尖晶石结构。表1为XRD分析所制得样品的相关参数,样品A、B、C、D的晶胞参数与标准LiNi0.5Mn1.5O4的晶胞参数(0.817 0 nm)相近。
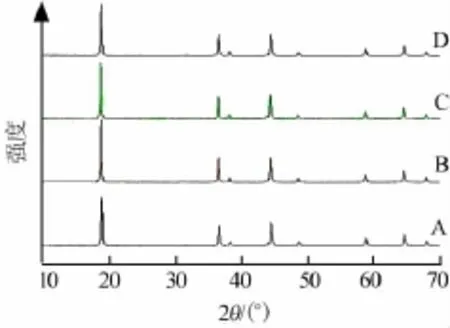
图1 LiCr0.2Ni0.4Mn1.4O4的XRD衍射图

表1 Jade软件计算出的样品参数

图2 样品的SEM图
图2为LiCr0.2Ni0.4Mn1.4O4的SEM图。由图2可以看出,样品呈棱角分明的颗粒状,晶型完整,颗粒形状比较规则,颗粒尺寸较小,为亚微米级。亚微米的材料往往集合了纳米颗粒(能承受高倍率)和微米颗粒(容量高、低倍率循环性能好)的优点[14]。其中,样品A、C有少量较粗颗粒,粒径分布不均,样品B、C有部分团聚。样品D的颗粒最为细小,粒径及分布较均匀。小的颗粒尺寸将有利于锂离子在固相电极中的扩散。4种样品的激光粒度分布如图3所示。由图3可知,样品A、C的平均粒径分别为0.765 μm和0.679 μm,粒度分布较宽;样品B的平均粒径为0.643 μm;样品D的平均粒径为0.624 μm,颗粒粒度分布几乎均在0.1~3 μm内,分布较窄。与图2结果基本吻合。可见碳源对合成样品的颗粒尺寸以及粒度分布起着重要影响。在原料混合的初级阶段,碳源主要起着分散作用,促使干燥后的前驱体原料颗粒更细且混合更加均匀;其次,在煅烧过程中产生的气体在晶粒间形成的空间位阻可防止产物晶粒尺寸过分长大。不同的碳源作用效果不一,柠檬酸优于葡萄糖及蔗糖。
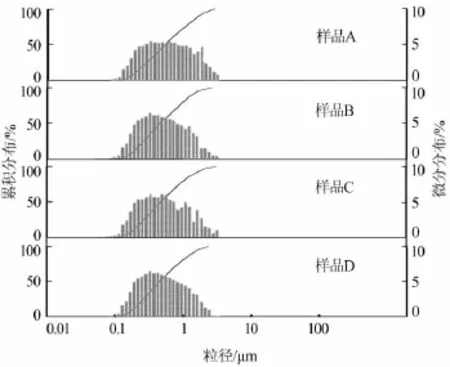
图3 样品的激光粒度测试图
2.2 电化学性能测试
在 3.4~5.2 V,LiCr0.2Ni0.4Mn1.4O4在 0.5 C充电和1 C放电的曲线见图4。图4显示,LiCr0.2Ni0.4Mn1.4O4有3个放电平台。第一个在4.1 V左右,对应Mn3+/ Mn4+的氧化还原反应;另两个平台分别在4.7 V和 4.8 V,涉及的氧化还原反应分别为Ni2+/Ni4+和Cr3+/ Cr4+。

图4 LiCr0.2Ni0.4Mn1.4O4在0.5 C充电和1 C放电的曲线
图5为LiCr0.2Ni0.4Mn1.4O4在3.4~5.2 V的循环性能测试图。由图5可知,样品A在1 C下放电比容量为 125 mA·h/g,循环 100次后容量保持率为96.0%。样品B在1C下放电比容量可达132mA·h/g,循环100次后容量保持率为93.9%。样品C在1 C下放电比容量可达137 mA·h/g,100次后容量保持率为94.5%。样品D在1 C下放电比容量可达149 mA·h/g,100次后容量保持率为98.0%。样品均有十分优异的循环稳定性,衰减甚微。添加碳源后,样品的电化学性能有所提升。不同碳源对产物的电化学性能影响有差异:当碳源为蔗糖及葡萄糖时,电化学性能提升有限,采用柠檬酸为碳源时所制得样品的颗粒尺寸更为细小,粒度分布较均匀,有效地缩短了锂离子和电子的扩散路径,减少了大电流条件下的极化,从而使其拥有良好的电化学性能。

图5 LiCr0.2Ni0.4Mn1.4O4循环性能测试图
3 结论
以 LiOH·H2O、Cr2O3、NiCO3·2Ni(OH)2·4H2O、MnCO3为原料,不同碳源为添加剂,通过固相球磨、高温煅烧制备出尖晶石型LiCr0.2Ni0.4Mn1.4O4。碳源在前驱体的制备过程中起着分散剂的作用,使原料混合更均匀;高温煅烧时其产生的空间位阻有利于获得晶粒细小的LiCr0.2Ni0.4Mn1.4O4。采用柠檬酸为碳源时,样品性能最佳:1 C放电比容量可达到149 mA·h/g,循环100次后容量保持率为98.0%。该方法步骤简单,制备时间短,能耗低,易于工业化生产。
[1] 赵灵智,汝强.锂离子电池材料的研究现状[J].广州化工,2009,37(4):3-14.
[2] Shukla A K,Kumar T P.Materials for next-generation lithium batteries[J].Current Science,2008,94(3):314-331.
[3] Tarascon J M,Mckinnon W R,Coowar F,et al.Synthesis conditions and oxygen stoichiometry effects on Li insertion into the spinel LiMn2O4[J].J.Electrochem.Soc.,1994,141(6):1421-1431.
[4] TajimiS,IkedaY,UematsuK.Enhancedelectrochemicalperformance ofLiFePO4prepared by hydrothermal reaction[J].Solid State Ionics,2004,175(1/2/3/4):287-290.
[5] LinChih-Yuan,DuhJenq-Gong,HsuChia-Haw,etal.LiNi0.5Mn1.5O4cathode material by low-temperature solid-stat62e method with excellent cycleability in lithium ion battery[J].Materials Letters,2010,64(21):2328-2330.
[6] Arunkumar T A,Manthiram A.Influence of chromium doping on the electrochemical performance of the 5 V spinel cathode LiMn1.5Ni0.5O4[J].Electrochim.Acta,2005,50(28):5568-5572.
[7] Liu G Q,Wen L,Liu G Y,et al.Rate capability of spinel LiCr0.1Ni0.4Mn1.5O4[J].Journal of Alloys and Compounds,2010,501(2):233-235.
[8] 季勇,王志兴,尹周澜,等.正极材料LiNi0.5Mn1.5O4的合成及性能[J].无机化学学报,2007,23(4):597-601.
[9] Aklalouch M,Amarilla J,Rojas R,et al.Chromium doping as a new approach to improve the cycling performance at high temperature of 5 V LiNi0.5Mn1.5O4-based positive electrode[J].Journal of Power Sources,2008,185(1):501-511.
[10] Hong Ki-Joo,Sun Yang-Kook.Synthesis and electrochemical characteristics of LiCrXNi0.5-XMn1.5O4spinel as 5 V cathode materials for lithium secondary batteries[J].Journal of Power Sources,2002,109(2):427-430.
[11] 刘国强,其鲁,闻雷.锂离子电池正极材料LiNixMn2-xO4的制备和电化学性能研究[J].稀有金属材料与工程,2006,35(2):299-302.
[12] Yi Tingfeng,Shu Jie,Zhu Yanrong,et al.Advanced electrochemical performance of LiMn1.4Cr0.2Ni0.4O4as 5 V cathode material by citricacid-assisted method[J].Journal of Physics and Chemistry of Solids,2009,70(1):153-158.
[13] Yang Tongyong,Sun Kening,Lei Zhengyu,et al.The influence of holding time on the performance of LiNi0.5Mn1.5O4cathode for lithium ion battery[J].Journal of Alloys and Compounds,2010,502(1):215-219.
[14] Arrebola J C,Caballero A,Hernán L,et al.PMMA-assisted synthesis of Li1-xNi0.5Mn1.5O4-δfor high-voltage lithium batteries with expanded rate capability at high cycling temperatures[J].Journal of Power Sources,2008,180(2):852-858.
Synthesis of high-voltage cathode material LiCr0.2Ni0.4Mn1.4O4by solid method
Li Yuan,Liu Heng,Xu Yilin,Wang Wei
(School of Materials Science and Engineering,Sichuan University,Chengdu 610065,China)
5 V spinel LiNi0.5Mn1.5O4is one of the most potential cathode materials for lithium-ion batteries because of its advantages of high energy density,low cost,and no pollution to the environment etc.Different carbon sources,such as sucrose,glucose,and citric acid,were adopted respectively as first,and then LiCr0.2Ni0.4Mn1.4O4was prepared by solid mixture,doping chromium,ball milling,and high temperature calcination.Structure,morphology,particle size,particle size distribution,and electrical performance of the samples were analyzed by XRD,EM,particle size measurement and constant current charge-discharge cycling test.Results showed that submicron spinel LiCr0.2Ni0.4Mn1.4O4with thinner particle size,narrower size distribution,and better electrical performance was obtained when glucose was added.Specific capacity of LiCr0.2Ni0.4Mn1.4O4cathode material was 149 mA·h/g charged at 3.4~5.2 V and 1 C and retained 98%of the initial capacity after 100 cycles.
lithium-ion batteries;cathode material;LiCr0.2Ni0.4Mn1.4O4;high-voltage
TQ131.11
:A
:1006-4990(2012)04-0055-04
2011-10-28
李渊(1986—),男,硕士研究生,研究方向为锂离子电池技术,已发表文章3篇。
国家科技支撑计划(2007BAE58B07)。
联系人:刘恒
联系方式:h_liu@scu.edu.cn
