磷石膏的净化处理及制备硫酸钙晶须的研究
2012-04-04杨荣华宋锡高
杨荣华,宋锡高
(1.泰山医学院化工学院,山东泰安271016;2.贵州瓮福剑峰化工股份有限公司)
环境·健康·安全
磷石膏的净化处理及制备硫酸钙晶须的研究
杨荣华1,宋锡高2
(1.泰山医学院化工学院,山东泰安271016;2.贵州瓮福剑峰化工股份有限公司)
实验研究磷石膏净化处理方法及化工综合利用新路。在对磷石膏样品进行粒度分布、XRD矿物分析、化学成分分析和SEM形貌分析等物性检测的基础上,利用廉价的碳酸氢铵和氨水及工业副产盐酸,对磷石膏进行净化处理,去除杂质提纯得到硫酸钙,副产氯化铵并回收二氧化碳。以磷石膏提纯得到的硫酸钙为原料,采用水热法制备硫酸钙晶须,提升磷石膏的利用价值。实验得到磷石膏净化处理和水热法制备硫酸钙晶须的最优化工艺条件,并通过POM与SEM对所得硫酸钙样品和硫酸钙晶须进行形貌分析。结果表明,工艺路线在技术上是可行的,工艺设备和操作条件简单、母液可循环使用、无三废污染,既减轻了环境污染,又降低了生产成本,具有较好的经济效益和社会效益。
磷石膏;净化处理;硫酸钙晶须;水热合成法
磷石膏是湿法磷酸生产中排出的以二水硫酸钙为主要成分,含有少量未分解的磷矿以及未洗涤干净的磷酸、氟化钙、铁等多种杂质的废渣。通常每生产1 t P2O5可产生4.5~5.0 t磷石膏。据统计,2007年世界磷石膏的排放量约5亿t,中国约为3 000万t。磷石膏的长期堆放不仅污染环境,而且占据大量土地,磷石膏的处理及综合利用已成为全球性问题[1]。由于硫酸钙的溶解度小且不易分离的缘故,迄今世界磷石膏平均利用率只有2%~3%,中国为3%~6%。当前,磷石膏主要应用在以下几个方面:作水泥缓凝剂;作石膏建材;制硫酸联产水泥;作土壤改良剂;制硫酸铵;制硫酸钾。笔者以贵州瓮福剑峰化工股份有限公司提供的磷石膏样品为原料,研究磷石膏净化处理方法及化工综合利用新路。
1 磷石膏样品的物性检测与分析
1.1 粒度分析
按照GB/T 5484—2000石膏化学分析方法,将样品于45℃烘干,去除吸附水后进行粒度分析,用孔径为180 μm的标准筛进行筛分,筛上粗颗粒用标准套筛分析,筛下物料用激光粒度分布仪进行检测,分析结果见表1。
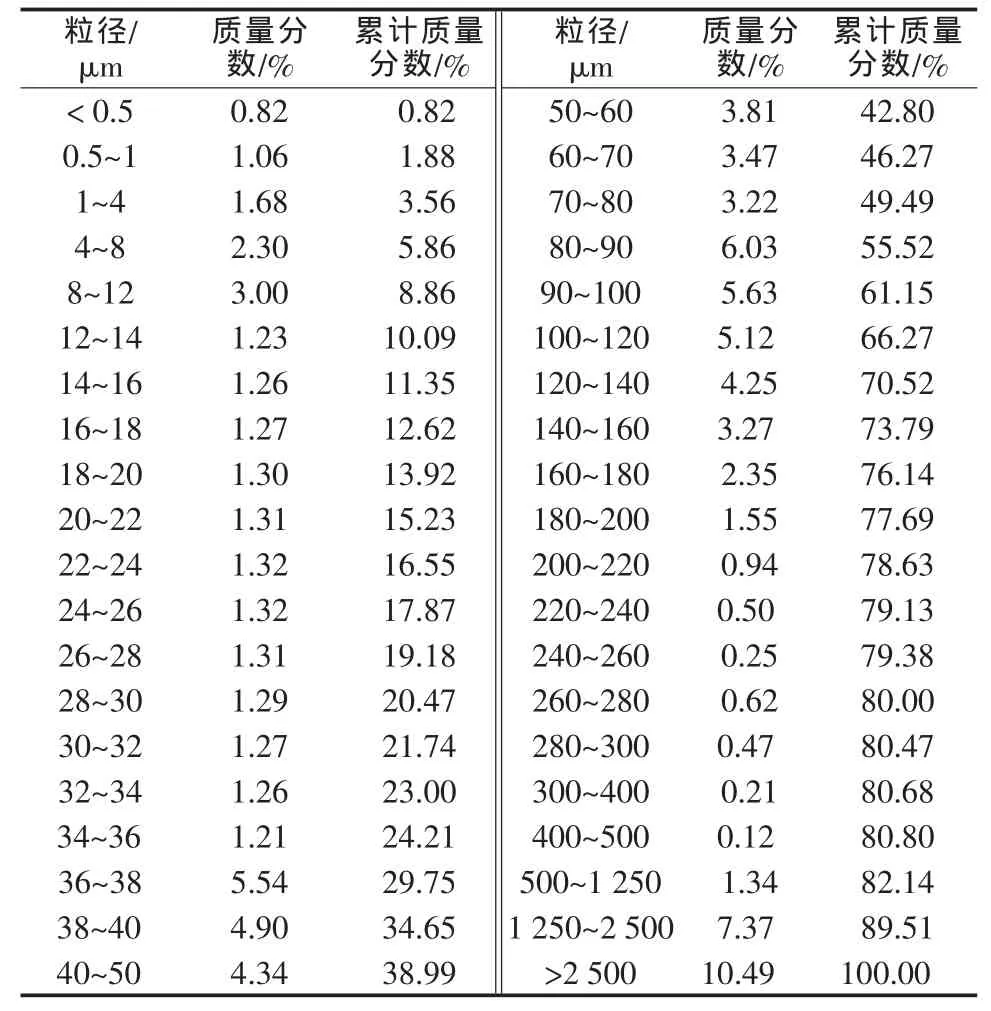
表1 磷石膏样品的粒度分析结果
粒度分析结果表明,磷石膏样品粒度分布主要集中在36~200 μm(质量分数为53.48%),60 μm以上粗颗粒质量分数为57.2%,粒度大于0.5 mm大颗粒和料块质量分数为19.2%。
1.2 XRD矿物分析
采用D/MAX2500型X射线衍射分析仪对样品进行XRD分析,结果见图1。由图1可知,磷石膏样品的主晶相是CaSO4·2H2O,含有一定量的SiO2。

图1 磷石膏样品的XRD谱图
1.3 化学成分分析
采用X射线荧光分析仪对样品进行化学成分分析。对于样品中的结晶水和吸附水分别按照石膏化学分析方法GB/T 5484—2000中规定方法进行,将物料精确称量后在45℃±3℃烘干至恒重,计算吸附水;然后将物料在230℃±5℃烘干至恒重,计算结晶水。将X射线荧光分析结果与水分析结果折合得到样品的化学组成。磷石膏样品的X射线荧光分析结果见表2,吸附水和结晶水分析结果见表3。

表2 磷石膏样品的化学成分 %
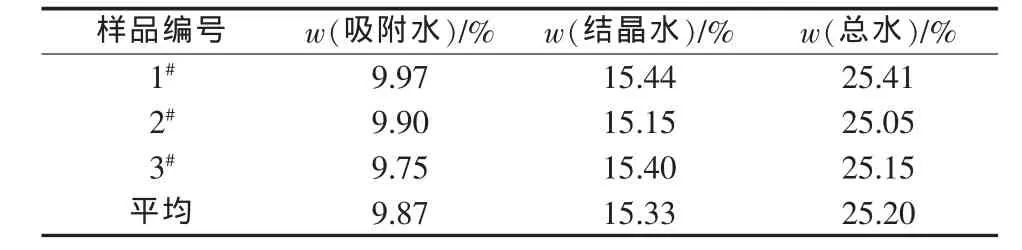
表3 磷石膏样品的水分析结果
分析结果表明,磷石膏样品中SO3和CaO的质量分数为89.12%,纯度较高;含吸附水9.87%,结晶水为15.33%;样品主要杂质为SiO2和F、P、Fe等成分。
1.4 SEM形貌分析
采用SEM对磷石膏样品进行形貌分析,SEM显微照片如图2所示。由图2可见,样品中磷石膏主要以板状或条状的聚集体形态存在,晶形规则,结晶度较好,大多数聚集体上都附着有细小板状颗粒。

图2 磷石膏样品的SEM照片
2 磷石膏净化处理提纯制硫酸钙
2.1 磷石膏净化处理方法原理
根据化学反应原理,将磷石膏中的CaSO4·2H2O与其他化学试剂反应,经过一系列化学反应得到纯硫酸钙,而将磷石膏中杂质留在残渣中。其反应原理为:
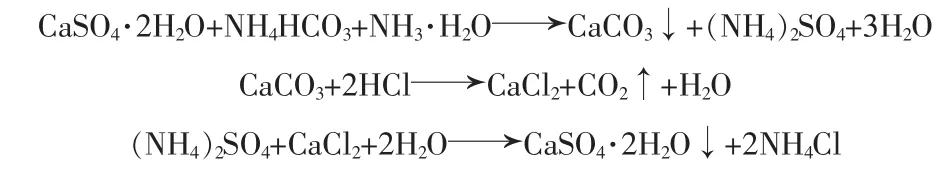
该方法可利用廉价的碳酸氢铵和氨水及工业副产盐酸,将磷石膏中的CaSO4提纯出来,从而去除杂质,达到磷石膏的净化处理和提纯,并能副产氯化铵和回收CO2。
2.2 磷石膏净化处理工艺过程
磷石膏净化处理的工艺过程如图3所示。
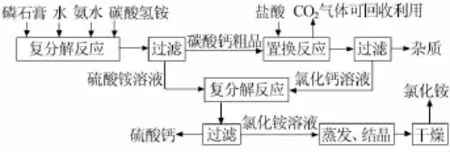
图3 磷石膏净化处理的工艺过程示意图
磷石膏先经漂洗去除部分杂质,然后将适量磷石膏及循环溶液(或水)加入反应器中,开动搅拌并加热到一定温度,按配比分批加入碳酸氢铵与氨水,搅拌反应一定时间后真空抽滤,得到硫酸铵溶液;所得滤饼经洗涤、干燥,得到副产品碳酸钙粗品,洗液返回反应器循环使用。用工业副产盐酸处理碳酸钙粗品,反应结束后经过滤去除杂质得到氯化钙溶液,反应过程产生的CO2气体可回收利用。将上述所得硫酸铵溶液与氯化钙溶液根据其浓度按照一定比例混合反应,经过滤得到固体硫酸钙及氯化铵溶液,氯化铵溶液经蒸发、结晶和干燥后得到产品氯化铵[2]。
2.3 产物浓度的分析检测方法
磷石膏净化处理过程所得各种产物的分析检测方法按照国家标准进行。溶液成分的检测方法如下:NH,采用甲醛法;SO,采用硫酸钡法;Ca2+,采用EDTA法;Cl-,硝酸银法。以硫酸铵溶液中SO的浓度计算天然石膏中硫酸钙的转化率X, 以X评价反应结果和界定复分解反应的工艺条件;以氯化钙母液中Ca2+的质量计算碳酸钙粗品Ca2+的转化率XCaO,以XCaO界定置换反应的工艺条件。以硫酸铵溶液中SO的浓度和氯化钙溶液Ca2+的浓度为基础确定硫酸铵和氯化钙反应的工艺条件,采用POM与SEM对所得硫酸钙样品进行形貌分析。
2.4 影响因素分析及工艺条件的确定
磷石膏与碳酸氢铵和氨水的反应是吸热反应,升高温度加快反应速度,有利于提高SO的转化率,但是温度太高易造成碳酸氢铵的分解及氨水的挥发,影响反应效果,反应温度宜控制在60℃以下。该反应是伴有传递过程的液固相反应,反应结果受到反应物的传递过程和液固接触面积的影响。由于NH的作用,磷石膏中的硫酸钙分子较易从固相进入液相进行反应,因而溶液中NH的浓度对X的影响较大[3-5],采取碳酸氢铵和氨水稍过量的方法,有利于转化率的提高;但过量后反应溶液中逸出的游离氨会影响工作环境。加强搅拌有助于扩散与加快反应速度,但搅拌速度过高时却容易诱发晶核的形成,导致生成细小的CaCO3结晶,不利于过滤,搅拌速度以300~600 r/min为宜。液固比的大小直接影响反应后的(NH4)2SO4的浓度,液固比太大,生成的硫酸铵浓度太低,不利于后续反应进行;液固比太小,溶液浓度高,黏性大,反应生成的CaCO3固体所吸附的(NH4)2SO4较难洗出,导致(NH4)2SO4收率下降,以液固比为1.4~1.6 mL/g为宜,以控制硫酸铵的浓度。
通过单因素实验和正交试验,在一定条件下考察反应温度、反应时间、配料比(NH4HCO3、NH3·H2O与CaSO4·2H2O的物质的量比)、液固比等因素对X的影响,寻找适宜的反应条件。实验结果表明,最适宜工艺条件为:反应温度为45℃,反应时间为1~2 h,配料比为1.1∶1.2∶1,液固比为1.4 mL/g。在此条件下进行反应,X可达77.6%以上,母液中硫酸铵质量分数为33%~36%,副产品碳酸钙的纯度在85%以上。
碳酸钙与盐酸反应得到氯化钙的反应中,影响氯化钙质量的主要因素包括碳酸钙纯度、盐酸浓度、配料比(HCl和CaCO3的物质的量比)、反应温度、反应时间等。实验证明,盐酸的浓度控制在2.5 mol/L左右,利于反应的顺利进行,浓度过低则后续工序能耗高。由于反应剧烈放热,并产生大量的CO2气体,反应中盐酸有部分损失,盐酸应稍微过量;同时碳酸钙粉末应分批投入,以反应平稳进行为宜,以防止反应液溢出反应器,减少盐酸的损失。反应结束后加入硫化物沉淀剂,使重金属离子沉淀完全[6]。在一定实验条件下考察反应温度、反应时间、配料比和盐酸浓度对XCaO的影响。实验结果表明,反应温度、反应时间和盐酸浓度对XCaO的影响较小,影响XCaO的主要因素是配料比。该反应适宜的工艺条件为:反应温度为20~30℃,反应时间为20~30 min,盐酸浓度为2.5 mol/L,配料比为2.5∶1。在上述条件下进行反应,反应结束后经过滤去除不溶性杂质,XCaO可达98.7%左右。
硫酸铵与氯化钙的反应较易进行,上述反应得到的硫酸铵溶液和氯化钙溶液,根据分析测量的浓度,按照理论配比,在常温下搅拌反应30 min左右即可。所得硫酸钙样品的POM与SEM照片如图4所示。

图4 磷石膏净化提纯所得硫酸钙样品的POM与SEM照片
3 硫酸钙晶须的制备
将磷石膏净化除杂后提纯得到的硫酸钙,采用水热法制备硫酸钙晶须[7]。将硫酸钙与水按照一定的比例加入10 L高压釜中,充分搅拌并调节pH,在一定温度下加热水合反应,反应结束后趁热过滤,脱水、干燥,得到硫酸钙晶须。
采用单因素分析考察物料配比、反应温度、反应时间、初始pH等因素对硫酸钙晶须的影响,通过正交实验选择最佳工艺条件,以电镜作为分析硫酸钙晶须形貌的手段,得出硫酸钙晶须的最优化工艺条件为:反应温度为120℃、料浆初始pH为8.0~10.0、料浆质量分数为4%~5%、反应时间为1.5~2.0 h。在此条件下,制备出了平均直径为0.8 μm、长径比为90~100的硫酸钙晶须产品。将所得硫酸钙晶须在680℃的马弗炉中高温处理后,用POM与SEM进行形貌分析,结果如图5所示。

图5 硫酸钙晶须的POM与SEM照片
4 结论
本实验的工艺路线在技术上是可行的。该工艺简化和粗放了磷石膏转化的工艺设备和操作条件,能耗低、成本低、产品质量好、易于工业化,为磷石膏处理和综合利用开辟了一个新思路。母液循环使用,无三废污染,既减轻了环境污染又降低了生产成本,具有较好的经济效益和社会效益。另外本工艺第一步所得的硫酸铵也可作为肥料及原料出售,具有较大的经营弹性。
[1] 吕庆胜,俞春明.云南磷肥厂引进1.2万t/a“曼海姆炉法”硫酸钾装置的技术、经济特点及生产、改造情况[J].化肥工业,1994(2):43-47.
[2] HG/T 2327—1992工业氯化钙[S].
[3] 张兴法,陈祥迎.液-固相反应薄片颗粒的宏观动力学[J].合肥工业大学学报:自然科学版,2000,23(4):518-521.
[4] Fernandez Lozano J A,Wint A.Double decomposition of gypsum and potassium chloride catalysed by aqueous ammonia[J].The Chemical Engineering Journal,1982,23(1):53-61.
[5] 卢芳仪,刘晓红,孙日圣,等.两步法磷石膏制硫酸钾工艺的改进[J].硫酸工业,2000(3):47-49.
[6] 张兴法,刘守强,陈敏.用磷石膏制备硫酸铵和氯化钙的研究[J].合肥工业大学学报:自然科学版,2002(1):67-70.
[7] 杨荣华,吴秀勇,冯晓宁.用天然石膏制备硫酸钙晶须的研究[J].无机盐工业,2010,42(1):44-47.
联系方式:rhyang@yeah.net
Research on purification of phosphogypsum and preparation of calcium sulfate whisker
Yang Ronghua1,Song Xigao2
(1.School of Chemical Engineering,Taishan Medical University,Taian 271016,China;2.Guizhou W engfu Jianfeng Chemical Co.,Ltd.)
New methods of purification and comprehensive utilization of phosphogypsum were experimentally studied.On the basis of physical testing of phosphogypsum samples,including particle size distribution,XRD mineral analysis,chemical analysis,and SEM morphology analysis,phosphogypsum was treated with low-cost ammonium bicarbonate,ammonia,and industrial by-product hydrochloric acid,and calcium sulfate(CaSO4)was obtained by removing impurities.Meanwhile,by-product ammonium chloride was also got and carbon dioxide could be recovered.Then CaSO4was applied as raw material to prepare calcium sulfate whisker by hydrothermal method,so as to enhance the application value of phosphogypsum.Optimal conditions of phosphogypsum purification and hydrothermal method of calcium sulfate whisker were obtained by experiments,the morphologies of calcium sulfate and calcium sulfate whisker were analyzed by POM and SEM.Results showed that the experimental process route was technically feasible,the process equipment and operating conditions were simple,the mother liquor could be recycled,no‘three waste’pollution,so it not only reduced environmental pollution,but also cut down the production costs.Therefore,it had good economic and social benefits.
phosphogypsum;purification;calcium sulfate whisker;hydrothermal method
TQ132.32
:A
:1006-4990(2012)04-0031-04
2011-10-18
杨荣华(1965—),男,副教授,硕士,从事化工专业教学及科研工作,已发表论文20余篇。
