白云石制备高纯氧化镁的工艺研究
2012-04-04聂鹏飞徐春和徐旺生
张 华,聂鹏飞,徐春和,徐旺生
(1.武汉工程大学化工与制药学院,绿色化工过程省部共建教育部重点实验室,湖北武汉430073;2.云南磷化集团科工贸有限公司)
白云石制备高纯氧化镁的工艺研究
张 华1,聂鹏飞2,徐春和1,徐旺生1
(1.武汉工程大学化工与制药学院,绿色化工过程省部共建教育部重点实验室,湖北武汉430073;2.云南磷化集团科工贸有限公司)
以白云石为原料,通过煅烧、消化、硫酸酸浸、过滤得硫酸镁溶液,采用氨水沉淀法制备氢氧化镁中间体,经煅烧得高纯氧化镁。研究了加入硫酸后白云石灰乳终点pH、反应温度、硫酸镁浓度和煅烧温度对镁的浸出率、沉淀率以及产品氧化镁纯度的影响,最终确定最佳工艺条件为:灰乳终点pH为6,反应温度为40℃,硫酸镁浓度为0.8 mol/L,煅烧温度为900℃。在此条件下制备的氧化镁纯度达到99.0%以上,满足高纯氧化镁的要求。
白云石;氢氧化镁;高纯氧化镁
氧化镁作为一种重要的无机化工产品,用途非常广泛,主要用于耐火材料和提炼金属镁,也用于纸浆、提铀、建筑材料、肥料、橡胶、塑料和粘合剂等[1]。高纯氧化镁一般指w(MgO)≥98%的产品,由于产品纯度高,使相应行业(如冶金、橡胶、电子等行业)的产品质量也得到提升[2]。高纯氧化镁的开发及实现工业化,将对电子、国防、航天及高级陶瓷等行业的发展起到极大的促进作用[3]。中国普通级别氧化镁产品产量很大,大量出口,市场疲软;而高纯氧化镁、活性氧化镁、硅钢氧化镁等一些精细氧化镁市场需求较大,产品大量进口。以w(MgO)≥99.0%的高纯氧化镁为例,国内仅有河南兴发镁业工业化生产,而国内每年的需求量约10万t,大量仍依靠进口,市场前景广阔[4]。所以促进镁业的结构调整,加快中国镁盐精细产品的研究开发,生产高质量氧化镁产品已成为当务之急。目前以白云石为原料生产氧化镁的方法有:碳化法、酸浸法、铵浸法。碳化法对钙镁分离不彻底,且对设备要求高;酸浸法成本高;铵浸法容易造成环境污染等。笔者以廉价的白云石为原料,成功制备纯度大于99.0%的高纯氧化镁,研究出制备高纯氧化镁的最佳工艺条件。该工艺简单,重复性良好,在工业生产中有很大的发展前景。
1 实验部分
1.1 实验原料
采用湖北蕲春的白云石为原料,主要成分:w(CaO)=32.50%,w(MgO)=20.58%,w(Fe2O3)=2.18%,w(SiO2)=0.96%,灼烧失量=43.78%。
1.2 实验原理
白云石在1 000℃煅烧后,在80~90℃下消化得白云石灰乳,主要成分为Ca(OH)2、Mg(OH)2和一些不溶于水的杂质氧化物(氧化铁、氧化硅等)。加入硫酸控制适宜pH,Ca(OH)2先与硫酸反应生成微溶于水的CaSO4,当Ca(OH)2反应完全后,Mg(OH)2再与硫酸反应生成溶解度较大的MgSO4,当终点pH不是太低时,杂质氧化物基本不溶解,这样可以实现杂质(如铁、锰)的分离。将加入硫酸后的白云石灰乳过滤,可得含少量CaSO4的MgSO4溶液,少量CaSO4在溶液中以Ca2+和SO形式存在,在适宜条件下用氨水作为镁的沉淀剂,Ca2+不与氨水发生沉淀反应,在镁沉淀后,用大量水洗涤即可除去少量Ca2+。将所得氢氧化镁沉淀煅烧即可制得高纯氧化镁,主要化学反应如下:
1.3 实验方法
1.3.1 工艺流程(见图1)

图1 白云石制备高纯度氧化镁的工艺流程图
1.3.2 分析方法
产品中氧化镁含量以及杂质钙含量采用EDTA络合滴定法测定。
2 结果与讨论
2.1终点pH对镁的浸出率和产品纯度的影响
在反应温度为40℃、MgSO4浓度为0.8 mol/L、煅烧温度为900℃、煅烧时间为2 h条件下,终点pH对镁的浸出率和产品纯度的影响如图2所示。由图2可看出,随加入硫酸后终点pH的上升,镁的浸出率逐渐下降,当pH不高于6时,镁的浸出率都能达到95.0%。主要原因是:Ca(OH)2是强碱,而Mg(OH)2是弱碱,加入的硫酸首先是和白云石灰乳中的Ca(OH)2反应,只有当Ca(OH)2反应完全后,灰乳中的Mg(OH)2才开始和硫酸反应。当加入的硫酸量不够时,就会使部分Mg(OH)2没有与硫酸反应而残留在滤饼中,最终影响镁的浸出率。随终点pH的上升,产品氧化镁的纯度逐渐上升。当pH≥6时,产品氧化镁的纯度都能达到99.0%。初步推测其原因是:当pH太低时,灰乳中的杂质氧化物会部分溶解而进入硫酸镁溶液,最终导致无法除去而影响产品氧化镁的纯度。本实验确定加入硫酸控制终点pH为6。

图2 终点pH对镁的浸出率和产品纯度的影响
2.2 反应温度对产品纯度的影响
反应温度是化学反应、晶核形成及晶体生长的重要影响因素。温度的改变,同样会引起溶液中的沉淀粒子过饱和度的改变,因此反应温度不仅决定反应速度的大小,而且对生成物晶核的形成与生长起着重要作用[5]。在控制终点pH为6、硫酸镁浓度为0.8 mol/L、煅烧温度为900℃、煅烧时间为2 h时,沉淀反应温度对产品纯度的影响如图3所示。由图3可看出,随着温度的上升,产品氧化镁纯度也逐渐升高,温度在40℃时,氧化镁的纯度达到最大值。原因可能是:温度过低,溶液容易达到过饱和状态,形成的氢氧化镁颗粒小,甚至凝胶化,从而吸附包裹大量杂质离子,使产品纯度下降[6];但是反应温度过高,会使晶核的生长和生成都比较快,这会导致一些杂质没有及时溶解而产生包夹现象,最终影响产品纯度,且温度过高,会加大沉淀剂氨水的挥发,导致操作环境恶化。本实验将反应温度定为40℃。

图3 反应温度对氧化镁纯度的影响
2.3 硫酸镁浓度对镁沉淀率和产品纯度的影响
在控制终点pH为6、反应温度为40℃、煅烧温度为900℃、煅烧时间为2 h时,将滤液浓缩成各种浓度的硫酸镁溶液,硫酸镁溶液浓度对镁离子沉淀率和产品纯度的影响见图4。由图4看出,随硫酸镁溶液浓度的增加,镁离子的沉淀率先增大后减小,在硫酸镁浓度为0.8 mol/L时,镁离子的沉淀率达到最大值。硫酸镁浓度从0.4 mol/L上升到0.8 mol/L,镁离子的沉淀率逐渐增大,主要原因可以用化学平衡原理解释,即反应物浓度高,有利于反应向右进行;而硫酸镁浓度从0.8 mol/L上升到1.5 mol/L,镁离子的沉淀率逐渐降低,原因是随着反应的不断进行,溶液中(NH4)2SO4的浓度不断增加,而(NH4)2SO4与NH3·H2O是共轭酸碱对,最终反应液中形成了(NH4)2SO4-NH3·H2O的缓冲体系,随着(NH4)2SO4浓度越来越高,反应液pH逐渐降低,当反应液的pH低于Mg2+的沉淀pH时,镁离子的沉淀反应就会结束,所以,当镁离子的浓度较高时,镁离子的最终沉淀率只与反应液中(NH4)2SO4的浓度有关。随硫酸镁浓度的增加,产品纯度逐渐降低,主要原因是:浓度高,生成的氢氧化镁粒子细小,呈现胶体状态,难以过滤,且浓度越高生成的沉淀越容易团聚,会包裹大量杂质,造成洗涤困难,最终影响产品纯度[7]。为了保证产品氧化镁的纯度以及提高白云石中镁的综合利用率,本实验将硫酸镁的浓度定为0.8 mol/L。
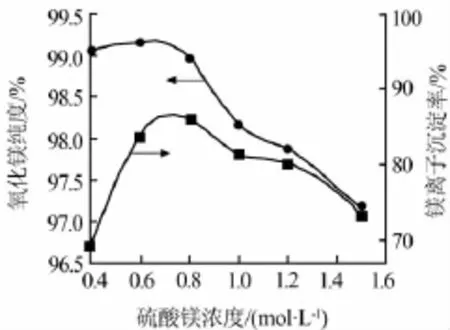
图4 硫酸镁溶液浓度对镁离子沉淀率和产品纯度的影响
2.4 煅烧温度对产品纯度的影响
在控制终点pH为6、反应温度为40℃、硫酸镁浓度为0.8 mol/L、煅烧时间为2 h时,煅烧温度对产品氧化镁纯度的影响如图5所示。由图5可看出,煅烧温度越高,产品氧化镁的纯度也越高,当温度达到800℃后,再升高温度产品氧化镁的纯度基本保持不变。煅烧温度太低,导致前驱体氢氧化镁分解不完全,为了使氢氧化镁分解完全,应在较高的温度下煅烧,且煅烧温度高,有利于一些杂质离子如SO的分解[8]。本实验将煅烧温度定为900℃。
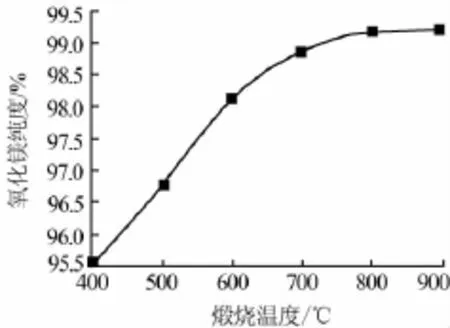
图5 煅烧温度对氧化镁纯度的影响
3 结论
以白云石为原料制备高纯氧化镁的工艺,其优点在于:通过控制H2SO4酸浸液pH,能够分离钙并除去大部分杂质如铁、锰,得到高纯度的产品氧化镁,并且使镁离子有较高的浸出率。制备高纯度氧化镁的最佳工艺条件为:控制H2SO4酸浸后终点pH为6、反应温度为40℃、硫酸镁浓度为0.8 mol/L、煅烧温度为900℃,在此条件下制得的氧化镁纯度在99.0%以上,原料白云石中镁的总利用率在80%以上。该工艺流程简单,重复性好,有很大的发展前景。
[1] 徐徽,蔡勇,石西昌,等.水镁石制取高纯氧化镁的研究[J].湖南师范大学自然科学学报,2006,29(1):52-55.
[2] Halmann M,Frei A,Steinfeld A.Magnesium production by the pidgeon process involving dolomite calcination and MgO silicothermic reduction:thermodynamic and environmental analyses[J].Ind.Eng.Chem.Res.,2008,47(7):2146-2154.
[3] 王亚芳,仲剑初,王洪志.制备高纯氧化镁的工艺研究[J].无机盐工业,2006,38(5):30-33.
[4] 陈侠,陈丽芳.用六水氯化镁工业化生产高纯氧化镁的新工艺[J].盐业与化工,2008,37(3):13-16.
[5] 颜文斌,石爱华,高峰,等.轻烧菱镁矿制备高纯纳米氧化镁[J].硅酸盐学报,2010,38(1):110-113.
[6] 宋长友,崔江丽.高纯氧化镁的制备研究[J].化工矿物与加工,2010(2):11-13.
[7] 任爽,王小娟,武艳妮,等.卤水-白云石法制备纳米氧化镁的研究[J].无机盐工业,2010,42(4):30-32.
[8] Alvarado E,Torres-Martinez L M,Fuentes A F,et al.Preparation and characterization of MgO powders obtained from different magnesium salts and the mineral dolomite[J].Polyhedron,2000,19(22/23):2345-2351.
联系人:徐旺生
联系方式:huazi123209@163.com
Preparation of high purity magnesium oxide from dolomite
Zhang Hua1,Nie Pengfei2,Xu Chunhe1,Xu Wangsheng1
(1.Key Laboratory for Green Chemical Process of Ministry of Education,School of Chemical Engneering and Pharmacy,Wuhan Institute of Technology,Wuhan 430073,China;2.Yunnan Phosphate Chemical Group Industry and Trade Co.,Ltd.)
Magnesium sulfate solution can be obtained from dolomite via the processes of calcination,digestion,acid leaching,and filtration.Using NH3·H2O as precipitating agent,Mg(OH)2intermediate can be obtained and the high purity magnesium oxide was prepared through calcination.Impacts of end-point pH of dolomite slurry,reaction temperature,concentration of MgSO4,and calcination temperature on the leaching and sedimentation rate of magnesium and on the purity of magnesium oxide were investigated,and the optimum processing conditions were obtained as follows:end-point pH of dolomite slurry was 6,reaction temperature was 40℃,concentration of MgSO4was 0.8 mol/L,and calcination temperature was 900℃.Under above conditions,the purity of magnesium oxide reached over 99.0%,which met the demand for high purity magnesium oxide.
dolomite;magnesium hydroxide;high purity magnesium oxide
TQ132.2
:A
:1006-4990(2012)04-0022-03
2011-10-29
张华(1986—),男,在读硕士研究生,研究方向为无机精细化工。
