胸腔积液CEA、NSE、CYFRA21-1和SF不同组合的联合检测对肺癌的诊断意义
2012-02-24解大治梁常兴
鲁 颖,解大治,安 月,梁常兴
(1.抚顺市中心医院,辽宁 抚顺 113006;2.抚顺市卫生学校实验中心;3.大连医科大学附属第二医院)
肿瘤标志物(Tumor Marker,TM)的检测在肺癌诊断中具有重要参考价值,因此建立一种理想的组合检测模式是十分必要的。由于癌性胸水在产生部位上更接近于肺癌病灶,甚至直接浸润病灶,所以检测胸水中的TM会为肺癌诊断提供更早、更有效的依据[1,2]。
1 对象和方法
1.1 研究对象
1.1.1 良性病变组 包括肺炎、炎性假瘤、结节病、结核、结核性胸膜炎等共50例,年龄58.3±9.2岁。为抚顺市中心医院2007年11月至2009年11月住院患者。
1.1.2 恶性病变组 41例,男32例,女9例,为抚顺市中心医院2007年11月至2009年11月住院患者,根据第六版《内科学》标准诊断均经影像诊断(CT、核磁共振)、血清学和免疫学及细胞学与组织学诊断确诊,年龄60.1±11.8岁。其中鳞癌13例,腺癌17例,大细胞肺癌3例,小细胞肺癌8例。
1.2 检测方法
1.2.1 标本 无菌采集胸腔穿刺液3 ml,离心10 min后取上清液2 h内检测。
1.2.2 仪器 Roche公司生产的Elecsy 2010型全自动电化学发光分析仪检测,试剂为配套原装试剂。
1.3 统计学分析 数据资料采用SPSS11.5软件包进行统计学处理,各组均用x—±s表示。
2 结果
2.1 参考值范围,CEA、NSE、CYFRA21-1分别为>5 ng/ml、>25.0 ng/ml、>3.6 ng/ml为阳性,SF值为15-240 mg/ml。
2.2 恶性病变组与良性病变组胸腔积液的CEA、NSE、CYFRA21-1、SF 4项指标水平的比较见表1。采用两独立样本均数的方差分析进行统计学分析,结果显示,恶性病变组4项指标均显著高于良性病变组(P<0.01)。
2.3 恶性病变组与良性病变组胸腔积液CEA、NSE、CYFRA21-1、SF 4种肿瘤标志物阳性率比较见表2。采用χ2检验进行统计学分析,结果显示恶性病变组4项指标在胸腔积液中与良性病变组有显著差异(P<0.05),恶性病变组明显高于良性病变组。
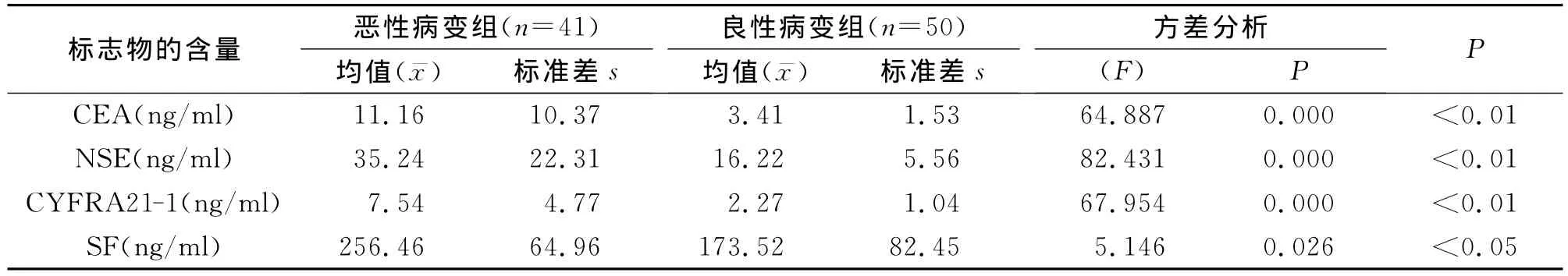
表1 两组患者胸水CEA、NSE、CYFRA21-1、SF 4项指标水平比较

表2 两组患者胸水CEA、NSE、CYFRA21-1、SF四项指标的阳性率(%)
2.4 不同组织类型肺癌的四项标志物水平比较见表3,结果显示腺癌组SF阳性率最高,鳞癌组CYFRA21-1阳性率最高,小细胞癌组中NSE阳性率最高。
2.5 胸腔积液中CEA、NSE、CYFRA21-1、SF四项肿瘤标志物的不同组合的联合检测的灵敏度及特异度见表4。结果显示,恶性胸腔积液中单项检测CEA的阳性率48.78%,NSE的阳性率46.34%,CYFRA21-1的阳性率60.98%,SF的阳性率65.85%。CEA、NSE和CYFRA21-1 3项联合检测胸腔积液的敏感度可达92.68%,特异度为80.00%。

表3 四种标志物CEA、NSE、CYFRA21-1和SF在不同类型肺癌中的阳性率(%)

表4 胸腔积液 CEA、NSE、CYFRA21-1、SF不同组合联检的灵敏度及特异度(%)
3 讨论
肺癌是一种恶性程度高、发病率和死亡率逐年上升的疾病,各种TM单项检测多缺乏高特异性和高敏感性,多项标志物联合检测可提高肿瘤诊断的阳性率[3]。
本研究结果显示,肺癌患者有4项TM(CEA、NSE、CYFRA21-1和SF)的胸腔积液水平明显高于良性病变组(P<0.01)。由表3可见,SF在腺癌组的阳性率最高76.5%,NSE在小细胞癌组的阳性率最高75.00%,CYFRA21-1在鳞癌组的阳性率最高84.62%,与文献得出结果一致[4,5],SF在肺癌四种病理型中阳性率均偏高。表2和表4提示该四项肿瘤标志物的检测中,单项测定的灵敏度和特异度不够理想,虽特异度高,但灵敏度不高,容易造成漏诊;两项联合检测灵敏度提高,但同时特异度在降低;3项联合检测虽灵敏度再次提高,但特异度与两项联合检测相比降低不明显;4项联合检测灵敏度可达95.12%,但特异度明显降低,降到52%。
联合检测CEA、NSE、CYFRA21-1和SF对肺癌的灵敏度最高95.12%,但其特异度很低52.00%。而联合检测CEA、NSE和CYFRA21-1 3项对肺癌的灵敏度与四项对肺癌的灵敏度无显著性差异,但特异度提高,达到80.00%。因此联合检测上述CEA、NSE和CYFRA21-1 3项TM,既可以减轻患者经济负担,也可达到最佳检测效果,且有助于对良恶性肿瘤的鉴别[6,7]。因此,建议采用 CEA、NSE和CYFRA21-1 3项TM联合检测。
[1]Shitrit D,Zingerman B,Shitrit AB,et al.Diagnostic value of CYFRA 2l-l,CEA,CA 19-9,CA 15-3 and CA 125 assays in pleural effusions:analysis of 116 cases and review of the literature[J].Oncologist,2005,10:501.
[2]刘晨梅,侯敏,张连祥,等.肺癌患者血清和胸水中肿瘤标志物联合检测的意义[J].临床检验杂志,2005,23:150.
[3]Muraki M,Tohda Y,Lwanga T,et al.Assessment of serum CYFRA21-l in lung cancer[J].Carcer,1996,77(7):1274.
[4]Wagner IC,Guimaraes MJ,da Silva LK,et al.Evaluation of serum and pleural levels of the tumor markers CEA,CYFRA21-1 and CA15-3 in patients with pleural effusion[J].Bras Pneumol,2007,33:185.
[5]Ghayumi SM,Mehrabi S,Doroudchhi M,et al.Diagnostic value of tumor markers for differentiating malignant and benign pleural effusions of Iranian patients[J].Pathol Oncol Res,2005,11:236.
[6]张敦华,主编.实用胸膜疾病学[M].上海:上海医科大学出版社,1997:175.
[7]刘运秋,于立群,林江涛.检测肿瘤标志物ProGRP、NSE、CYFRA21-I、CEA对胸腔积液鉴别诊断价值的研究[J].中国肺癌杂志,2006,9:273.
