聚合硫酸铁的制备及其对含镍废水处理的研究
2012-02-16刘存海韩利萍
刘存海, 刘 刚, 韩利萍
(陕西科技大学 化学与化工学院 教育部轻化工助剂化学与技术重点实验室, 陕西 西安 710021)
0 引言
聚合硫酸铁(PFS),简称聚铁,是在无机絮凝剂硫酸铁的基础之上发展衍生出来的新一类无机高分子絮凝剂.因为聚铁中含有羟基,因此又被称为羟基硫酸铁或者碱式硫酸铁.
分子通式为[Fe2(OH)n(SO4)3-n/2]m,由于其含有多羟基,从而使其对重金属离子的去除有很好的效果.另外,对COD及高色度造纸废水的处理也有较好的效果.因其具有矾花大、水解速度快、絮凝体密度大、pH适用范围广、对设备腐蚀性小、生产成本低、无害等特点.从而使其广泛应用于工业废水,生活污水,饮用水净化等领域[1,2].
合成聚合硫酸铁的方法有很多,有直接氧化法,催化氧化法,生物氧化法,其他氧化法等[3,4].直接氧化法则是采用一种强氧化剂将Fe2+氧化为Fe3+.该方法由于反应速率快,工艺路线简单,设备要求简单,反应投资少,产品质量高等优点,已被广泛工业化.直接氧化法所用的氧化剂有H2O2、HNO3、KClO3或NaClO、MnO2、C12、O2、KMnO4等.胡成松[5]等在常温常压下,以H2O2为氧化剂、钛白粉厂副产品硫酸亚铁为原料经过水解、氧化、聚合最终得到聚合硫酸铁絮凝剂.所制PFS的稳定性好、品质高.利用双氧水作为氧化剂的方法具有反应速度快,设备简单,并且不会将其他杂质离子引入反应体系中,制得的PFS具有较高的纯度.因为氧化反应和水解反应中升高一定温度能有效的提高PFS的盐基度,而聚合反应降低温度能有效提高聚合度.因此本文采取程序升温(高温到低温)不仅可以减少反应时间,而且可以制得高盐基度的产品,适合中小型企业的规模生产液体聚合硫酸铁.
1 实验部分
1.1 仪器设备
原子吸收光谱仪z2000(日本日立公司);JJ-1精密电动搅拌器(国华仪器厂);30%双氧水(A.R):天津市致远化学试剂有限公司;高锰酸钾(A.R):西安化学试剂厂;氟化钾(A.R):天津市耀华化学试剂有限责任公司;七水合硫酸亚铁(A.R):天津市红岩化学试剂厂;氢氧化钠(A.R):天津市恒兴化学试剂制造有限公司;盐酸(A.R):四川西陇化工有限公司;酚酞(A.R):北京市化学试剂研究所;二苯胺磺酸钠(A.R):公私合营新中化学厂;硫酸(西安化学试剂厂);磷酸(开封化学试剂总厂);氯化汞(A.R):贵州省铜仁仪器化学试剂厂.
1.2 实验内容
1.2.1 实验原理
本实验采用双氧水作为氧化剂,具体反应分为氧化、水解和聚合3部分.具体反应原理如下:
(1)氧化反应:2FeSO4+H2O2+H2SO4=Fe2(SO4)3+2H2O,此反应过程最慢,也是决定反应速率的一步.而且在此过程中硫酸和硫酸亚铁的摩尔比直接影响着氧化过程.此反应为放热反应.
(2)水解反应:Fe2(SO4)3+ nH2O=[Fe2(OH)n(SO4)3-n/2]+n/2 H2SO4,此反应为吸热反应.
(3)聚合反应:m[Fe2(OH)n(SO4)3-n/2]= [Fe2(OH)n(SO4)3-n/2]m,此反应为放热反应.
1.2.2 实验方法
通过改变硫酸和硫酸亚铁的摩尔比、双氧水和硫酸亚铁的比例、水用量和反应温度,采用先升高温度再降低温度的程序控温法,以盐基度(采用GB 14591-2006中盐基度的测定方法)作为表征参数,探究出了双氧水氧化硫酸亚铁的最佳工艺条件.并检验产品的除镍效果,镍含量采用原子吸收光度法.
2 结果与讨论
2.1 最佳n(H2O2)/n(FeSO4·7H2O)的确定
称取5.560 4 g FeSO4·7H2O,加入10 mL蒸馏水,加入0.004 mol硫酸,将转速调制120 r/min,开动搅拌器,以每5 s一滴的速度分别加入0.02 mol,0.026 mol,0.03 mol,0.034 mol,0.04 mol,0.046 mol,0.05 mol双氧水,继续搅拌10 min后过滤,分别测其盐基度.绘制盐基度与双氧水用量关系曲线.结果如图1所示.温度采取程序控温的方法(将最高温度设置到25 ℃,其温度在15 min内升至25 ℃,然后保温10 min,迅速用自来水冷却10 min).

图1 盐基度与双氧水用量关系曲线
由图1结果可知:在定量的硫酸下,双氧水的用量在0.46 mol之前,随着其用量的增加,盐基度有明显的提高,但在用量大于0.46 mol以后,盐基度几乎不再升高.由于双氧水用量的增加,可以增加Fe2(SO4)3的生成,有利于Fe2(OH)n(SO4)3-n /2单体的生成,从而可以明显提高产品的盐基度.但在0.46 mol以后,由于反应体系中的Fe2+已经被氧化完全,从而导致对产品的盐基度影响很小.
2.2 最佳n(H2SO4)/n(FeSO4·7H2O)的确定
称取5.560 4 g FeSO4·7H2O,加入10 mL蒸馏水,分别加入0.002 mol,0.003 mol,0.004 mol,0.005 mol,0.006 mol H2SO4,放入25 ℃水浴中,将转速调制120 r/min,开动搅拌器,以每5 s一滴的速度滴加0.046 mol双氧水,继续搅拌10 min后,过滤分别测盐基度,绘制盐基度与硫酸用量关系曲线,结果如图2所示.温度采取程序控温的方法(将最高温度设置到25 ℃,其温度在15 min内升至25 ℃,然后保温10 min,迅速用自来水冷却10 min).
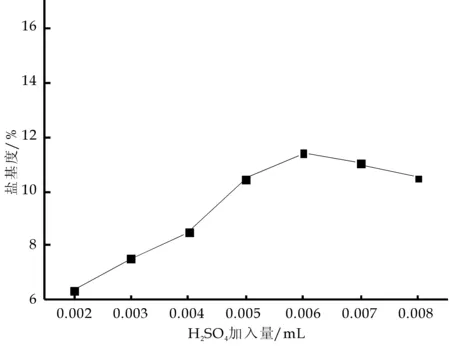
图2 盐基度与硫酸用量关系曲线
由图2结果可知:在双氧水一定量的情况下,在一定范围内随着硫酸用量的增加,Fe2(SO4)3的生成速率随之增加,并且有利Fe2(OH)n(SO4)3-n /2单体的生成,提高了聚合反应速率,从而使铁结合的羟基数增加,盐基度也随之增大.但当硫酸用量超过一定量时,会抑制Fe3+水解反应的发生,不利于聚合反应的进行,甚至使聚合硫酸铁发生分解,导致盐基度下降.
2.3 最佳n(H2O)/n(FeSO4·7H2O)的确定
称取5.560 4 g FeSO4·7H2O,分别加入3.0 mL,4.0 mL,5.0 mL,6.0 mL,7.0 mL,8.0 mL,9.0 mL,10.0 mL蒸馏水,加入0.68 mL H2SO4,将转速调至120 r/min,开动搅拌器,以每5 s一滴的速度滴加0.46 mol双氧水,继续搅拌10 min后过滤,分别测其盐基度.绘制盐基度与用水量关系曲线.结果如图3所示.温度采取程序控温的方法(将最高温度设置到25 ℃,其温度在15 min内升至25 ℃,然后保温10 min,迅速用自来水冷却10 min).
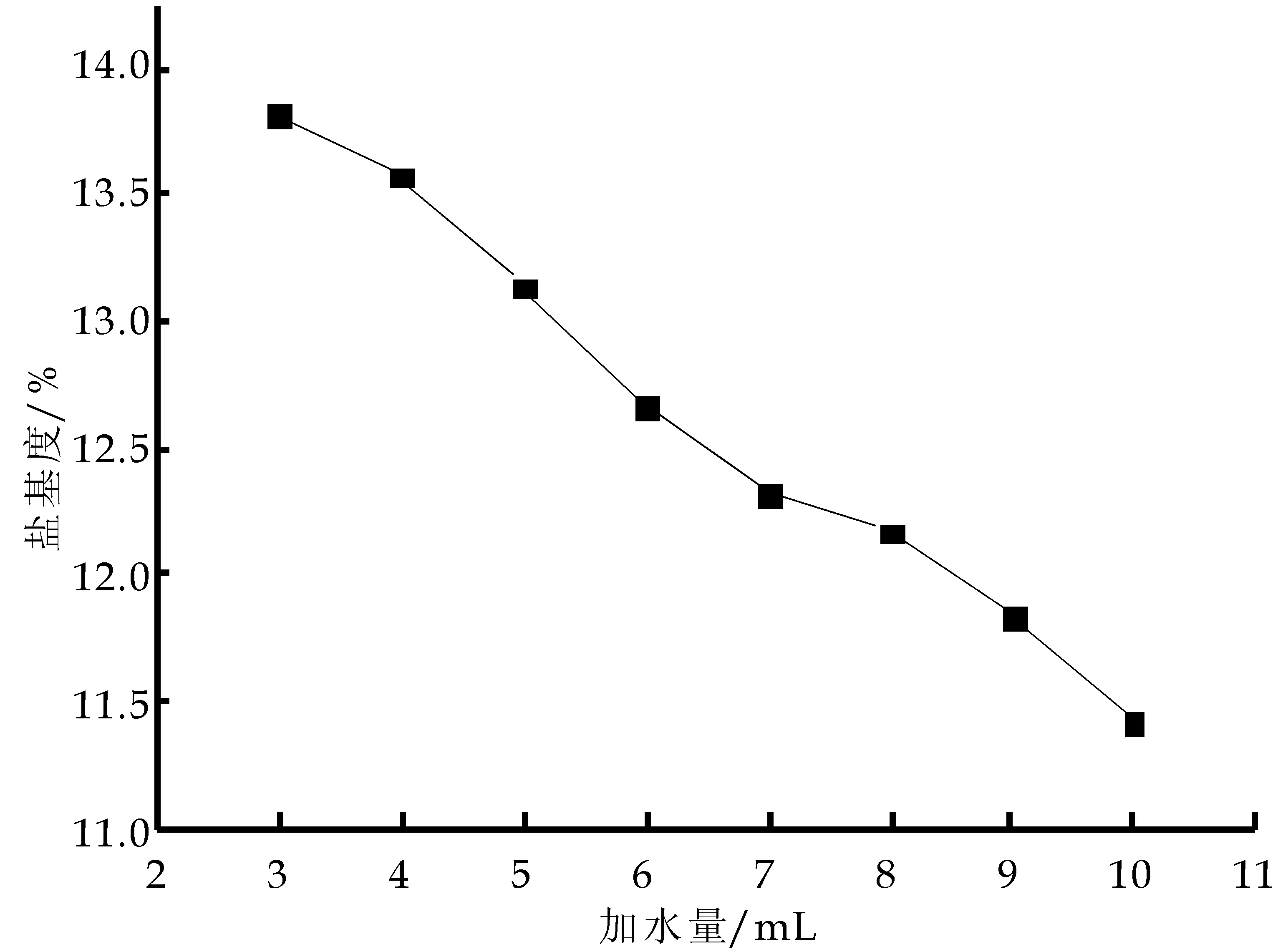
图3 盐基度与加水量关系曲线
由图3可知:减少水的用量对盐基度的提高是有利的,影响程度不大.但是,减少水的用量可明显提高全铁的含量.水量过少则会导致溶解不完全,从而导致氧化时间加长,而且氧化不均匀.因此,取最佳水用量为3.0 mL,既可以使硫酸亚铁完全溶解,又可以得到盐基度较高的产品.
2.4 程序控温和传统恒温的比较
一种选用程序升温(先升温再降温)的方法,一种采取传统固定温度的方法,按上面所讨论所得的最佳配方分别进行反应,分别测其盐基度.绘制盐基度与温度曲线.结果如图4所示.
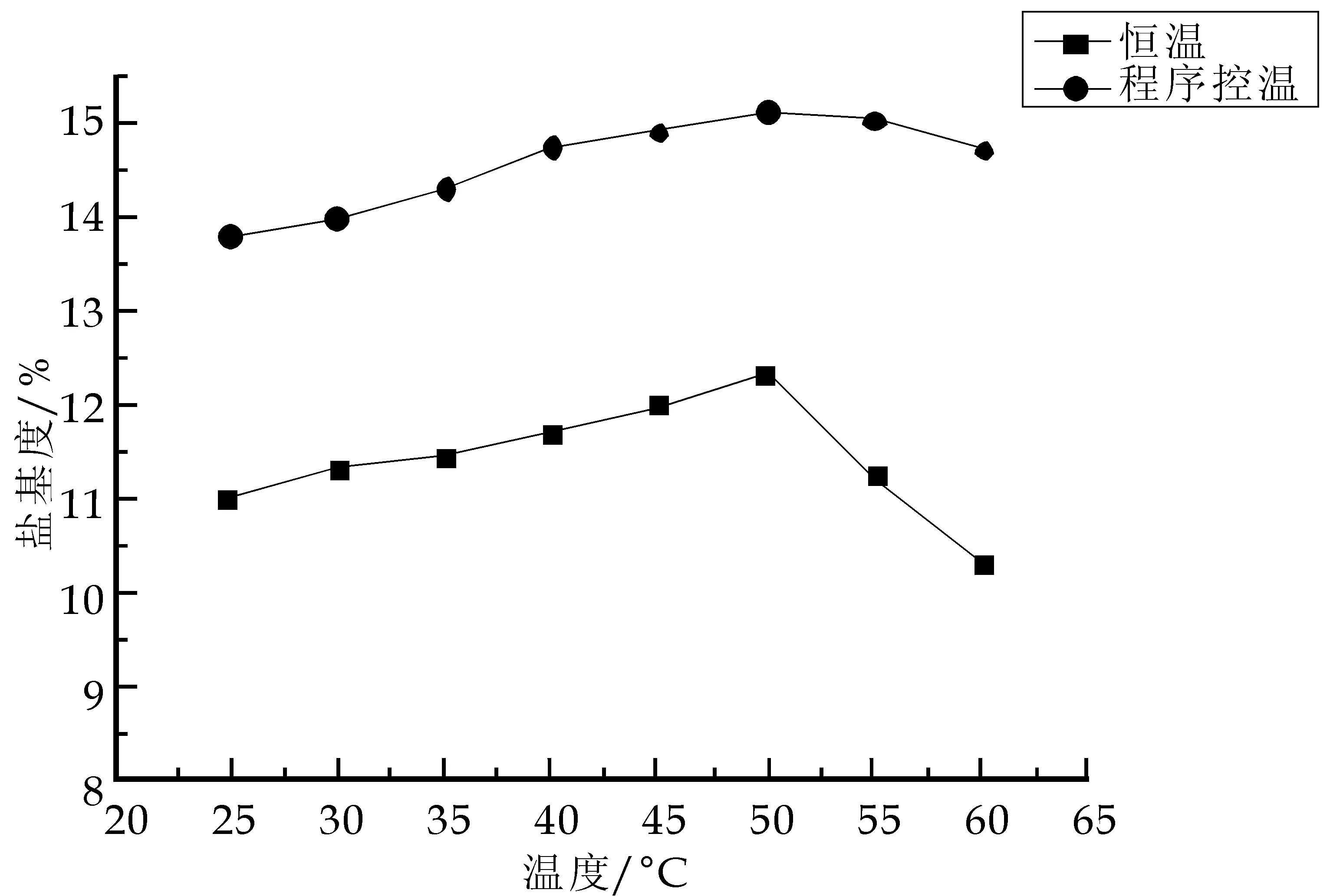
图4 盐基度与程序控温和恒温条件下温度关系曲线
由图4可知:在最高温度相同条件下,通过程序控温法所获得的产品盐基度较高,最适温度均为50 ℃.程序升温之所以可以得到盐基度较高的产品.是由于氧化反应为放热反应,但是反应程度比较大可以认其为不可逆反应,适当升高温度有利于盐基度的增加.而水解反应为吸热反应,此反应也是决定盐基度高低的关键一步,所以升高温度则利于盐基度的增加.最后一步聚合反应则为放热反应.因此,快速冷却降低温度有利于反应向正反应方向进行,可以明显提高聚合度,有利于盐基度的增加.
2.5 产品表征
所得产品各指标表征与国标对比如表1所示.

表1 产品各项指标表征
2.6 产品除镍效果的研究
水样取自宝鸡市长岭集团的电镀生产车间,含镍量约为336.3 mg/L.取一定量水样,将其pH调至9.3,投加适量该产品,静置4 h,取上层清液,利用原子吸收仪测其吸光度.通过标准曲线得出含镍量为0.48 mg/L,除镍率高达99.8%.另外,可得出此产品在pH等于8~12范围内对镍都有很好的絮凝作用.三个月后,再次利用本产品对含镍废水进行处理.结果表明:除镍率仍高达98%,说明其具有较长的保质期.
3 结束语
根据本文的实验结果可以得出如下结论:利用程序控温法,当n(H2O2)∶n(H2SO4)∶n(H2O)∶n(FeSO4·7H2O)为2.3∶0.3∶0.83∶1时,最佳温度为50 ℃时,制得的聚合硫酸铁的各项指标均满足国标GB14951-2006.水处理剂聚合硫酸铁标准,且盐基度高于同等条件下利用恒温法所制得的产品.
而且该方法具有反应速率快、无二次污染、设备简单、投资少、保质期长等特点,适合于中小企业的自产废水处理利用.并利用本产品处理含镍废水,结果表示:除镍率可达99.8%,使絮凝后的废水中镍含量达到GB21900-2008的排放要求.
[1] 潘碌亭,吴锦峰. 聚合硫酸铁制备技术的研究与进展[J].工业水处理,2009,29(9):1-5.
[2] 张瑛洁,杨 榕,曹天静,等.聚合硫酸铁的制备及改性研究进展[J].工业水处理,2011,31(9):11-14.
[3] 李家贵,朱万仁,韦庆敏,等.聚合硫酸铁的制备及处理制衣厂水洗废水研究[J].当代化工,2011,40(11):1 118-1 120.
[4] 赵志雄. 直接氧化法合成聚合硫酸铁的工艺研究[J].辽宁化工,2011,40(3):238-240.
[5] 胡成松,唐金斌,陶冠红.聚合硫酸铁合成新工艺[J].应用化工,2004,33(2):55-56.
