过表达Baff转基因斑马鱼的构建
2012-02-03刘树锋
张 力,谢 英,刘树锋
(河北医科大学河北省实验动物重点实验室,石家庄 050017)
斑马鱼具有繁殖能力强、体外受精和发育、胚胎透明、性成熟周期短、个体小易养殖,可针对治疗药物进行高通量筛选等诸多特点,使其成为后基因组时代生命科学研究中重要的模式脊椎动物之一[1,2]。B细胞活化因子(B cell activating factor,baff)是1999年发现的肿瘤坏死因子超家族新成员,在B细胞发育、功能调节和自身免疫病发病机制中的作用受到关注[1]。研究发现,系统性红斑狼疮(system ic lupus erythematosus,SLE)患者血清中Baff水平与IgG及抗dsDNA自身抗体水平均显著升高[4]。NZB、(NZB/NZW)F1、MRL/lpr等经典SLE模型同样表现出高滴度Baff的发病特征[2]。有文献报道,过表达baff的转基因小鼠可导致SLE样疾病,而拮抗Baff可延缓狼疮易感小鼠的疾病进展[3]。近年来,Baff拮抗剂的筛选成为SLE靶向药物筛选的研究热点之一。
本研究旨在通过分别构建baff过表达重组质粒pEGFP-C1-baff、pEGFP-N1-baff、p IRES2-EGFP-baff,通过胚胎显微注射获得过表达Baff蛋白的转基因斑马鱼,为SLE转基因斑马鱼疾病模型的建立与高通量药物筛选研究提供良好基础。
1 材料和方法
1.1 材料
1.1.1 实验动物
性成熟Tuebingen品系斑马鱼引自北京大学生命科学研究院,全自动化控温控光水处理、循环的斑马鱼专用养殖系统日常维护成鱼,水温28℃,pH 7.5,14∶10 h昼夜时间交替,以孵化的丰年虫(artemia)喂养。
1.1.2 试剂
质粒测序工作由上海生工测序公司完成; DM2000marker(北京康为世纪公司);凝胶回收试剂盒、DNA连接试剂盒、各种限制性内切酶(TaKaRa公司),Trizol(Invitrogen),Phusion聚合酶(NEB),反转录试剂盒(Fermentas Co.),humanβ-actin一抗与GFP抗体(SantaCruz Co.),质粒大小提试剂盒(北京天根生化公司),大肠杆菌Trans1-T1 Phage Resistant Chem ically competent cells(全式金公司),pEGFP-C1、pEGFP-N1、p IRES2-EGFP购自Clontech公司。
1.2 基因克隆与表达载体构建
Trizol法提取成年斑马鱼脾脏RNA,反转录为cDNA。根据Zf baff序列(GenBank:NM_ 001113590)设计克隆引物,并通过RT-PCR法克隆807 bp蛋白编码序列。引物序列见表1,下划线部分为引入酶切位点序列。PCR反应条件:98℃30 s,98℃10 s,59.5℃30 s,72℃30 s,72℃5 m in终延伸,循环数33。
PCR产物经酶切并回收长度807 bp片段,酶切后回收保存。p IRES2-EGFP质粒经BglⅡ与EcoRⅠ内切酶消化回收5.1 kb大片段,pEGFP-C1质粒经BglⅡ与EcoRⅠ内切酶消化回收4.7 kb片段回收pEGFP-N1质粒经BglⅡ与PstⅠ酶切回收4.7 kb大片段,PCR产物与载体通过T4 DNA Ligase 16℃连接过夜,连接产物经转化DH5α感受态后,挑取单克隆菌落,LB培养基震荡培养12 h后,通过质粒提取试剂盒提取质粒,后经BglⅡ与EcoRⅠ内切酶消化鉴定,送测序公司测序。

表1 载体构建引物序列Tab.1 Primer designated for plam id construction
1.3 细胞的培养转染与荧光观察
将HEK293细胞传至24孔板,传代后24 h细胞汇合度达90%时进行脂质体转染。转染方法按照Invitrogen lipofectamin 2000严格操作,每孔质粒量为0.8μg,脂质体量2μL。转染后48 h,在450~490 nm蓝光激发下观察GFP表达情况。
1.4 蛋白的提取与Westernblot
分别提取瞬时转染有pEGFP-C1-baff,pEGFPN1-baff及p IRES2-EGFP-baff质粒HEK293细胞总蛋白,方法如下:使用含PMSF和蛋白酶抑制剂的1xSDS裂解液冰上裂解细胞,煮沸10 min,裂解液冰上超声3 sX15次。离心后吸取上清,-20℃保存。所得蛋白进行SDS-PAGE凝胶电泳,将蛋白转移到0.45μm孔径硝酸纤维素膜上,置于5%脱脂奶粉封闭液中,室温孵育1 h,加入TBS稀释的兔抗GFP多克隆抗体(1∶1000)(ab290,abcam,美国),4℃孵育过夜,用TBST洗膜三次,每次10 min。然后加入1∶10000 KPL-Odyssey远红外抗兔二抗,TBST洗膜3次,每次5 m in,弃去二抗,室温孵育1 h。采用βactin(ab1801,abcam,美国)作为内参,将膜置于Odyssey机器中扫描成像。
1.5 斑马鱼胚胎注射
斑马鱼受精卵的获取:受精前将雌雄亲鱼分开饲喂1d后按1∶1~2比例放入产卵池中进行产卵交配。分选和洗净的卵移到有琼脂糖的表面皿中,注射外源 D NA浓度为0.25μg/μL,DNA体积约2 nL。受精卵的动物极注射完毕后,缓慢抽出注射针,将受精卵放入装有无菌水的培养皿中,使其恢复发育;25~28℃培养胚胎,分别在1~11 d后,荧光显微镜下观察筛选具有绿色荧光蛋白表达的胚胎。
2 结果与分析
2.1 pEGFP-C1-baff、pEGFP-N1-baff、pIRES2-EGFP-baff表达载体的鉴定
pEGFP-C1-baff、pEGFP-N1-baff两种表达载体均表达GFP-Baff融合蛋白,Baff分别融合于GFP蛋白的C端与N端。p IRES2-EGFP-baff分别独立表达GFP和Baff蛋白。3种载体各自经BglII与EcoRI,BglII与PstI,BglII与EcoRI酶切后均有807 bp左右条带,结果表明3种载体的构建正确,与测序结果一致。
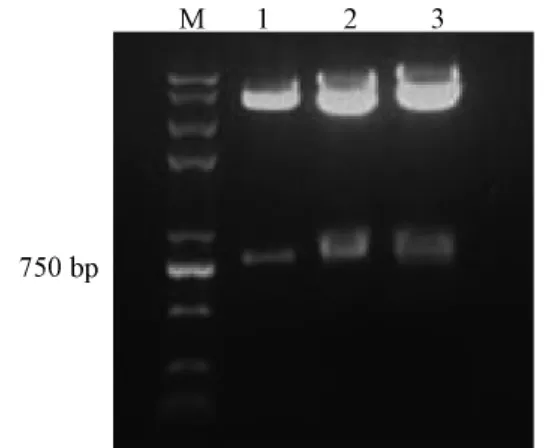
图1 pEGFP-C1-baff、pEGFP-N1-baff、p IRES2-EGFP-baff质粒酶切鉴定注,Note:M:DNA marker;1-3:pEGFP-C1-baff,pEGFP-N1-baff,p IRES2-EGFP-baff重组质粒分别经BglII and EcoRI,BglII and PstI,BglII and EcoRI酶切鉴定结果Fig.1 Identification of recombinants by enzyme digestion
2.2 重组载体的体外细胞验证
为进一步确定融合蛋白的正确表达,将p IRES2-EGFP-baff、pEGFP-C1-baff、pEGFP-N1-baff质粒转染HEK293细胞,转染后48 h观察其荧光表达情况。体外细胞转染结果表明(彩插4图2),p IRES2-EGFP-baff、pEGFP-C1-baff、pEGFP-N1-baff 3种重组质粒均可成功表达绿色荧光蛋白。
2.3 免疫印迹验证融合蛋白表达
为验证GFP-Baff融合蛋白的表达,HEK293细胞经pEGFP-C1、pEGFP-C1-baff、pEGFP-N1-baff质粒转染后进行免疫印迹实验,结果发现转染pEGFPC1空载体的细胞仅表达位于26 KDa的GFP蛋白,转染有pEGFP-C1-baff和pEGFP-N1-baff质粒的细胞均表达有分子量57 KDa的EGFP-Baff融合蛋白,说明了Baff蛋白完整表达。
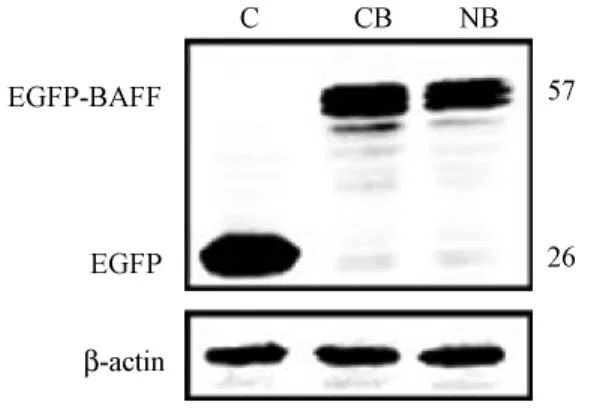
图3 pEGFP-C1,pEGFP-C1-baff,pEGFP-N1-baff质粒转染HEK293细胞蛋白表达情况注:C:pEGFP-C1空载体转染HEK293细胞蛋白表达;CB:pEGFP-C1-baff转染后蛋白表达;NB:pEGFP-N1-baff质粒转染后蛋白表达Fig.3 GFP expression in HEK293 cells transfected withpEGFP-C1,pEGFP-C1-baff,pEGFP-N1-baff Note:Lane C:HEK293 transfected by pEGFP-C1 empty vector; CB:HEK293 transfected by pEGFP-C1-baff;NB:HEK293 transfected by pEGFP-N1-baff
2.4 斑马鱼转基因表达载体的表达分析
pEGFP-C1-baff、pEGFP-N1-baff、p IRES2-EGFP-baff表达质粒纯化后显微注射到斑马鱼单细胞期胚胎,24~48 h后,在荧光显微镜下可以观察到绿色荧光蛋白在斑马鱼胚胎早期已成功表达(彩插4图4),与pEGFP-C1-baff和pEGFP-N1-baff注射后GFP阳性胚胎相比,p IRES2-GFP-baff质粒注射的GFP阳性胚胎表达强度较弱且表达时间相对缓慢。
3 讨论
鱼类是最早发生获得性免疫的脊椎动物,这使得对斑马鱼免疫系统的研究成分为了人们了解非特异性免疫系统和获得性免疫系统相互关系的重要模式动物[2,7]。Baff主要表达于T细胞和单核细胞,巨噬细胞、树突细胞等抗原呈递细胞[4],Baff属于Ⅱ型跨膜蛋白,胞外部分可被水解酶剪切为具有特定生物功能的可溶片段进入血液[9-11]。有研究表明,过表达baff蛋白的转基因小鼠存在B细胞异常激活和多种致病性自身抗体的分泌,肾脏中抗原与自身抗体复合物的出现[6,12-14]。Baff拮抗剂在动物模型中可有效清除B细胞,延缓肾病出现并延长生存,抗Baff单克隆抗体的临床研究也初步显示出疗效[15]。因此,构建Baff过表达斑马鱼,利用其作为SLE模型可以为高通量筛选SLE治疗药物提供一种易于获得的条件。
斑马鱼baff基因蛋白编码区域由807 bp碱基组成,其中包括跨膜蛋白组成部分以及胞外功能区域。我们首先分离提取斑马鱼Baff高表达的脾脏组织RNA,RT-PCR克隆了编码完整Baff蛋白的全长序列,为了避免融合蛋白的胞外部分剪切造成功能上的影响同时便于对外源转入baff基因表达情况进行跟踪,本实验分别构建了Baff融合于EGFP N端和C端的融合蛋白重组质粒,同时为了确保Baff行使正常的蛋白功能我们进一步构建了Baff与GFP共同独立表达的p IRES2-EGFP-baff质粒。通过体外细胞转染实验与免疫印迹实验验证了蛋白的正确表达,并通过斑马鱼卵胞质注射获得了转基因阳性幼鱼。
为建立并筛选表达完整功能Baff蛋白且具GFP荧光筛选功能的纯合子,未来的研究工作需要在纯化转基因品系的同时开展对SLE相关疾病指标的检测,例如抗dsDNA自身抗体表达水平,血清IgM表达水平以及肾脏、肝脏等器官病理变化等,进一步探讨其作为人类SLE疾病模型意义。
[1]A llen,J.P.and M.N.Neely.Trolling for the idealmodel host:zebrafish take the bait.Future Microbiol,2010.5(4):563-9.
[2]Langenau,D.M.and L.I.Zon.The zebrafish:a new model of T-cell and thymic development.Nat Rev Immunol,2005.5(4):307-17.
[3]Rolink,A.G.and F.Melchers.baffled B cells survive and thrive:roles of baff in B-cell development.Curr Opin Immunol,2002.14(2):266-75.
[4]Enzler T,Bonizzi G,Silverman GJ,et al.Alternative and classical NF-kappa B signaling retain autoreactive B cells in the splenic marginal zone and result in lupus-like disease.Immunity,2006.25(3):403-15.
[5]Marston,B.and R.J.Looney.Connective tissue diseases:Translating the effectsof baff in SLE.Nat Rev Rheumatol,2010.6(9):503-4.
[6]StohlW,Jacob N,Guo S,et al.Constitutive overexpression of baff in autoimmune-resistant mice drives only some aspects of system ic lupus erythematosus-like autoimmunity.Arthritis Rheum,2010.62(8):2432-42.
[7]Levraud JP,Colucci-Guyon E,Redd MJ,et al.In vivo analysis of zebrafish innate immunity.Methods Mol Biol,2008.415:337 -63.
[8]Ota M,Duong BH,Torkamani A,et al.Regulation of the B cell receptor repertoire and self-reactivity by baff.J Immunol,2010.185(7):4128-36.
[9]Bossen C,Cachero TG,Tardivel A,et al.TACI,unlike baff-R,is solely activated by oligomeric baff and APRIL to support survival of activated B cells and plasmablasts.Blood,2008.111(3):1004-12.
[10]Gross JA,Johnston J,Mudri S,et al.TACI and BCMA are receptors for a TNF homologue implicated in B-cell autoimmune disease.Nature,2000.404(6781):995-9.
[11]Gavin AL,Duong B,Skog P,et al.deltabaff,a splice isoform of baff,opposes full-length baff activity in vivo in transgenic mouse models.J Immunol,2005.175(1):319-28.
[12]Groom J,Kalled SL,Cutler AH,et al.Association of baff/BLyS overexpression and altered Bcell differentiation with Sjogren's syndrome.JClin Invest,2002.109(1):59-68.
[13]Stohl W,Xu D,Kim KS,et al.baff overexpression and accelerated glomerular disease in mice with an incomplete genetic predisposition to systemic lupus erythematosus.Arthritis Rheum,2005.52(7):2080-91.
[14]Thorn M,Lewis RH,Mumbey-Wafula A,et al.baff overexpression promotes anti-dsDNA B-cell maturation and antibody secretion.Cell Immunol,2010.261(1):9-22.
[15]Hsu H,Khare SD,Lee F,et al.A novel modality of BAFF-specific inhibitor AMG623 peptibody reduces B-cell number and improves outcomes in murinemodels of autoimmune disease.Clin Exp Rheumatol,2012.30(2):197-201
