国内外实验动物病毒检测的比较
2012-02-03佟巍
佟巍
(中国医学科学院北京协和医学院医学实验动物研究所,北京 100021)
实验动物病毒学检测是确保实验动物质量的有效措施之一,国外许多实验动物机构都建有自己的病毒学质量监测体系,我国实验动物病毒学检测技术和监测能力也不断发展,达到了一定的标准化水平[1]。然而随着生命科学研究不断发展,实验动物病毒检测工作的不断深入,发现实验动物病毒检测内容、检测方法、检测能力和检测试剂等仍存在诸多问题。本文以常用实验动物(包括大鼠、小鼠、猴以及实验用小型猪)为代表,介绍国内外实验动物病毒检测项目的异同。
1 实验动物病毒学检测检测内容的比较
1.1 小鼠、大鼠病毒学检测内容比较
小鼠、大鼠在各种实验研究中用量最大,用途最多。许多国家和地区都建立了啮齿类实验动物的专门机构进行着实验动物和动物实验的各方面科学研究工作,并制定了啮齿类实验动物的病毒学控制标准[2-5](表1)。

表1 SPF级啮齿类实验大鼠、小鼠病毒学标准对比Tab.1 Comaprison of virological standards for SPF rats and mice
1.2 猴病毒检测内容比较[3,7,8]
欧洲FELASA以及日本筑波灵长类动物研究中心对非人灵长类的病毒学检测都有较高的标准。特别是FELASA对常用的食蟹猴、恒河猴、绿猴、狒狒、松鼠猴、狨猴,也包括猩猩,都有自己特定的病毒学控制要求,值得我国参考(表2)。

表2 SPF级非人灵长类实验动物病毒学质量标准对比Tab.2 Comparison of virological standards for SPF non-human primate laboratory animals
1.3 小型猪病毒检测内容比较
我国生物医学科学事业的发展使实验用小型猪得到了越来越广泛的应用,因而对标准化的实验用猪提出了更高要求。我国目前尚无国家标准,北京、上海相继出台了小型猪的实验动物地方标准。台湾省规定SPF猪应排除的病毒仅为:Herpes virus (Aujeszky's virus)、Coronavirus(TGE)、PRRS virus。欧洲各国、瑞典和美国实验动物中心对于猪病毒健康监控内容也不尽相同[9](表3)。
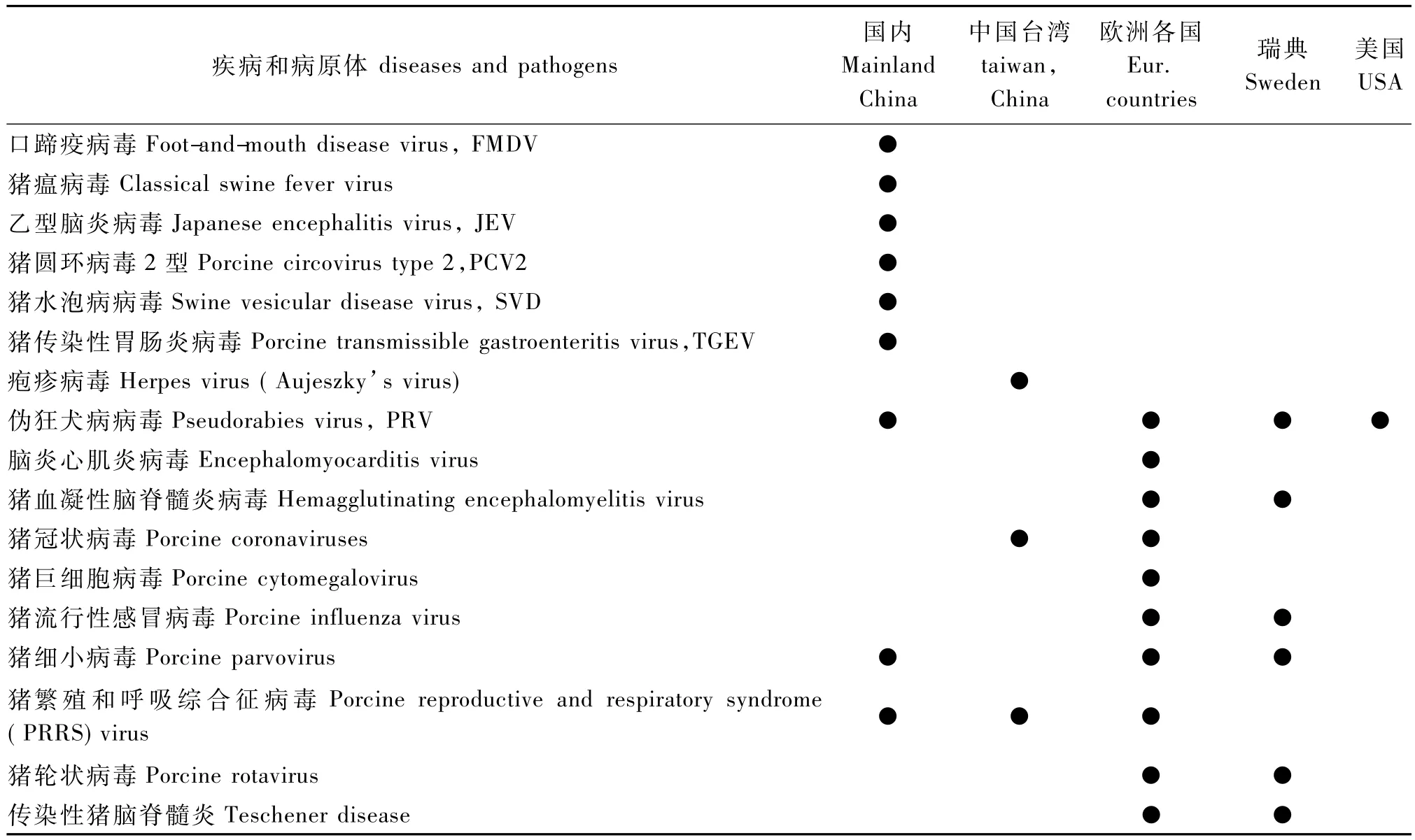
表3 SPF级小型猪病毒学质量标准对比Tab.3 Comparison of virological standards for SPFminipigs
以上举例介绍了大、小鼠,猴和小型猪的检测内容比较,其他实验动物也存在类似情况,应引起同样重视。
2 实验动物病毒检测方法
实验室检查主要分为血清学诊断和病原学检查[10],目前国内外实验动物病毒检测多采用血清学检测方法。由于方法简便快速,对仪器设备要求不高,测定成本低廉等优点,被广泛应用于实验动物病毒检测工作中。
2.1 国外检测方法
国外的方法包括MFIA(多重免疫荧光)[11,12]、ELISA(酶联免疫吸附试验)、IFA(间接免疫荧光试验)、HAI(血凝抑制试验)、Enzyme(serum chemical analysis of lactate dehydrogenase,乳酸脱氢酶血液生化分析方法)或CHEM(biochemical,生物化学方法)、WB(杂交免疫印迹试验)、PCR(聚合酶链反应)等方法。初次检测选多选用MFIA或ELISA,复检多选用IFA、HAI和PCR等方法[13,14]。
2.2 国内检测方法
国内的方法包括ELISA、IFA、IEA(免疫酶染色实验)、HAI、PCR等方法。其中初次检测选多选用ELISA和IEA,复检多选用IFA和HAI等方法。
2.3 新方法的应用
环介导等温扩增技术(Loop-mediated isothermal amplification,LAMP)技术在病原微生物检测方面已有广泛应用[15]。日本专家Fukuda等利用ALMP原理设计RT-ALMP成功检测了不同亚型的诺瓦克病毒[16]。基因芯片技术使得同时对成千上万的基因的检测成为可能。我国军事医学科学院军事兽医研究所已建立了麻疹病毒属病毒检测基因芯片检测方法,其特异性强,敏感性是PCR方法的100倍。
3 实验动物病毒学质量检测工作中发现的若干问题
3.1 为使我国实验动物标准尽快与国际接轨,现有检测标准应拓展更多项目
Taconic Laboratory与Charles River Laboratories对大鼠、小鼠病毒检测内容均达24种之多;日本筑波灵长类动物研究中心SPF食蟹猴检测病毒9种;欧洲小型猪病毒检测10种。我国微生物学、寄生虫学等级标准中对大鼠、小鼠病毒检测内容仅为15种;猴病毒检测5种;小型猪病毒检测9种。
Charles River Laboratories针对小鼠、大鼠都有LCMV病毒检测要求,而国内未将该检测项目列在大鼠病毒检测项目中。国内有文献报道在普通环境饲养的大鼠有LCMV抗体的检出[17]。鼠诺沃克病毒(MNV)也是人兽共患病病原,国外应用血清学方法检测,小鼠对该病毒有较高的感染率(北美32.64%、欧洲24.03%),我国也未将该病毒列入实验动物质量标准予以控制,这一情况应引起我们注意,并尽快建立监测方法,对我国实验动物MNV感染情况进行调查[18]。小鼠微小病毒(MPV)在北美及欧洲也有1.65%~3.64%的检出率,我国也未将其列入常规检测范围。
日本筑波灵长类动物研究中心针对SPF食蟹猴的病毒学检测内容达9种之多。从表2中可以看出,尽管FELASA对恒河猴的病毒学检测内容仅有6种,未列出的是FELASA针对不同种类非人灵长类实验动物有不同的病毒学质量标准。而我国没有针对不同种类非人灵长类实验动物的病毒学标准。
从表3中可以看到,FELASA与我国制定的实验用小型猪地方(北京、上海)标准在病毒学标准上有较大差异。我国应参照标准化程度较高的国际标准,尽快建立适合我国国情以及能与国际接轨的国家标准。
3.2 应逐步将实验动物新资源纳入实验动物病毒学质量检测体系中
近年来实验动物资源的开发得到较快的发展,为实验动物新品种、品系的建立提供了有利条件,例如东方田鼠在抗血吸虫方面、雪貂在流感病毒研究方面、土拨鼠在鼠疫研究方面都显出良好的势头。研究由野生动物驯化培育的实验动物所携带的病毒以及这些病毒对其自身、其他动物和人的致病性,研究制定相关的病毒学标准和监测体系,并依据标准进行监测与评价,是实验动物化的前提。已有的实验动物质量标准和检测体系不能完全适应实验动物新资源开发利用的需求,质量标准滞后和检测手段不完善已成为制约实验动物新资源开发、标准化研究与推广利用的瓶颈,建立和制定新资源的质量标准和检测体系,是今后一段时期内的研究重点[6]。尽快制定相关质量标准、建立相应的质量检测技术、促进新资源的标准化是目前急需解决的问题[1]。
3.3 检测试剂的标准化及检测结果的质量控制
我国实验动物病毒诊断试剂及检测方法尚未达到标准化要求,某些检测项目的检测方法尚未建立,直接影响检测工作质量以及检测工作的发展。尤其是病毒检测试剂制备所使用的毒株来源复杂,在一定程度上制约了检测试剂的标准化。以致由多个检测实验室制备的诊断试剂的质量存在差异,影响了检测工作进一步发展[10]。
为促进检测试剂的标准化,应在引进实验动物国际标准毒株及找到国内病毒流行株的基础上,借鉴发达国家检测试剂标准化的成功经验,尽快建立和完善我国实验动物病毒学检测标准化体系。参照医学临床实验室质量管理体系,结合实验动物质量检测特点,由国家级检测实验室发放统一的质控用标准品,开展实验室间的质量评价,提高我国实验动物质量检测结果的可比性。
3.4 检测方法的选择缺乏多样性
选择合适的检测方法是保证实验动物质量评价的科学性和检测结果准确性的基础。病毒感染动物机体后,疾病病程具有明显的规律性,一般分为潜伏期、前驱期、临床明显期和转归期。因此,对病毒性疾病的诊断要根据疾病的不同阶段选用适当的检测技术。常规的实验动物病毒检测方法包括病原学诊断(例如病毒分离)、血清学检测(例如抗体检测)、变态反应诊断(例如结核菌素实验)和病理组织学诊断等。在实际工作中,通常仅采用血清学方法对动物进行健康检测,然而对于处于疾病感染初期的动物或免疫缺陷动物来说,检测结果则不能真实反映疾病感染的真实情况。只有采用几种方法联合应用,取长补短,才能提高检测结果的准确性和可靠性。
3.5 质量检测频率缺乏灵活性
CharlesRiver实验室、Taconic则根据病原特性不同进行监测。有的病毒2~4周检测一次,有的每个季度检测一次,有的则半年或一年检测一次[13,14]。相比之下,我国实验动物病毒检测针对性不强,检测频次相对较少[19]。在根据不同病原的特性及时有效的掌握动物群中疾病的流行情况,及时诊断、发现并控制疾病的传播方面存在欠缺。因此,根据本地的感染谱、病原特性和检测方法的敏感性,调整监测计划,有目的的增加检测频率,既保证动物质量,又可节省经费,使检测工作在确保实验动物质量方面起到应有的作用[6]。
3.6 哨兵动物的正确使用
由于哨兵动物的成本低,在动物疫病监测中使用方便,操作性强,被发达国家普遍采用[20]。随着实验动物科学的发展,我国实验动物生产单位为加强对自由动物饲养环境设施和动物质量的自查,也已经把哨兵动物的使用作为自觉行为。然而,在哨兵动物的选择和使用方式上却存在一些问题(例如:哨兵动物种类、品系及大小的选择,在生产单位放置位置的选择以及饲养方式等[21])。使哨兵动物不能真实反映特定环境中传染因子的存在状况,往往问题被发现时后果已经非常严重,造成了很大的经济损失[22]。
总之,加强质量检测,是保证实验动物标准化的重要举措,病毒学检测是实验动物质量控制的一项重要内容。随着中国对外交往日益增加,实验动物微生物学质量评价标准和检测方法必须尽快与国际取得一致,否则不仅会严重影响我国生物医学研究等领域与国际的交流,也将对实验动物产业化、动物进出口带来不利影响。
由此,为更好的适应实验动物产业的发展,为遵循整体性、全面性、连续性原则,首先,应参照其他国家对实验动物病毒控制要求,尽快实现与国际先进标准接轨,满足实验动物质量的国际化要求。其次,实验动物病毒学监测还要根据我国国情,根据实验动物种类、品系和级别的不同,并根据病原的不同以及病原的流行情况适时调整检测计划,增加检测力度和检测频率,最大限度的应用适合的检测手段,定期对动物的健康进行监测,完善实验动物质量检测档案。另外,我国实验动物病毒检测试剂及检测方法需尽快达到标准化要求,引进更为先进的实验动物病毒检测方法及检测手段,建立良好的实验动物检测实验室管理体系,提高检测结果的准确性,满足检测需要。实验动物病毒检测这项工作的完善,将在保证实验动物的健康、保证工作人员健康和生命安全、确保科研和检定工作的准确性方面起重要作用。
[1]中国科学技术委员会主编.实验动物学学科发展报告(2008 -2009)[M].中国科学技术出版社.3-26.
[2]Taconic’s International Health Monitoring SystemTM.A worldwide standard of microbiological testing for laboratory mice and rats[EB/OL].http://www.taconic.com/user-assets/ Documents/Quality/overview_US.pdf.
[3]Nicklas W,Baneux P,Boot R,et al.Recommendations for the health monitoring of rodent and rabbit colonies in breeding and experimental units[J].Laboratory Animals Ltd.Lab Animals, 2002,36:20-42.
[4]实验动物管理与使用指南编辑委员会主编.实验动物管理与使用指南[M].中华实验动物学会出版,2004:50-51.
[5]施新猷,王四旺,顾为旺,等.比较医学[M].陕西科学技术出版社.2003:29-61.
[6]张丽芳.实验动物细菌学监测工作中存在的问题及建议[J].中国比较医学杂志,2011,21(8):74-78.
[7]Yasutomi Y.Establishment of specific pathogen-free macaque colonies in Tsukuba Primate Research Center of Japan for AIDS research[J].Vaccine.2010,28(Supp l):75-77
[8]Weber H(Convenor),Berge E,Finch J,et al.FELASA Working Group on Non-Human Primate Health:Health monitoring of non-human primate colonies.Recommendations of the FELASA Working Group on Non-Human Primate Health accepted by the FELASA Board of Management,21 November 1998[J].Laboratory Animals Ltd.Lab Animals.1999,33 (Suppl.1):3-18.
[9]Rehbinder C,Baneux P,Forbes D,et al.FELASAWorking on Animal Health:FELASA recommendations for the health monitoring of breeding colonies and experimental units of cats,dogs and pigs[J].Laboratory Animals Ltd.Lab Animals,1998,32:1-17.
[10]方喜业,邢瑞昌,贺争鸣.实验动物质量控制[M].中国标准出版社.2008:294-345.
[11]Serologic Methods Manual:Multiplexed Fluorometric ImmunoAssayTM[EB/OL].http://www.criver.com/SiteCollectionDocuments/rm_ld_r_ MFIA_Rodent_Methods_Manual.pdf 8/2007
[12]MFIA Summary Report[EB/OL].http://www.criver.com/ SiteCollectionDocuments/rm_ld_r_MFIA_summary_report.pd f
[13]Cifford CB.Routine Health Monitoring of Charles River Barrier Production Colonies in Europe and North America[EB/OL].http://www.criver.com/SiteCollectionDocuments/hmsummary.pdf,2009-05-04/2009-11-11.
[14]Taconic's International Health Monitoring SystemTM.A worldwide standard of microbiological testing for laboratory mice and rats[EB/OL].http://www.taconic.com/user-assets/ Documents/Quality/overview_US.pdf与文献2重复一周
[15]张如胜.LAMP技术在病原微生物检测中的应用[J].华南预防医学,2007,33(5):45-49.
[16]Fukuda S,Takao S,Kuwayama M,et al.Rapid detection of norovirus from fecal specimens by real-time reverse transcriptionloop-mediated isothermal amplification assay[J].JClin Microbiol,2006,44(4):1376-1381.
[17]佟巍,乔红伟,魏强,等.淋巴细胞脉络丛脑膜炎病毒在实验大鼠中的感染状况[J].医学动物防治,2010,27(4):46 -48.
[18]肖镜,贺争鸣.诺瓦克病毒及实验动物感染[J].实验动物科学,2009,26(3):46-48.
[19]中国人民共和国国家质量监督检疫检疫总局.实验动物微生物学等级及监测[S].GB/T14922.2-2001,2001:1-6.
[20]蔺长明.巴西应用哨兵动物监测口蹄疫[J].畜牧与兽医,2003,35(2):27-28.
[21]A laboratory animal Health monitoring Program:Rationale and Development.W inter 1990[EB/OL].http://www.criver.com/SiteCollectionDocuments/rm_ld_r_ health_monitoring_program_rationale.pdf
[22]车路平,卢胜明.从Jackson实验室对一次污染事件的处理反观我国实验动物管理存在的差距[J].实验动物科学与管理,2002,19(3):22-23.
