O/W 型丹皮酚微乳处方设计及质量评价
2012-01-26开伟华桂双英
开伟华,桂双英
(1.铜陵职业技术学院,安徽铜陵244000;2.安徽中医学院药学院,安徽合肥230031;3.安徽省中药制剂工程技术研究中心,安徽合肥230031)
丹皮酚(paeonol,Pae)是毛莨科植物牡丹根皮和萝摩科植物徐长卿干燥根或全草的主要活性成分。现研究表明,丹皮酚具有解热镇痛、抗菌消炎、抗过敏、增强细胞免疫等多种药理作用[1-2]。丹皮酚和丁香油为市售丹皮酚软膏主要药理活性成分,具有解热、抗炎和抑制变态反应的作用,两者配伍,相得益彰。然而,市售软膏涂于皮肤表面,药物丹皮酚和丁香油具有挥发性,易挥发损失。微乳是由水相、油相、表面活性剂及助表面活性剂按适当比例自发形成的一种低黏度、透明或半透明、各向同性、粒径在10~100 nm之间且热力学稳定的体系[3-4]。它是一种新型透皮传递系统,具有其它透皮制剂不可比拟的优点,如能够显著增加难溶性药物的溶解度,并将药物以较高浓度贮存于皮肤一定深度,具有良好的角质层和真皮贮药性能[5-6]。本实验通过伪三元相图法,以丁香油为油相研究丹皮酚微乳形成条件,并对所丹皮酚微乳的粒径大小、体系类型及理化性质等进行初步研究。
1 仪器与试剂
1.1 仪器79-1磁力加热搅拌仪(江苏金坛市环宇科学仪器厂),DDS-11A数显电导率仪(上海虹益仪器仪表有限公司),BS110S电子天平(上海赛多利斯天平有限公司)。
1.2 材料丁香油(天津光复精细化工研究所,061012),Tween80(上海申宇医药化工有限公司),Span80(化学纯,广东汕头市西陇化工厂),Tween20(化学纯,天津市光复精细化工研究所),聚氧乙烯辛基苯基醚(简称OP)(天津市光复精细化工研究所),聚乙二醇硬脂酸酯15(简称Solutol HS 15)(德国BASF公司),甘油(分析纯,天津市福晨化学试剂厂),丙二醇(分析纯,上海苏懿化学试剂有限公司),乙醇(分析纯,上海中试化工总公司),正丁醇(n-butanol)(宜兴市第二化学试剂厂出品),异丙醇(简称IPA)(天津市博迪化工有限公司),聚乙二醇400(PEG400)(分析纯,天津市光复精细化工研究所),丹皮酚原料(上海紫源制药有限公司,纯度98.9%),丹皮酚对照品(中国药品生物制品检定所提供,批号:0708-9704)。
2 方法与结果
2.1 表面活性剂和助表面活性剂的筛选本实验选择Tween80、Solutol HS 15、OP-10、Tween20、Poloxamer188 5种HLB值符合O/W微乳要求的非离子表面活性剂,分别与助表面活性剂配制成Km比(表面活性剂与助表面活性剂的质量比)为1的混合乳化剂,滴定1%的丁香油水溶液,结合偏光显微镜,以澄清透明综合判定微乳是否形成,见表1。结果:以丁香油为油相的微乳体系中,Tween20、Tween80与正丁醇,OP-10与异丙醇,Solutol HS 15与1,2丙二醇、乙醇、异丙醇均可形成微乳,但Tween20与正丁醇形成的微乳体系不稳定,放置后变浑浊。
2.2 伪三元相图的绘制按一定质量比精密称取表面活性剂和助表面活性剂混合均匀,制成混合表面活性剂。精密称取定量的油和水按质量比(m1∶m2)为9∶1、8∶2、7∶3、6∶4、5∶5、4∶6、3∶7、2∶8、1∶9混合均匀,在20℃条件下恒温磁力搅拌,边搅拌边用混合表面活性剂滴定,直至澄清透明的微乳形成,记录混合表面活性剂的临界加入量。按混合表面活性剂、油、水在临界点的质量比,绘制伪三元相图,确定微乳区域。澄清者为微乳(microemulsion),用M表示;乳浊状态者为普通乳状液(emulsion),用E表示,用偏光显微镜观察,有折射现象为液晶(liquid crystal),用LC表示,不发亮者为凝胶(gelatum),用G表示。
2.2.1 表面活性剂和助表面活性剂的确定微乳区大小、粒径和稳定性为微乳的主要性质评价指标[7]。微乳区域的大小为主要评价指标,它直接影响微乳的稳定性,形成的微乳区越大,微乳越稳定。本实验通过绘制伪三元相图从表面活性剂、助表面活性剂、Km值、pH等方面考察影响微乳形成的因素。
以丁香油为油相,分别以Tween80为表面活性剂,正丁醇为助表面活性剂;Solutol HS 15为表面活性剂,1,2丙二醇、乙醇、异丙醇为助表面活性剂;OP-10为表面活性剂,异丙醇为助表面活性剂,Km=1,绘制伪三元相图,结果见图1。
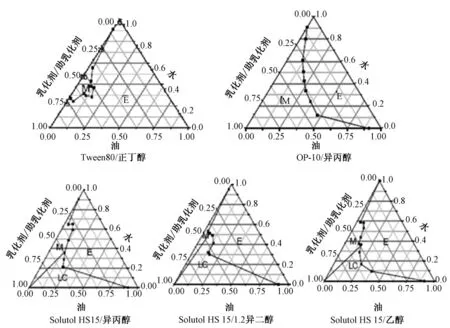
图1 不同表面活性剂和助表面活性剂对相图的影响Fig.1 Effect of different surfactants and cosufactants on the phase diagram s
由伪三元相图可知,以丁香油为油相,以OP-10为表面活性剂形成的微乳区域面积大于分别以Tween80和Solutol HS 15为表面活性剂形成的微乳区域面积,因此,本实验采用OP-10/异丙醇为混合表面活性剂。
2.2.2 Km和pH值的确定以丁香油为油相,OP-10为表面活性剂,异丙醇为助表面活性剂,不同Km绘制伪三元相图,结果OP-10为表面活性剂的微乳体系中,随着Km值从3∶2到1∶4变化,微乳区先增大后减小,Km=1微乳区最大,选择OP-10/IPA质量比为1。
而以OP-10/异丙醇(Km=1)为混合表面活性剂,分别以PBS6.8、双蒸水、PBS7.4为水相,绘制伪三元相图,考察不同pH对微乳区的影响,结果OP-10/异丙醇微乳体系中,弱酸、水和弱碱对微乳区无显著影响。
2.2.3 油水比例的确定将适量的丁香油与一定量的水搅拌混合,加入OP-10/异丙醇(Km=1)混合表面活性剂,20℃恒温磁力搅拌器搅拌至澄清透明,利用电导率判断微乳的类型[8],当油水比例<0.45时为O/W型微乳,确定油水比例为0.4。
3 丹皮酚微乳的处方确定
称取适量的丹皮酚溶于丁香油中,按油水比例为0.4加入蒸馏水,20℃磁力搅拌器搅拌下加入OP-10/异丙醇(Km=1)混合表面活性剂,继续搅拌至透明得到丹皮酚微乳。当丹皮酚/丁香油的比例<0.4,可形成O/W型丹皮酚微乳,本实验选丹皮酚/丁香油的比例为0.35。确定丹皮酚微乳处方:丹皮酚5%,丁香油15%,OP-10 15%,异丙醇15%,水50%。
4 丹皮酚微乳的性质及稳定性考察
4.1 丹皮酚微乳类型的鉴别将水溶性的伊文思蓝和油溶性的苏丹红分别滴加到丹皮酚微乳制剂中,观察两种染色剂在微乳制剂中的扩散速度[9]。经观察,伊文思蓝的扩散速度均明显快于苏丹红,表明所制备的丹皮酚微乳为O/W型。
4.2 微乳性质参数测定20℃恒温下测定丹皮酚微乳黏度、电导率、折光率,结果见表1。
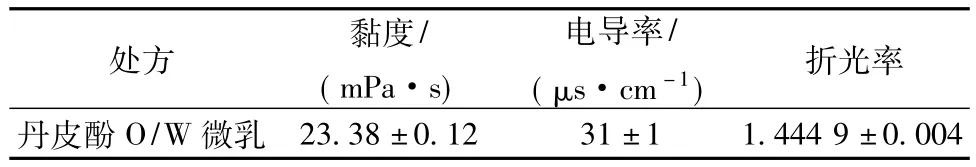
表1 微乳各项参数测定(n=6)Tab.1 Parameters of m icroemulsion property(n=6)
4.3 丹皮酚微乳形态与粒径分布取含药微乳适量,采用负染色法制备样品:将载有Formvar支持膜的铜网置于蜡板上,在膜上滴加丹皮酚微乳液,自然晾干20 min。再滴加2%磷钨酸一滴,自然晾干10 min,用滤纸吸走多余的液体,置于透射电子显微镜下观察,微乳粒子呈圆球形,分布较均匀,其平均粒径为62.3 nm(见图2)。用动态光散射法测定微乳各处方粒径分布图,空白微乳与丹皮酚微乳平均粒径分别为56.8 nm、63.4 nm,粒径基本呈正态分布(见图3)。

图2 微乳电镜图Fig.2 M icroemulsion under transm ission electron m icroscope
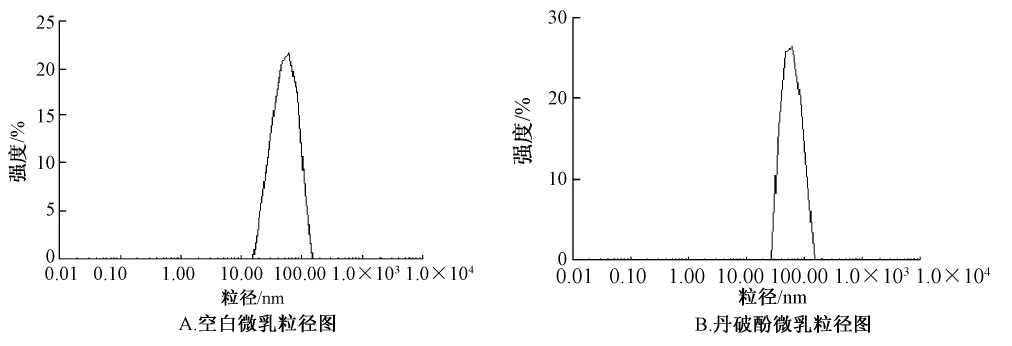
图3 微乳粒径图Fig.3 Particle size and distribution of m icroemulsion measured by laser analytical method
4.4 微乳稳定性初步考察将微乳放入高速离心机中,以10 000 r/min速度离心10 min,观察,未见沉淀、分层、浑浊等现象,微乳溶液均保持透明澄清[10]。对于外观透明或是半透明、流动性很好的水-油-乳化剂分散体系,保持100倍重力加速度离心5 min,未发生相分离,初步判断微乳稳定[11]。
5 HPLC法丹皮酚测定
5.1 色谱条件与系统适应性Hypersil ODS柱(大连依利特公司,5 μm,4.6 mm×150 mm);流动相为甲醇-水-乙酸(52∶48∶2);检测波长274 nm;柱温为室温;体积流量1.0 mL/min;进样量20 μL;在此色谱条件下,微乳辅料对丹皮酚的测定无干扰,理论塔板数按丹皮酚计算应不低于5 000。见图4。
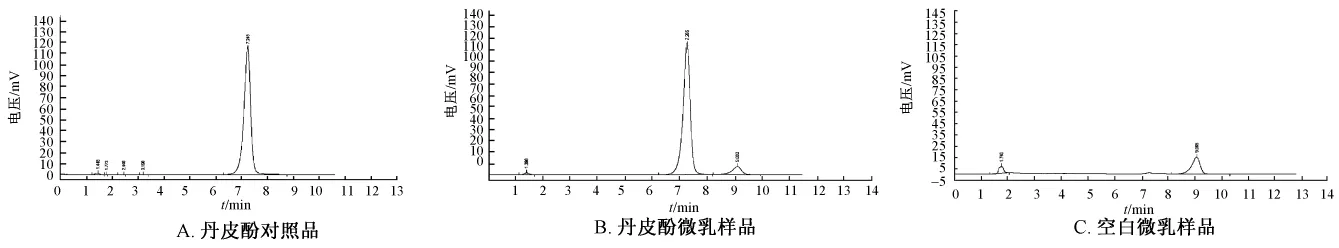
图4 丹皮酚HPLC色谱图Fig.4 HPLC chromatograms of paeonol
5.2 标准曲线的绘制取丹皮酚对照品约16 mg,精密称定,置50 mL量瓶中,加甲醇适量,使溶解,用甲醇稀释至刻度,摇匀,得质量浓度为312.4 μg/mL对照品贮备液。分别精密量取对照品贮备溶液0.1、0.4、0.7、1.0、1.3、1.6 mL,置10 mL量瓶中,加甲醇稀释至刻度,摇匀。按上述色谱条件分别进样20μL,测定峰面积,以峰面积(A)为纵坐标,以对应的丹皮酚对照品溶液的质量浓度(C)为横坐标,绘制标准曲线,求得线性回归方程:A=6.368 9×104C+1.762 6×104,r=0.999 9,n=6。结果表明丹皮酚在3.13~49.98 μg/mL范围内线性关系良好。
5.3 精密度试验分别取低、中、高浓度的对照品溶液,在一天内连续进样6次,考察日内精密度,RSD分别为0.52%,0.94%,1.06%;连续6d分别进样,考察日间精密度,RSD分别为0.88%,1.07%,1.22%。
5.4 稳定性和重复性试验取样品溶液分别在0,6 h,12 h,24 h,48 h,72 h进样测定峰面积,结果RSD为0.59%,说明3 d内样品溶液稳定。同一批样品溶液6份,进样测定,计算丹皮酚微乳中的丹皮酚含有量,RSD为0.38%(n=6),表明重复性良好。
5.5 回收率试验按处方比例配制空白微乳,精密加入低、中、高剂量的丹皮酚对照品9份,混合均匀,照含量测定项下方法测定微乳中丹皮酚的含量,计算平均回收率为99.22%,RSD为1.43%(n=9),见表2。

表2 加样回收率试验结果Tab.2 Results of recovery experiments of the methods
5.6 样品定量测定取丹皮酚微乳约0.12 g,精密称定,置50 mL量瓶中,加甲醇50 mL,超声30 min,称定质量(加甲醇补足损失质量),滤过,精密量取续滤液2.0 mL转至10 mL量瓶中,加甲醇稀至刻度,按上述色谱条件进行测定,计算丹皮酚的量,结果3批样品的含量分别相当于标示量的102.1%,101.4%,97.8%。
6 讨论
6.1 表面活性剂通常以亲水亲油平衡值(HLB)设计微乳配方,选择HLB值为8~18时配制O/W型乳剂。本实验选用HLB值大于8的表面活性剂OP-10、Tween80、Tween20、Solutol HS 15,但Tween20、Poloxamer188作为表面活性剂不能形成微乳,可能是HLB值比较高,亲水性比较强,乳化能力较弱[12]。
6.2 助表面活性剂的作用主要是增加界面膜的流动性,降低界面张力,调节HLB值。醇与表面活性剂形成的界面膜柔性高,易于弯曲,易形成微乳[12]。同时,羟基的引入使得亲水性增加,易和表面活性剂中聚氧乙烯基上的氧形成氢键,增强油水间界面膜的刚性,与水易形成液晶或凝胶,不利于形成微乳[13]。PEG400、甘油、1,2-丙二醇与表面活性Tween80、OP-10均形成凝胶。
6.3 从微乳区域角度看,Km减小,微乳区先增大再减小,这是由于当助表面活性剂正好完全镶嵌到表面活性剂中,此时,表面活性剂与助表面活性剂形成最佳的配比,微乳结构中增溶空间最大,载油量最大。当Km增大时,有形成液晶的趋势,增大到一定程度不能形成微乳。
6.4 HPLC法测丹皮酚含量时,以甲醇-水(55∶45)[14]为流动相,丹皮酚峰分离度差;而用甲醇-水(52∶48)为流动相,虽然丹皮酚峰与干扰组分峰达到基线分离,但柱效低,因此在流动相中加入少量乙酸调节柱效[15],当乙酸占流动相2%时得到柱效很好的峰,乙酸占流动相3%时柱效无显著改变,最终确定甲醇-水-乙酸(52∶48∶2)为最佳流动相,此时,微乳中丹皮酚峰与干扰组分峰达基线分离,方法专属性强,重复性好,回收率好。
6.5 本实验研制丹皮酚微乳,并考察其理化性质,处方中选用丁香油为油相,抑菌活性成分为丁香酚[16];非离子型表面活性剂为OP-10,对皮肤无任何刺激性反应,生物相容性好,毒性低,溶血性小,具有良好的安全性[17-18];且异丙醇为助乳化剂,亦是很好的杀菌剂[19]。这为后续进一步研制丹皮酚微乳凝胶透皮给药系统奠定实验基础。
[1]吕成明,刘海燕.丹皮酚的药理作用研究进展[J].医药导报,2005,24(2):142-143.
[2]张旃,李明昌.丹皮酚的药理作用及机制[J].中医药信息,2006,23(2):21-23.
[3]陆彬主编.药物新剂型与新技术[M].北京:人民卫生出版社,1998.59-89.
[4]Schechter R S.Microemulsions and Related Systems[M].New York:Marcel Dekker,1998.1-200.
[5]Chen HB,Chang X,Weng T,et al.A study of microemulsion systems for transdermal delivery of triptolide[J].J Control Release,2004,98(3):427-436.
[6]Sintov AC,Shapiro L.New microemulsion vehicle facilitates percutaneous penetrationin vitroand cutaneous drug bioavailabilityin vivo[J].J Control Release,2004,95(2):173-183.
[7]平其能.现代药剂学[M].北京:中国医药科技出版社,1998.1-856
[8]莫春生,邻实华.十六烷基三甲基溴化胺/正丁醇/正庚烷/水四组份体系的相行为及微乳结构研究[J].江西师范大学学报:自然科学版,2001,25(2):144-150.
[9]HO H O,Hsiao C C,Sheu M T.Preparation of microemulsions using polyglycerol fatty acid esters as surfactant for the delivery of protein drugs[J].J Pharm Sci,1996,85(2):138-143.
[10]梁臻,毛声俊,尹宗宁,等.丹参酮ⅡA静脉乳剂的制备与质量评价[J].中国中药杂志,2008,33(11):1249-1251.
[11]黄清臻,邵新玺,周广平,等.微乳缓释气雾杀虫剂的研制[J].中国媒介生物学及控制杂志,2000,11(4):276-278.
[12]王晓黎,蒋雪涛,李干佐,等.非离子型表面活性剂微乳的基础研究[J].解放军药学学报,2001,17(6):297-300.
[13]吴顺芹,李三鸣,郎轶咏,等.水包油型微乳形成因素的考察[J].沈阳药科大学学报,2005,22(2):96-99.
[14]谢文健,陈燕芬,吴打红.HPLC法测定调肠消炎片中丹皮酚的含量[J].中药材,2007,30(6):740-741.
[15]张佳佳,戴静波.高效液相色谱法测定妇乐泡腾颗粒剂中丹皮酚的含量[J].时珍国医国药,2007,18(8):1911-1912.
[16]楼兴隆,李晓明,张鞍灵.丁香油抑菌成分研究[J].西北农业学报,2006,15(3):91-93.
[17]赵国玺,朱瑶.表面活性剂作用原理[M].北京:中国轻工业出版社,2003:589-634.
[18]安红丽,欧阳五庆,王俊,等.非离子型表面活性剂微乳的研制[J].西北农林科技大学学报:自然科学版.2007,35(3):65-69.
[19]叶海英,张忠义,高申.法莫替丁微乳的研制及其质量评价[J].第一军医大学学报,2003,23(1):68-70.
