杯芳烃及其衍生物的应用研究进展
2012-01-14谢媛媛
夏 旺 谢媛媛
(浙江工业大学药学院,浙江 杭州 310014)
杯芳烃是由酚醛缩合而得到的环状低聚体[1],具有独特的空腔结构,因其良好的化学稳定性、高熔点,以及空腔大小可以调节等独特的物理、化学性能而倍受广大科学工作者的关注。杯芳烃具有易于衍生化的特点,与所需功能基团反应得到各种功能化的杯芳烃衍生物,可应用于各种目的。目前,杯芳烃广泛应用于分子离子识别、模拟酶、相转移催化剂、光学传感器等方面,在医药方面的研究也取得了突破性的进展。本文介绍了杯芳烃及其衍生物在医药、分子离子识别、模拟酶、相转移催化剂等方面的研究进展。
1 杯芳烃及其衍生物在医药方面的应用
通过对杯芳烃骨架的化学修饰,功能化的杯芳烃在抗菌活性、抗病毒活性、药物的增溶剂或分散剂、药物缓释剂及药物载体等方面的研究取得了可喜的成绩。
Tsou等[2]研究发现,下缘四丁基取代杯[4]芳烃衍生物具有潜在的抗艾滋病病毒和丙型肝炎病毒活性的双重作用,构效关系研究表明,杯[4]芳烃烷基化后保持锥式构象和杯[4]芳烃上缘的基团对其活性起到了至关重要的作用。
Bezouska等[3]发现了一类新的对CD69白细胞细胞膜受体有高亲和力的配体--含羧基的杯芳烃衍生物。他们研究了三个含羧基的杯芳烃衍生物(图1,化合物1,2,3)对CD69白细胞细胞膜受体的亲和力强弱,结果表明硫杂杯芳烃衍生物(化合物2)对CD69白细胞细胞膜受体的亲和力最强。这些含羧基的杯芳烃衍生物也被证明具有保护CD69high淋巴细胞的作用。

图1
喹诺酮类萘啶酸和β-内酰胺类青霉素V是两种经典的抗菌杂环化合物。Salem等[4]将这两种化学结构的一种或两种引入对叔丁基杯[4]芳烃的下缘制备了三个二取代对叔丁基杯[4]芳烃衍生物(图2,化合物4,5,6)。以2个革兰氏阴性菌(E.coli ATCC 25922,P.aeruginosa ATCC 27853)和3个革兰氏阳性菌(S.aureus ATCC 25923,S.aureus ATCC 29213,E.faecalisATCC 29212)评估其抑菌活性,研究发现只有同时含有喹诺酮类萘啶酸和β-内酰胺类青霉素V两种结构的化合物6对其中的一个革兰氏阳性菌(S.aureus ATCC 25923)菌株具有抑菌活性,原因有待进一步研究。

图2
Moure等[5]对对位胍基取代的杯[4]芳烃进行修饰,得到二噻唑环和二吡啶环取代的杯[4]芳烃衍生物,并对其抑菌活性进行研究。以革兰氏阴性菌和革兰氏阳性菌评估其抑菌活性,修饰后的对位胍基取代的杯[4]芳烃衍生物的抑菌活性比母体化合物对位胍基取代的杯[4]芳烃的抑菌活性更强,研究证实是由于杯[4]芳烃上取代的胍基和杂环协同作用的结果。此外,Moure等[6]还用一系列杯[4]芳烃衍生物,包括磺酸盐、羧酸盐、磷酸盐,对其中6种化合物的下缘环进行噻唑环二取代。评估这几种杯[4]芳烃衍生物对各种HIV病毒和淋巴细胞的抗HIV活性。实验证明,杯芳烃衍生物无细胞毒性,在10~50μmol/L的范围内,均具有一定的抗病毒活性,特别是磺酸盐衍生物,活性最佳。杯芳烃及其衍生物已被证明在体内无毒,不引起免疫反应,此特性必将引起人们在这方面的研究兴趣。郑炎松等[7]研究发明了一种用作增溶剂或者分散剂的两亲性树枝状杯芳烃,在杯芳烃的上缘连接有树枝状的聚氧乙烯醚链,在下端连接有烷基链,既能溶于非极性有机溶剂,又能溶于水中。这种两亲性杯芳烃能够使难溶于水的消炎止痛药萘普生以及布洛芬等在水中易于溶解,能使抗癌药物喜树碱在水中有效地分散,成为稳定的悬浊液。
2 杯芳烃及其衍生物在分子离子识别方面的应用
杯芳烃的空腔显示优良的识别、配合性能。杯芳烃化合物不但可以进行分子内包合外,还能够进行分子间包合。借助于氢键、静电作用、范德华力、疏水作用及诱导契合等非共价键协同作用,杯芳烃化合物可以很好的识别多数碱金属离子、碱土金属离子、副族及过渡金属离子以及多种有机分子。
杯芳烃及其衍生物对金属离子等具有优良的识别性能。利用杯芳烃衍生物能从有机溶剂中萃取Ag2+,Cu2+,Ca2+,Zn2+,Co2+,Ni2+等碱金属、碱土金属离子。并且利用杯芳烃对其他族系的金属离子,例如镧系、锕系金属离子进行萃取取得成功。由于杯芳烃及其衍生物能萃取金属离子,因此这一特性被应用于除去废水中的Co2+、高价Cr、Ce2+等重金属离子。Lee等[8]用紫外光谱法研究了杯冠醚(图3,化合物7,8)对碱金属离子和过渡金属离子的识别作用,杯冠醚化合物7对金属离子选择性顺序为K+>Rb+>Cs+>Na+>Ca2+>Li+;而杯冠醚化合物8的选择性顺序为Cs+>Rb+>K+>Ca2+>Li+>Na+。刘芳等[9]的研究表明,对叔丁基杯[4]芳烃及其酯类衍生物在强酸性条件下对Ag+均有一定的萃取能力,且对叔丁基杯[4]芳烃乙酸乙酯对Ag+的萃取能力明显高于对叔丁基杯[4]芳烃。Psychogios等[10]在杯[4]芳烃上缘引人磷酸酯基团,在下缘引入2,2ˊ-双吡啶结构,磷酸酯基团的引入增大了杯芳烃的水溶性,对水中的Cu+有良好的识别作用,可将Cu+从水中分离。
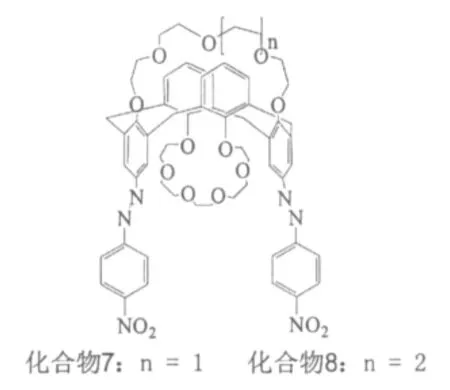
图3
杯芳烃及其衍生物在阴离子识别方面的报道还比较少,主要是由于杯芳烃内部结构与电荷特征所致。经化学修饰后的杯芳烃具有识别阴离子的作用,如将阳离子、酰胺、胍、脲等基团引入杯芳烃骨架后能很好的识别阴离子。其识别功能主要是通过氢键作用和静电作用进行的。Tongraung等[11]在杯[4]芳烃上缘苯环上引人脲基结构(图4,化合物9,10),研究发现这两个化合物对几种阴离子的选择性顺序为:H2PO4->C1->Br->NO3-,其中含冠醚结构的化合物10比化合物9对C1-和Br-的亲和力更强,但对H2PO4-的亲和力更弱。Lang等[12]在杯芳烃上缘引入卟啉环和脲的组合基团,通过紫外光谱法发现它们对卤素离子有较好的选择性。Wolf等[13]在杯[4]芳烃下缘引入N,N-二乙基甲酰基后,研究发现一系列的此类杯[4]芳烃衍生物能很好地从水溶液中萃取出HPO42-,SeO42-,VO3-,ReO4-,CrO42-,WO42-,MoO42-等含氧酸根离子,此方法可应用于治理重金属污染。
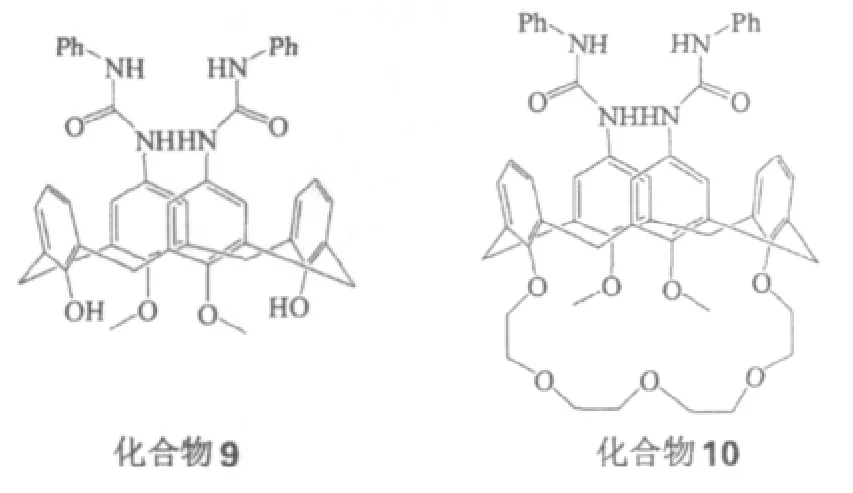
图4
杯芳烃及其衍生物对中性分子也具有识别作用。Gutsche等研究认为,杯芳烃通过与有机分子形成固态和液态包合物能够识别多种有机小分子(如括二氯甲烷、氯仿、甲醇、苯甲醚、苯、甲苯、吡啶、氧化吡啶、二氧六环等),其识别方式主要是以氢键作用、静电作用和疏水作用为推动力,并以孔穴大小作为选择性依据[14]。一般来说,杯芳烃及其衍生物的亲脂性,空腔与有机分子的空间大小及构型的匹配影响着识别的性能,而其中杯芳烃及其衍生物对生物活性分子(如蛋白质、氨基酸、糖类化合物等)的识别也是杯芳烃化学重要的发展方向之一。
3 杯芳烃及其衍生物在模拟酶方面的应用
酶是细胞内产生的具有高度专一性和催化效率的蛋白质,又称生物催化剂,可以催化很多反应。以模仿天然酶对底物识别和高效催化活性为目的的模拟酶是近年来的研究热点。杯芳烃及其衍生物能选择性识别分子离子,是良好的离子载体和酶模拟物,可作为人工酶模拟天然酶的生物催化功能。
1992年,Cacciapaglia等[15]在杯[4]芳烃上缘引入一个冠醚基团,合成了一系列杯[4]冠醚-Ba2+配合物,研究发现此类配合物在乙酸对硝基苯酯的醇解中具有优良的酯酰基转移酶活性。Molenveld等[16]在杯[4]芳烃上缘引入吡啶基团,合成了含吡啶基的杯[4]芳烃-Cu2+配合物,该模拟酶具有很高的催化性能,能使RNA模型底物2-羟基丙基-对硝基苯基磷酸二酯的酯键裂解和环化反应加速1×104倍。2006年,Cacciapaglia等[17]又合成了水溶性杯[4]芳烃-Cu2+配合物(图5,化合物11,12,13),在pH=7.0的水溶液中,化合物11和13作为模拟酶使对磷酸二酯的水解速率提高了1×104倍,化合物12作为模拟酶在裂解RNA的反应中加速了5×105倍。

图5
4 杯芳烃及其衍生物在相转移催化剂方面的应用
相转移催化剂需要同时具有亲脂和亲水性基团,可以在两相介质中进行物质的传递。杯芳烃的上缘和下缘经过修饰后可满足这种需要,因此经化学修饰后的杯芳烃具有优良的相转移催化性能。
Buriks等[18]研究发现下缘连有乙氧链的对叔丁基杯芳烃(图6,化合物14)在非极性介质中具有相转移催化能力,可以解决油水乳化问题,还可应用于石油精馏。此外,化合物14(n=6,m=3)在醚合成反应、酯化反应、氧化反应、加成反应、脱水反应等有机反应中具有很高的相转移催化活性[19]。在下端含有酯基的杯芳烃也具有很好的相转移催化性能。丙烯酸正丁酯在醋酸酯中用过硫酸盐催化聚合时,加入易得的含酯杯芳烃衍生物(图6,化合物15),能使过硫酸盐进入有机相,迅速引发自由基聚合反应,其效果比这类反应最佳的催化剂15-冠-5还要好。

图6
5 结语
近年来,杯芳烃及其衍生物在医药、分子识别、催化剂、模拟酶等领域中的研究取得了很大的进展,在超分子化学研究中具有无可比拟的优势。杯芳烃及其衍生物的研究发展与人类的需求密切相关,可以预见今后对杯芳烃的研究将更关注其实际应用,尤其将会在生命科学、材料学、医药学等学科中具有更广阔的应用前景。
[1]Iwamoto K,Araki K,Shinkai S.Synthesis of all possible conformational isomers of O-alkyl-p-t-butylcalix[4]arenes[J].Tetrahedron,1991,47:4325-4342.
[2]Tsou L K,Dutschman G E,Gullen E A,et al.Discovery of a synthetic dual inhibitor of HIV and HCV infection based on a tetrabutoxy-calix[4]arene scaffold[J].Bioorg.Med.Chem.Lett.,2010,20:2137-2139.
[3]Bezouska K,Snajdrova R,Krenek K,etal.Carboxylated calixarenes bind strongly to CD69 and protect CD69+Killeer cells from suicidal cell death induced by tumor cell surface ligands[J].Bioorg.Med.Chem.,2010,18:1434-1440.
[4]Salem A B,Sautrey G,Fontanay S,et al.Molecular drug-organiser:Synthesis,characterization and biological evalution of penicillin V and/or nalidixic acid calixarene-based podands[J].Bioorg.Med.Chem.,2011,19:7534-7540.
[5]Mourer M,Dibama H M,Fontanay S,et al.p-Guanidinoethyl calixarene and parent phenol derivatives exhibiting antibacterialactivities.Synthesisand biological evaluation[J].Bioorg.Med.Chem.,2009,17:5496-5498.
[6]Mourer M,Psychogios N,Laumond G,et al.Synthesis and anti-HIV evaluation of water-soluble calixarene-based bithiazolyl podands[J].Bioorg.Med.Chem.,2010,18:36-38.
[7]刘炎松,黄宏.用作溶剂或者分散剂的两亲性树枝状杯芳烃:CN,101921210 A[P].2010-12-22.
[8]Lee S H,Kim J H,Ko J,et al.Regioselective complexation of metal ion in chromogenic calix[4]biscrowns[J].J.Org.Chem.,2004,69:2902-2905.
[9]刘芳,罗欣,等.杯[4]芳烃及其酯类衍生物对贵金属离子银的回收研究[J].云南环境科学,2005,24(1):1-3.
[10]Psychogjios N,Bernard J,Devaains R.A new watersoluble calix[4Jarene podand incorporating-phosphonate groups and 2.2'-bipyrdine units[J].Tetrahedron Lett.,2002,43:7691-7693.
[11]Tongraung P,Chantarasiri N,Tuntulani T.Calix[4]arenes containing urea and crown/urea moieties:effects of the crown ether unit and Na+towards anion binding ability[J].Tetrahedron Lett.,2003,44:29-32.
[12]Dudic M,Lhotak P,Stibor I,et al.Calix[4]areneprophyrin conjugates as versatilemolecular receptors for anions[J].Org.Lett.,2003,5:149-152.
[13]Wolf N J,Georgiev E M,Yordanov A T,et al.Synthesis and crystal structures of lower rim amine and carbamoyl substituted calixarenes astransfer agents for oxyanions between an aqueous and a chloroform phase[J].Polyhedron,1999,18:885-896.
[14]史春越,曹家庆,范平.杯芳烃对有机小分子识别作用的研究进展[J].辽宁大学学报,2003,30(1):82-86.
[15]Cacciapaglia R,Casnati A,Mandolini L,et al.The Barium(II)complex of p-tert-butylcalix[4]arene-crown-5:a novel nucleophilic catalyst with transacylase activity[J].J.Am.Chem.Soc.,1992,114:10596-10598.
[16]Molenxeld P,Engbersen J F,Kooijman H,et al.Efficient catalytic phosphate diester cleavage by the synergetic action of two Cu(II)centers in a dinuclear cis-diaqua Cu(II)calyx[4]arene enzyme model[J].J.Am.Chem.Soc.,1998,120:6726-6737.
[17]Cacciapagia R,Casnati A,Mandolini L,et al.Catalysis of diribonuleoside monophosphate cleavage by water soluble copper(II)complexes of calix[4]arene based nitrogen ligands[J].J.Am.Chem.Soc.,2006,128:12322-12330.
[18]Buriks R S,Fauke A R,Mange F E.Oxyalkylated cyclic phenol-aldehyde resins and uses therefore:US,4032514[P].1997-06-28.
[19]王腾凤,杨世柱.杯芳烃催化剂在有机反应中的应用[J].化学试剂,2000,22(1):274-278.
