Au@Ag核壳纳米粒子的合成及其催化性能研究
2012-01-05胡兰兰金珊霞刘自纯李文嘉刘禅刘丽娜叶勇
胡兰兰,金珊霞,刘自纯,李文嘉,刘禅,刘丽娜,叶勇
(湖北大学化学化工学院,湖北 武汉 430062)
芳香胺作为一类重要的有机合成中间体,被广泛应用于化工、医药、燃料、农药、高分子材料等行业中[1].在芳香胺的合成中,由于以芳香硝基化合物为前体物的反应过程具有操作简便、原料易得等优点,所以极大多数的芳香胺是由其相对应的芳香硝基化合物还原得到的.将芳香硝基化合物还原的方法主要有水合肼还原法[2]、催化加氢还原法[3]、硫化碱还原法[4]、一氧化碳还原法[5]、铁屑还原法[6]、光化学还原[7]及电化学还原法[8].由于在常温下硼氢化钠对该反应的还原能力很弱,文中首先用柠檬酸钠法合成了一系列Au@Ag核壳纳米粒子,然后以该纳米粒子为催化剂,用紫外光谱作为分析手段研究该反应,同时讨论了影响反应速率的部分条件,为进一步研究金属纳米粒子的催化活性打下基础.
1 实验部分
1.1试剂与仪器柠檬酸钠(Na3C6H5O7·2H2O)购于汕头市光华化学厂,纯度为99.0%;氯金酸(HAuCl4·4H2O)购于国药集团化学试剂有限公司,纯度为99.0%;硝酸银(AgNO3)购于天津市天感化工技术开发公司,纯度为99.5%;对硝基苯酚购于Acros Organics公司;硼氢化钠(NaBH4)购于国药集团化学试剂有限公司,纯度为99.0%,所有溶液均用二次去离子水配制.KQ-160TDE型数显温控超声波清洗仪(昆山市超声仪器有限公司),UV2300型紫外-可见光谱仪(上海天美科学仪器有限公司),Technai型透射电子显微镜(日本电子公司).
1.2Au@Ag核壳纳米粒子的制备第1步:参考Frens法[9]制备金溶胶:将0.01%(质量分数)的氯金酸溶液加热至沸腾,向其中一次性加入3 mL 1%(质量分数)的柠檬酸钠溶液,保持沸腾15 min后自然冷却待用.第2步:取上述金溶胶19 mL加水稀释至95 mL,向其中加入一定量1%(质量分数)的柠檬酸钠溶液,快速搅拌加热至沸腾后缓慢滴加5 mL一定浓度的硝酸银溶液,保持沸腾1 h后自然冷却.通过改变Au和Ag的物质的量之比获取不同粒径的核壳纳米粒子溶液.
1.3Au@Ag核壳纳米粒子对对硝基苯酚的催化还原向1 cm×1 cm×3 cm的石英比色皿中依次加入一定浓度的对硝基苯酚、硼氢化钠,混合均匀后加入适量Au@Ag核壳纳米粒子,然后进行紫外跟踪测试,观察吸收峰的变化.
2 结果与讨论
2.1Au@Ag核壳纳米粒子的表征图1为不同n(Au)∶n(Ag)比的Au@Ag核壳纳米粒子的TEM图.由图可见,其粒径分布均匀且都近似为球形.由于金银对电子的散射能力不同,因而从TEM图明暗程度可以判断粒子中金银的分布情况,如果颜色不同则为核壳结构[10].图1中三图粒子的颜色明暗分明,证明这些粒子是核壳结构.随着硝酸银浓度的增大,核壳纳米粒子的平均粒径呈增大趋势.

图1 不同n(Au)∶n(Ag)的Au@Ag核壳纳米粒子TEM图(a.1∶1;b.1∶2;c.1∶3)
图2是不同比例的核壳结构的UV-vis光谱图,相对于单纯的金纳米(519 nm),核壳结构的表面等离子共振吸收峰随银浓度的增加而发生蓝移,吸收峰谱带变宽.当n(Au)∶n(Ag)<1∶3时仍然呈此趋势且位移很大,谱峰出现在400 nm左右,表明此时在金的外层已经包覆了很厚的银层.

图2 不同物质的量比的Au@Ag核壳纳米粒子的UV-vis光谱图
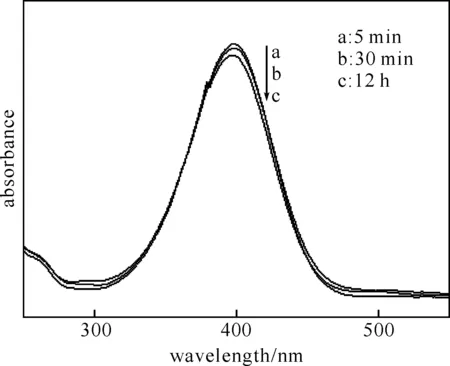
图3 对硝基苯酚与硼氢化钠混合溶液的吸收光谱
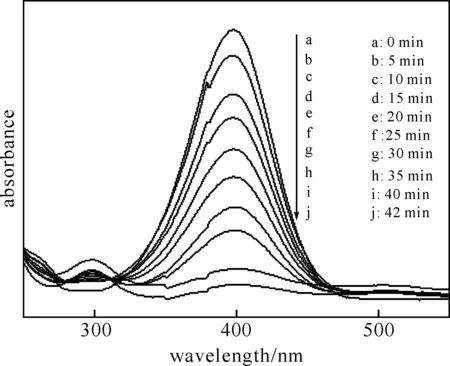
图4 n(Au)∶n(Ag)=1∶1纳米粒子催化对硝基苯酚还原吸收光谱随时间的变化
2.2Au@Ag核壳纳米粒子对对硝基苯酚的催化还原从图3可以看出,在室温下对硝基苯酚很难被硼氢化钠还原,当把硼氢化钠和0.2 mL Au@Ag纳米粒子(n(Au)∶n(Ag)=1∶1)溶液依次加入到对硝基苯酚溶液中时,可以看到溶液颜色从浅黄色变成黄绿色直至最后退为无色,表明反应进行完全.用紫外对此过程进行追踪测试,其对应谱峰变化如图4所示,对硝基苯酚位于400 nm左右的特征吸收峰随时间逐渐降低至消失,同时在300 nm附近出现新的吸收峰,其强度随时间逐渐增强.该新峰为对氨基苯酚的特征谱峰,表明对硝基苯酚被还原成了对氨基苯酚.当反应进行到42 min时,各谱峰的强度几乎不再发生变化,表明此时反应已基本趋于完成.
2.3催化剂用量对反应速率的影响一般情况下,化学反应速率会受到催化剂用量的影响.如图5所示,保持对硝基苯酚和硼氢化钠的浓度不变,考察了催化剂用量对反应速率的影响.图5中(a)、(b)和(c)分别为加入核壳纳米粒子溶液0.4 mL、0.8 mL和1.0 mL时对硝基苯酚还原反应的紫外追踪图,结合图4我们以反应完全所需的时间t为横坐标,以反应过程中对硝基苯酚的吸光度为纵坐标作图(d),可见,随着催化剂用量的增多反应物谱峰的下降速度加快.即催化剂用量越多反应速率越快.

图5 n(Au)∶n(Ag)=1∶1的核壳纳米粒子催化剂用量对催化反应的影响a:0.4 mL;b:0.8 mL;c:1.0 mL
2.4氧化物自身性质的影响氧化物自身的性质是影响催化反应的一个重要因素.对于给定浓度的纳米粒子,诱导时间随硝基化合物种类的不同而改变,通常由于静电相互作用,带正电荷的硝基化合物比带负电荷的硝基化合物具有更高的催化活性[11].对硝基苯酚与硼氢化钠反应开始时,形成对硝基苯酚的钠盐,苯环上的羟基变成氧负离子,由于氧负离子的共轭效应和吸电子性,使硝基上的电子云密度较对硝基苯胺硝基上的电子云密度小.图6是研究硼氢化钠还原对硝基苯胺的速率图,与图4比较,对硝基苯酚在40 min左右已经接近反应完全,而在此时间内经计算对硝基苯胺的转化率不到20%,由此可得对硝基苯酚的还原速率明显比对硝基苯胺快.

图6 n(Au)∶n(Ag)=1∶1的核壳纳米粒子催化对硝基苯胺还原吸收光谱随时间的变化

图7 0.8 mL n(Au)∶n(Ag)=1∶3的核壳纳米粒子催化对硝基苯酚还原吸收光谱随时间的变化
2.5粒径对反应速率的影响随着n(Au)∶n(Ag)比的增大,核壳纳米粒子的粒径增大,而纳米粒子的尺寸大小会影响其催化效率.因为金属纳米粒子的氧化还原电势依赖于粒径,电势随着粒径的增加而增加.对于给定浓度的金属纳米粒子,粒径越小,电势越负,使得金属纳米粒子与硝基化合物之间的电势差越大,以至具有更高的催化活性,反应能够更快进行[11].图7为n(Au)∶n(Ag)=1∶3的Au@Ag核壳纳米粒子(0.8 mL)对对硝基苯酚催化还原的紫外追踪图,反应进行到27 min时已趋于完成,反应物特征峰相比较于图5中(a)而言下降的要快,说明Au@Ag纳米粒子的粒径会影响对硝基苯酚的催化还原,且粒径越大反应速率越慢.
3 结论
用柠檬酸钠法合成了不同粒径的Au@Ag核壳纳米粒子,利用TEM和UV-vis光谱对其进行了表征;探讨了所合成的核壳纳米粒子对芳香族硝基化合物的催化还原作用,结果显示该核壳纳米粒子对芳香族硝基化合物的还原具有较好的催化作用,其还原产物为相对应的芳香胺;通过对影响反应速率因素的考查为下一步研究催化作用机理打下基础.
[1] Lauwiner M,Rys P,Wissmann J. Reduction of aromatic nitro compounds with hydrazine hydrate in the presence of an iron oxide hydroxide catalyst.(Ⅰ):the reduction of monosubstituted nitrobenzenes with hydrazine hydrate in the presence of ferrihydrite[J].Appl Catal Agene,1998,172:141-148.
[2] Furst A,Hooton B R. Hydrazine as a reducing agent for organic compounds[J].Chem Rev,1965,65:51-68.
[3] Coq B,Tijani A. Influence of support,metallic precursor on the hydrogenation of p-chloronitrobenzene over supported platinum catalysts[J].J Mol Catal,1993,79:25-264.
[4] 马金华.邻氨基苯乙醚的相转移催化合成[J].精细化工,1997,14:59-61.
[5] Nose A,Kudo T.Reduction with sodium borohydride-transition metal salt systems reduction of aromatic nitro compounds with the sodium borohydride-nickelous chloride system[J].Chem Pharm Bull,1981,29:1159-1161.
[6] Hung H M,Ling F H.Kinetics and mechanism of the enhanced reductive degradation of nitrobenzene by elemental iron in the presence of ultrasound[J].Environ Sci Technol,2000,34:1758-1763.
[7] 张天永,由兰英,张有兰.石英反应器中硝基物的光催化还原[J].精细化工,2005,22:231-233.
[8] Jiang J H,Zhai R S,Bao X H.Electrocatalytic properties of Cu-Zn amorphous alloy towards the electrochemical hydrogenarion of nirobenzene[J].Allays Comp,2003,354:248-258.
[9] Frens G. Controlled nucleation for the regulation of the particle size in monodisperse gold suspensions[J].Nat Phys Sic,1973,241:20-24.
[10] 崔颜,顾仁敖.Ag核Au壳金属复合纳米粒子的制备及表面增强拉曼光谱研究[J].高等学校化学学报,2005,26:2092-2098.
[11] Jiang Z J,Liu C Y,Sun L W.Catalytic properties of silver nanoparticles supported on silica sphere[J].Ph-ys Chem B,2005,109:1730-1735.
