黑液高温气化合成混合醇的操作条件分析
2012-01-05孙振丽
王 逊 高 峻 孙振丽
(1.中国科学院先进能源动力重点实验室,中国科学院工程热物理研究所,北京,100190;2.中国科学院能源动力研究中心,北京,100190;3.中国城市建设研究院,北京,100120)
造纸黑液高温富氧气化不仅可用于回收黑液中的化学品,而且可将黑液中的有机物转化为合成气[1-6]。该气体由 H2、CO、CO2及少量 CH4、N2等组成,可用于合成甲醇等燃料和化学品[4-8]或进行热电利用[9]。虽然目前对用其合成低碳混合醇(以下简称混合醇)的报道较少,但由于混合醇合成原料气的最佳氢碳摩尔比[10-11]接近黑液气化合成气的氢碳摩尔比,利用黑液气化合成混合醇可简化甚至取消氢碳摩尔比调节过程。此外,混合醇可作为代用燃料、燃料添加剂、化工产品和化工原料,具有广阔的应用前景。因此,本研究将黑液气化与混合醇合成结合,提出一种黑液资源化利用新途径并加以分析。
在各种合成催化剂中,碱金属掺杂的硫化钼催化剂(ADM催化剂)突出的特点是具有良好的抗硫性和良好的水-气变换反应活性,且合成产物为直链混合醇、含水量低。采用ADM催化剂的CO加氢合成直链正构醇是一个复杂的化学反应体系。在甲醇和乙醇的形成机理和碳链增长模型研究方面,根据实验结果提出了CO逐级插入机理[12]、包含CO插入反应的合成反应动力学网络[13];在合成建模和产物预报方面,文献[14]对CO插入机理和产物分布进行简化,由实验结果回归出甲醇、乙醇、丙醇和碳烃化合物的生成速率。文献[15]在反应动力学网络中引入水-气变换反应、并考虑温度对反应动力学参数的影响,建立了详细反应动力学机理模型,可预报反应温度、反应压力、催化剂装填比、氢碳摩尔比对CO单程转化率和产物选择性的影响。文献[16]采用固定床工艺进行了混合醇试验(设计催化剂装填量为5 L),得到CO单程转化率、总醇选择性、烃选择性、总醇时空产率、C2+醇质量分数等反应性能。
文献[13-16]给出的结果均基于不含CO2的反应气,而文献[17]表明,反应气中CO2含量增多不利于混合醇合成,而黑液气化炉出口合成气中CO2含量较高,进行合成前需要脱除部分或全部CO2,这又会产生公用工程消耗。因此,研究以含碳合成气为原料的混合醇合成反应性能变化规律及反应气中CO2含量对反应性能的影响具有现实意义。此外,有必要考虑反应气中CO2含量对脱碳热负荷、吸收剂消耗的影响,将合成与净化集成起来,以确定反应气中适宜的CO2含量及相应的合成操作条件。因此,对混合醇合成过程,分析用不同CO2含量的反应气进行低碳醇合成的反应性能,得到反应气中CO2含量、催化剂装填比、反应温度、反应压力对CO单程转化率、总醇选择性、烃选择性、CO2选择性、总醇时空产率、C2+醇质量分数的影响规律;对合成气脱碳脱硫过程,分析反应气中CO2含量与H2S含量、吸收剂流量、再生器热负荷的关系;综合考虑净化、合成的特性规律,最终得到黑液气化制备混合醇的合成反应条件。
1 混合醇合成的产物预报模型
1.1 反应速率模型
采用钼系耐硫催化剂合成混合醇的主要反应产物为:直链正构醇(CnH2n+1OH),碳烃化合物(CnH2n+2,CnH2n),CO2,酯(CnH2n-1COOCH3),H2O。以CO加氢机理[12]和反应网络机理[13]为基础,文献[15]提出了一个详细的反应机理模型,它考虑了所有可能反应路径的表面活性中心浓度的影响。按此机理将合成反应分为:并行反应(见式(1)~式(4))、串行反应(见式(5)~式(8))和变换反应(见式(9))。
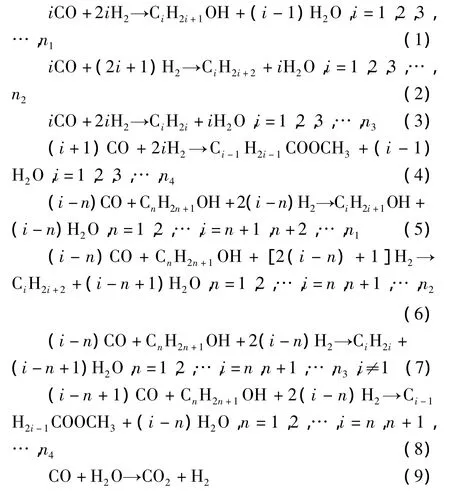
n1、n2、n3、n4表示产物中醇、烷、烯、酯碳的最大个数。该模型参数由固定床单管反应器实验结果回归得出,反应速率为LHHW型,用式(10)~式(19)表示。

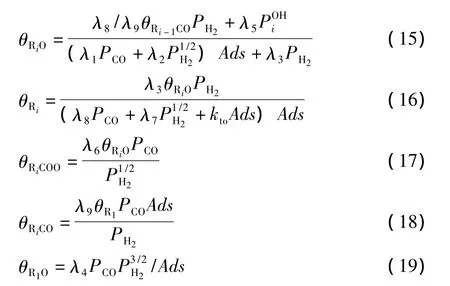
式中,参数 θRiO、θRiCOO、θRi、Ads、kto、Ki、λi是反应温度和反应物分压的函数,取值见文献[15]。
1.2 反应器模型
反应器内各组分的质量平衡和能量平衡见式(20)~式(30):

式中,OH、Para、Ole、E分别代表醇、烷、烯、酯;N为摩尔流量,kmol/s;Wcata表示催化剂装填量;ρcata表示催化剂堆密度,kg/m3;i表示碳的个数或化学反应系数;rji为生成j组分(碳的个数为i)的化学反应速率,kmol/(kg·s);Q为反应器放热,kW;ΔHi为第i个化学反应热,J/mol;As为反应管总横截面积,m2;L为沿反应管高度,m;WGS代表变换反应。
初始条件:L=0,各组分的流量已知,由低温甲醇洗出口流量给定。
1.3 影响参数和评价指标确定
催化剂装填比影响反应物和生成物的转化总量。温度直接影响反应速率。组分分压也影响反应速率。本研究的合成原料气的碳氢摩尔比由黑液高温气化决定,可视为已知,而反应气中CO2含量不仅影响混合醇合成性能,也影响气体净化的公用工程消耗。因此,选取催化剂装填比、温度、压力、反应气中CO2含量(干基)作为参数影响分析的重点。
采用 CO单程转化率(XCO)、总醇选择性(Xa)、烃选择性(XP)、酯选择性(XE)、CO2选择性(XCO2)、总醇时空产率(γ)、C2+醇质量分数(φ)评价合成性能变化和参数影响规律,定义见式(31)~式(35):

C2+醇质量分数φ为合成产物中C2+醇质量与总醇质量之比。总醇时空产率γ表示单位体积催化剂的总醇产量,定义见式(36)和式(37)。

式中,WOH表示总醇产量,g/h;τ为催化剂装填比,定义为合成塔催化剂装填质量与反应进气中的CO摩尔流量之比,g·h/mol。
1.4 模型验证
将混合醇合成的模拟结果与文献[15]的相应结果进行对比。结果表明,计算值与文献数据相符,可用于参数影响分析。
2 粗合成气制备混合醇的流程
粗合成气参数见表1[5]。来自黑液高温气化的粗合成气进入气体净化环节,以低温甲醇为吸收剂,脱除部分或全部CO2和H2S后成为净化气,然后经压缩、预热后作为反应气进入合成塔,生成混合醇,副产物为烷、烯、酯和CO2。高温产物放热后进入产物分离、精制单元,最终得到产品(见图1)。本研究模拟只涉及混合醇合成单程转化和粗合成气净化,高温气化及产物分离、精制等未涉及。
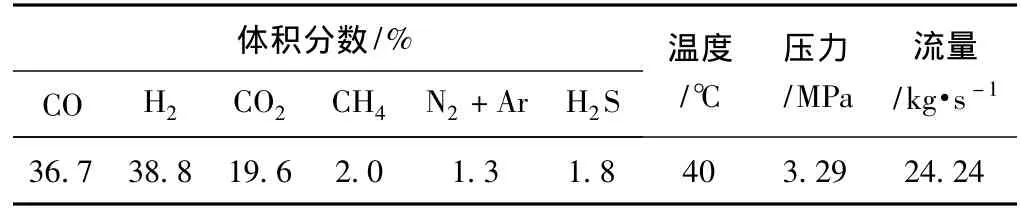
表1 粗合成气参数
3 结果与分析
3.1 产物选择性的变化规律
3.1.1 催化剂装填比影响
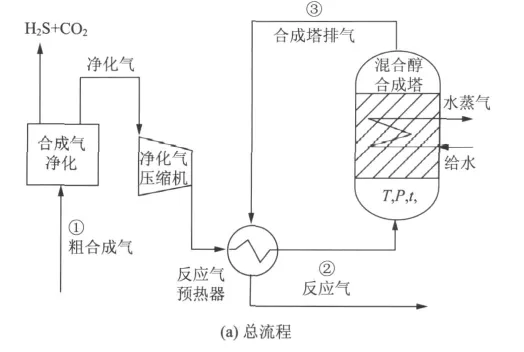
图2为给定合成温度(320℃)、合成压力(5 MPa,13 MPa)时,催化剂装填比对总醇选择性的影响。黑液气化合成气经过净化、预热后成为反应气,进入合成塔参与混合醇合成,反应气的CO2含量以参数YCO2表示,分别取0、10%、19.6%,即气化合成气脱除全部CO2、部分CO2、不脱除CO2。由图2可知,存在最佳催化剂装填比使总醇选择性最高,且随反应气CO2含量增多,该最佳值减小,但变化幅度较小,当CO2含量由0提高至19.6%,最佳装填比由30 g·h/mol降至20 g·h/mol;反应气 CO2含量对最大选择性取值影响较大,不脱CO2和完全脱CO2的情况相比,最大选择性由9.6%降至6.8% (13 MPa)、2.1%降至1.4%(5 MPa)。此外,还分析了不同反应气CO2含量下CO单程转化率、CO2选择性、烃选择性、酯选择性随催化剂装填比的变化。由分析结果可知,反应气CO2含量越低,催化剂装填比对各产物选择性影响越大,CO单程转化率随催化剂装填比增大呈近似线性增大,但增幅主要归结于CO2和烷烯等合成副产物的选择性明显增加,而混合醇不但没有增加反而减少。从总醇选择性角度,当反应气CO2含量在0~19.6%变化时,适宜的催化剂装填比范围是20 ~ 30 g·h/mol。
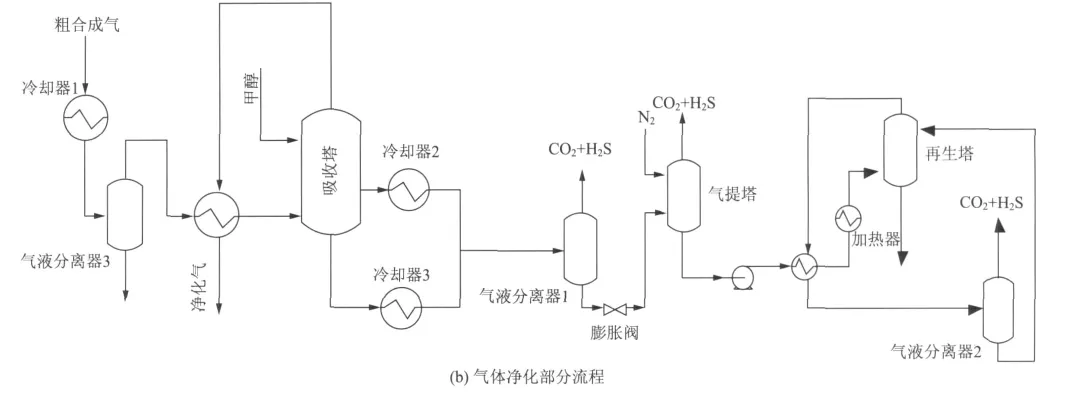
图1 粗合成气制备混合醇的流程
3.1.2 合成温度影响
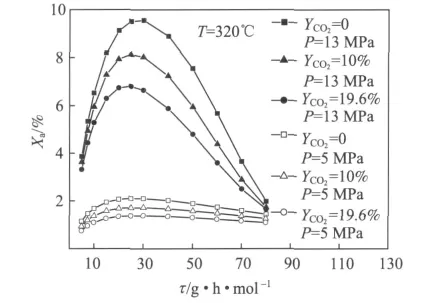
图2 催化剂装填比和反应气CO2含量对总醇选择性的影响
图3为给定催化剂装填比(20 g·h/mol)、合成压力(9 MPa)时,合成温度对总醇选择性的影响。由图3可知,存在最佳合成温度使总醇选择性最大,且该最佳温度随反应气CO2含量增加而下降,但变化幅度也较小,当CO2含量由0提高至19.6%,最佳合成温度在310~320℃之间。但合成温度在300~330℃之间,总醇选择性取值受反应气CO2含量影响较大,全部脱除CO2较不脱除CO2选择性增大46%(合成温度320℃)。此外,还分析了不同反应气CO2含量下CO单程转化率、CO2选择性、烃选择性、酯的选择性随合成温度的变化。由分析结果可知,提高合成温度有利于提高CO单程转化率,但温度高于320℃后,其增幅主要来自生成更多CO2、烷烃、烯烃等副产物。从总醇选择性角度,合成温度适宜范围为310~320℃。
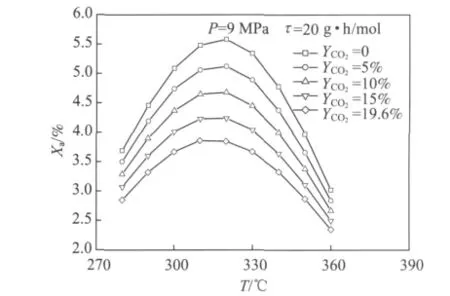
图3 合成温度和反应气CO2含量对总醇选择性的影响
3.1.3 合成压力影响
图4为给定催化剂装填比、合成温度时,合成压力对总醇及产物的选择性的影响。如图4(a)所示,随合成压力的增大,总醇选择性提高,但高压下反应气CO2含量对总醇选择性影响更大。图4(b)为CO单程转化率、CO2选择性、烃选择性、总醇选择性、酯选择性随合成压力的变化。可见与合成温度和催化剂装填比相比,提高合成压力不仅可以提高CO单程转化率,同时对总醇选择性提高的作用更大。改变反应气CO2含量进行分析可知,CO2含量越低,提高合成压力的效果越好。
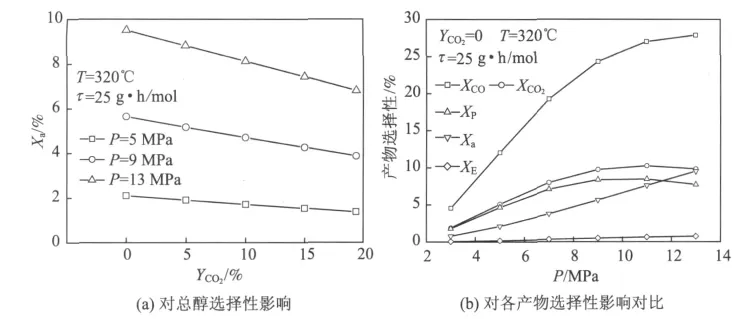
图4 合成压力和反应气CO2含量对产物选择性影响
3.2 产物组成的变化规律
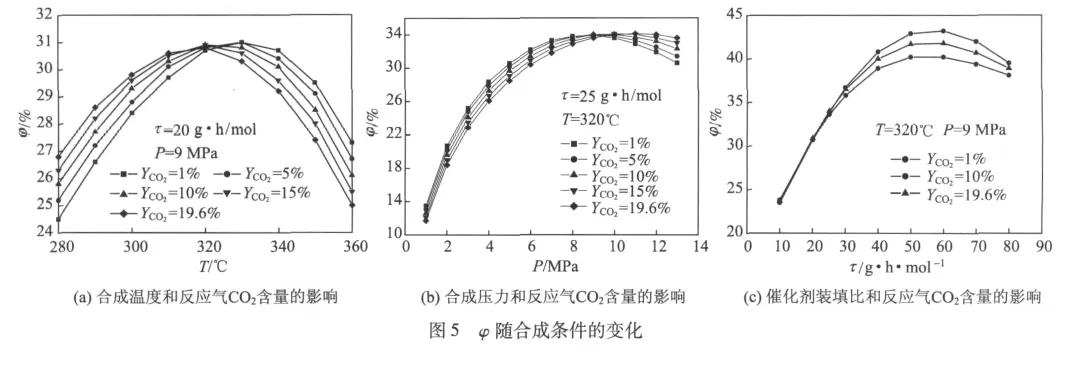
图5分析了C2+醇质量分数φ的变化规律。图5(a)给出了合成温度和反应气CO2含量对φ的影响,由此可见,存在最佳合成温度使φ最高,且随反应气 CO2含量变化,最佳合成温度取320~330℃,反应气CO2含量越低,该最佳合成温度越高。但当合成温度在320℃左右时,CO2含量对φ影响很小。因此,当合成温度取320℃时,即使反应气CO2含量在0~19.6%变化,也不会对φ造成较大影响;当合成温度低于320℃时,采用高CO2含量的反应气,总醇中的φ反而高,这是由于在此区间降低合成温度虽然导致各碳数醇选择性下降,但甲醇选择性下降幅度最大,而高于320℃时则相反。在分析的参数范围内,使φ最高的参数范围是:T=330℃,YCO2=0~5%。图5(b)给出了合成压力和反应气CO2含量对φ的影响,由此可见,对不同的反应气CO2含量,存在最佳合成压力使φ最大,且该值随反应气CO2含量增加而增大。当合成压力小于9 MPa时,脱除CO2有利于提高φ,但当合成压力继续升高,由于反应气 CO2含量越低,其甲醇的选择性增大越快,所以相同合成压力下,φ随反应气CO2含量增加而增大。取合成压力9~11 MPa时,即使反应气CO2含量在0~19.6%变动,φ仍可达到33%~34%。图5(c)为催化剂装填比和反应气CO2含量对φ的影响,可见选择适宜的催化剂装填比可使φ最高,该值高于总醇选择性最高的催化剂装填比,约为50~60 g·h/mol;当催化剂装填比≤30 g·h/mol时,CO2含量对φ影响很小;但CO2含量越低,φ受催化剂装填比影响越大。
3.3 总醇时空产率的变化规律
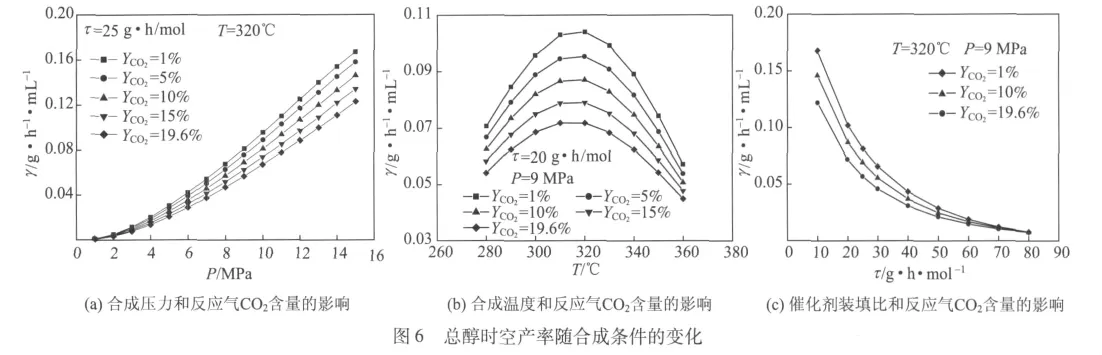
图6分析了总醇时空产率γ的变化规律。由图6可知,降低反应气CO2含量可以提高总醇时空产率;在最佳合成温度310~320℃下可使总醇时空产率最高,且在该温度区间总醇时空产率受反应气CO2含量影响较大;降低催化剂装填比、提高合成压力有利于提高总醇时空产率,但当催化剂装填比≤50 g·h/mol、合成压力≥3 MPa,总醇时空产率受反应气CO2含量影响较大。
3.4 净化气CO2含量与净化过程的关系
分析净化气CO2含量与净化过程的关系可得到,当吸收剂与粗合成气摩尔流量之比大于1.24时,可脱除CO2至1%以下;吸收剂与粗合成气摩尔流量之比为1.6时,可将合成气中的CO2基本脱除。当CO2含量降至 16.2% ~16.6%时,H2S含量已达到40.178~80.357 mg/m3,属于钼系催化剂可容忍的硫含量范围,而文献[17]还提出适宜的H2S含量有利于基于ADM催化剂的混合醇合成;CO2含量降至1.6%后,继续降低CO2含量,吸收剂消耗量迅速上升。因此,净化气或反应气中CO2含量的选取应同时兼顾混合醇合成性能、净化过程的各项公用工程消耗及净化气H2S含量。
4 结论
通过分析混合醇合成过程的反应性能随合成条件的变化规律及反应气CO2含量对气体净化过程公用工程消耗的影响,得到以下结论:
·兼顾总醇选择性、总醇时空产率、C2+醇质量分数等指标,优化的合成条件为:当反应气CO2含量在0~19.6%范围内变动时,合成温度310~330℃、催化剂装填比20~30 g·h/mol、合成压力9~11 MPa。
·在优化的合成条件下操作时,C2+醇质量分数受反应气CO2含量影响较小,特别是反应气CO2含量≤5%时,但反应气CO2含量对总醇选择性和时空产率影响较大,以合成温度320℃、压力9 MPa、催化剂装填比20 g·h/mol为例,采用完全脱CO2反应气较采用含19.6%CO2的反应气,总醇选择性增大46%、时空产率提高超过50%。
·为避免过高的净化公用工程消耗,反应(净化)气CO2含量不宜低于1.6%。
目前工作还有以下不足:本研究的模型采用的反应动力学参数基于脱碳反应气的实验结果,CO2对反应速率的影响体现在改变各反应物浓度上,今后可根据含碳气体的实验结果进一步加以修正;需考虑H2S对反应性能的影响;对更先进的混合醇合成工艺进行模拟分析,并以其为核心构成能量转化利用系统,从系统层面分析优化反应条件。
[1]Carlsson P,Wiinikka H,Marklund M,et al.Experimental Investigation of an Industrial Scale Black Liquor Gasifier.1.The Effect of Reactor Operation Parameters on Product Gas Composition[J].Fuel,2010,89:4025.
[2]袁洪友,阴秀丽,李志文,等.黑液气化技术发展历程及趋势[J].中国造纸学报,2009,24(4):109.
[3]王双飞,农光再.黑液气化研究进展及其工业化应用展望[J].中华纸业,2008,29(21):48.
[4]Nykomb Synergetics A B.Technical and Commercial Feasibility Study of Black Liquor Gasification with Methanol/DME Production as Motor Fuels for Automotive Uses-BLGMF[R].ALTENER programme report(Energy Framework Programme),2003.
[5]Consonnia S,Katofsky R E,Larson E D.A Gasification-Based Biorefinery for the Pulp and Paper Industry[J].Chemical Engineering Research and Design,2009,87:1293.
[6]Naqvi M,Yan J,Dahlquis E.Black Liquor Gasification Integrated in Pulp and Paper Mills:A Critical Review[J].Bioresource Technology,2010,101:8001.
[7]Joelsson J M,Gustavsson L.Reductions in Greenhouse Gas Emissions and Oil use by DME(di-methyl ether)and FT(Fischer-Tropsch)Diesel Production in Chemical Pulp Mills[J].Energy,2012,39:363.
[8]杨丰科,姜晶晶.黑液气化技术在制浆造纸中的应用[J].中国造纸,2011,30(6):69.
[9]杨懋暹.制浆工业的热电联产及相关的重大技术发展[J].中国造纸,2007,26(7):56.
[10]Spath P L,Dayton D C.Preliminary Screening-Technical and Economic Assessment of Synthesis Gas to Fuels and Chemicals with Emphasis on the Potential for Biomass-Derived Syngas[R].Springfield:U.S.Department of Commerce National Information Service,2003.
[11]Herman R G.Advances in Catalytic Synthesis and Utilization of Higher Alcohols[J].Catalysis Today,2000,55:233.
[12]Santiesteban J G,Bogdan C E,Herman R G,et al.Mechanism of C1-C4alcohol synthesis over alkali/MoS2and alkali/Co/MoS2catalysts[C]//Proc 9th Int Congr Catal,1988:561.
[13]Smith K J,Kevin J,Herman R G,et al.Kinetic Modelling of Higher Alcohol Synthesis over Alkali-Promoted Cu/ZnO and MoS2Catalysts[J].Chemical Engineering Science,1990,45(8):2639.
[14]Gunturu A K,Kugler E L,Cropley J B,et al.A Kinetic Model for the Synthesis of High-Molecular-Weight Alcohols over a Sulfided Co-K-Mo/C Catalyst[J].Ind Eng Chem Res,1998,37:2107.
[15]Park T Y,Nam In-Sik,Kim Y G.Kinetic Analysis of Mixed Alcohol Synthesis from Syngas over K/MoS2Catalyst[J].Ind Eng Chem Res,1997,36:5246.
[16]张 侃,李文怀,孙予罕,等.合成气制低碳混合醇公升级模试[J].石油与天然气化工,2004,33(增刊):29.
[17]Ni Y H,Cheng L J,Yu F.Synthesis of Mixed Alcohols from CO2Contained Syngas on Supported Molybdenum Sulfide Catalysts[J].Applied Catalysis A:General,1997,150:243.
