吐温-80制备食品级微乳的稳定性评价
2011-12-18赵嘉敏陈中林伟锋
赵嘉敏,陈中,林伟锋
(华南理工大学轻工与食品学院,广东广州,510640)
吐温-80制备食品级微乳的稳定性评价
赵嘉敏,陈中,林伟锋
(华南理工大学轻工与食品学院,广东广州,510640)
以吐温-80为表面活性剂 (S),乙醇、丙二醇和甘油为助表面活性剂 (CS),大豆油、中链甘油三酸酯(MCT)和丁酸乙酯为油相(O)制备食品级微乳,通过测定粒径以及观察离心、温度、盐度、酸碱等环境因素对微乳外观上的影响,从而评价微乳的稳定性,并比较不同微乳的稳定性差异。结果表明:微乳的稳定性很好,是一个热力学稳定体系;以乙醇为助表面活性剂,以丁酸乙酯为油相,所制得的吐温-80食品级微乳稳定性最好。
微乳,食品级,吐温-80,稳定性
微乳是由油、水、表面活性剂以及助表面活性剂所形成的热力学稳定的、各向同性的、外观透明或半透明的分散体系[1-2]。微乳的显著特征是:不需要外界供能,能够自发形成;粒径为 1~100 nm[3-5]。文中采用吐温-80为表面活性剂,以不同的食品级助表面活性剂以及油相,制备出一系列吐温-80食品级微乳,并通过测定粒径以及观察离心、温度、盐度、酸碱等环境因素对微乳外观上的影响,从而评价微乳的稳定性,并比较不同组分制备出来的微乳稳定性差异。
1 材料与方法
1.1 仪器与试剂
吐温-80市售,食品级;丙二醇,日本产,食品级;甘油,市售,食品级;大豆油,金龙鱼;中链甘油三酸酯 (MCT),市售,食品级;丁酸乙酯,广州市仟壹生物技术有限公司;无水乙醇、NaCl、NaOH,国药集团化学试剂有限公司;HCl,广州市东红化工厂;去离子水,实验室自制。
TH-1000梯度混合器,上海沪西分析仪器厂;Mettler PL403电子天平、SevenEasy S20K酸度计,梅特勒-托利多仪器有限公司;马尔文粒度分布仪,马尔文仪器有限公司;TGL-16G台式高速离心机,上海安亭科学仪器厂。
1.2 粒径的测定
取少量静置 1周的微乳样品,用去离子水稀释至样品含水量约为 98%,用旋涡混合器混合均匀,再经过 0.22μm微孔滤膜过滤,过膜后的样品注入纳米粒度分布仪的样品池中,设定温度为 25℃和各种油相的折光率,进行粒径测定,每个样品平行测定 2次。
1.3 离心试验
取适量的微乳样品,置于高速离心机中,以15000 r/min的速度离心 30 min,观察微乳性状的变化。
1.4 高低温试验
高温试验的条件:分别在 60℃和 80℃水浴中加热 30 min;低温试验的条件:分别在冷藏室 (4℃)和冷冻室 (-18℃)均进行放置 12 h和放置 15d处理。观察不同温度对微乳性状的影响。
1.5 盐度试验
取适量的微乳样品,加入适量的固体 NaCl,使样品中的 NaCl浓度分别达到 0.1,0.2,0.5和 1 mol/L。观察不同浓度的 NaCl对微乳性状的影响。
1.6 酸碱试验
取适量的微乳样品,滴加 0.2 mol/L HCl或者0.2 mol/L NaOH调节体系的 pH值在 1~12波动。观察微乳在酸碱变化过程中的性状变化情况。
2 结果与分析
2.1 微乳粒径比较
2.1.1 不同油相
以吐温-80为表面活性剂,乙醇为助表面活性剂,分别采用大豆油、MCT和丁酸乙酯等作为食品级长、中、短链脂肪酸酯的代表来制备微乳,结果见图1。从图 1可以看出,所有样品的粒径均在 1~100 nm内,证明这些澄清透明或者半透明的样品均达到微乳粒径的要求。纳米级的粒径,使样品在储存过程中相当稳定[6-10]。本文制备的微乳样品能在室温下存放 6个月以上,并一直保持澄清透明或半透明状态。

图 1 不同油相的微乳粒径比较
对于 3种不同油相的微乳样品,样品的粒径都随着含油量的减少而减小。含油量减少,体系所需要增溶的油分子就会减少,从而减小分散相的尺寸,使测定的粒径减小。当表面活性剂 (surfactant,简称 S)的质量与助表面活性剂 (co-surfactant,简称 CS)和油(oil,简称 O)的质量之和的比例 (即 S/(CS+O))相同时,3种油相微乳样品的粒径从大到小依次为:大豆油 >MCT>丁酸乙酯。因为在相同的表面活性剂浓度下,形成的胶团聚集数相同,被增溶物质的分子结构越大,所形成分散相的尺寸就会越大,从而使测定的粒径增大。此外,所有样品的多分散系数均小于0.2,表明每个体系中分散相的粒径大小都较为一致,而且大小分布都较为集中。2.1.2 不同助表面活性剂
以吐温-80为表面活性剂,丁酸乙酯为油相,分别采用乙醇、丙二醇和甘油为助表面活性剂制备微乳,结果见图 2。从图 2可以看出,所有样品的粒径均在 1~100 nm内,证明这些澄清透明或者半透明的样品均达到微乳粒径的要求,在储存过程中相当稳定。对于 3种不同助表面活性剂的微乳样品,样品的粒径都随着含油量的减少而减小。在相同的 S/(CS+O)条件下,3种助表面活性剂微乳样品的粒径从大到小依次为:乙醇 >甘油 >丙二醇。
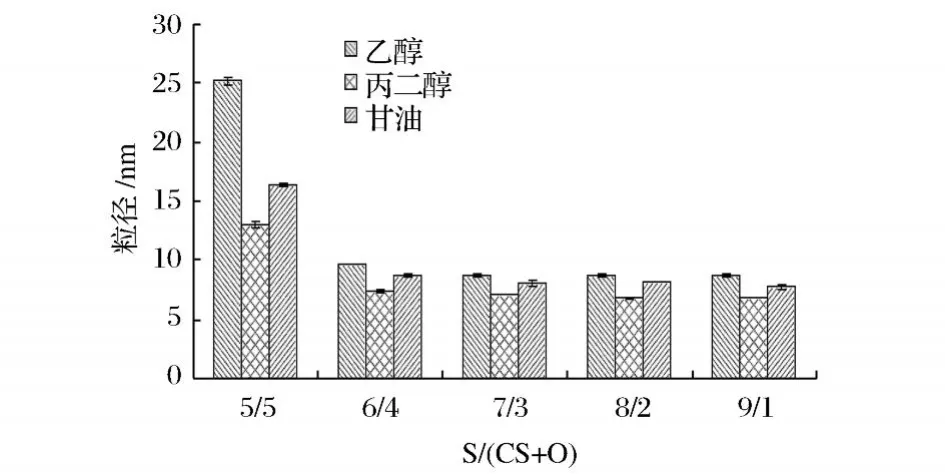
图 2 不同助表面活性剂的微乳粒径比较
2.2 离心稳定性
以吐温-80为表面活性剂,分别以乙醇、丙二醇和甘油为助表面活性剂,分别以大豆油、中链甘油三酸酯 (MCT)和丁酸乙酯为油相制备食品级微乳,在15 000 r/min离心 30 min的条件下,所有微乳样品均能保持澄清透明状态,无分层或絮凝现象。
2.3 温度稳定性
2.3.1 高温条件
高温处理对所制备微乳的影响见表 1。从表 1可以看出,60℃对各种吐温-80食品级微乳样品均没有明显影响。在 80℃高温下,各种微乳样品都会发生暂时分层,但静置一段时间后会复原。原因可能是高温会导致吐温-80的溶解度大大降低,影响其对油分子的增溶能力,从而表现为样品发生浑浊或者分层;当温度下降,又会使吐温-80的溶解度升高,恢复其对油分子的增溶能力,从而使样品变回澄清透明状态。从表 1还可以看出,以丁酸乙酯为油相,分别以乙醇 /丙二醇 /甘油为助表面活性剂,各种微乳样品对高温的热稳定程度从大到小依次为:乙醇 >>丙二醇≈甘油。原因可能是高温对丙二醇和甘油的黏度影响较大,破坏整个微乳体系的微观结构,从而导致体系较不稳定。
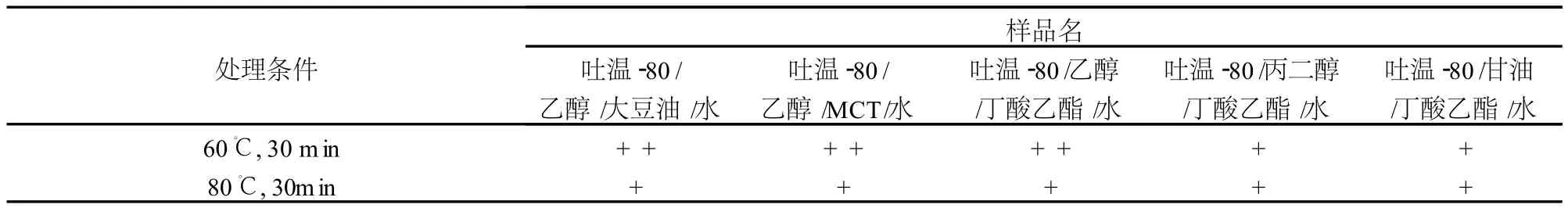
表1 各种微乳样品的高温稳定性试验结果
2.3.2 低温条件
低温处理对所制备微乳的影响见表 2。从表 2可以看出,冷藏对所有微乳样品均没有影响。冷冻时间较短对微乳体系的影响很小,而且体系会慢慢复原,但长时间冷冻对微乳体系的影响较大。原因可能是长时间冷冻处理会破坏微乳体系的微观结构,结实锋利的冰结晶会刺破界面膜,导致界面张力迅速上升,使体系变成油水不相容的状态。
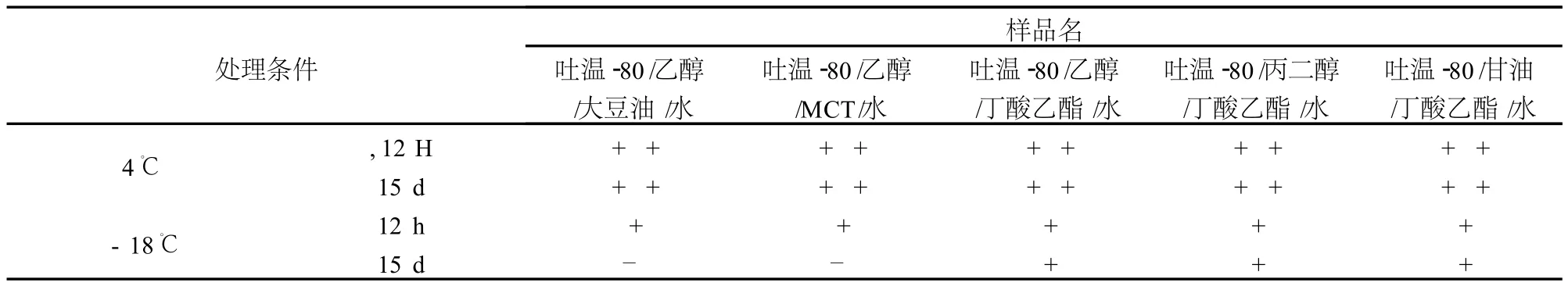
表2 各种微乳样品的低温稳定性试验结果
从表 2还可以看出,以乙醇为助表面活性剂,分别以丁酸乙酯 /MCT/大豆油为油相,各种微乳样品在冷冻较长时间后的稳定程度从大到小依次为:丁酸乙酯 >>MCT≈大豆油。原因可能是丁酸乙酯的极性较大,使丁酸乙酯在静置过程中重新与其他组分相混合,所以长时间冷冻处理只会使体系发生暂时分层。以丁酸乙酯为油相,分别以乙醇 /丙二醇 /甘油为助表面活性剂,各种微乳样品在冷冻较长时间后都能保持一定的稳定性。
2.4 盐稳定性
当微乳体系的 NaCl浓度从 0.1 mol/L增加到 1 mol/L时,所有微乳样品都没有任何外观变化,均保持很好的稳定性。主要是因为吐温 -80是非离子表面活性剂,不带电荷而受离子的影响小,从而使体系较稳定。
2.5 酸碱稳定性
所制备微乳在酸溶液和碱溶液中的情况见表 3。从表 3可以看出,所有微乳样品在酸性和碱性环境中都能保持很好的稳定性,其中耐酸性比耐碱性更强。主要是因为吐温 -80是非离子表面活性剂,不带电荷而受 H+浓度的影响小,从而使体系较稳定。
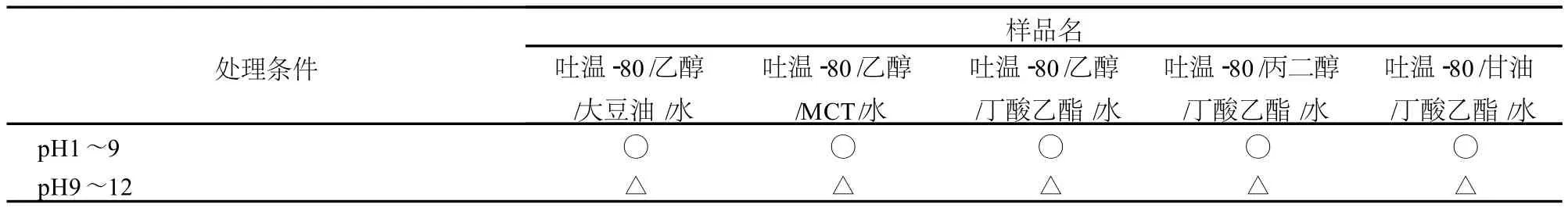
表3 各种微乳样品的酸碱稳定性实验结果
3 讨论
以吐温-80为表面活性剂,分别以乙醇 /丙二醇 /甘油为助表面活性剂,分别以大豆油 /MCT/丁酸乙酯为油相制备食品级微乳,各种微乳样品的粒径均在 1~100 nm,使得样品在储存过程中非常稳定。本文制备的微乳能在室温下存放 6个月以上,并一直保持澄清透明或半透明状态。在离心、温度、盐度以及酸碱等环境因素的影响下,微乳仍能保持很高的稳定性。在吐温-80系列食品级微乳的稳定性比较中,以乙醇为助表面活性剂和以丁酸乙酯为油相,所制得的微乳稳定性最好。
[1] 安红丽等.非离子表面活性剂微乳的研制[J].西北农林科技大学学报 (自然科学版),2007,35(3):65-69.
[2] 王晓黎等.非离子表面活性剂微乳的基础研究[J].解放军药学学报,2001,12(6):297-300.
[3] 王桂香,韩恩山,许寒.微乳状液的理论研究进展[J].化学工程师,2007(12):31-33,51.
[4] 王李节,周艺峰,聂王焰.微乳形成与应用研究进展[J].安徽化工,2007,33(1):16-19.
[5] 陈红兰等.微乳技术的应用[J].江西食品工业,2008,(2):36-41.
[6] Nissim G.Microemulsions as microreactors for food applications[J].Current Opinion in Colloid and Interface Science,2003,8:197-211.
[7] Ajit SN,David D,Danchen G.Stable drug encapsulation in micelles and microemulsions[J]. International Journal of Pharmaceutics,2007,345:9-25.
[8] Anna K,Nissi m G.Microemulsions as transdermal drug delivery vehicles[J].Advances in Colloid and Interface Science,2006,123-126:369-385.
[9] Aviram S,Abraham A.Microemulsions as carriers for drugs and nutraceuticals[J].Advances in Colloid and Interface Science,2006,128-130:47-64.
[10] Chuan-Chuan L.Stability and characterization of phospholipid-based curcumin-encapsulated microemulsions[J].Food Chemistry,2009,25:79-85.
Stability Evaluation of Food-gradeM icroemulsions with Tween-80
Zhao Jia-min,Chen Zhong,LinWei-feng
(College ofLight Industry and Food Science,South China University of Technology,Guangzhou 510640,China)
In this study,food-grade microemulsions were prepared with t ween-80 as the surfactant phase(S),ethanol,propylene glycol and glycerol as the co-surfactant phase(CS)and soybean oil,medium chain triglycerides and ethyl butyrate as the oil phase(O).Stability ofmicroemulsionswas evaluated by particle size deter mination and visual observation ofmicroemulsions affected by environment factors,including centrifugal effect,temperature,salinity and pH acidity.Stability comparison of differentmicroemulsionswas also estimated with the same method.The results indicated that stability ofmicroemulsionswaspretty good and microemulsionswere thermostable systems.Stability of the microemulsion system composed of tween-80 as the surfactant phase,ethanol as the co-surfactant phase and ethyl butyrate as the oil phase was best.
microemulsions,food-grade,t ween-80,stability
硕士研究生。
2010-05-20,改回日期:2010-08-23
