用水合肼还原芳香亚磺酰胺合成二芳基二硫醚*
2011-11-27朱瑞恒聂良邓施小新
朱瑞恒,董 菁,聂良邓,施小新
(华东理工大学 药学院,上海 200237)
二硫醚具有生物活性[1],在材料科学领域具有广泛的应用[2],其合成方法倍受化学家的关注[3]。二硫醚通常由硫醇通过氧化而得[4],但原料硫醇一般具有恶臭味,不适合大规模生产;也可以通过磺酸衍生物和亚磺酸衍生物还原而得[5,6],但是适用亚磺酸衍生物的还原试剂只有几种[6]。Curtius[7]和Kobayashi[8]在制备亚磺酰肼时意外发现用水合肼可以还原亚磺酸酯和亚磺酰氯得到二芳基二硫醚,并对水合肼与亚磺酸酯和亚磺酰氯的还原反应作了深入研究。但到目前为止,还没有文献报道水合肼还原亚磺酰胺制备二硫醚的反应。
本文首次研究并报道一种在DMSO中用水合肼还原芳香亚磺酰胺(1a~1j)制备二芳基二硫醚(2a,2c,2e,2h,2i和2j,Scheme 1)的简便方法。
1 实验部分
1.1 仪器与试剂
SWG X-4型显微熔点仪;Bruker AVANCE 500 MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);Nicolet Mafna-IR 550型红外光谱仪(KBr压片);HP 59898A型质谱仪;Vario EL Ⅲ型元素分析仪。所用试剂均为分析纯。
1.2 2的合成(以2a为例)
在圆底烧瓶中加入苯亚磺酰肼(1a)2.82 g(20 mmol)的DMSO(20 mL)溶液,搅拌下滴加98%水合肼5.01 g(100 mmol),滴毕,于80 ℃反应3 h(TLC跟踪)。冷却至室温,加水100 mL,用苯(2×60 mL)萃取,合并有机层,用30%NaOH溶液(50 mL)洗涤,无水硫酸镁干燥,减压蒸除溶剂,残余物经硅胶柱层析[洗脱剂:V(正己烷)∶V(乙酸乙酯)=9∶1]纯化得白色固体2a1.85 g,收率85%;1H NMRδ: 7.21(t,J=7.5 Hz, 2H), 7.29(dd,J=7.5 Hz, 7.8 Hz, 4H), 7.49(d,J=7.8 Hz, 4H);13C NMRδ: 127.8, 128.1, 129.7, 137.6; IRν: 2 925, 1 947, 1 864, 1 575, 1 475, 1 436, 1 296, 1 072, 1 022, 738, 687, 464 cm-1; EI-MSm/z(%): 218(M+, 100), 185(15), 154(14), 140(3), 109(36), 77(2), 65(7).Anal.calcd for C12H10S2: C 66.01,H 4.62; found C 66.14, H 4.55。
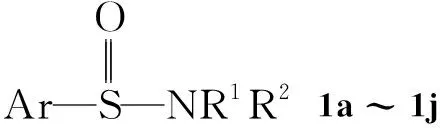
Scheme1
用类似方法合成白色晶体2c,2e,2h,2i和2j,其表征数据[9]与Scheme 1预期吻合。
2 结果与讨论
以1a的还原反应为例,考察了部分常用溶剂的影响,结果发现DMSO为溶剂的产率较MeOH, THF, DMF为溶剂时高。室温下1a还原反应很慢,反应20 h收率只有10%左右;于80 ℃反应3 h收率85%。
扩展底物于80 ℃反应的结果见表1。由表1还发现,苯环上有吸电子官能团的底物,反应比较快,水合肼用量只需1.5 eq.,反应时间也比较短;苯环上有推电子官能团的底物,反应比较慢,水合肼用量需5.0 eq,且反应时间较长。当温度较高时,水合肼可以将部分二硫醚过度还原成硫酚,苯环上有吸电子官能团的底物更易过度还原,也是产率比较低的原因[10]。
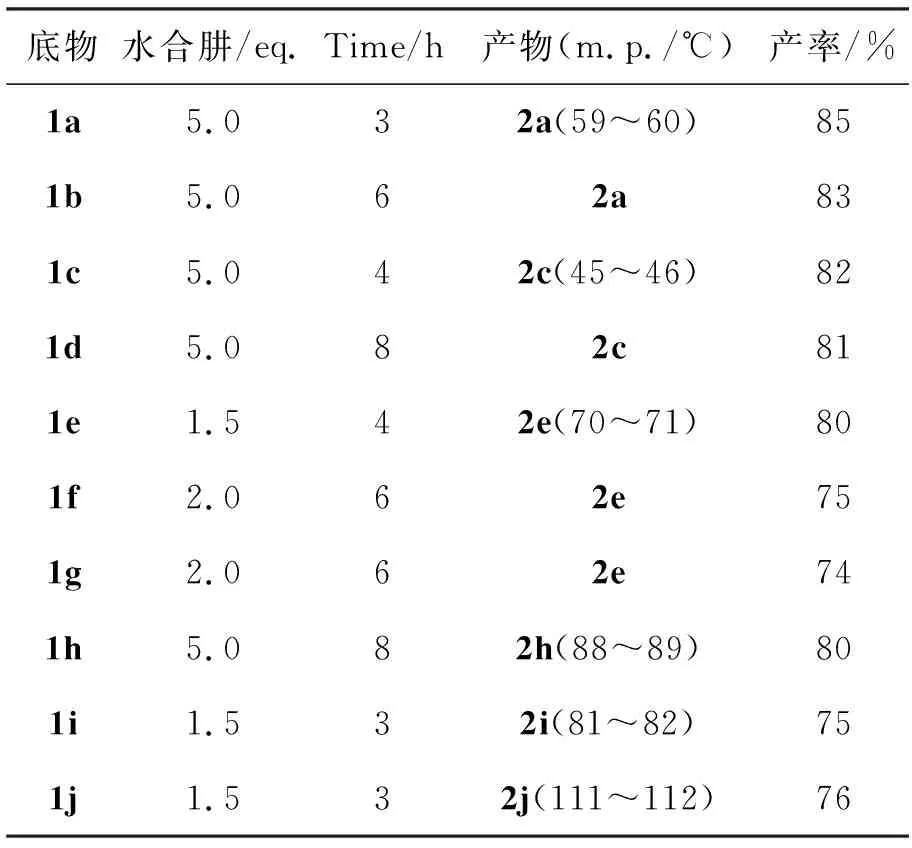
表1 扩展底物的实验结果*
*反应温度80 ℃,其余反应条件同1.2
[1] Kapanda C N, Muccioli G G, Labar G,etal.Bis(dialkylaminethiocarbonyl)disulfides as potent and selective monoglyceride lipase inhibitors[J].J Med Chem,2009,52(22):7310-7314.
[2] Umali A P, Simanek E E.Thiol-disulfide exchange yields multivalent dentrimers of melamine[J].Org Lett,2003,5(8):1245-1247.
[3] Firouzabadi H, Jamalian A.Reduction of oxygenated organosulfur compounds[J].J Sulfur Chem,2008,29(1):53-97.
[4] Witt D.Recent developments in disulfide bond formation[J].Synthesis,2008,16:2491-2509.
[5] Kabalka G W, Reddy M S, Yao M-L.Synthesis of diaryl disulfides via the reductive coupling of arylsulfonyl chlorides[J].Tetrahedron Lett,2009,50(52):7340-7342.
[6] Pinnick H W, Reynolds M A, McDonald R T Jr,etal.Reductive coupling of aromatic sulfinate salts to disulfides[J].J Org Chem,1980,45(6):930-932.
[7] Curtius T, Lorenzen F.Hydrazide and azide of organic acid:Report ⅪⅤ.40.Hydrazide and azide of aromatic sulfonic acids[J].J Pr Chem,1898,58(2):160-189.
[8] Kobayashi M, Yamamoto A.Organic sulfur compounds.ⅪⅤ.Reactions of sulfinic esters and related compounds with hydrazine[J].Bull Chem Soc Jpn,1966,39(12):2736-2738.
[9]2c:1H NMRδ: 2.32(s, 6H), 7.10(d,J=8.0 Hz, 4H), 7.38(d,J=8.0 Hz, 4H);13C NMRδ: 21.7, 129.2, 130.4, 134.6, 138.0; IRν: 3 020, 2 915, 1 894, 1 633, 1 488, 1 398, 1 377, 1 182, 1 117, 1 077, 1 014, 802, 480 cm-1; MS(EI)m/z(%): 246(M+, 100), 213(4), 182(7), 123(48), 91(3), 77(5); Anal.calcd for C14H14S2: C 68.25,H 5.73; found C 68.60, H 5.65.2e:1H NMRδ: 7.27(d,J=8.5 Hz, 4H), 7.40(d,J=8.5 Hz, 4H);13C NMRδ: 129.9, 130.2, 134.3, 135.8; IRν: 3 078, 1 896, 1 645, 1 568, 1 471, 1 429, 1 386, 1 112, 1 093, 1 010, 816, 741, 491 cm-1; MS(EI)m/z(%): 290(M++4, 15), 288(M++2, 68), 286(M+, 100), 222(7), 145(29), 143(82), 108(29); Anal calcd for C12H8S2Cl2: C 50.18,H 2.81; found C 49.87, H 2.60.2h:1H NMRδ: 1.29(s, 18H), 7.32(d,J=8.4 Hz, 4H), 7.44(d,J=8.4 Hz, 4H);13C NMRδ: 31.9, 35.2, 126.8, 128.4, 134.7, 151.1; IRν: 2 964, 2 902, 1 905, 1 590, 1 486, 1 397, 1 266, 1 114, 1 010, 828, 556 cm-1; MS(EI)m/z(%): 332(M++2, 6), 331(M++1, 13), 330(M+, 62), 315(100), 286(6), 165(4), 150(18), 122(6), 91(3); Anal.calcd for C20H26S2: C 72.67,H 7.93; found C 72.71, H 7.84.2i:1H NMRδ: 7.16(dd,J=8.5 Hz, 2.3 Hz, 2H), 7.30(d,J=8.5 Hz, 2H), 7.52(d,J=2.3 Hz, 2H);13C NMRδ: 127.5, 128.9, 130.8, 131.4, 134.6, 136.5; IRν: 3 050, 2 975, 1 565, 1 446, 1 417, 1 375, 1 241, 1 140, 1 091, 1 031, 855, 808, 578 cm-1; MS(EI)m/z(%): 360(M++4, 11), 358(M++2, 45), 356(M+, 100), 354(M+-2, 70), 288(19), 286(29), 179(36), 177(56), 144(20), 142(56), 107(8); Anal.calcd for C12H6S2Cl4: C 40.47,H 1.70; found C 40.42, H 1.73.2j:1H NMRδ: 7.23(dd,J=8.4 Hz, 2.1 Hz, 2H), 7.40(d,J=8.4 Hz, 2H), 7.64(d,J=2.1 Hz, 2H);13C NMRδ: 120.6, 123.1, 130.5, 132.1, 134.9, 138.8; IRν: 2 923, 1 635, 1 557, 1 436, 1 401, 1 365, 1 239, 1 084, 1 011, 798, 762 cm-1; MS(EI)m/z(%): 538(M++4, 20), 536(M++2, 68), 534(M+, 100), 532(M+-2, 65), 530(M+-4, 16), 376(21), 374(40), 372(19), 295(12), 267(19), 188(37), 186(35), 107(12); Anal.calcd for C12H6S2Br4: C 26.99,H 1.13; found C 27.35, H 1.18.
[10] Maiti S N, Spevak P, Singh M P,etal.Reductive cleavage of symmetrical disulfides with hydrazines[J].Synth Commun,1988,18(6):575-581.
