东当归化学成分研究及定量分析
2011-11-23刘向前李丽丽郑礼胜
刘向前,李丽丽,倪 娜,郑礼胜
1中南大学制药工程系,长沙410083;2湖南中医药大学药学院,长沙410007;3扬子江药业集团有限公司,泰州225321
东当归化学成分研究及定量分析
刘向前1,2*,李丽丽1,倪 娜3,郑礼胜1
1中南大学制药工程系,长沙410083;2湖南中医药大学药学院,长沙410007;3扬子江药业集团有限公司,泰州225321
从当归属植物东当归的根的乙醇溶液中分离得到了4个化合物,通过理化特性和波谱分析分别鉴定为双(5-甲酰基糠基)醚(bis(5-formylfurfuryl)ether,1)、5-羟甲基糠醛(5-hydroxymethyl-2-furaldehyde,2)、豆甾醇(stigmasterol,3)、十七烷酸(heptadecanoic acid,4)。所有化合物均为首次从该植物中分离得到,其中1为首次从该属植物中分离得到。采用高效液相色谱法对东当归所含该属特征活性成分紫花前胡素进行了定量分析。
当归属;东当归;双(5-甲酰基糠基)醚;高效液相色谱法;紫花前胡素
伞形科(Umbelliferae)当归属(Angelica)植物属温带性属,全球约90种,主要分布于北温带(中国、朝鲜、韩国、日本)和新西兰,多具有补血活血、调经止痛的功效[1]。东当归为当归属植物东当归Angelica acutiloba(sieb.et Zucc)kigusticum acutilobum.Siebet Zuce的根,别名日本当归、大和当归、延边当归。早在20世纪70年代,东当归在中国吉林省延吉市引种成功,作为朝鲜族的民族药材,广泛应用于民间。国内除四川从1991年开始引种栽培外,其他地区尚未有栽培[2]。《日本药局方》记载的“和当归”,即为延边地区引种的东当归,具有补血调经、活血止痛、润肠通便的作用,与中国当归的功能主治相一致。目前,国内外学者仅对四川引种栽培的东当归挥发油成分采用GC-MS联用法进行了分析,未见其化学成分研究和定量分析的报道[3]。在系统研究当归属植物化学分类的基础上[4],为了进一步开发利用我国延边地区的东当归资源,本文对其化学成分进行研究,从中分离得到4个化合物;同时,采用HPLC法对其中所含的当归属植物的特征活性成分紫花前胡素进行了定量分析。
1 仪器与材料
Bruker DRX 500超导核磁共振波谱仪;Pekin-Elmer 983G型红外光谱仪;ZAB-HS型质谱仪;X-4型显微熔点仪。GF254薄层色谱硅胶、200~300目柱色谱硅胶(青岛海洋化工厂);Sephadex LH-20(amersham pharmacia biotech公司)。实验用甲醇和乙腈为色谱纯,水为三蒸水,其他试剂均为分析纯。
东当归药材购于吉林延边,经湖南中医药大学药学院刘向前教授鉴定为东当归Angelica acutiloba (sieb.et Zucc)的根。标本(编号:20070827)存放于中南大学制药工程系标本室。
2 提取分离
取干燥的东当归根1.0 kg,以85%乙醇冷浸2次,分别为20、30 d。合并2次冷浸滤液,浓缩回收乙醇,得东当归粗浸膏110.0 g。粗浸膏用水混悬,乙醚萃取,除去溶剂后得到干浸膏25.0 g,取约15.0 g进行硅胶柱层析分离,以正己烷∶乙酸乙酯= 12∶1→2∶1梯度洗脱,得到Fr.EA(10∶1),Fr.EB(8∶1),Fr.EC(5∶1),Fr.ED(2∶1)4个粗组分。经反复硅胶柱层析及Sephadex LH-20凝胶柱层析纯化,由Fr.ED(2∶1)部分分得化合物1(70 mg)和2(40 mg),Fr.EB(8∶1)部分分得化合物3(45 mg),Fr.EC (5∶1)部分分得化合物4(30 mg)。
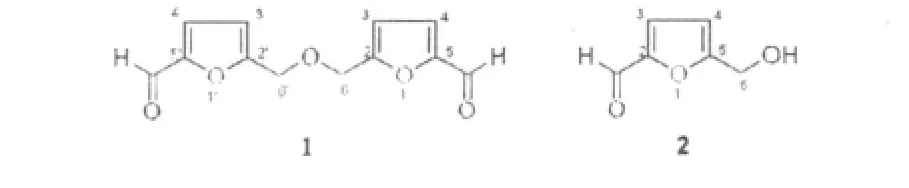
图1 化合物1和2的结构Fig.1 Stuctures of compounds 1 and 2
3 结构鉴定
化合物1 淡黄色针晶(甲醇),mp.108~109℃。EI-MS m/z:234,205,138,125,109(基峰),95; TOF-HRMS m/z:235.0585[M+H]+(计算值为235.0606),分子式为C12H10O5;IR(KBr)νmax: 3111,2849,1671,1523 cm–1。质子核磁共振谱(δ 9.62)和碳谱核磁共振谱(δ 177.7)的信号说明该化合物含有醛基。质子核磁共振谱显示四组峰号,其峰面积比为1∶1∶1∶2,碳谱核磁共振谱只有6个碳信号,说明该化合物为对称结构。13C NMR(125 MHz,CDCl3)δ:64.6(C-6,C-6'),177.7(CO),4个芳碳信号:157.2(C-2,C-2'),111.8(C-3,C-3'),121.8(C-4,C-4'),152.8(C-5,C-5'),为呋喃环;1H NMR(600 MHz,CDCl3)δ:4.63(H-6,H-6',-CH2O-部分结构),6.57(H-3,H-3'),7.21(H-4,H-4'),9.62(CHO,5'-H)。且数据与文献报道[5](5-甲酰基糠基)醚一致。
化合物2 棕黄色油状化合物,EI-MS m/z: 126;IR(KBr)νmax:3386,2846,1673,1522,1397,1192,1023,811 cm–1;1H NMR(600 MHz,CDCl3)δ: 3.91(-OH),4.67(H-6),6.49(H-4),7.21(H-3),9.51(CHO);13C NMR(125 MHz,CDCl3)δ:57.4 (C-6),161.1(C-5),110.0(C-4),123.4(C-3),152.2(C-2),177.8(CO)。以上数据与文献报道[6]的5-羟甲基糠醛一致。
化合物3 白色粉末(正己烷-乙酸乙酯),mp.127~128℃,Liebermann-Burchard反应阳性。IR (KBr)νmax:801,1064,1381,1465,1641,2867,2937, 2960,3429;1H NMR(600 MHz,CDCl3)δ:0.68(s,3H,H-18),1.01(s,3H,H-19),0.90(d,3H,J=6.6 Hz,H-29),0.93(d,6H,J=6.9 Hz,H-26和H-27),0.82(d,3H,J=6.8 Hz,H-21),5.35(d,1H,H-6),5.14(dd,1H,J=15.5,8.5 Hz,H-22),5.03(dd,1H,J=15.0,8.5 Hz,H-23),3.52(m,1H,H-3);13C NMR(150 MHz,CDC13)δ:37.2(C-1),31.7(C-2),71.8(C-3),42.3(C-4),140.8(C-5),121.7(C-6),31.7(C-7),31.7(C-8),50.2(C-9),36.2(C-10),21.0(C-11),39.7(C-12),42.2(C-13),56.9(C-14),23.1(C-15),28.3(C-16),56.0(C-17),12.0 (C-18),19.8(C-19),42.2(C-20),21.2(C-21),138.3(C-22),129.3(C-23),51.3(C-24),34.0(C-25),21.1(C-26),18.8(C-27),26.1(C-28),12.3 (C-29),140.8,121.7,138.3,129.3,71.8。以上数据与文献报道[7]的豆甾醇一致。
化合物4 白色粉末(氯仿),mp.60~61℃。IR(KBr)νmax:2918,2849,1702,1468,1410,1294,1272,从红外谱中看出有一系列的饱和烃基存在,还有羰基吸收峰以及 C-O伸缩振动的吸收峰。1H NMR(600 MHz,CDCl3)δ:1.185(s,26H),0.810(m,3H),2.27(m,2H),1.56(m,2H);13C NMR(150 MHz,CDCl3)δ:14.10(C-1),22.7(C-2),31.9(C-3),29.68,29.68,29.66,29.65,29.63,29.58,29.42,29.35,29.23,29.05(10C,C-4~C-14),24.67 (C-15),34.02(C-16),179.92(C-17)。以上数据与文献报道[8]的十七烷酸一致。
4 紫花前胡素的定量分析
4.1 色谱条件[9]
AT.LICHROM C18色谱柱(250 mm×4.6 mm;5 μm),流动相为pH=5.0的磷酸-磷酸二氢钠缓冲液(稀释10倍):乙腈(1∶1),检测波长为280 nm,流速为1.0 mL/min,柱温为30°C,进样量10 μL。
4.2 对照品溶液的制备
精密称取紫花前胡素对照品8.25 mg,甲醇溶解并定容至50 mL,精密移取1 mL,用甲醇稀释并定容至25 mL。经0.45 μm微孔滤膜过滤,即得。
4.3 供试品溶液的制备
精密称取东当归药材粉末10.3 g,加乙醚100 mL水浴提取4 h,过滤,浓缩,残渣用甲醇溶解,转移至50 mL容量瓶中,加甲醇至刻度,摇匀。经0.45 μm微孔滤膜过滤,即得。
4.4 东当归中紫花前胡素的含量测定
将“4.3”项下供试品溶液按照“4.1”项下色谱条件测定紫花前胡素含量,结果表明:东当归药材中紫花前胡素含量为10.05 μg/g。
5 讨论
近年来关于东当归挥发油组分[10]和提取物药理作用[11]曾见报道,但对其化学组分及药理作用却未有报道。本文首次对延边地区东当归的根进行化学成分分析。紫花前胡素是1995年韩国学者研究发现的一种吡喃型香豆素,其对白血病、糖尿性高血压以及降低肾毒素具有显著效果[12],有望开发成为抗肿瘤等疾病的新药。笔者曾用HPLC法测定过不同批次、不同产地的12种当归属植物中紫花前胡素的含量,结果表明12种植物均含有紫花前胡素;在此基础上,本文测定了东当归中紫花前胡素的含量,结果亦含有紫花前胡素。由此可知,紫花前胡素可能为当归属的特征活性成分,广泛存在于当归属植物中。本研究为东当归的质量控制、今后作为正式药材纳入国家标准以及当归属植物的化学分类提供了实验依据。
1 Li LL(李丽丽),Liu XQ(刘向前),Gao JM(高敬铭),et al.Studies on the volatile oils and determination of total coumarins from Angelica spp.growing in China,Japan and Korea.China Pharm(中国药师),2009,12:1344-1347.
2 Sun RW(孙仁文),Piao HS(朴惠善).Advances in studies on plants of Angelica acutiloba Kitagawa..Mod Chin Med(中国现代中药),2006,8(11):31-33.
3 Du LL(杜蕾蕾),Wang XJ(王晓静),Cai CZ(蔡传真),et al.Constituent analysis of essential oils from radix of Angelica acutiloba Kitagawa.J Chin Med Mat(中药材),2002,25: 477-478.
4 Li LL(李丽丽),Liu XQ(刘向前),Zhang XD(张晓丹).Advances in studies on plants of Angelica spp..Chin Tradit Patent Med(中成药),2009,31:601-607.
5 Zhang HQ(张涵庆),Ding YM(丁云梅),Chen GY(陈桂英),et al.Studies on active constituents of root of Euphorbia ebracteolata Hayata.Acta Bot Sin(植物学报),1987,29: 429-431.
6 Liu ZL(刘振丽),Li LF(李林福),Chao ZM(巢志茂),et al.Chemical constituents from radix Polygoni multiflori thumb.after Preparing.Nat Prod Res Dev(天然产物研究与开发),2009,21:239-241.
7 Huang S(黄帅),Zhou XL(周先礼),Wang HY(王洪燕).Chemical studies on the flowers of Tagetes erecta L..Nat Prod Res Dev(天然产物研究与开发),2006,18(Supp1): 57-59.
8 Sadtler Research Laboratories.Sadtler Standard NMR Spectra.USA:Sadtler Research Laboratories,1980.2594.
9 Liu XQ(刘向前).One examination method of Decursin.ChinaPatent(中国专利),ZL 200610103386.4,2008-02-13.
10 Sun RW(孙仁文),Piao HS(朴惠善).Extraction and analysis of constituents of essential oil from Angelica acutiloba Kitag.with supercritical fluid CO2and GC-MS method.Lishizhen Med Mat Med Res(时珍国医国药),2007,18:1136-1138.
11 Hatano R,Takano F,Fushiya S,et al.Water-soluble extracts from Angelica acutiloba Kitagawa.enhance hematopoiesis by activating immature erythroid cells in mice with 5-fluorouracil-induced anemia.Exp Hematol,2004,10:918-924.
12 Kang YG,Lee JH,Chae HJ,et al.HPLC Analysis and extraction methods of decursin and decursinol angelate in Angelica gigas roots.Korean J Pharmacogn,2003,34:201-205.
Chemical Constituents and Quantitative Analysis of Angelica acutiloba kitag.
LIU Xiang-qian1,2*,LI Li-li1,NI Na3,ZHENG Li-sheng11Department of Pharmaceutical Engineering,Central South University,Changsha 410083,China;2College of Pharmacy,Hunan University of Chinese Medicine,Changsha 410007,China;3Yangtze River Pharmaceutical Group,Taizhou 225321,China
Four compounds were isolated from the roots of Angelica acutiloba kitag.and their structures were identified as bis(5-formylfurfuryl)ether(1),5-hydroxymethyl-2-furaldehyde(2),stigmasterol(3),heptadecanoic acid(4)by spectroseopic evidences(1H NMR,13C NMR,HR-MS,etc).All the compounds were isolated from this plant for the first time and compounds 1 was obtained from this genus for the first time.The relative contents of decursin which was the special active constituent of Angelica genus were analyzed by HPLC.
Angelica;Angelica acutiloba kitag.;bis(5-formylfurfuryl)ether;HPLC;decursin
1001-6880(2011)04-0693-03
2009-11-09 接受日期:2010-01-14
*通讯作者 Tel:86-731-88995848;E-mail:lxq0001cn@163.com
R284.2
A
