黄酮碳苷类化合物ESIMS-MS裂解规律初探
2011-11-23吴新安都模勤
吴新安,都模勤
中国人民解放军第105医院感控科,合肥230031
黄酮碳苷类化合物ESIMS-MS裂解规律初探
吴新安*,都模勤
中国人民解放军第105医院感控科,合肥230031
本研究通过ESIMS-MS技术分析一系列黄酮化合物的裂解情况,探讨黄酮碳苷类化合物ESIMS-MS的裂解规律。结果表明,六碳黄酮碳苷ESIMS-MS的子离子谱图中出现[M-H-60]–、[M-H-90]–和[M-H-120]–的离子碎片;五碳黄酮碳苷ESIMS-MS的子离子谱图中只能产生脱去60和90质量单位的碎片峰。该研究表明黄酮碳苷类化合物ESIMS-MS裂解具有一定的规律性,并有助于发现微量黄酮碳苷类成分。
黄酮碳苷;ESIMS-MS
随着分析技术的发展,以发现活性成分为目的的中药及天然药物研究已经进入了较为快速的阶段,如何借助先进的分析技术较为快速的发现和分析中药及天然产物中活性成分成为天然药物化学领域的关键问题之一[1]。黄酮碳苷类化合物近年来研究越来越深入,已经形成一个较大的体系[2-5]。但是有关该类化合物的波谱学规律方面较少见专门的研究报道,本文利用从短瓣金莲花中分离得到的一系列黄酮碳苷类化合物作为研究对象,运用ESIMS-MS技术分析这些黄酮碳苷类化合物的质谱裂解规律,初步总结出黄酮碳苷类化合物的ESI-MS/MS裂解规律;并运用这些规律来进一步分析短瓣金莲花中其他可能存在的微量黄酮碳苷类成分。
1 材料和方法
1.1 药材与对照品
短瓣金莲花采集于大兴安岭,经生药学鉴定为Trollius ledebouri Reichb;对照品牡荆苷、荭草苷、2''-O-(3''',4'''-二甲基苯甲酰基)牡荆苷、2''-O-(3''',4'''-二甲基苯甲酰基)荭草苷、2''-O-(2'''-甲基丁酰基)牡荆苷、2''-O-(2'''-甲基丁酰基)荭草苷等酰化的黄酮碳苷均由作者从短瓣金莲花中分离得到[3,4],纯度达到95%以上。
1.2 仪器和试剂
API3000串联四级杆型液相色谱/串联质谱联用仪(美国ABI公司);硅胶薄层层析板(青岛海洋化工厂);大孔树脂HP20(日本三菱公司)。分析用的试剂为色谱纯。
1.3 提取与分离
短瓣金莲花用60%乙醇提取后,醇提取物经过简单的溶剂处理后,除去脂溶性成分,得到样品供测试。
1.4 结构分析方法
对照品和样品经过Q1扫描得到其分子量信息,然后进行子离子扫描得到具有碎片离子信息的二级质谱,结合已知化合物的离子信息规律、文献报道等方法分析并获得其可能的结构。
1.5 质谱分析条件
电喷雾离子化原(ESI);负离子检测;照射电压(IS)为-4000 V;源温度(TEM)为50℃;DP电压为-60 V;雾化气(NEB)为8;气帘气(CUR)为10。
2 结果与讨论
2.1 对照品的MS-MS分析
对照品经过Q1扫描得到其分子量信息,对其负离子进行子离子扫描,得到各自的子离子信息(Fig.1)。结合对照品的结构分析Fig.1中出现的子离子信息,对照品1荭草苷(Fig.1b)的负离子一级质谱中出现的m/z447的子离子扫描图中出现,m/z 387为[M-H-CHO-CH2OH]–([M-H-60]–),m/ z 357为[M-H-CHO-CHO-CH2OH]–([M-H-90]–),m/z 327为[M-H-CHO-CHO-CHO-CH2OH]–([MH-120]–);同理对对照品2牡荆苷(Fig.1a)的一级质谱负离子图谱中出现的准分子离子峰431进行子离子扫描,存在以下子离子出现:m/z 371为[M-HCHO-CH2OH]–([M-H-60]–),m/z 341为[M-HCHO-CHO-CH2OH]–([M-H-90]–),m/z 311为[MH-CHO-CHO-CHO-CH2OH]–([M-H-120]–);而被酰化的黄酮碳苷首先脱去酰化基团,如对照品3 (2''-O-(2'''-甲基丁酰基)牡荆苷,Fig.1c)m/z 427 (M-H-isobutyryl)及对照品4(2''-O-(2'''-甲基丁酰基)荭草苷,Fig.1d)m/z 443(M-H-isobutyryl),然后也出现上述碎片离子峰信息m/z 367为[427-HCHO-CH2OH]–([427-H-60]–),m/z 337为[427-H-CHO-CHO-CH2OH]–([427-H-90]–),m/z306为[427-H-CHO-CHO-CHO-CH2OH]–([427-H-120]–);m/z 383为[443-H-CHO-CH2OH]–([443-H-60]–),m/z 353为[443-H-CHO-CHO-CH2OH]–([443-H-90]–),m/z 323为[443-H-CHO-CHOCHO-CH2OH]–([443-H-120]–);对照品5(2''-O-(3''',4'''-二甲基苯甲酰基)荭草苷)和6(2''-O-(3''',4'''-二甲基苯甲酰基)牡荆苷)同样也是先脱去苯甲酰基团,然后出现类似的子离子碎片信息(Fig.1e,f)。

图1 标准品的ESI-MS色谱图Fig.1 ESI-MS chromatogram of standard compounds
通过以上对照品分析,我们发现在苷类化合物的ESI-MS/MS中,如果不首先出现脱糖基的碎片峰,而是在黄酮碳苷MS-MS的子离子谱图中存在以下有规律的离子碎片:[M-H-60]–、[M-H-90]–和[M-H-120]–,基本上可以断定为六碳黄酮碳苷类化合物,此结果与乔善义等研究[1]基本一致,但是乔善义等研究表明如果黄酮碳苷类化合物所连接的糖为五碳糖,只能产生脱去60和90质量单位的碎片峰,不产生脱120质量单位的碎片峰,这也进一步在本实验中得到印证。对负离子质谱图中出现准分子离子峰进行子离子扫描,碎片峰由于强度的差异,脱60、90和120质量单位的碎片并不都能出现,本实验中采取局部谱图放大的方式才能见到强度弱的碎片峰,但是脱120质量单位的碎片峰均可见。
2.2 样品的HPLC-MS-MS分析
样品经过HPLC-MS分析后,发现一个分子量为490的化合物(A),分析该化合物的MS谱图(Fig.2),我们发现质谱图中没有直接出现脱糖的离子峰,推测其为黄酮碳苷。

图2 化合物A的ESI-MS色谱图Fig.2 ESI-MS chromatogram of compound A
进一步分析MS图谱,该化合物脱去一个28(甲酰基)及30(甲氧基)质量数后的离子峰出现碳苷的MS碎片规律,结合我们前面的已知化合物的碎片规律和结构特点,认为该化合物可能为葡萄糖的2位被甲酰基及有甲氧基取代的黄酮碳苷。谱图中出现牡荆苷的碎片离子峰,故其母体可能为牡荆苷,可能结构如下[6]:
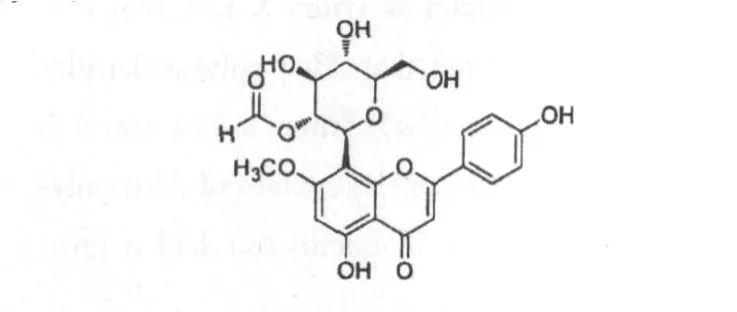
图3 化合物A的结构式Fig.3 Stucture of compound A
3 讨论
采用常规植物化学手段对所研究的对象进行粗分离,结合文献调研,运用HPLC-MS/MS的分析方法快速分离鉴定植物中的化学成分或活性成分具有快速、简单、低成本等优点,为天然活性成分研究提供了新方法和思路;但是本实验仅仅就部分黄酮碳苷的ESI-MS/MS的子离子扫描图谱进行分析总结,反映黄酮碳苷类化合物在软电离条件下的裂解规律,只能为该类化合物的结构解析提供另一个侧面的证据支持,尤其对分析植物已知该类化学成分中活性成分会起到事半功倍作用;完全阐明该类化合物的质谱裂解规律,探讨质谱上鉴定该类化合物的可能性,还需要从EI裂解、FAB裂解等进一步总结分析。
1 Qiao SY(乔善义),Guo JF(郭继芬),Zhao YM(赵毅民),et al.Rapid discovery and analysis of C-glycosylflavones from Stellaria media(L.)Cyr.by MS/MS.Chin J Nat Med(中国天然药物),2003,1:120-123.
2 Wu XA(吴新安),Zhao YM(赵毅民).Advance of study on natral flavone C-glycosides.Pharm J Chin People's Liber Army(解放军药学学报),2005,21:135-138.
3 Wu XN,Zhao YM,Yu NJ.A novel analgesic pyrazine derivative from the leaves of Croton tiglium.J Asian Nat Prod Res,2007,9:437-441.
4Wu XA(吴新安),Zhao YM(赵毅民),Zhao G(赵刚).Flavone C-glycosides from Trollius ledebouri.China J Chin Mat Med(中国中药杂志),2007,32:864-865.
5 Xinan Wu,Yimin Zhao,Nengjiang Yu.Flavone C-glycosides from Trollius ledebouri.J Asian Nat Prod Res,2006,8:541-544.
6 Yu DQ,Yang JS.The Handbook of Analysis Chemistry,2nded.Beijing:Chemistry Industry Publishing House,1996.
Rule of ESIMS-MS on C-glycosyflavonnes
WU Xin-an*,DOU Mo-qin
Department of infection control,No.105th Hospital of PLA,Hefei 230031,China
In this research the cracking situation of a series of C-glycosyflavonnes compounds was analyzed by the ESIMS-MS chromgraphy technology.The results showed that the ion peaks of[M-H-60]–,[M-H-90]–and[M-H-120]–were found in C-glycosyflavonnes with hexose and the ion peaks of[M-H-60]–and[M-H-90]–were obtained in the choromgraphy of ESIMS-MS on C-glycosyflavonnes with pentose.Conclusively,C-glycosyflavones had their own craking law by C-glycosyflavonnes chromagraphy method which is helpful in finding some new and trace C-glycosyflavonnes compounds.
C-glycosyflavonnes;ESIMS-MS
1001-6880(2011)06-1085-03
2010-02-25 接受日期:2011-06-18
中国人民解放军南京军区十一·五项目(06MA54);南京军区学科带头人培养计划项目(122工程)
*通讯作者 Tel:86-551-2143632;E-mail:xinanw@21cn.com
R284.1
A
