采用热力学分析白云石中二氧化硅对硅热法炼镁的影响
2011-11-23窦韶旭游国强李爱听龙思远章宗和
窦韶旭,游国强,,李爱听,龙思远,,章宗和
(1. 重庆大学 材料科学与工程学院,重庆 400044;2. 重庆大学 国家镁合金材料工程技术研究中心,重庆 400030)
采用热力学分析白云石中二氧化硅对硅热法炼镁的影响
窦韶旭1,游国强1,2,李爱听1,龙思远1,2,章宗和2
(1. 重庆大学 材料科学与工程学院,重庆 400044;2. 重庆大学 国家镁合金材料工程技术研究中心,重庆 400030)
采用热力学方法针对西南地区的白云石SiO2含量偏高不利于硅热法炼镁的情况进行研究。对硅热法炼镁工艺的白云石煅烧过程和真空还原过程的物料体系进行热力学分析,得到各体系中有 SiO2参与化学反应的ΔrGΘ-T 关系。结果表明:SiO2对炼镁结果的影响在于其在白云石煅烧过程的最后阶段会消耗 CaO生成2CaO·SiO2;然而该过程中 SiO2参与的反应很复杂,并可能生成多种硅化合物(2MgO·SiO2、2CaO·SiO2和3CaO·MgO·2SiO2)。计算表明:随着白云石中SiO2的增多,单罐镁产量急剧减少;当SiO2含量小于4%时,减少量约为SiO2含量的4倍。
硅热法;影响;二氧化硅;炼镁;热力学分析
作为迄今为止最轻的商用金属材料,镁合金在汽车制造、3C产品、航空航天和军事工业等众多领域日益显示出重要的应用价值和广阔的应用前景[1-3]。我国是镁产业大国,自1998年至今,镁产量及出口量均居全球首位[4-5]。原镁的生产方法有电解法和热还原法[6-9]两大类。硅热法炼镁(即“皮江法”)作为热还原法的一种,是目前最为成熟、应用最广的炼镁技术。该工艺的主要原料包括白云石、硅铁(还原剂)和萤石(矿化剂)。一般而言,硅热法用白云石的化学成分要求如下:w(MgO) 19%~21%,w(CaO) 30%~33%,w(SiO2)<0.5%、w(Fe2O3)<0.5%、w(Al2O3)<0.5%,w(Na2O)<0.005%、w(K2O)<0.005%,w(Mn)<0.0005%,其中m(CaO)/m(MgO)=1.394、n(CaO)/n(MgO)=1.0[10]。
我国西南地区白云石储量丰富,其白云石钙镁比(接近 1.39)适合炼镁,但 SiO2含量偏高(一般高于0.5%,多在1.5%~3.0%之间)对炼镁不利。为充分利用该地区的高SiO2白云石发展炼镁产业,当前的关键是要研究理解 SiO2对硅热法炼镁的影响并开发出相应的防治技术。
有关 SiO2对硅热法炼镁影响的文献很少。PIDGEON和ALXANDER[11]认为,在白云石中聚集成较大块状分布的SiO2只起到“惰性稀释剂”的作用,而弥散分布的 SiO2则可能会降低煅烧白云石的反应性从而降低镁产量。近期的文献则认为,SiO2的危害体现在两个方面:1) 在白云石煅烧过程中,白云石中的 SiO2、Al2O3和 Fe2O3杂质会生成低熔点化合物(2MgO·SiO2、mCaO·nFe2O3、mCaO·nAl2O3)。这些物质的生成会降低有效CaO和MgO量;还会使煅烧白云石发生粘结,降低其水化活性;发生粘结的白云石表面会生成一种玻璃熔体,不利于其煅烧分解[10,12]。2) 在真空还原过程中,一方面,SiO2会与CaO反应,降低有效CaO的量(生成2CaO·SiO2),导致部分MgO参与反应Si+4MgO=2MgO·SiO2+2Mg↑,使还原温度增高;另一方面,SiO2还会与MgO反应降低有效MgO的量(生成 2MgO·SiO2),导致镁产量降低;生成的2MgO·SiO2还会引起炉料粘结,影响镁蒸气的逸出,从而影响还原过程[10]。
然而,这两种观点都值得商榷。首先,对于含SiO2、Al2O3和Fe2O3杂质的白云石体系,最低熔点在1 200~1 300 ℃之间的只有CaO-Fe2O3相和CaO-Al2O3-SiO2相,并没有 MgO-SiO2和 CaO-Al2O3相;其次,尽管反应Si+4MgO=2MgO·SiO2+2Mg↑的反应温度较高,但其在真空还原条件下是可以进行的。
为研究SiO2对硅热法炼镁的危害机理,本文作者全面考查并用热力学方法分析硅热法炼镁各过程中SiO2可能参与的化学反应。最后通过配料计算,给出了镁产量减少率与SiO2含量的关系式。
1 白云石中硅的存在形式
考查SiO2参与的化学反应,首先要明确白云石中的硅化合物是否以SiO2的形式存在。白云石样品取自重庆万盛某地采矿现场,对其进行 X射线衍射分析(XRD)和化学分析,以明确其物相和化学组成。XRD分析采用Rigaku D/max-2500PC型X射线衍射仪,对白云石样品磨粉后检测。结果显示,白云石中硅以石英(SiO2)形式存在(见图1)。化学分析依照GB 3286.1~GB 3286.12—82,结果显示,SiO2含量为
2.74 %(见表 1)。
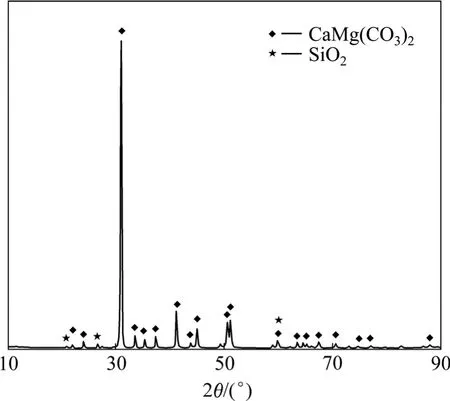
图1 重庆某地白云石的XRD谱Fig.1 XRD pattern of dolomite sample in Chongqing
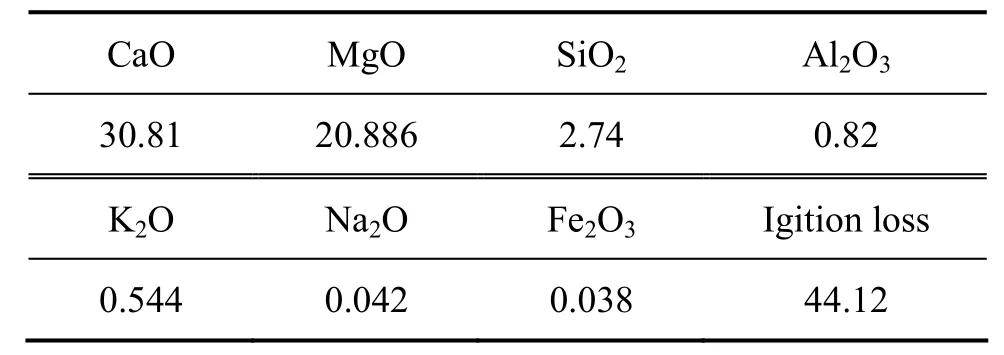
表1 重庆某地白云石的化学组成Table1 Chemical compositions of dolomite in Chongqing(mass fraction, %)
2 热力学原理和分析
2.1 热力学原理
通过计算某一反应的吉布斯自由能变ΔrG,可以确定一定等温、等压、只做体积功的条件下该反应的反应趋势。某一反应在标准状态下的标准吉布斯自由能 ΔrGΘ容易求得[13],在非标准状态下的吉布斯自由能ΔrG,可以对ΔrGΘ使用范特霍夫等温式(式(1))来求得。但是由于ΔrG与实际条件有关,许多情况下对反应实际条件的分析又很复杂,故常用 ΔrGΘ代替ΔrG 来近似分析[14]。 ΔrGΘ或ΔrG值负值越大,反应向右自发进行的可能性越大。

式中:R为摩尔气体常数,R=8.314;T为温度,K;Q为实际条件下物质的压力比或活度比。
2.2 白云石煅烧过程的热力学分析
关于白云石煅烧热分解的研究已经很多,比较一致的看法是其热分解分两个阶段:第一阶段,白云石首先分解为CaCO3、MgO和CO2;第二阶段,CaCO3分解为CaO和CO2。然而,关于这两个阶段的开始温度,目前的文献报道存在很大差异[12,15-19],这是由于不同地区的白云石在化学组成、晶体结构和岩石构造上差异很大。进一步分析发现,热力学计算得到的MgCO3·CaCO3热分解的第一阶段开始于 314 ℃(式(2)),这与白云石的实际分解温度(约750 ℃)也不符。这样,想要把白云石的热分解划分成几个温度确定的分解阶段,并对每个阶段的物质体系分别进行热力学分析,就显得很困难。
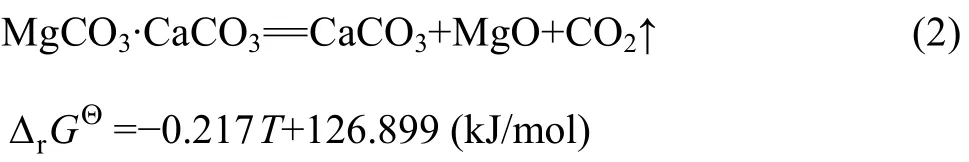
式中:T为温度,K。
为简化问题,对于白云石的热分解,本研究中不考虑其实际分解温度,只用热力学方法分析该过程的物质体系。并用MgCO3的分解来代替和近似白云石的第一阶段分解,分解温度为729 K,尽管白云石分解为CaCO3和MgCO3的步骤实际上并不存在[15-16];第二阶段分解用 CaCO3的分解来表示,分解温度为1 130 K。热力学分析用白云石的组分为 n(CaCO3):n(MgCO3):n(SiO2)=12.05:11.36:1(参考表 1),无其它杂质。
基于上面的分析和假设,热力学分析分为3步:第一步:300~729 K,白云石未分解,考察的反应物体系为mCaCO3-nMgCO3-SiO2;第二步:729~1 130 K,白云石发生第一阶段分解(MgCO3→MgO+CO2↑),考察的反应物体系为mCaCO3-nMgO-硅化合物α;第三步:1 130~1 523 K,白云石发生第二阶段分解(CaCO3→CaO+CO2↑), 考 察 的 反 应 物 体 系 为mCaO-nMgO-硅化合物 β。若第一步结束时没有生成新的硅化合物,则α为SiO2;否则,α为第一步结束时新生成的硅化合物。同样,若第二步结束时没有生成新的硅化合物,则β为α;否则,β为第二步结束时新生成的硅化合物。
下面就这3步分别进行热力学分析。
1) 第一步,300~729 K煅烧温度内,考察的反应物体系为 mCaCO3-nMgCO3-SiO2且 n(CaCO3):n(MgCO3):n(SiO2)=12.05:11.36:1。该体系中SiO2参与反应而可能生成的物质有:MgO·SiO2、2MgO·SiO2、CaO·SiO2、2CaO·SiO2、3CaO·2SiO2、3CaO·SiO2、CaO·MgO·SiO2、CaO·MgO·2SiO2、2CaO·MgO·2SiO2、3CaO·MgO·2SiO2。
这些反应的rGΘΔ 见表2。容易看出,在约300~500 K 内生成 MgO·SiO2和 CaO·MgO·2SiO2,其rGΘΔ 的负值最大;在约500~729 K内生成2MgO·SiO2,其反应rGΘ Δ 的负值最大,因此升温至729 K最可能得到的硅化合物为 2MgO·SiO2。因此第一步结束时(729 K)的产物为 n(CaCO3):n(MgCO3):n(2MgO·SiO2)=12.05:9.36:1。
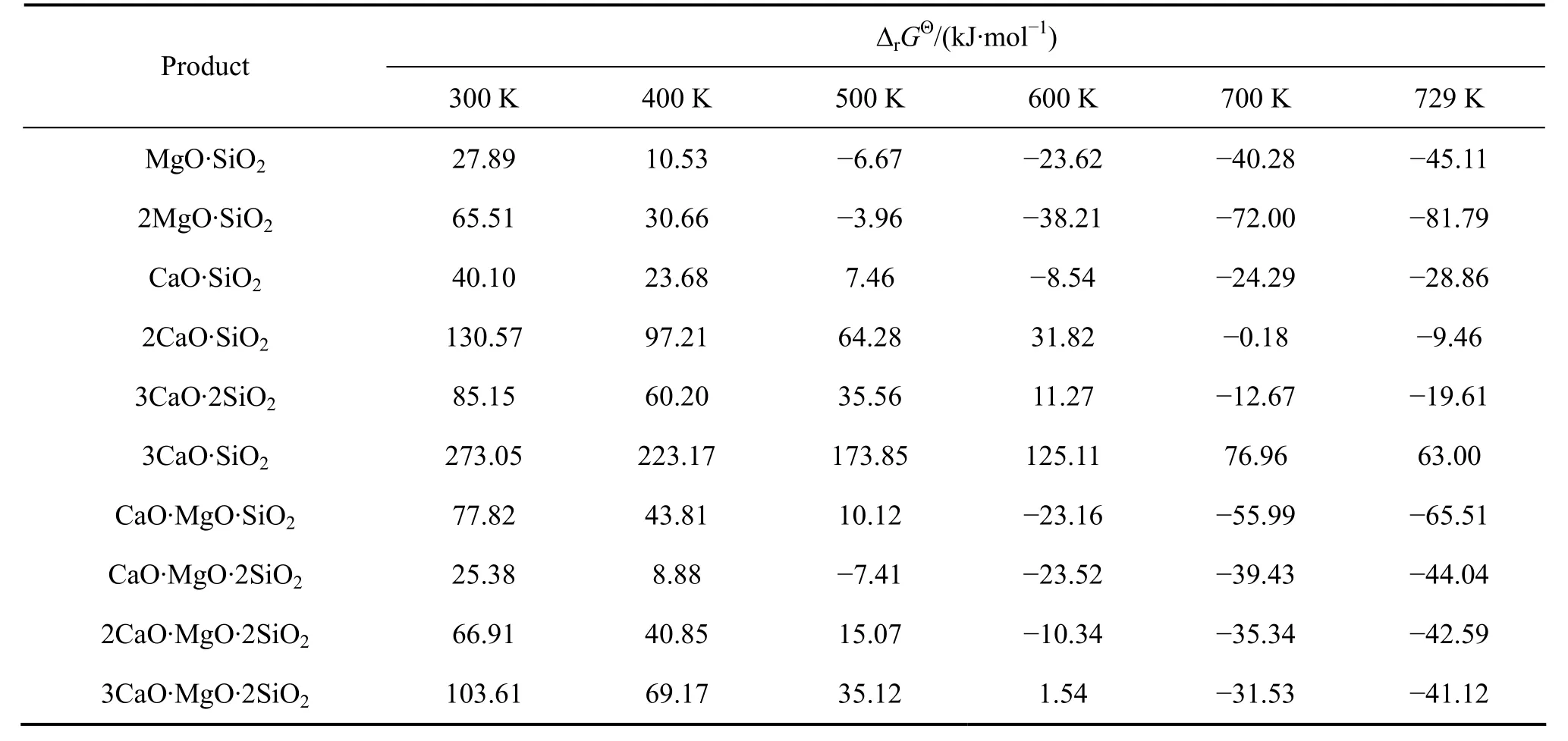
表2 300~729 K时mCaCO3-nMgCO3-SiO2体系中各产物的 Δ rGΘTable2 Δ r GΘ of products in mCaCO3-nMgCO3-SiO2 system during 300-729 K
2) 第二步,在729~1 130 K煅烧温度内,考察的反应物体系为mCaCO3-nMgO-硅化合物α。第二步的反应物体系可以根据第一步的结果分两种极端情况进行考虑:第一种情况,假设第一步中实际没有发生生成2MgO·SiO2的反应(反应太慢或动力学条件不满足),则该体系为n(CaCO3):n(MgO):n(SiO2)=12.05:11.36:1;第二种情况,假设第一步中生成2MgO·SiO2的反应充分进行,则该体系为n(CaCO3):n(MgO):n(2MgO·SiO2)=12.05:9.36:1。
第一种情况下反应体系的rGΘΔ 见表3。在 1 100~1 130 K时,2CaO·SiO2的反应,其rGΘΔ 的负值最大,生成 3CaO·MgO·2SiO2的生成势与之很接近。再考察2CaO·SiO2和 3CaO·MgO·2SiO2相互转化的反应式(3)的rGΘ
Δ ,从表4容易看出,在729~1 130 K时,式(3)的rGΘ
Δ ≤0,即 3CaO·MgO·2SiO2有结合 CaO 并生成 2CaO·SiO2的趋势。因此第一种情况下,第二步结束时(1 130 K)的产物可能为 n(CaCO3):n(MgO):n(2CaO·SiO2)=10.05: 11.36:1。
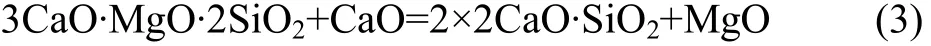
第二种情况下反应体系的rGΘΔ 见表5。同样可以得出,在1 100~1 130 K时,生成2CaO·SiO2反应的rGΘ Δ 的负值最大,生成 3CaO·MgO·2SiO2反应的rGΘ Δ 与之很接近;通过前面分析又知道,3CaO·MgO·2SiO2有结合 CaO 并生成 2CaO·SiO2的趋势。因此第二种情况下,第二步结束时(1 130 K)的产物 可 能 为 n(CaCO3):n(MgO): n(2CaO·SiO2)=10.05:11.36:1。
综上分析,不论是第一种情况还是第二种情况,即不论第一步中生成2MgO·SiO2的反应进度如何,第二步结束时(1 130 K)的产物均为 n(CaCO3):n(MgO):n(2CaO·SiO2)=10.05:11.36:1。
3) 第三步,1 130~1 523 K煅烧范围内,考察的反应物体系为mCaO-nMgO-硅化合物β。根据第一、二步的分析,第三步的反应体系可分4种极端情况分别考虑,如图2所示。
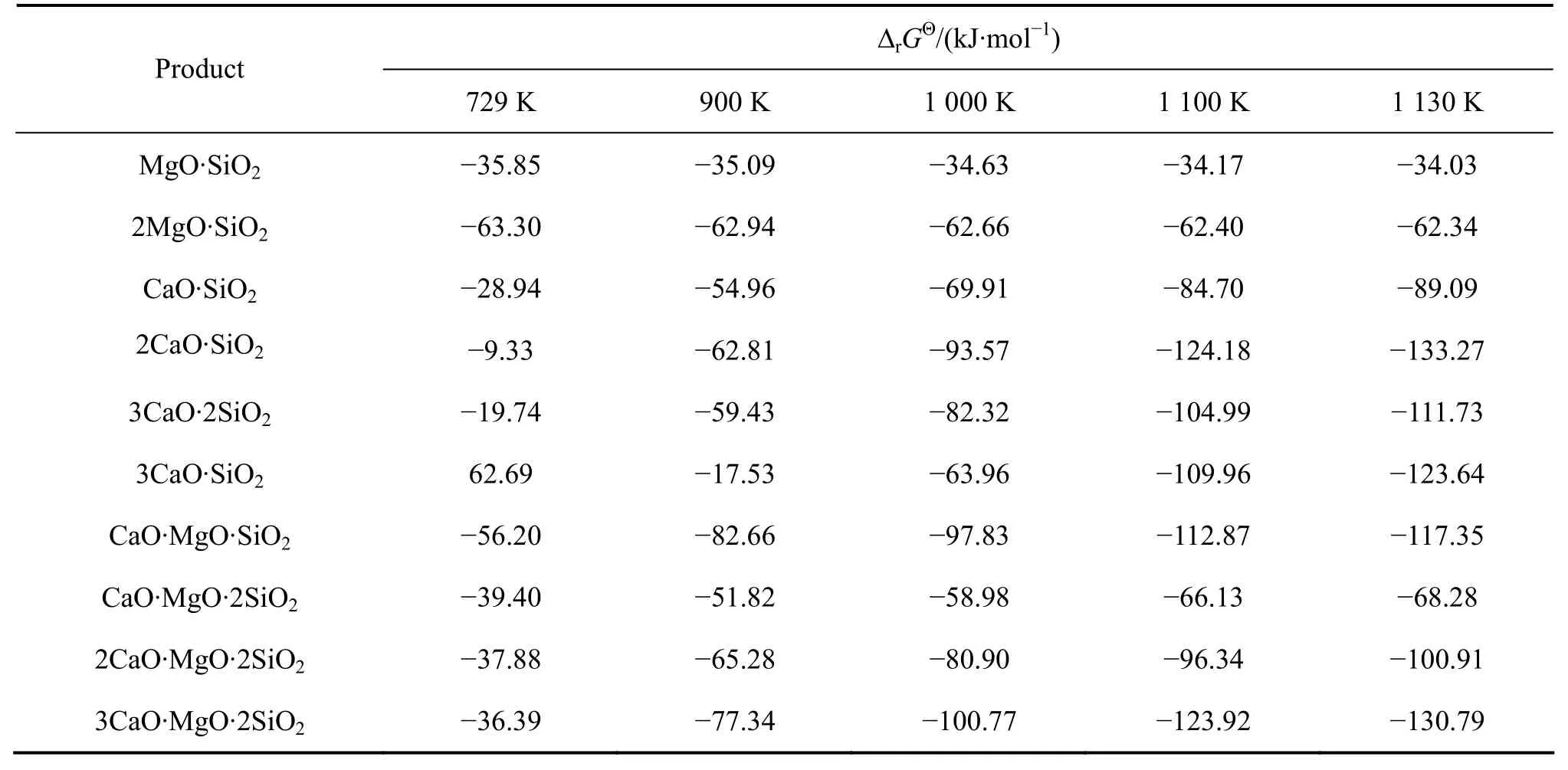
表3 729~1 130 K时mCaCO3-nMgO-SiO2体系中各产物的 Δ rGΘTable3 Δ r GΘ of products in mCaCO3-nMgO-SiO2 system during 729-1 130 K

表4 729~1 130 K式(3)的 Δ rGΘTable4 Δ r GΘ of Eq.(3) during 729-1 130 K

表5 729~1 130 K时mCaCO3-nMgO-M2S体系中各反应的 Δ rGΘTable 5 Δ r GΘ of reactions in mCaCO3-nMgO-M2S system during 729-1 130 K

图2 300~1 13 0K内的反应路径及其生成物Fig.2 Reaction paths and products during 300-1 130 K
如果反应体系为A(即mCaO+nMgO+SiO2),从表6和7可以看出,生成2CaO·SiO2反应的rGΘΔ 负值最大,生成3CaO·MgO·2SiO2反应的rGΘΔ 与之很接近,且 3CaO·MgO·2SiO 有结合 CaO 并生成 2CaO·SiO2的趋势。如果反应体系为 B或 D(即 mCaO+nMgO+2CaO·SiO2),该体系化学上很稳定,不会继续发生反应。如果反应体系为C(即mCaO+nMgO+2MgO·SiO2),从表6和8可以看出,生成2CaO·SiO2反应的rGΘΔ 的负值最大,生成3CaO·MgO·2SiO2反应的rGΘΔ 为与之很接近,且 3CaO·MgO·2SiO2有结合 CaO并生成2CaO·SiO2的趋势。

表6 1 130~1 523 K时式(3)的 Δ r GΘ 关系Table 6 Δ r GΘ of Eq.(3) during 130-1 523 K
综上分析,不论第三步的反应体系为A、B(D)或是C,反应结束时(1 523 K)的产物都应该为n(CaO):n(MgO):n(2CaO·SiO2)=10.05:11.36:1。
2.3 球团炉料真空还原过程的热力学分析
球团炉料真空还原过程是将球团炉料装入还原罐,在约1 200 ℃的高温和小于13 Pa的真空条件下发生还原反应产生镁蒸气,镁蒸气冷凝后得到结晶镁。球团炉料由煅烧白云石、硅铁(多为 75%硅铁)和萤石(CaF2)按一定比例混匀、压球得到。考虑该过程的煅烧白云石中硅化合物—硅铁—萤石体系,分析煅后硅化合物对该过程产生的影响。
通过前面的分析可知,如果煅烧过程中反应进行不彻底,则煅烧白云石中可能同时含有 SiO2、2MgO·SiO2、3CaO·MgO·2SiO2和 2CaO·SiO2。在真空镁还原过程中,这些硅化合物会继续反应并最终转化为 2CaO·SiO2,这一结论可以由真空镁还原过程和白云石煅烧过程有相同的最高温度得到[11]。
萤石(CaF2)主要起催化剂的作用,可提高镁还原反应的速度,但不影响反应平衡,本身也不发生化学反应[10]。
硅铁中的Fe不参与化学反应,Si还原煅烧白云石并生成镁蒸气和 2CaO·SiO2。该过程中 Si和 SiO2可能同时存在,所以需要对反应(4)进行考虑。在1 200~1 250 ℃、13 Pa真空条件下,反应(4)的吉布斯自由能 ΔrG ≤0,热力学意义上是可以进行的。然而,近年来研究工作者认为,硅热法炼镁只是固-固反应,镁还原过程中并没有SiO气体生成[10]。

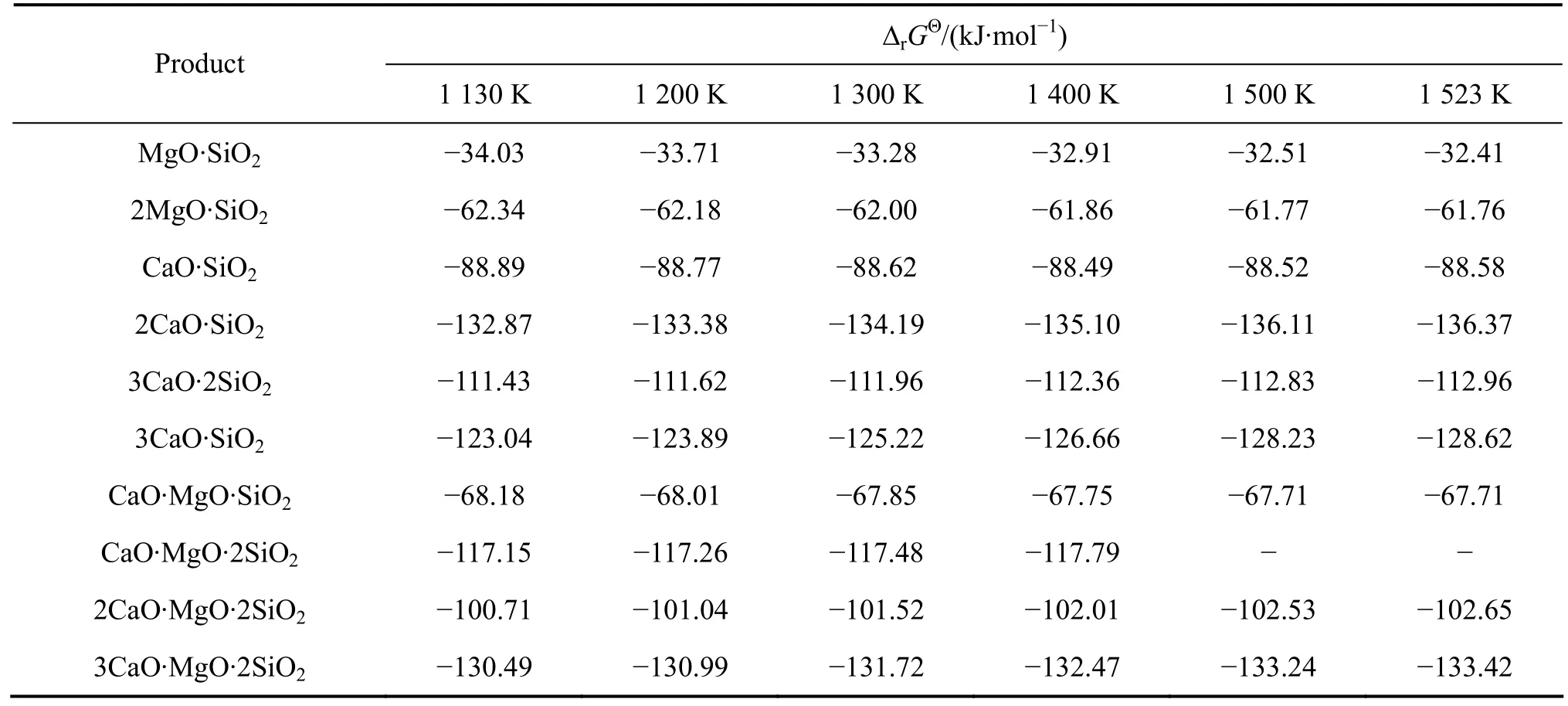
表7 1 130~1 523 K时mCaO-nMgO-SiO2体系中各产物的 Δ rGΘTable 7 Δ r GΘ of products in mCaO-nMgO-SiO2 system during 1 130-1 523 K
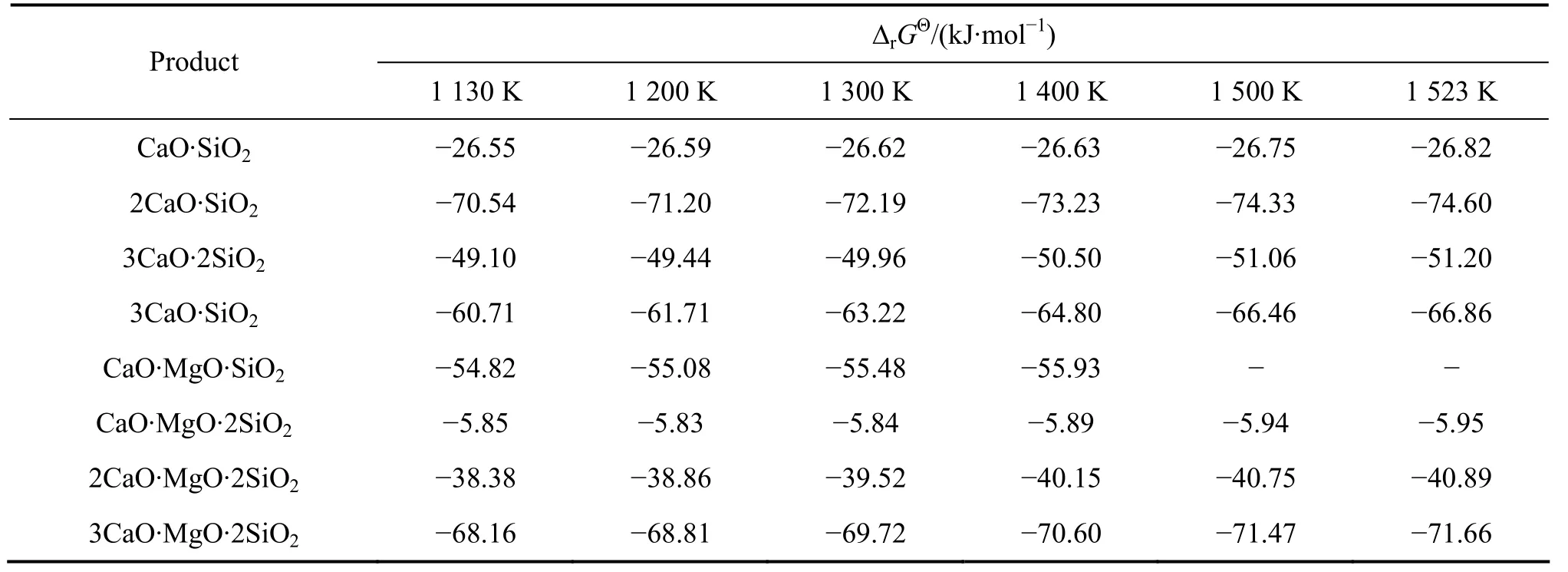
表8 1 130~1 523 K时mCaO+nMgO+2M2S体系中各产物的 Δ rGΘTable 8 Δ r GΘ of products in mCaO+nMgO+2M2S system during 1 130-1 523 K
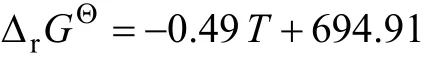
式中:T为温度,K。
综上分析,真空镁还原过程中主反应是 Si还原CaO·MgO并生成镁蒸气和2CaO·SiO2;如果煅烧过程中反应进行不彻底,那么煅烧白云石中的非2CaO·SiO2硅化合物会继续反应并最终转化为2CaO·SiO2;煅烧白云石中的硅化合物不会与硅铁和萤石反应。
2.4 白云石中SiO2的量对炼镁结果的影响
如上所述,白云石中的SiO2最终会结合CaO生成2CaO·SiO2。假设白云石组分为n(CaCO3):n(MgCO3):n(SiO2)=n:n:1,则煅烧白云石的组分为 n(CaO):n(MgO):n(2CaO·SiO2)=(n-2):n:1。如果配料时不添加CaO,还原过程中就会有 2 mol MgO参与反应Si+4MgO=2Mg↑+2MgO·SiO2(热力学计算表明该反应可以进行),1 mol MgO不能被还原,这无疑会降低单罐镁产量。因此,配料时应根据白云石中SiO2的量加入一定的CaO。
尽管如此,SiO2杂质和配料时添加CaO会导致还原罐装载的MgO减少,所以即使配料时添加CaO,单罐镁产量也还会在一定程度上有所减少。为了量化SiO2含量对镁产量的影响,用单罐镁产量来表示炼镁效果:假定还原罐单罐装料 120 kg,白云石中n(CaCO3)/n(MgCO3)=1,炉料配比计算详见文献[10]。从表9可看出,随着白云石中SiO2的增多,单罐镁产量急剧减少。镁产量减少率与SiO2含量的关系如式(5)所示。容易看出,白云石中SiO2含量较低(≤4%)时,镁产量减少率约为SiO2含量的4倍。
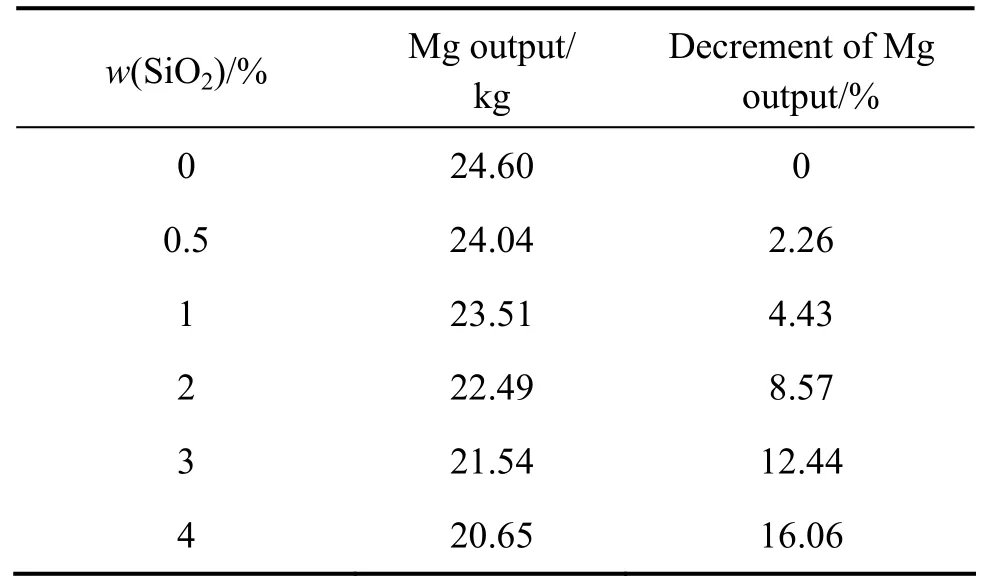
表9 白云石中SiO2含量对单罐镁产量的影响Table 9 Effect of SiO2 content in dolomite on magnesium output per retort

式中:w为白云石中SiO2的含量,%;De为白云石中SiO2的含量为w%时的镁产量减少率。
3 结论
1) SiO2的影响发生在白云石煅烧阶段,使用含SiO2白云石进行硅热法炼镁,配料时应添加一定量的CaO。
2) 白云石煅烧过程中,SiO2参与的反应很复杂,其间可能生成多种硅化合物(2MgO·SiO2、2CaO·SiO2和 3CaO·MgO·2SiO2);最后得到的煅烧白云石中的硅化合物为 2CaO·SiO2。
3) 随着白云石中 SiO2的增多,单罐镁产量急剧减少。计算得到的镁产量减少率与SiO2含量之间的关系式表明,当白云石中SiO2含量较低(≤4%)时,镁产量减少率约为SiO2含量的4倍。
REFERENCES
[1] CLOW B B. Magnesium industry overview[J]. Advanced Mater Proc, 1996, 15: 33-34.
[2] EVANS R W, WILSHIRE B. Creep of metals and alloys[M].London: Institute of Metals, 1985.
[3] RAMAKRISHNAN S, KOLTUN P. Global warming impact of the magnesium produced in China using the Pidgeon process[J].Resources, Conservation and Recycling, 2004, 42: 49-64.
[4] 龚 涛. 产品科技含量与规模效益并重是我国镁工业的立身之本[J]. 轻金属, 2000(12): 40-44.GONG Tao. Both technological content of the product and scale economic benefit are key to Chinese magnesium industry[J].Light Metals, 2000(12): 40-44.
[5] 郁青春, 杨 斌, 马文会, 李志华, 戴永年. 氧化镁真空碳热还原行为研究[J]. 真空科学与技术学报, 2009(5): 68-71.YU Qing-chun, YANG Bin, MA Wen-hui, LI Zhi-hua, DAI Yong-nian. Study of carbothermic reduction of magnesia in vacuum[J]. Journal of Vacuum Science and Technology, 2009(5):68-71.
[6] 刘红湘, 戴永年, 马文会, 李一夫. 中国镁工业研究方向探讨[J]. 轻金属, 2007(1): 46-49.LIU Hong-xiang, DAI Yong-nian, MA Wen-hui, LI Yi-fu. The research direction of China’s magnesium industry in the future[J].Light Metals, 2007(1): 46-49.
[7] BROOKS G, TRANG S, WITT P, KHAN M N H, NAGLE M.The carbo-thermic route to magnesium[J]. JOM, 2006, 58(5):51-55.
[8] 彭建平, 陈世栋, 武小雷, 胡文鑫, 冯乃祥. 碳化钙热法炼镁试验研究[J]. 轻金属, 2009(3): 47-49.PENG Jian-ping, CHEN Shi-dong, WU Xiao-lei, HU Wen-xin,FENG Nai-xiang. Study on thermal reduction of calcined dolomite by calcium carbide[J]. Light Metals, 2003(3): 47-49.
[9] YANG J, KUWABARA M, LIU Z Z, ASANO T, SANO M. In situ observation of aluminothermic reduction of MgO with high temperature optical microscope[J]. The Iron and Steel Institute of Japan, 2006, 46: 202-209.
[10] 徐日瑶. 硅热法炼镁生产工艺学[M]. 长沙: 中南大学出版社,2003.XU Ri-yao. Silicon-thermal reductive method in magnesium production[M]. Changsha: Central South University Press, 2003.
[11] PIDGEON L M, ALEXANDER W A. Thermal production of magnesium—Pilot-plant studies on the retort ferrosilicon process[J]. Trans Am Inst Mining Mater Eng, 1944, 159:315–352.
[12] 熊呈辉, 周天瑞, 徐 河, 谢水生. 煅烧白云石质量对还原过程的影响[J]. 有色金属: 冶炼部分, 2006(3): 26-28.XIONG Cheng-hui, ZHOU Tian-rui, XU He, XIE Shui-sheng.The influence of the quality of calcined dolomite on reduction process[J]. Nonferrous Metals: Extractive Metallurgy, 2006(3):26-28.
[13] 叶大伦, 胡建华. 实用无机物热力学数据手册[M]. 北京: 冶金工业出版社, 2002.YE Da-lun, HU Jian-hua. The handbook of inorganic thermodynamic data[M]. Beijing: Metallurgical Industry Press,2002.
[14] MOORE J J. Chemical metallurgy[M]. London: Butterworths,1981: 61-67.
[15] 翟学良, 张 越. 太行山脉武安白云石热分解机理[J]. 矿物学报, 2006(6): 160-164.ZHAI Xue-liang, ZHANG Yue. Study of the thermal decomposition mechanism of Taihangshan dolomite[J]. Acta Mineralogical Sinica, 2006(6): 160-164.
[16] 马保国, 崔 崇, 崔可浩, 彭长琪. 白云石热分解过程及影响因素的研究[J]. 武汉工业大学学报, 1994, 16(2): 56-61.MA Bao-guo, CUI Chong, CUI Ke-hao, PENG Chang-qi. On dolomite heat decomposition and relevant factors[J]. Journal of Wuhan university of Technology, 1994, 16(2): 56-61.
[17] 吴芸芸, 何明中, 赵敏伦, 许聚良. 岩峰白云岩的热分解特性研究[J]. 武汉科技大学学报, 2009, 32(5): 500-504.WU Yun-yun, HE Ming-zhong, ZHAO Min-lun, XU Ju-liang.Thermo-decomposition characteristics of Yanfeng dolomite[J].Journal of Wuhan University of Science and Technology, 2009,32(5): 500-504.
[18] 蒋汉祥, 梁 莉, 林 琳, 张延波, 李 明. 微波加热白云石生产煅白的反应机理[J]. 重庆科技学院学报:自然科学版,2008, 10(1): 36-39.JIANG Han-xiang, LIANG Li, LIN Ling, ZHANG Yan-bo, LI Ming. Reaction mechanism of heating dolomite product burnt dolomite by microwave[J]. Journal of Chongqing University of Science and Technology: Natural Sciences Edition, 2008, 10(1):36-39.
[19] 李红霞. 耐火材料手册[M]. 北京: 冶金工业出版社, 2007:146.LI Hong-xia. The handbook of refractories[M]. Beijing:Metallurgical Industry Press, 2007: 146.
Thermodynamics analysis effect of silicon dioxide in dolomite on magnesium production by silicothermic process
DOU Shao-xu1, YOU Guo-qiang1,2, LI Ai-ting1, LONG Si-yuan1,2, ZHANG Zong-he2
(1. College of Materials Science and Engineering, Chongqing University, Chongqing 400044, China;2. National Engineering Research Center for Magnesium Alloys, Chongqing University, Chongqing 400030, China)
The condition of high-SiO2dolomite unfavorable for the magnesium production at the silicothermic process by thermodynamic was investigated. The thermodynamics analysis was used to study the processes of the dolomite calcination and the magnesium production by reduction, and ΔrGΘ- T relations of the chemical reactions involving SiO2were obtained. The results show that the effect of SiO2is the formation of 2CaO·SiO2in the final calcined dolomite,which reduce the CaO. The reactions involving SiO2in the calcination process are complex and several intermediate product, such as 2MgO·SiO2, 2CaO·SiO2and 3CaO·MgO·2SiO2form. With the increase of SiO2in dolomite, the magnesium output sharply decreases, and the decrease is about 4 times of the SiO2content when SiO2is less than 4%.
silicothermic process; effect; silicon dioxide; magnesium production; thermodynamics analysis
TF822
A
1004-0609(2011)12-3129-08
重庆市重大科技攻关项目(CSTC009AA4002);重庆市科技攻关计划项目(CSTC2010AA4045);中央高校基本科研业务费资助(CDJXS11132226);重庆市国土资源和房屋管理局科技计划项目(CIGMR0908);重庆大学大型仪器设备开放基金资助(2010011507)
2010-11-30;
2011-04-02
游国强,讲师,博士;电话:13657676560;E-mail: you_cqu@yahoo.com.cn
(编辑 李艳红)
