我院2010 年186 例药品不良反应报告分析
2011-11-20庞士禄张开国姜德文
庞士禄 张开国 姜德文
(安徽铜陵有色职工总医院药剂科,安徽 铜陵244000)
药品不良反应(Adverse Drug Reaction,ADR)是指合格药品在正常用法、用量下出现的与用药目的无关或者意外的有害反应。通过ADR 监测、分析,将报告反馈临床,可提高临床治疗水平,减少药源性疾病,并对药物上市再评价等方面有重要作用[1]。现就我院2010 年上报的186例ADR 报告进行总结,分析,为临床合理用药及ADR 的预防提供参考。
1 资料与方法
收集我院医生、护士、药师2010 年1 - 12 月上报的ADR 报告186 例,按患者一般情况、给药途径、涉及药物种类、ADR 损害类型及临床表现进行统计和分析。
2 结果
2.1 患者一般情况
男性103 例(55.38%),女性83 例(44.62%)。年龄5 ~91岁,具体性别、年龄分布情况见表1。
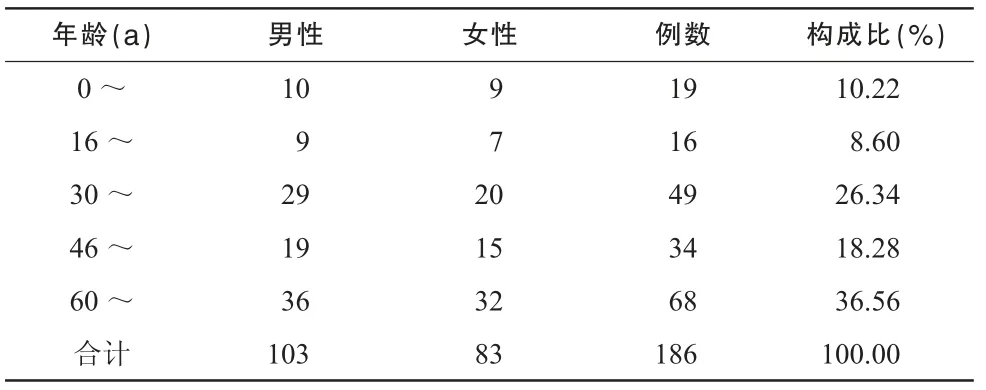
表1 ADR 性别、年龄分布情况
2.2 给药途径
186 例ADR 报告中,静脉给药174 例(93.55%),口服给药10 例(5.38%),吸入给药1 例(0.54%)。
2.3 涉及药物种类
186 例ADR 报告中,涉及化学药品49 个品种,中药制剂2 个品种;化学药品引起ADR 165 例(88.71%),中药制剂引起ADR 21 例(11.29%),药品种类及构成比见表2。具体涉及的抗感染药物情况见表3。
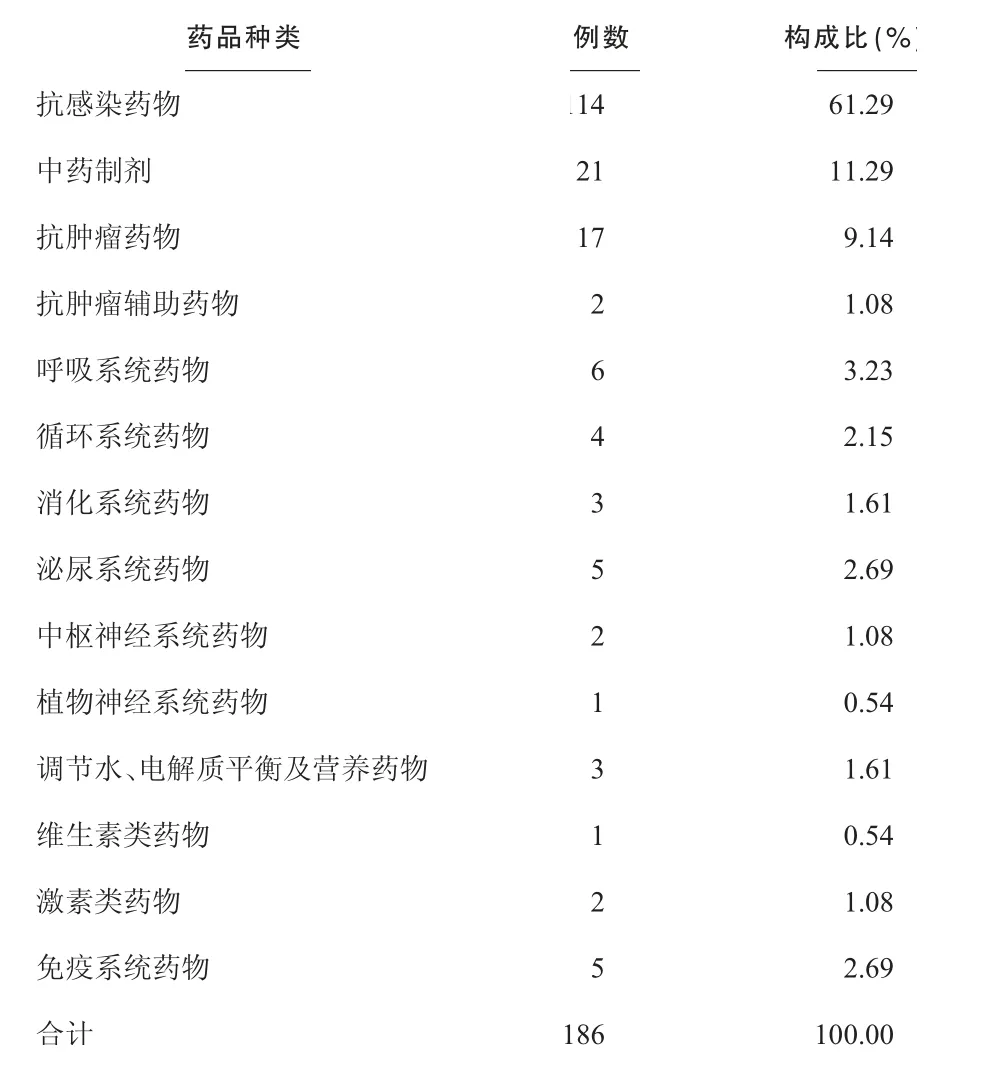
表2 引起ADR 涉及的药品种类及构成比
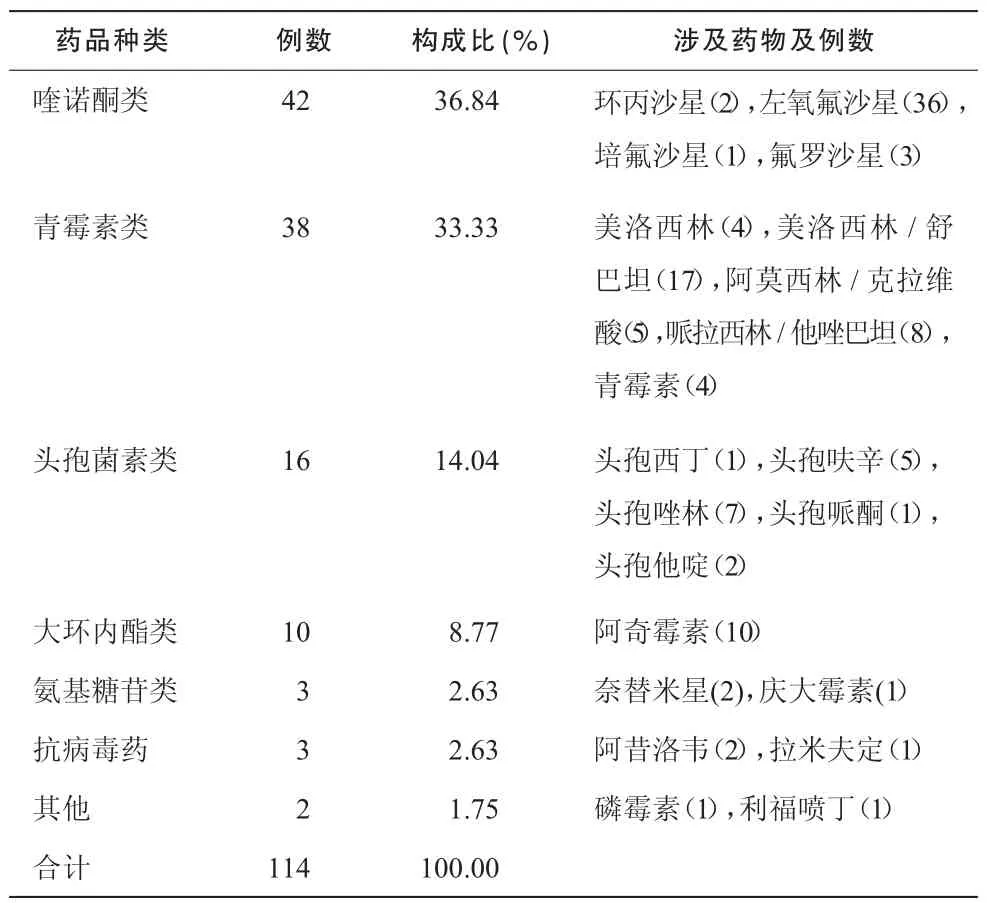
表3 引起ADR 的抗感染药物种类、品种及构成比
2.4 ADR 累及器官/ 系统及临床表现(见表4)
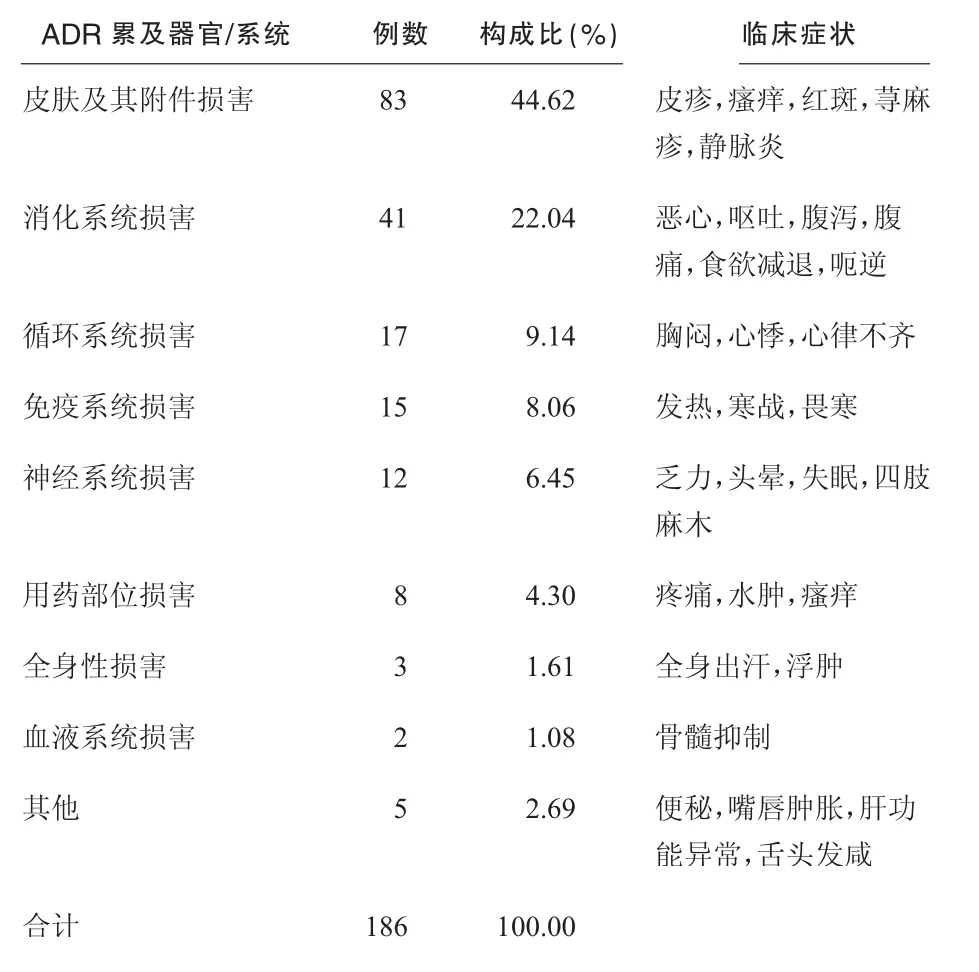
表4 ADR 累及器官/系统及临床表现
2.5 ADR 因果关系评价
根据国家ADR 监测中心制定的ADR 因果关系判断标准,186 例ADR 报告中肯定92 例(49.46%),很可能94例(50.54%)。其中治愈87 例(46.77%),好转98 例(52.69%),有1 例(0.54%)出现后遗症,无死亡和特别严重ADR 报告。
3 讨论
3.1 由表1 可知,186 例ADR 报告中,男性略多于女性,中老年患者ADR 发生率较高,这可能与医院就诊的人群分布有关。中老年尤其是65 岁以上的老年患者各项生理机能减退,血浆蛋白与药物的结合能力减弱,肝肾代谢与排泄功能减弱,药物代谢速度降低,从而易发生体内药物蓄积[2],导致ADR 发生率较高。临床用药中应考虑年龄因素对ADR 的影响,遵循个体化原则,并加强对中老年患者的用药监测,以确保用药安全,避免ADR 的产生。
3.2 从“2.2”项可知,186 例ADR 报告中,静脉给药为引起ADR 的主要给药途径,占93.55%。主要原因是静脉给药具有直接进入血液、无肝脏首过效应、起效快的优点,大多数医师和患者都选择这种给药方式;同时,由于药物直接进入血液,药物的内在理化性质、配制方法相互作用以及溶剂选择、输液速度、放置时间、药物制剂中杂质等[3]因素均可引发ADR。因此,建议在临床用药方面,如无必要最好采取“先口服后静脉”的给药原则,特别是对于流动性很大不易监测的急诊患者。在使用静脉给药治疗时,临床应加强输液过程中的巡视,加强用药期间ADR 监测,一旦发生ADR 应立即停药并对症处理,尽量减少ADR 对患者的损害。
3.3 我院ADR 涉及的器官/ 系统以皮肤及其附件损害最多,占44.62%,主要为皮疹,瘙痒,荨麻疹等。一般症状较轻,停药或使用抗过敏药物进行对症治疗后,症状即可缓解或消失。其次是消化系统损害,占22.04%。统计结果与其他医院基本一致[4],主要原因是上述两类ADR 易于观察和识别并能被及时上报,这也与我国ADR 监测工作处于初始阶段,上报ADR 以易于发现、识别的ADR 为主有关[5]。
3.4 由表2、3 可见,186 例ADR 报告中引起ADR 较多的是抗感染药物,其中喹诺酮类报告例数最多,其次是β-内酰胺类抗菌药。喹诺酮类药物抗菌谱广,抗菌作用强,使用方便,应用广泛,其引发的ADR 所占的比例也最高。β- 内酰胺类抗菌药所占的比例较高,与其价格相对较低,抗菌效果好,临床应用广泛有关。目前,国内医院抗菌药物不合理使用的问题仍较严重,由此引发的ADR 不断发生,这就要求临床应严格按照《抗菌药物临床应用指导原则》和药品的说明书规定的适应证、用法、用量、注意事项的要求合理地选择、正确地使用抗感染类药物[6],避免用药剂量过多或过少,减少不必要的联合用药。无指征的预防性用药等情况的发生,把引发ADR 的可能性降到最低。
目前,基层医院ADR 的监测和呈报尚处在初始阶段,而药物在使用过程中,不可避免地会由于各种原因而产生ADR,这就要求ADR 监管部门加强宣传教育力度,特别是针对临床一线的医护人员,使其认识到呈报ADR 的重要性,在药物的使用过程中,提高对药物使用的观察性,不断建立和完善ADR 监测和报告制度,从而真正达到用药安全、经济、有效的目的。
[1] 周银才.我院187 例药品不良反应报告分析[J].中国药业,2010,19(17):56.
[2] 陈新谦,金有豫,汤光.新编药物学[M].16 版,北京:人民卫生出
版社,2007:14-18.
[3] 王俊,王奕,程鹏.27 例药品不良反应报告分析[J].中国医院药
学杂志,2009,29(4):338.
[4] 杨惠萍,赵蕊,张小影.287 例药品不良反应分析[J].中国药事,2007,21(4):284.
[5] 邓晟,尹桃,杨芝春,等.国内外加替沙星不良反应病倒报告浅析[J].中国药物警戒,2006,3(5):267.
[6] 刘文丽.六安市2006 年药品不良反应监测报告分析[J].安徽医药,2007,11(12):1149.
