肥厚性硬脑膜炎1例报道及文献复习
2011-11-20姜亚平石飞飞
王 丽 姜亚平 石飞飞 吴 倩
肥厚性硬脑膜炎(hypertrophic cranial pachymengitis,HCP)是以颅内硬脑膜弥漫性肥厚和纤维化炎症过程为特征的一种少见疾病。1869年Charcot首次报道了此病,国外迄今有200 余篇文献报道;国内对此病认识较晚,1995 年始有报道,且国内、外文献均多以个案报道为主,较多病例数的综合文献较少,加之该病临床表现多样,极易与其他疾病混淆,造成临床上的误诊,本研究报道了本院确诊的1例HCP患者的临床资料并复习相关文献,目的是加强对本病的认识,做到早诊断,早治疗,改善患者预后。
1 临床资料
患者,男,41 岁,因“右侧耳鸣、听力下降1 年余,右眼失明3月”入院;患者于2008年8月无明显诱因突发右侧耳鸣,耳鸣呈持续性,逐渐出现右侧听力下降,伴右眼胀痛,2008年10月1日出现右侧口角歪斜,右面部麻木,在当地医院诊断为“多组颅神经炎”,10月20日入住北京武警医院,经治疗面瘫消失,11月3日出现头痛、眼胀、水平向复视,11月5日就诊于北京同仁医院耳鼻喉科,行头部MRI检查示右侧乳突炎,右侧颞区硬脑膜及小脑幕明显肥厚并强化,行乳突探查术,病理诊断为“右乳突慢性炎性假瘤”,使用抗生素及甲强龙等治疗4 d后,除复视外其余症状均消失,出院后继续使用强的松口服治疗,停用激素后,右耳鸣、听力下降,右眼胀痛、视力下降,右面部麻木再次复发,2009年2月16日就诊于本院,诊断为多组颅神经炎,经抗感染加激素治疗后症状好转出院,随后反复出现复发-住院-好转-复发,先后在本院住院2次,最后于2009年8月因右眼逐渐失明,11月左眼开始出现视力下降再次入住本院,诊断为耳源性肥厚性硬脑膜炎,在使用激素的同时加用依木兰(硫唑嘌呤)治疗后症状减轻出院,随后一直门诊随访至2011年5月,患者双眼视力基本恢复,右耳听力稍差,偶尔出现右耳耳鸣,体检除右眼底可见视乳头颞侧苍白外,其余颅神经未见异常。在诊疗过程中患者始终无发热、无脑膜刺激征。辅助检查:血、尿常规,血生化,肝炎全套,免疫全套,肿瘤标记物,心电图,胸片未见明显异常;腰椎穿刺检查,脑脊液(CSF)总蛋白594mg/L,细胞数及糖、氯化物正常,CSF 免疫分析示鞘内有IgG 产生,未找到病源菌及肿瘤细胞;视觉诱发电位(VEP)提示双眼P100波潜伏期延长并伴波幅反应低,脑干听觉诱发电位(BAEP)提示听觉神经通路有脑干中枢段损伤可能(右耳明显);头颅MRI平扫、增强及治疗前后对比见图1~6。
2 讨 论
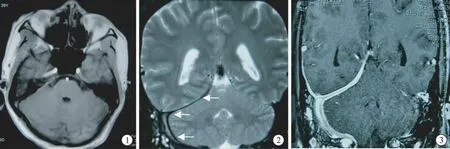
图1 头部MRI平扫示T1WI上肥厚的小脑幕呈等信号 图2 头部MRI平扫示T2WI上肥厚的小脑幕呈明显低信号。图3 头颅MRI增强扫描示右侧颞叶区硬脑膜及小脑幕明显增厚并强化,肥厚的硬脑膜表现为“轨道征”,右侧乳突炎

图4 治疗前头颅MRI增强扫描示右侧颞叶区硬脑膜、小脑幕及视交叉区硬脑膜明显增厚并强化;右侧乳突炎

图5 示右侧颞叶区硬脑膜、小脑幕及视交叉区硬脑膜明显增厚并强化,较图4 有明显好转,右侧乳突炎

图5 示右侧小脑幕稍增厚并强化,较图5明显好转
目前HCP 的病因及发病机制尚未完全明确,一般按病因将其分为特发性HCP(idiopathic HCP,IHCP)和继发性HCP(secondary HCP,SHCP)。IHCP在临床上找不到确切的病因,多数学者认为其与自身免疫有关,近年关于IHCP 患者血液检查中发现髓过氧化物嗜中性粒细胞胞浆抗体(MPO-ANCA)报道[1-3]日益增多。MPO-ANCA 是一种提示血管炎的标记物,主要见于自身免疫性疾病;最近Simone Rossi等报道了4例IHCP 患者,其中2例患者硬脑膜活检发现有显著的CD4+T 细胞浸润,故其推测细胞介导的免疫机制可能是特发性HP的一种发病机制[4];Nakamura等报道了1 例HLAA24(+)、脑膜活检以CD8+T 细胞占绝对优势的HP患者,并认为免疫失调和自身免疫在HP 的发展进程中起了重要作用[5]。SHCP多继发一些感染性疾病,病原菌可能经副鼻窦、中耳、乳突及骨折的颅骨等侵犯硬脑膜,根据本研究总结的国内文献报道的所有HCP 患者的临床资料中证实有副鼻窦、中耳、乳突等感染或感染史者64(64/154)例,因此本研究推测,头面部感染性疾病对硬脑膜的波及以及感染后免疫过度或失调可能是SHCP 的主要原因。
HCP多为慢性起病,好发于成年人,男性多于女性,病程长短不等,主要临床表现为慢性反复发作性头痛、多发性颅神经受损、共济失调及脑功能障碍等,在Parney IF等的报道中头痛、颅神经麻痹及共济失调分别占88%,62%及32%[6]。(1)头痛。头痛是HCP临床最常见的症状,也是最常见的首发症状,以慢性进展性或频繁发作为特征;Kupersmith MJ等人总结HP患者头痛占92%,多数患者刚开始以搏动性头痛起病,后逐渐演变成严重的持续性剧烈头痛[7]。Okuma H 对22例长期慢性头痛的患者进行了统计分析,发现其中有4.5%的患者最终诊断为肥厚性脑膜炎,因此对长期慢性头痛,无论是哪种形式的头痛,行头部MRI,尤其MRI增强扫描是非常必要的[8];头痛可持续数日、数月甚至数年,有的患者头痛可为唯一的症状;Simone Rossi等报道了4 例IHCP 的患者,分别进行了长达24 至120个月的随访,但患者仅仅表现为头痛,无其他神经系统受损表现,头痛原因可能为炎症刺激硬脑膜和(或)肥厚的硬脑膜压迫引起颅高压所致,而颅高压的机制可能是脑膜肥厚压迫致脑脊液循环不畅,或视网膜中央静脉闭塞所致[9];有少数患者的头痛在坐位或立位时出现或加重,表现为体位性头痛,且腰穿检查脑脊液压力偏低,低颅压的机制目前尚不清楚,可能与下丘脑功能功能紊乱,静脉窦和蛛网膜颗粒吸收功能亢进等有关[10];(2)颅神经损害。根据病变硬脑膜位置的不同,颅神经病变取决于两种模式[11],一种为海绵窦到眶上裂的硬脑膜受累,此时可出现Ⅱ~Ⅵ对脑神经受损表现;另一种为大脑镰小脑幕到后颅窝的硬脑膜受累,此时多出现IXXII组颅神经受损表现。根据目前文献报道,颅神经损害的原因为硬脑膜肥厚导致颅神经穿出颅骨的间隙变窄,使颅神经受压及肥厚的脑膜引起颅神经局部缺血所致[10]。I~XII对颅神经均可损害,可单根神经受损,也可多根神经损害。在国内外较多例数的统计中以视神经、展神经、听神经损害为最多见[7][12]。(3)小脑性共济失调。主要由于小脑幕增生肥厚压迫小脑及桥小脑角所致;(4)其他。肥厚的硬脑膜刺激大脑皮层致癫痫间;脑实质受损致精神异常、躯体感觉障碍、瘫痪、病理征阳性等。
IHCP实验室检查,白细胞计数及百分比、CRP及ESR 可轻至中度升高,血液呈非特异性改变。脑脊液检查亦无特异性,可完全正常,也可表现为蛋白、细胞轻度升高,但脑脊液蛋白多<1000 mg/L,细胞多<50×106/L,糖、氯化物基本正常,少数患者脑脊液免疫球蛋白可升高。但目前在多数情况下难以明确IHP和SHP的CSF的确切异同。
在影像学检查上MRI增强扫描对诊断最有价值,表现为在T1WI上增厚的硬膜呈等或低信号,在T2WI上肥厚的脑膜呈低信号,其周边可见高信号影,注射增强剂在T1像上对比增强明显,可见增生肥厚的硬膜明显强化,大部分呈条带状或结节状均匀强化,若为结节样强化,则表明硬膜增厚不均等,可能与不同部位感染程度不一、反复感染及不同病因感染有关,一般结节样强化多提示预后不佳[13];强化根据病变部位不同可位于大脑镰、小脑幕、额、颞、顶、枕部,海绵窦部硬脑膜等一个或多个部位,其中HCP患者以大脑镰及小脑幕强化为最多见,且大脑镰和小脑幕的硬脑膜强化具有特征性,多表现为中心线样无强化区,两侧呈轨道样强化,即轨道征[14]。若为邻近组织的感染播散所致,主要可见中耳乳突炎、副鼻窦炎等MRI平扫及增强团块样表现;此外还可探查到脑水肿、静脉窦栓塞、静脉阻塞、继发性脑白质改变、脑积水、脑梗死及继发性颅内出血等改变。本研究报道的1例HCP患者发病初期的MRI增强扫描就具有上述特征性的双轨征(图3~4)。
目前国际上尚无统一、公认的诊断标准,确诊主要依赖硬脑膜活检,临床诊断主要依靠临床表现、影像学特征、激素治疗有效等特征,早期仅表现为头痛时很难做出准确诊断。本病需与以下疾病相鉴别:(1)偏头痛,HCP 患者早期头痛性质与偏头痛性质相似,为发作搏动性疼痛,但偏头痛无神经损害的临床表现,且影像学检查无异常;(2)软脑膜病变,尤其是结核性软脑膜炎,也可表现为头痛及多组颅神经损害,但软脑膜蛛网膜增强后可见其卷入脑回或基底池周围显影明显,而肥厚的硬脑膜增强后强化处呈条带状或斑片状,沿颅顶或颅底的内层显影,或累积大脑镰及(或)小脑幕等处,却不深入脑回或脑池内;(3)低颅压综合症,患者亦可表现为慢性头痛,头颅MRI增强扫描可见硬脑膜强化效应,但具特征性的体位相关性头痛,腰穿压力明显降低,以补液治疗为主,激素治疗无效,当患者表现为体位性头痛时,应注意与其鉴别;(4)蛛网膜下腔出血,CT 检查可见脑沟、脑回内高密度影;(5)多组颅神经炎,也可表现为头痛及多组颅神经损害,但行头部MRI检查多无异常表现;本文报道的1例即被多次误诊为多组颅神经炎;(6)其他,如自身免疫性疾病的神经系统表现,如结节病、类风湿性关节炎等。
在治疗上若为SHCP,则应根据不同的病因采取相应的治疗;若为IHCP,目前主要用大剂量激素冲击后长期小剂量维持,在激素减量过程中病情加重者可重新加大激素用量或加用免疫抑制剂治疗,目前多数观点认为,由于单用皮质类固醇激素治疗后病情易复发,甚至进行性加重,故在激素减量过程中加用免疫抑制剂是非常有必要的[7,11,14];Bosman等报道了1例IHCP患者,对激素治疗毫无反应,口服甲氨蝶呤6周后临床症状及神经影像学均得到了完全的缓解[15];Horinouchi T 等报道3例IHCP的患者,口服强的松龙60mg/d 或静脉用地塞米松20mg/d,最初所有患者的头痛症状有不同程度的缓解,但对皮质类固醇形成了依赖,加用硫唑嘌呤后患者的临床症状及影像学完全恢复,故他们认为高剂量的皮质类固醇激素冲击治疗后,长期口服免疫抑制剂可能是最理想的治疗模式[16]。也有人主张对不能耐受激素治疗者可单用免疫抑制剂[15];若症状不改善或出现脑实质受压明显者可考虑手术切除部分肥厚的硬脑膜,Horiguchi等认为,当视神经受压损害,对激素治疗的反应为暂时性时,应立即手术减轻视神经受压情况,避免视神经出现不可逆性损害[17]。
1 Uruha A,Koide R,Bandoh M,et al.Neuro-ophthalmic manifestations of hypertrophic cranial pachymeningitis associated with antineutrophil cytoplasmic antibody for myeloperoxidase.Neuro-Ophthalmology,2010,34(4):308-310.
2 Seino H,Nagahata F,Nagahata M,et al.A case of idiopathic hypertrophic spinal pachymeningitis:interesting dural signal intensity on repeat MRI Imaging.Neuroradiology,2010,52(7):678-679.
3 Horino T,Takao T,Taniguchi Y,et al.Hypertrophic pachymeningitis with MPO-ANCA-positive vasculitis.Clinical Rheumatology,2010,29(1):111-113.
4 Rossi S,Giannini F,Cerase A,et al.Uncommon findings in idiopathic hypertrophic cranial pachymeningitis.Journal of Neurology,2004,251(5):548-555.
5 Nakamura T,Hirakawa K,Higashi SI,et al.CD8+T lymphocytes infiltrate predominantly in the inflammatory foci of MPOANCA-positive thoracic hypertrophic pachymeningitis in a patient with HLA-A24.Modern Rheumatology,2007,17(1):75-80.
6 Parney IF,Johnson ES,Allen PB,et al."Idiopathic"cranial pachymeningitis responsive to antituberculous therapy:case re-port.Neurosurgery,1997,41(4):965-971.
7 Kupersmith MJ,Martin V,Heller G,et al.Idiopathic hypertrophic pachymeningitis.Neurology,2004,62(1):686-694.
8 Okuma H.Prevalence rates of hypertrophic pachymeningitis in patients with prolonged headache.Cephalalgia,2009 ,29(1):158-159.
9 Rossi S,Giannini F,Cerase A,et al.Uncommon findings in idiopathic hypertrophic cranial pachymeningitis.Journal of Neurology,2004,251(5):548-555.
10 黄光,刘兴洲.特发性肥厚性硬脑膜炎.中华内科杂志,2006,45(1):68.
11 Shigeo Riku ,Shigenori Kato.Idiopathic hypertrophic pachymeningitis.Neuropathology,2003,23(1):335-344.
12 Cao DR,Murong SX,Ni XH,et al.Clinical presentations and magnetic resonance imaging features in twelve patients with hypertrophic cranial pachymeningitis.Chinese Journal of Neurology,2005,38(3):171-174.
13 Rudnik A,Larysz D,Gamrot J,et al.Idiopathic hypertrophic pachymeningitis:case report and literrature review.Folia Neuropathol,2007,45(1):36-42.
14 Wiesemann E,Berding G,Goetz F,et al.Spontaneous intracranil hypotension:correlation of imaging findings with clinical features.Eur Neurol,2006,56(4):204-210.
15 Bosman T,Simonin C,Launay D,et al.Idiopathic hypertrophic cranial pachymeningitis treated by oral methotrexate:A case report and review of literature.Rheumatology International,2008,28(7):713-718.
16 Horinouchi H,Mori T,Ueyama H,et al.A case of chronic hypertrophic cranial pachymeningitis causing cranial polyneuropathy and unilateral central retinal vein occlusion.Clinical Neurology,2000,40(9):937-940.
17 Horiguchi T,Gotoh K,Yoshida K,et al.A successful case of hypertrophic cranial pachymeningitis treated by optic nerve decompression.Neurological Surgery,1996,24(3):281-285.
