磁性阳离子水凝胶的合成及其对六价铬的吸附去除*
2011-11-08饶品华张文启黄中子郑佳运顾敦罡
饶品华 张文启 黄中子 郑佳运 顾敦罡,2
(1.上海工程技术大学化工学院,上海,201620;2.华东师范大学资源与环境科学学院,上海,200062)
磁性阳离子水凝胶的合成及其对六价铬的吸附去除*
饶品华1**张文启1黄中子1郑佳运1顾敦罡1,2
(1.上海工程技术大学化工学院,上海,201620;2.华东师范大学资源与环境科学学院,上海,200062)
本文通过自由基聚合反应合成了一种带永久正电荷的磁性阳离子水凝胶,评价了该水凝胶对水体中六价铬的吸附去除效果.结果表明,磁性阳离子水凝胶具有较强的热稳定性和磁性,水凝胶中的磁性粒子γ-Fe2O3约占总质量10%,红外光谱测试表明水凝胶表面含有酰胺基和季铵基团.在pH 3—12,磁性阳离子水凝胶具有较好的化学稳定性,其表面Zeta电位在+30 mV以上.吸附实验表明,磁性阳离子水凝胶对六价铬的吸附量较高,最大吸附量达到285 mg·g-1,吸附等温线可用Freundlich方程和Langmuir方程模拟.解吸实验表明,NaCl对水凝胶上六价铬的解吸效果优于NaOH.磁性阳离子水凝胶在对六价铬4次吸附再生后,仍保持高达85%以上的吸附容量,说明该磁性阳离子水凝胶具有较好的应用前景.
磁性,阳离子水凝胶,六价铬,合成,吸附去除.
近年来,随着环境保护的日益重视,重金属对水体的污染已经引起国内外的广泛关注[1-3].污染水体中的重金属离子可通过食物链被人体所吸收,破坏人体的新陈代谢活动,产生致癌、致畸、致突变作用,从而对人类健康带来极大威胁.铬是目前污染水体中常见的重金属之一,其中六价铬具有强致癌性.目前,六价铬的常见去除方法是化学还原沉淀方法[4],然而该方法将产生大量的有害污泥.基于此,许多研究者开始尝试用吸附方法去除水体中的六价铬离子[5-9].吸附方法不仅可以去除六价铬离子,而且吸附剂可以多次再生重复使用,再生液中高浓度的六价铬离子可以回收,具有较好的减排减污效果.常见的吸附剂包括粉煤灰、活性炭、壳聚糖、金属氧化物以及人工合成的聚合物等[10-12].
水凝胶是一种具有强吸水性的三维高分子聚合物.天然的淀粉、壳聚糖是水凝胶中的典型代表,其中壳聚糖被相关研究者用作吸附剂去除水体中的污染物[9,13].研究表明[13],壳聚糖表面携带的是随溶液pH变化的可变电荷,其吸附容量受溶液pH影响大.为此,有关研究者设计合成了带永久电荷的水凝胶,并按照需要改变其膨胀特性、表面电荷类型以及网络结构[14].然而,水凝胶在吸附污染物后的有效快速分离是面临的一个新问题.
磁性材料由于具有较好的分离特性而备受关注.其中γ-Fe2O3是最常见的一种磁性材料,其不仅在环境条件下化学特性稳定且廉价易得.利用γ-Fe2O3的磁性和水凝胶的高吸附容量等优势,制备出新的吸附剂并用于环境中污染物的去除应该是一个有效方法.
目前,磁性水凝胶的合成方法通常是将水凝胶浸没在一定浓度的Fe2+和Fe3+混合溶液中,以在水凝胶的界面形成Fe3O4,该类磁性水凝胶对环境条件的耐受性不够.本文合成了一种带永久正电荷的磁性阳离子水凝胶,通过水凝胶包裹磁性粒子γ-Fe2O3的方式增加磁性水凝胶的化学稳定性,并运用红外光谱、热失重等手段表征了该水凝胶的化学和物理特性,探讨了该水凝胶对六价铬的吸附去除效果.
1 实验部分
1.1 磁性 γ-Fe2O3的制备:
将24.4 g FeCl3·6H2O 和 16.6 g FeSO4·7H2O 溶解在 400 mL 蒸馏水中,向混合溶液中加入0.13 mol·L-1的NaOH 200 mL,持续搅拌3 h后在25℃下静置沉淀3 h,倒去上清液,余下的黑色沉淀物即为Fe3O4.此沉淀物在150℃下加热3 h得到棕色粉末,经XRD衍射分析确定为γ-Fe2O3.
1.2 磁性水凝胶的制备:
称取2.5 g(3-丙烯酰胺丙基)三甲基氯化铵(APTMACl)单体,向其中加入0.05 g交联剂N,N'-亚甲基双丙烯酰胺(MBA),再加0.8 mL纯水.待交联剂MBA全部溶解后,加入加速剂N,N,N',N'-四甲基乙二胺(TEMED)和0.2 g磁性γ-Fe2O3.当以上物质混合均匀后,加引发剂0.6 mL饱和过硫酸钾(KPS)溶液.在60℃水浴中搅拌反应15 min.将生成的磁性水凝胶转移到玻璃瓶中,浸没在纯水里5 d.每8 h换一次水,以洗去未反应的物质如单体,交联剂,引发剂和加速剂等.然后将磁性水凝胶冷冻干燥,磨成颗粒备用.
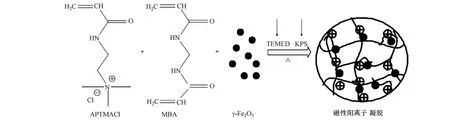
图1 磁性阳离子水凝胶合成示意图Fig.1 Synthesis diagram of magnetic cationic hydrogel
1.3 磁性阳离子水凝胶的固相表征
称取一定量水凝胶粉末在烧杯中,加入蒸馏水制备成0.05 g·L-1的悬浮液,然后取一定量悬浮液在Zeta电位仪(Zetaplus,LaborScience S.A)中测定水凝胶表面电位.同时取一定量的水凝胶粉末在热失重分析仪(Linseis STA PT1000)中测定其热稳定性,利用红外光谱仪(Nicolet AVATAR 370)测定其表面官能团组成.
1.4 磁性阳离子水凝胶对六价铬的吸附去除实验
称取水凝胶粉末1.2 g倒入带玻璃塞的玻璃瓶中,加蒸馏水1000 mL,制备成浓度为1.2 g·L-1的水凝胶悬浮液.然后将水凝胶悬浮液稀释成不同浓度供吸附实验使用,每次使用前摇匀.同时用重铬酸钾配制1000 mg·L-1的六价铬溶液.
吸附动力学实验在45 mL螺口玻璃瓶中进行.将1000 mg·L-1的六价铬溶液稀释成10 mg·L-1,移取稀释后的六价铬溶液35 mL至螺口玻璃瓶中,然后加入7 mL 0.6 g·L-1的水凝胶悬浮液,盖上瓶盖后放入摇床中在 27 r·min-1的转速中混合(混合后六价铬初始浓度为 8.33 mg·L-1,水凝胶浓度为0.1 g·L-1),在一定时间间隔取出样品过滤,分析滤液中六价铬含量.另取一系列45 mL的螺口玻璃瓶,在瓶中加入35 mL 10 mg·L-1的六价铬溶液和不同浓度的水凝胶悬浮液7 mL,盖上瓶盖后放入摇床中旋转混合反应.反应24 h后取出过滤分析滤液中六价铬含量以评价水凝胶剂量对六价铬吸附的影响.吸附等温线实验也在45 mL的螺口玻璃瓶中进行.首先在螺口玻璃瓶中加入7 mL 0.3 g·L-1水凝胶悬浮液和35 mL不同浓度的六价铬溶液,然后放入摇床中旋转混合反应,反应24 h后取出过滤.滤液中的六价铬含量用二苯碳酰二肼分光光度法测定.所有实验重复2次.
1.5 解吸实验
根据等温吸附实验结果,用高浓度的六价铬溶液饱和磁性阳离子水凝胶,然后过滤并用蒸馏水清洗固体水凝胶3次,将清洗后的水凝胶冷冻干燥后,分别加入不同浓度NaCl和NaOH溶液解吸吸附在水凝胶上的六价铬,解吸时间24 h,然后测定解吸出来的六价铬含量,将再生后的水凝胶再次用来吸附溶液中的六价铬,之后再次解吸水凝胶上的六价铬,如此反复进行多次.
2 结果与讨论
2.1 磁性阳离子水凝胶的固相表征
图2显示的是磁性阳离子水凝胶的外形及固相特性.水凝胶呈现棕红色是因为加入了γ-Fe2O3.从图2a可以看出,水凝胶对磁铁的响应性较强,说明较容易在磁场作用下进行分离.粒径分析显示80%的水凝胶粒径在9.6—28.8 μm之间,扫描电镜显示水凝胶颗粒外表呈不规则形状(图2b).在所研究的pH范围内(pH3—12),水凝胶的表面Zeta电位随pH变化较小,且均在+30 mV以上(图2c).较高的表面Zeta电位有利于水凝胶通过静电相互作用吸附去除溶液中的阴离子.溶解实验表明,磁性阳离子水凝胶在pH3—12范围内未发现γ-Fe2O3的溶出现象(数据未显示).热失重分析显示水凝胶可以耐受高达260℃的温度,同时从热失重分析图中可以看出在500℃以上,水凝胶仍有接近10%左右的残留物(图2d).此残留物为γ-Fe2O3粒子.由此可推断出水凝胶中γ-Fe2O3的含量大概在10%左右.此外,从图2e中的红外光谱图可以看出,磁性阳离子水凝胶表面含有C==O基团(1647 cm-1,C==O伸缩振动峰)和 C—N 基团 (1260 cm-1、1546 cm-1,C—N 伸缩振动峰)[15-16];在 1485 cm-1和1095 cm-1附近为—CH2和—CH3振动峰[17-18];而在966 cm-1处的透射峰说明水凝胶表面存在季铵基团[19],这与图2c中水凝胶表面具有较高Zeta电位的结果相互印证.
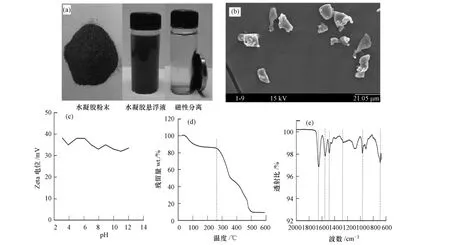
图2 磁性阳离子水凝胶的固相表征(a)外观形状及磁性分离图;(b)粒径分布与扫描电镜图;(c)Zeta电位与pH的关系;(d)热失重分析;(e)红外光谱分析Fig.2 Characterization of magnetic cationic hydrogel
2.2 磁性阳离子水凝胶对六价铬的吸附去除
图3显示的是磁性阳离子水凝胶对六价铬的吸附去除动力学及水凝胶浓度对六价铬吸附的影响.由图3a可知,水凝胶对六价铬的吸附较为迅速,在5 min内对六价铬的去除率达到50%,在3 h左右达到吸附平衡,最终去除率在90%左右.由图3b可知,随着水凝胶浓度的增加,六价铬的去除率增加.0.13 g·L-1左右的水凝胶悬浮液可对8.33 mg·L-1的六价铬溶液实现完全去除.根据图2可知,水凝胶表面带有季铵类基团—N+(CH3)3,这些基团使得水凝胶表面呈正电特性,溶液中的六价铬离子可通过静电吸引作用吸附在水凝胶表面,从而导致了六价铬的去除.
图4显示的是磁性阳离子水凝胶对六价铬的吸附等温线及其拟合情况.由图4a可知,六价铬在水凝胶上的吸附呈现较常见的L型吸附.实验获得的最大的吸附量达到285 mg·g-1,显著高于其它吸附剂如金属氧化物、活性炭、壳聚糖等[5-6,9].使用Freundlich和Langmuir等温方程对图4a吸附等温数据进行拟合,结果如图4b和图4c.其中Qe为吸附达到平衡时六价铬在水凝胶上的吸附量(mg·g-1);Ce为吸附达到平衡时六价铬在溶液中的平衡浓度(mg·L-1),Qm为依据 Langmuir假设拟合得到的最大吸附量(mg·g-1),n,Kf,b 为特征常数.
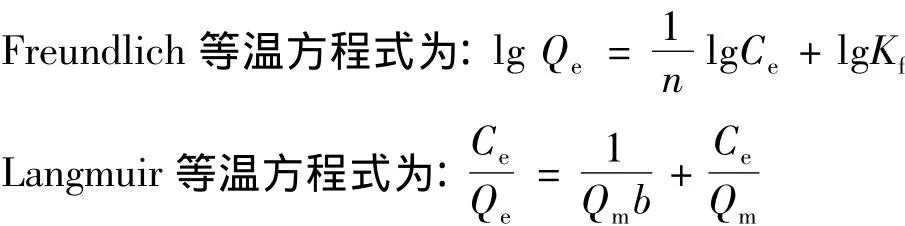
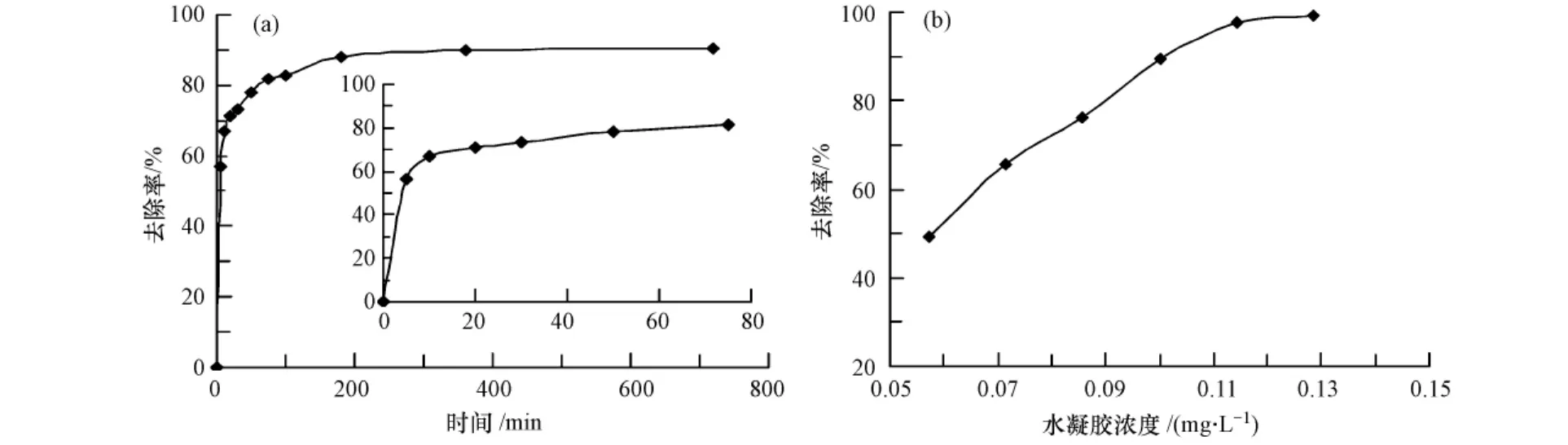
图3 磁性阳离子水凝胶对六价铬的吸附去除(a)动力学;(b)水凝胶浓度对吸附的影响Fig.3 Adsorption kinetics of chromium(Ⅵ)on magnetic cationic hydrogel
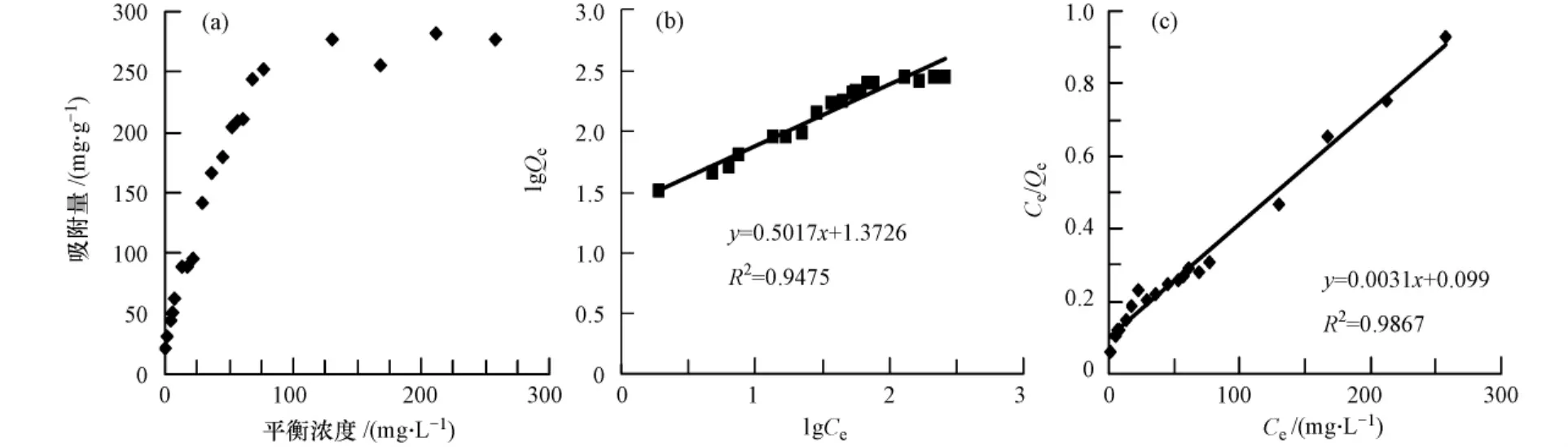
图4 六价铬在磁性阳离子水凝胶上的吸附等温线及其拟合(a)吸附等温线;(b)拟合至Freundlich方程;(c)拟合至Langmuir方程Fig.4 Adsorption isotherm and fitting of chromium(Ⅵ)adsorption on magnetic cationic hydrogel
根据拟合结果可知,六价铬在水凝胶上的吸附等温线与Freundlich和Langmuir方程拟合程度较高,相关系数分别达到0.9475和0.9867,其中Langmuir方程更适合用来描述吸附过程,说明六价铬在水凝胶上的吸附属于单分子层吸附.此外,根据计算可以得出以上两个方程的n,Kf,b值分别为1.99,23.58,0.031.Qm值为 322.6 mg·g-1,与实验获得的最大吸附量接近.
2.3 磁性阳离子水凝胶的再生和六价铬的解吸
为考察磁性阳离子水凝胶的重复使用性,本文探讨了NaCl和NaOH对吸附在水凝胶上六价铬的解吸效果,结果见图5.

图5 (a)解吸剂种类及浓度对对六价铬解吸效果的影响;(b)水凝胶的再生与吸附容量Fig.5 (a)Effect of desorption agents and concentration on desorption of chromium(Ⅵ)from hydrogel;(b)Re-adsorption capacity of hydrogel after regeneration
由图5a可知,NaCl解吸六价铬的效果明显优于NaOH.1 mol·L-1NaCl可以解吸出约90%吸附在水凝胶上的六价铬.当NaCl浓度从1 mol·L-1增加至2 mol·L-1时,六价铬的解吸率进一步上升,达到95%左右,但更高浓度的NaCl意味着需要更高的水处理成本.因此,采用1 mol·L-1的NaCl溶液来研究水凝胶的多次再生能力.由图5b可知,在经过4次的吸附-解吸循环后,水凝胶仍保持将近85%的吸附容量,说明本文合成的磁性阳离子水凝胶具有较好的应用前景.
3 结论
(1)合成了一种带永久正电荷的磁性阳离子水凝胶,固相表征表明该水凝胶具有较强的热稳定性、化学稳定性和磁性,磁性阳离子水凝胶表面含有带正电的季铵基团,其表面Zeta电位在+30 mV以上.
(2)磁性阳离子水凝胶可以通过静电相互作用快速吸附溶液中的六价铬.实验获得的最大吸附量为285 mg·L-1.Freundlich和Langmuir方程可以较好地拟合六价铬在磁性阳离子水凝胶上的等温吸附线.
(3)与NaOH相比,NaCl更适合用来解吸吸附在磁性阳离子水凝胶上的六价铬.经过4次吸附-解吸循环,水凝胶仍保持高达85%的吸附容量.
[1]马前,张小龙.国内外重金属废水处理新技术的研究进展[J].环境工程学报,2007,1(7):10-14
[2]Babel S,Kurniawan T A.Low-cost adsorbents for heavy metals uptake from contaminated water:A review[J].J Hazard Mater,2003,97(1/3):219-243
[3]Kurniawan T A,Chan G Y S,Lo W H,et al.Physico-chemical treatment techniques for wastewater laden with heavy metals[J].Chem Eng J,2006,118(1/2):83-98
[4]Lo I M C,Surampalli R Y,Lai K C K.Zero-Valent Iron Reactive Materials for Hazardous Waste and Inorganics Removal[M].Virginia:ASCE,2006
[5]Mor S,Ravindra K,Bishnoi N R.Adsorption of chromium from aqueous solution by activated alumina and activated charcoal[J].Bioresource Technology,2007,98(4):954-957
[6]Liu S X,Chen X,Chen X Y,et al.Activated carbon with excellent chromium(Ⅵ)adsorption performance prepared by acid-base surface modification[J].J Hazard Mater,2007,141(1):315-319
[7]Dubey S P,Gopal K.Adsorption of chromium(Ⅵ)on low cost adsorbents derived from agricultural waste material:A comparative study[J].J Hazard Mater,2007,145(3):465-470
[8]Pradhan J,Das S N,Thakur R S.Adsorption of hexavalent chromium from aqueous solution by using activated red mud[J].J Colloid Interface Sci,1999,217(1):137-141
[9]Baran A,Biçak E,Baysal Ş H,et al.Comparative studies on the adsorption of Cr(Ⅵ)ions on to various sorbents[J].Bioresource Technology,2006,98(3):661-665
[10]贾金平,李侃,方海军等.活性炭及活性炭纤维对CS2的吸附行为研究及其方法探讨[J].环境化学,2011,30(1):351-356
[11]韩彩芸,张六一,邹照华等.吸附法处理含砷废水的研究进展[J].环境化学,2011,30(2):517-523
[12]李秋荣,李俊华,贺君等.NiO/γ-Al2O3复合氧化物低温吸附NOx的性能[J].环境化学,2010,29(4):721-725
[13]Boddu V M,Abburi K,Talbott J L,et al.Removal of hexavalent chromium from wastewater using a new composite chitosan biosorbent[J].Environ Sci Technol,2003,37(19):4449-4456
[14]Ozay O,Ekici S,Baran Y,et al.Removal of toxic metal ions with magnetic hydrogel[J].Water Res,2009,43(17):4403-4411
[15]Guiney L M,Agnello A D,Thomas J C,et al.Thermoresponsive behavior of charged Nisopropylacrylamide-based hydrogels containing gold nanostructures[J].Colloid Polym Sci,2009,287(5):601-608
[16]Rani A U,Sundaraganesan N,Kurt M,et al.FT-IR,FT-Raman,NMR spectra and DFT calculations on 4-chloro-N-methylaniline[J].Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy,2010,75(5):1523-1529
[17]Malek K,Puc A,Schroeder G,et al.FT-IR and FT-Raman spectroscopies and DFT modeling of benzimidazolium salts[J].Chemical Physics,2006,327(2/3):439-451
[18]Ramalingam S,Prabhu T,Periandy S.Experimental study(FTIR and FT Raman),computed vibrational frequency analysis and computed IR intensity and Raman activity analysis on 2,6-lutidine:HF and DFT calculations[J].International Journal of Industrial Chemistry,2011,2(1):12-22
[19]Chen N,Chen Y,Wang L,et al.Preparation,characterization,and blood compatibility of polylactide-based phospholipid polymer[J].J Mater Sci,2009,44(23):6317-6324
SYNTHESIS OF MAGNETIC CATIONIC HYDROGEL AND ITS ADSORPTION FOR CHROMIUM(Ⅵ)
RAO Pinhua1ZHANG Wenqi1HUANG Zhongzi1ZHENG Jiayun1GU Dungang1,2
(1.School of Chemistry and Chemical Engineering,Shanghai University of Engineering Science,Shanghai,201620,China;2.School of Resources and Environment Science,East China Normal University,Shanghai,200062,China)
Magnetic cationic hydrogel with permanent positive charge was synthesized via radical polymerization.Its adsorption capacity for chromium(Ⅵ)was evaluated.It was found that magnetic cationic hydrogel had strong thermostability and magnetism.The weight percentage of magnetic γ-Fe2O3in cationic hydrogel was about 10%.FTIR spectroscopic analysis showed the existence of amide and trimethyl amine on the surface of magnetic cationic hydrogel.In the range of pH 3 to 12,high chemical stability and low swelling property were observed,and the zeta potential on its surface was above+30 mV.Adsorption experimental results showed that a high adsorption capacity for chromium(Ⅵ)(maximum 285 mg·g-1)was found.Adsorption isotherm of chromium(Ⅵ)on the hydrogel fitted both Freundlich model and Langmuir model well.NaCl had a stronger ability in desorbing chromium(Ⅵ)from the magnetic cationic hydrogel than NaOH.Over 85%recovery rate was attained after four consecutive adsorption-desorption cycles, indicating good perspective for real applications.
magnetism,cationic hydrogel,hexavalent chromium,synthesis,adsorption removal.
2011年2月13日收稿.
*上海市自然科学基金项目(10ZR1412600);上海市教委科研创新项目(12YZ153,11ZZ176)资助.
**通讯联系人,Tel:021-67791214,E-mail:raopinhua@hotmail.com